Неорганические материалы, 2022, T. 58, № 3, стр. 277-282
Синтез порошков, содержащих карбиды молибдена, безвакуумным электродуговым методом с изменением силы тока
Ю. З. Васильева 1, *, А. Я. Пак 1, П. Н. Кононенко 1, Т. Ю. Якич 1, А. В. Мостовщиков 1, 2, 3, И. И. Шаненков 1
1 Томский политехнический университет
634050 Томск, пр. Ленина, 30, Россия
2 Томский государственный университет систем управления и радиоэлектроники
634050 Томск, пр. Ленина, 40, Россия
3 Томский государственный архитектурно-строительный университет
634003 Томск, пл. Соляная, 2, Россия
* E-mail: yzv1@tpu.ru
Поступила в редакцию 06.10.2021
После доработки 18.12.2021
Принята к публикации 29.12.2021
- EDN: VOQMXI
- DOI: 10.31857/S0002337X22030137
Аннотация
В работе представлены результаты экспериментальных исследований по получению ультрадисперсных материалов на основе карбидов молибдена безвакуумным электродуговым методом. Установлены параметры разрядного контура, обеспечивающие практически полную переработку исходного молибдена. В продукте присутствуют кристаллы микронных размеров, а также углеродные графеноподобные объекты с погруженными в них наноразмерными частицами карбидов молибдена. Приведены первичные результаты оценки каталитической активности полученных образцов без их модификации драгоценными металлами.
ВВЕДЕНИЕ
В условиях существующих экологических проблем, вызванных потреблением традиционного ископаемого топлива, повышается актуальность в использовании возобновляемых источников энергии. Как известно, возможным решением задачи снижения углеродного следа является применение энергетических технологий, основанных на водороде. Для получения водорода активно применяют метод электролиза с использованием катализаторов для снижения энергоемкости процесса [1, 2]. На сегодняшний день наиболее эффективным катализатором является платина, но ввиду высокой стоимости и надзора за оборотом актуален вопрос ее замены на более дешевые аналоги со схожими свойствами. Перспективными в этой области считаются материалы на основе карбида молибдена в углеродной графитоподобной матрице [3]. Несмотря на то что их свойства в реакциях получения водорода из воды активно изучаются, достичь схожих с платиновыми катализаторами характеристик пока не удается. Известно, что каталитическая активность может быть дополнительно увеличена за счет повышения удельной поверхности, нанесения катализаторов на углеродные наноматериалы, допирования структуры атомами азота [4, 5].
Есть множество способов получения материалов на основе карбидов молибдена: механосинтез [6], карботермическое восстановление [7], пиролиз, ультразвуковое распыление [8], плазменные методы [9, 10]. Одним из важных аспектов развития группы плазменных методов является перевод электродуговых реакторов на работу в условиях использования атмосферного воздуха в качестве рабочей среды [11]. Достоинством данного метода является отказ от вакуумного оборудования и инертных газов, что повышает энергоэффективность системы и может улучшить технико-экономические и массово-габаритные показатели. Использование воздуха в качестве рабочей среды возможно благодаря автономной среде, экранирующей реакционный объем от окисления кислородом воздуха, которая создается самопроизвольно за счет эмиссии газов СО и СО2 [12].
Возможность применения безвакуумного метода для электродугового синтеза катализаторов реакций получения водорода из воды на основе карбидов молибдена показана ранее [13]. Недостатком проведенной серии экспериментов является значительное загрязнение продукта синтеза в результате практически неконтролируемой эрозии графитового анода, что значительно затрудняет поиск заявляемого состава катализатора. Для оценки возможности минимизации массы примесного графита было принято решение рассмотреть две различные схемы подвода энергии дугового разряда: схема 1 – с пропусканием тока разрядного контура через исходное сырье и инициированием разряда непосредственно на поверхности засыпки исходного сырья (прямой нагрев), схема 2 – без пропускания тока разрядного контура через исходное сырье с организацией горения разряда в непосредственной близости к исходному сырью (косвенный нагрев).
Целью данной работы является проведение экспериментальных исследований по получению каталитически активных материалов на основе карбида молибдена, синтезированных при различной силе тока разрядного контура с использованием двух описанных выше схем подвода энергии дугового разряда. Стоит отметить, что, согласно анализу литературы, ранее подобные исследования не проводились.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Экспериментальные исследования были проведены в двух лабораторных электродуговых реакторах с разной системой разрядного контура: “схемой 1” [14] (с пропусканием тока через исходное сырье) и “схемой 2”, обеспечивающей косвенный нагрев исходных реагентов [15] (рис. 1). Исходным сырьем служила смесь микроразмерных порошков чешуйчатого графита и меламина, а также наноразмерного молибдена после обработки в шаровой мельнице марки SamplePrep 8000M-230 Mixer/Mill (SPEX) в течение 30 мин. Масса исходной смеси в каждом эксперименте составляла 0.50 ± 0.01 г. При схеме 1 в качестве анода был использован графитовый стержень, в качестве катода – графитовый тигель, на дно которого закладывалась исходная смесь. При схеме 2 анодом и катодом служили графитовые стержни, которые заводились в полость графитового тигля через отверстия в боковых стенках; исходная смесь располагалась на дне графитового тигля, в полости которого поджигали дуговой разряд. При проведении серии экспериментов изменяли силу тока источника питания в диапазоне от 80 до 200 А с использованием обеих схем подведения энергии дугового разряда.
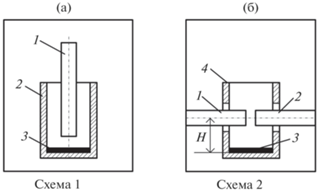
Рис. 1.
Схемы разрядного контура лабораторных электродуговых реакторов: 1 – анод, 2 – катод, 3 – исходная смесь, 4 – тигель.
Полученные образцы анализировали с помощью известных методик: рентгеновской дифрактометрии (Shimadzu XRD-7000, CuKα-излучение, λ = 1.54060 Å), растровой электронной микроскопии (Tescan VEGA 3 SBU) и просвечивающей электронной микроскопии (ПЭМ) (JEOL JEM-2100F). Оценка электрохимических свойств получаемых материалов выполнена с использованием электролитической трехэлектродной ячейки и рабочей станции CHI 604E в растворе 0.5 М H2SO4 (pH 0.3). Электродами выступали: насыщенный каломельный электрод (SCE), платиновая нить, цилиндрический стеклоуглеродный электрод L-типа.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
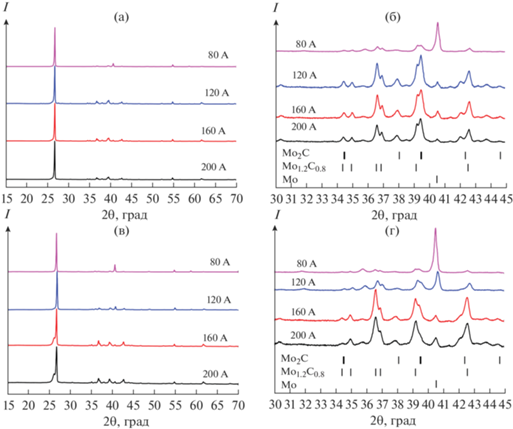
По результатам рентгеновской дифрактометрии (рис. 2) видно, что образцы представляют собой смесь нескольких кристаллических фаз. Следует отметить, что исходный чешуйчатый графит является материалом с высокой степенью преимущественной ориентации, вследствие чего на всех дифрактограммах идентифицируется высокоинтенсивный максимум, соответствующий семейству плоскостей (002). В общем случае наблюдается наличие двух фаз карбида молибдена – Мо2С и Мо1.2С0.8, фазы исходного кубического молибдена и графитоподобной фазы. Близкими кристаллическими фазами в международной базе данных PDF4+ можно считать ICDD № 04-016-3695, ICDD № 04-006-2272, ICDD № 01-077-8340, ICDD № 04-015-2407 соответственно.
При минимальном токе источника питания, равном 80 А, подведенной энергии недостаточно для переработки исходных компонентов, вследствие чего на дифрактограммах четко видны рефлексы графита и молибдена. При увеличении тока до 120 А энергии прямого нагрева (~40 кДж) достаточно для начала образования фаз карбида молибдена, преимущественно фазы Мо2С. Однако при косвенном нагреве при такой же силе тока подведенной энергии не хватает для переработки исходной смеси, так как она расположена на расстоянии ~10 мм от электрической дуги. При силе тока 160 А на рис. 2в можно заметить, что главный максимум состоит из двух рефлексов: 2θ ~ 26.03° и ~26.6°, принадлежащих исходному графиту и электроэрозионному графиту. Чем больше ток, тем более выражен процесс эрозии анода. При этом в отличие от схемы 1 , в которой исходный порошок синтезируется при одинаковых режимах обработки, в схеме 2 смесь исходных компонентов расположена на расстоянии от электрической дуги и ввиду высокого градиента температур реализуются разные параметры обработки. При силе тока 200 А количество исходного молибдена минимально, поскольку благодаря достаточной энергии (~60 кДж) он практически весь перерабатывается в карбиды молибдена. Таким образом, как можно заметить из приведенных дифрактограмм, при схеме 1 доминирующей фазой карбида молибдена является Мо2С, при схеме 2 – Мо1.2С0.8.
Для исследования морфологии частиц и элементного состава были выбраны образцы, полученные при силе тока 200 А, поскольку именно при данной силе тока количество исходного молибдена в продукте минимально. Карбид молибдена, синтезированный прямым нагревом, имеет тонкозернистую, плотную структуру и находится в основном на поверхности углеродных агрегатов (рис. 3а, 3б). Размер агрегатов варьируется от 1 до 50 мкм, при этом в синтезированном продукте присутствуют кристаллы с размером менее 10 нм. Согласно анализу элементного состава, основными элементами являются C (~48.1%), Mo (~44.9%) и О (~4.8%). Также обнаруживаются примеси Ti, W, изредка Ni, Pb, Bi, S, суммарная масса которых в среднем не превышает ~2%.
Рис. 3.
Тонкозернистые агрегаты синтезированного карбида молибдена (светло-серый цвет) и его спектр (темно-серый цвет) в обратно рассеянных (а) и вторичных (б) электронах при схеме 1 ; плотные агрегаты карбида молибдена (светло-серый цвет) и его спектр на зернистых агрегатах графита (темно-серый цвет) в обратно рассеянных (в) и вторичных (г) электронах при схеме 2 .
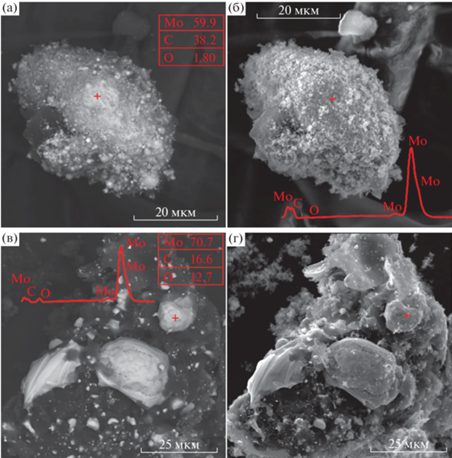
Аналогично предыдущему образцу карбид молибдена, синтезированный косвенным нагревом, представлен пленками и натечными агрегатами, реже – мелкими округлыми зернами с оплавленными и гладкими очертаниями. При этом встречаются сравнительно цельные сростки кристаллов с многочисленными центрами кристаллизации (рис. 3в, 3г). Элементный состав аналогичен и содержит C (~36.4%), Mo (~52.3%), О (~5.2%) и примеси (Fe, Ti, Si и т.д.).
При сравнительной характеристике химического состава полученных продуктов установлено, что количество молибдена выше в образце, полученном при использовании схемы 2 , но в его составе больше кислорода. Большее количество молибдена при косвенном нагреве объясняется неполной переработкой исходного молибдена ввиду недостаточного количества подведенной энергии, что также видно по данным рентгеновской дифрактометрии. Бóльшая доля кислорода в составе продукта, синтезированного с использованием схемы 2, может быть связана с наличием отверстий в стенках катода для размещения электродов, что влияет на протекание газогидродинамических процессов в системе и препятствует экранированию реакционного объема [12], вследствие чего может происходить окисление продуктов синтеза кислородом воздуха.
На рис. 4 представлены результаты ПЭМ. Видно, что структура образца представляет собой углеродную графитоподобную матрицу, которой на картине электронной дифракции (рис. 4б) соответствуют кольца с межплоскостными расстояниями ~3.41, 2.15, 1.71, 1.21 Å. При этом в матрице находятся частицы карбида молибдена. Межплоскостные расстояния отдельной частицы, определенные по ПЭМ-снимку высокого разрешения (рис. 4в), соотносятся с эталонными для фазы Мо1.2С0.8 с учетом погрешности ~3.65 ± ± 0.02 Å.
Рис. 4.
ПЭМ-снимок (а), картина электронной дифракции на выделенной области (б), ПЭМ-снимок высокого разрешения (в).

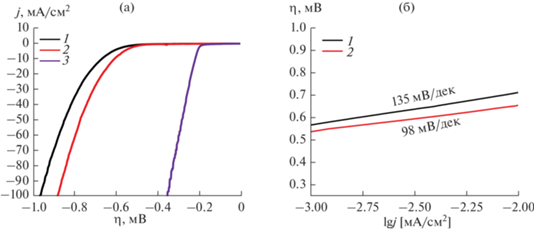
Электрокаталитическую активность образцов измеряли с использованием стандартной трехэлектродной ячейки в 0.5 М растворе H2SO4. На рис. 5а показаны снятые вольтамперограммы. Начальное перенапряжение для образца, полученного при схеме 1 , составляет η1 = 260 мВ, тогда как для образца, синтезированного с применением схемы 2 , данное значение выше и равно η1 = = 285 мВ. Перенапряжение при 10 мА/см2 составляет 367 и 420 мВ для образцов, полученных при схемах 1 и 2 , что значительно выше в сравнении с платиновым электродом Pt(20%)/C (η10 < 100 мВ). Расчетные значения тафелевского наклона линейного участка кривых на рис. 5а, описывающего кинетику процесса на поверхности катализатора, показали, что электрод, изготовленный из образца, синтезированного прямым нагревом, имеет более высокую скорость протекания реакций (98 мВ/дек) в сравнении с образцом, полученным косвенным нагревом (135 мВ/дек).
Рис. 5.
Вольтамперограммы (а) и тафелевский наклон линейного участка (б): 1 – образец, полученный при схеме 2 ; 2 – образец, полученный при схеме 1 ; 3 – платиновый электрод Pt(20%)/C.
Наиболее вероятным механизмом образования карбида молибдена является следующий. Известно, что при температуре ~345°С меламин C3H6N6 разлагается на аммиак NH3 и мелем C6H6N10. В свою очередь аммиак при нагревании проявляет восстановительные свойства: при температуре ~1300°С он полностью разлагается на азот и водород. Учитывая, что эти процессы происходят в бескислородной среде реакционной ячейки в атмосфере CO и CO2, при ее насыщении водородом он не соединяется с O2, а создает восстановительную атмосферу. Создание такой атмосферы способствует протеканию реакции ${\text{Mo}} + {\text{C}}\xrightarrow{{{\text{H}},{{{\text{H}}}_{2}}}}{\text{MoC}},$ которая более эффективно осуществляется в присутствии водорода.
Таким образом, в системе Mo + C + C3H6N6 в атмосферной электродуговой плазме возможно протекание следующих реакций:
(3)
${\text{N}}{{{\text{H}}}_{3}}\xrightarrow{{t = 1300^\circ {\text{C}}}}{{{\text{N}}}_{2}} + {{{\text{H}}}_{2}},$Образование карбида молибдена в атмосферной плазме дугового разряда постоянного тока представляет собой сложный физико-химический процесс, протекающий в несколько стадий (реакции (1)–(4)).
ЗАКЛЮЧЕНИЕ
Представлены результаты экспериментальных исследований, посвященных синтезу каталитически активных материалов на основе карбидов молибдена безвакуумным электродуговым методом. При этом изменялись схема разрядного контура и сила тока в целях регулирования фазового состава продукта синтеза. Установлено, что при обработке исходного сырья плазмой дугового разряда при силе тока 200 А в продукте синтеза количество исходного молибдена минимально.
На данном этапе исследований полученные образцы проявляют относительно невысокую каталитическую активность. Поиск состава катализатора, режимов работы установки, а также путей повышения каталитической активности получаемых продуктов является предметом дальнейших исследований.
Список литературы
Wang W., Liu C., Zhou D., Yang L., Zhou J., Yang D. In-situ Synthesis of Coupled Molybdenum Carbide and Molybdenum Nitride as Electrocatalyst for Hydrogen Evolution Reaction // J. Alloys Compd. 2019. V. 792. P. 230–239. https://doi.org/10.1016/j.jallcom.2019.03.397
Huang Yu., Wang C., Song H., Bao Ya., Lei X. Carbon-Coated Molybdenum Carbide Nanosheets Derived from Molybdenum Disulfide for Hydrogen Evolution Reaction // J. Hydrogen Energy. 2018. V. 43. P. 12610–1617. https://doi.org/10.1016/j.ijhydene.2018.03.233
Cui T., Dong J., Pan X., Yu T., Fu Q., Bao X. Enhanced Hydrogen Evolution Reaction over Molybdenum Carbide Nanoparticles Confined inside Single-Walled Carbon Nanotubes // J. Energy. Chem. 2019. V. 28. P. 123–127. https://doi.org/10.1016/j.jechem.2018.03.006
Xia K., Guo J., Xuan C., Huang T., Deng Z., Chen L., Wang D. Ultrafine Molybdenum Carbide Nanoparticles Supported on Nitrogen Doped Carbon Nanosheets for Hydrogen Evolution Reaction // Chin. Chem. Lett. 2019. V. 30. P. 192–196. https://doi.org/10.1016/j.cclet.2018.05.009
Wei H., Xi Q., Chen X., Guo D., Ding F., Yang Z., Wang S., Li J., Huang S. Molybdenum Carbide Nanoparticles Coated into the Graphene Wrapping N-Doped Porous Carbon Microspheres for Highly Efficient Electrocatalytic Hydrogen Evolution both in Acidic and Alkaline Media // Adv. Sci. 2018. V. 5. P. 170073. https://doi.org/10.1002/advs.201700733
Baklanova O.N., Vasilevich A.V., Lavrenov A.V. et al. Molybdenum Carbide Synthesized by Mechanical Activation an Inert Medium // J. Alloys Compd. 2017. V. 698. P. 1018–1027. https://doi.org/10.1016/j.jallcom.2016.12.186
Guil-Lopez R., Nieto E., Botas J.A., Fierro J.L.G. On the Genesis of Molybdenum Carbide Phases during Reduction-Carburization Reactions // J. Solid State Chem. 2012. V. 190. P. 285–295. https://doi.org/10.1016/j.jssc.2012.02.021
Lv C., Huang Z., Yang Q., Wei G., Chen Z., Humphrey M.G., Zhang C. Ultrafast Synthesis of Molybdenum Carbide Nanoparticles for Efficient Hydrogen Generation // J. Mater. Chem. A. 2017. V. 43. P. 2280–22812. https://doi.org/10.1039/C7TA06266D
Zhao H., Kang C., Ma Z., Cheng Z., Jia T., Kimura H., Fu Q., Tao H., Xiong L. Synthesis of Molybdenum Carbide Superconducting Compounds by Microwave-Plasma Chemical Vapor Deposition // J. Appl. Phys. 2018. V. 123. № 5. P. 053301. https://doi.org/10.1063/1.5010101
Yan Z., Zang J., Han C., Jia S., Tian P., Gao H., Wang Ya. Molybdenum Oxide and Molybdenum Carbide Coated Carbon Black as an Electrocatalyst for Hydrogen Evolution Reaction in Acidic Media // Int. J. Hydrogen Energy. 2017. V. 42. №. 44. P. 26985–26994. https://doi.org/10.1016/j.ijhydene.2017.09.077
Arora N., Sharma N.N. Arc Discharge Synthesis of Carbon Nanotubes: Comprehensive Review // Diamond Relat. Mater. 2014. V. 50. P. 135–150. https://doi.org/10.1016/j.diamond.2014.10.001
Pak A.Y., Shanenkov I.I., Mamontov G.Y., Kokorina A.I. Vacuumless Synthesis of Tungsten Carbide in a Self-Shielding Atmospheric Plasma of DC Arc Discharge // Int. J. Refract. Met. Hard Mater. 2020. V. 93. P. 105343. https://doi.org/10.1016/j.ijrmhm.2020.105343
Vassilyeva Y.Z., Butenko D.S., Li S., Han W., Pak A.Y. Synthesis of Molybdenum Carbide Catalyst by DC Arc Plasma in Ambient Air for Hydrogen Evolution // Mater. Chem. Phys. 2020. V. 254. P. 123509. https://doi.org/10.1016/j.matchemphys.2020.123509
Пак А.Я. Устройство для получения порошка, содержащего карбид молибдена: Патент РФ № 2716694 C1; заявл. 24.05.2019; опубл. 13.03.2020, Б.И. № 8.
Мартынов Р.С., Пак А.Я., Мамонтов Г.Я. Устройство для получения порошка на основе карбида бора: Патент РФ № 2019111857/19; заявл. 19.04.2019; опубл. 10.09.2019, Б.И. № 26.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы