Неорганические материалы, 2022, T. 58, № 4, стр. 389-396
Синтез и исследование люминофора KBaGd(MoO4)3:Er3+/Yb3+ с шеелитоподобной структурой
Н. М. Кожевникова *
Байкальский институт природопользования СО Российской академии наук
670047 Улан-Удэ, ул. Сахьяновой, 6, Россия
* E-mail: nicas@binm.ru
Поступила в редакцию 23.06.2021
После доработки 31.10.2021
Принята к публикации 21.12.2021
- EDN: GZUVRK
- DOI: 10.31857/S0002337X2204008X
Аннотация
Изучены фазовые отношения в субсолидусной области системы K2MoO4–BaMoO4–Gd2(MoO4)3 по разрезам методами рентгенографического и дифференциального термического анализа, проведена триангуляция системы. Синтезирован тройной молибдат KBaGd(MoO4)3, который кристаллизуется в моноклинной шеелитоподобной структуре (пр. гр. P21/n). Легированием KBaGd(MoO4)3 ионами Er3+/Yb3+ получен ап-конверсионный люминофор, обладающий антистоксовой люминесценцией в области 400–700 нм при возбуждении ИК-излучением (λвозб = 977 нм). Синтезированный люминофор исследован методами рентгенографии, дифференциального термического анализа и колебательной спектроскопии, изучены его спектрально-люминесцентные характеристики.
ВВЕДЕНИЕ
Молибдаты и вольфраматы, содержащие щелочноземельные и редкоземельные элементы, структуры которых производны от шеелита, обладая низким коэффициентом термического расширения, высокой химической и термической устойчивостью, находят широкое применение в таких областях, как квантовая электроника, волоконная оптика, люминофоры, лазерные устройства, ап-конверсионные материалы, преобразующие излучение с низкой энергией в излучение с более высокой энергией [1–4].
Поиск перспективных соединений и создание на их основе полифункциональных люминофоров, обладающих интенсивной люминесценцией при УФ-облучении и антистоксовой люминесценцией при ИК-возбуждении, является актуальной задачей для материаловедения. Эффективным способом воздействия на люминесцентные свойства материалов является легирование их ионами Er3+, Yb3+, способными поглощать ИК-излучение и преобразовывать его в видимую антистоксовую люминесценцию [5–18].
Обширность поля кристаллизации индивидуальных соединений и твердых растворов с шеелитоподобной структурой определяется возможностью изо- и гетеровалентных замещений щелочноземельных элементов катионами различной природы, которые заселяют кристаллографические позиции каркаса структуры и ее полости. Широкий изоморфизм катионов различной природы приводит к дисбалансу зарядов в структуре шеелита вследствие геометрических особенностей расположения ближайших полиэдров, возникновению локальных и кооперативных искажений и позволяет регулировать оптические свойства фаз. Такие особенности строения шеелитоподобных молибдатов определяют перспективы их использования в качестве люминесцентных и лазерных материалов, химических сенсоров, ап-конверсионных материалов, что обуславливает интенсивные теоретические и экспериментальные исследования этой группы неорганических соединений [1–4, 14–16].
Среди тройных молибдатов, содержащих щелочноземельные и редкоземельные элементы, известны ряды кальциевых, стронциевых соединений MM'Ln(MoO4)3 (M = K, Rb, Cs; M' = Ca, Sr; Ln = Nd, Sm, Eu, Y, Lu) [6, 15]. Возможность других комбинаций катионов металлов не была проанализирована.
Цель настоящей работы – изучение фазовых равновесий в субсолидусной области системы K2MoO4–BaMoO4–Gd2(MoO4)3, синтез ап-конверсионного люминофора на основе тройного молибдата KBaGd(MoO4)3:Er3+/Yb3+ с шеелитоподобной структурой и изучение его люминесцентных и физико-химических свойств.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходными компонентами для изучения фазообразования в системе K2MoO4–BaMoO4–Gd2(MoO4)3 служили предварительно синтезированные твердофазным способом K2MoO4, BaMoO4 и Gd2(MoO4)3 из K2CO3, BaCO3, Gd2O3 и MoO3 в интервале температур 400–700°С с многократной промежуточной гомогенизацией через каждые 20–30 ч. Время прокаливания при каждой температуре составляло 100–120 ч. После обжига образцы медленно охлаждали вместе с печью. Неравновесные образцы отжигали дополнительно, равновесие считали достигнутым, если фазовый состав образцов оставался неизменным при двух последовательных отжигах.
Продукты синтеза идентифицировали методами рентгенофазового анализа (РФА) на дифрактометре D8 Advance фирмы Bruker (CuKα-излучение). Расчет рентгенограмм проводили с использованием программ “Рентген”. Колебательные спектры поликристаллических образцов KBaGd(MoO4)3 зарегистрированы на спектрометрах Bruker FT-IR и Specord М-80 с использованием для возбуждения лазера с излучением в ближней ИК-области 1.06 мкм (геометрия обратного рассеяния, разрешение 3–5 см–1). Образцы готовили в виде суспензии в вазелиновом масле на полиэтиленовой подложке и таблеток с KBr. Для приготовления изотопозамещенных по молибдену образцов использовали оксиды 92MoO3 и 100MoO3 с содержанием основного изотопа не менее 95%. Дифференциальный термический анализ (ДТА) проводили на дериватографе ОД-103 фирмы МОМ, скорость подъема температуры составляла 10°С/мин, навеска 0.3–0.4 г.
Для введения различных концентраций иона-активатора оксид гадолиния в KBaGd(MoO4)3 эквимолярно заменяли на оксиды эрбия и иттербия. Таким способом были получены образцы люминофора, содержащие 1–6 мол. % Er2O3 и 1–9 мол. % Yb2O3. Спектры люминесценции образцов люминофора с различной концентрацией ионов эрбия и иттербия – KBaGd0.97Er0.01Yb0.02(MoO4)3, KBaGd0.95Er0.01-Yb0.04(MoO4)3, KBaGd0.90Er0.01Yb0.09(MoO4)3 – измеряли на спектрометре Ocean Optics QE 65000. Для возбуждения люминесценции в ИК-диапазоне использовали лазерный диод InGaAs (λвозб = = 977 нм). Энергетический выход ап-конверсионной люминесценции измерен в видимом диапазоне спектра с помощью интегрирующей сферы. Приемником излучения являлся кремниевый фотодатчик TSL 237 с диапазоном чувствительности 300–1100 нм. Интенсивность возбуждающего пучка измерялась с помощью сферы. Энергетический выход люминофора определялся как отношение излученной мощности к поглощенной (Pem/Pabs). Поглощенную мощность рассчитывали как разницу между рассеянием от стандартного образца, не содержащего легирующих ионов, и от исследуемого образца. Времена жизни ап-конверсионной люминесценции ионов Er3+ определены в люминофоре с максимальным значением Ben = 0.37% при переходах между уровнями 2H11/2 → 4I15/2 и 4S3/2 → 4I15/2 (зеленая область спектра) и 4F9/2 → 4I15/2 (красная область спектра) с использованием интегрирующей сферы.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Взаимодействие в системе K2MoO4–BaMoO4–Gd2(MoO4)3 изучено методом перекрещивающихся разрезов в области температур 450–800°С. Исследование системы K2MoO4–BaMoO4–Gd2(MoO4)3 проведено в две стадии. Первоначально изучали фазовый состав точек пересечения разрезов, исходящих из средних и двойных молибдатов, образующихся в ограняющих двойных системах. На второй стадии изучали выявленные квазибинарные до 800°С разрезы, что позволило провести триангуляцию системы.
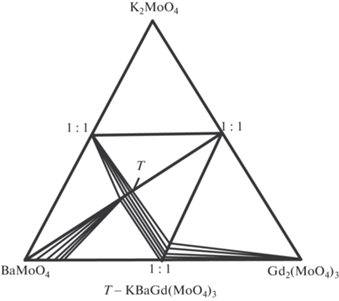
На рис. 1 представлены фазовые отношения в системе K2MoO4–BaMoO4–Gd2(MoO4)3.
В ограняющей двойной системе K2MoO4–Gd2(MoO4)3 установлено образование молибдатов состава 1 : 1, 5 : 1, кристаллизующихся в различных структурных типах [1, 6, 14]. При взаимодействии K2MoO4 с BaMoO4 зафиксировано образование двойного молибдата K2Ba(MoO4)2, обладающего структурой пальмиерита. В системе BaMoO4–Gd2(MoO4)3 синтезирован молибдат BaGd2(MoO4)4, принадлежащий к слоистой шеелитоподобной структуре с моноклинным искажением (пр. гр. С2/с) [2].
Наиболее подробно (через 1–2 мол. %) изучено взаимодействие на разрезе BaMoO4–KGd(MoO4)2, где установлено образование тройного молибдата KBaGd(MoO4)3 при 650–750°С. Для достижения равновесия необходимо прокаливать реакционные смеси в течение 150–170 ч с промежуточной гомогенизацией.
Для системы K2MoO4–BaMoO4–Gd2(MoO4)3 квазибинарными разрезами являются KGd(MoO4)2– KBaGd(MoO4)3, K2Ba(MoO4)2–KBaGd(MoO4)3, K2Ba(MoO4)2–KGd(MoO4)2, BaMoO4–KBaGd(MoO4)3, BaGd2(MoO4)4–KBaGd(MoO4)3, BaGd2(MoO4)4–KGd(MoO4)2. Методом РФА установлено, что в тройном молибдате KBaGd(MoO4)3 растворяется 3.5 мол. % BaMoO4, растворимость тройного молибдата в BaMoO4 составляет 12 мол. %. Фазовые отношения в системах K2Ba(MoO4)2–KBaGd(MoO4)3 и BaGd2(MoO4)4–KBaGd(MoO4)3 характеризуются двухфазными областями, системы эвтектические с областью гомогенности тройной фазы до 3 мол. %. Растворимость KGd(MoO4)2 в KBaGd(MoO4)3 составляет 3.0 мол. %, в KGd(MoO4)2 растворяется не более 1.5 мол. % KBaGd(MoO4)3. Разрез K2Ba(MoO4)2–K5Gd(MoO4)4 не является квазибинарным, так как при температуре 800°С он нестабилен из-за термической неустойчивости фазы K5Gd(MoO4)4, которая плавится инконгруэнтно при 775°С. Разрез K2Ba(MoO4)2–KGd(MoO4)2 является простым эвтектическим без заметной растворимости компонентов.
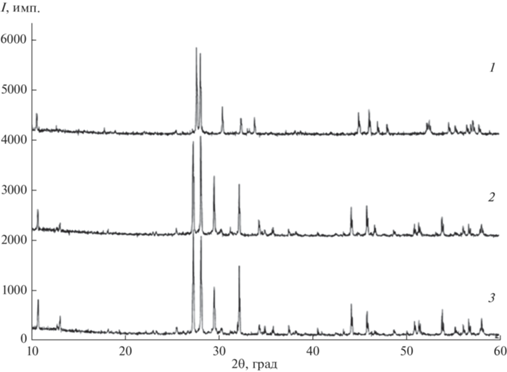
Рентгенографическое исследование показало, что тройной молибдат KBaGd(MoO4)3 имеет шеелитоподобную структуру с моноклинным искажением и проявляет большое сходство в расположении наиболее интенсивных линий на рентгенограмме с α-KSm(MoO4)2, что свидетельствует об общности структурных мотивов тройного и двойного молибдатов. Для сравнения на рис. 2 приведены рентгенограммы α-KSm(MoO4)2, KBaSm(MoO4)3 и KBaGd(MoO4)3. Рентгенограммы KBaSm(MoO4)3 и KBaGd(MoO4)3 проиндицированы в моноклинной сингонии (пр. гр. P21/n, Z = 9). Соединения изоструктурны между собой, а также двойному молибдату α-KSm(MoO4)2 и принадлежат к структурному типу моноклинно искаженного шеелита.
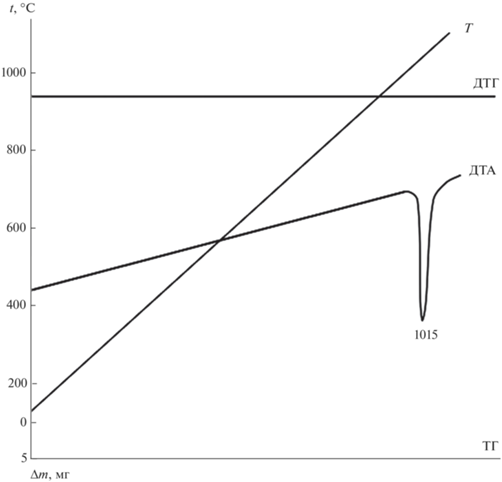
Структуру KBaGd(MoO4)3 можно рассматривать как продукт гетеровалентного замещения щелочноземельного элемента в структуре шеелита по схеме: 2Ba = K+ + Gd3+. Параметры кристаллической решетки KBaGd(MoO4)3 равны: а = = 12.172(3) Å, b = 11.806(2) Å, с = 16.907(3) Å, β = = 95.00(3)°, V = 2420.4 Å3. Плавится KBaGd(MoO4)3 инконгруэнтно при 1015°С, не претерпевая полиморфных превращений (рис. 3).
Измеренные значения колебательных частот ИК- и КР-спектров KBaGd(MoO4)3, KBaSm(MoO4)3, α‑KSm(MoO4)2 приведены в табл. 1. Здесь же даны частоты колебаний BaMoO4 и их отнесение к внутренним колебаниям групп MoO4 и колебаниям кристаллической решетки (либрационным колебаниям MoO4-групп (R) и трансляционным колебаниям различных подрешеток кристалла (Т)) [6, 19].
Таблица 1.
Частоты колебаний в КР- и ИК-спектрах KBaGd(MoO4)3, KBaSm(MoO4)3, α-KSm(MoO4)2, ВaMoO4
| ν, см–1 | Отнесение | |||||||
|---|---|---|---|---|---|---|---|---|
| KBaGd(MoO4)3 | KBaSm(MoO4)3 | α-KSm(MoO4)2 | ВaMoO4 | |||||
| КР | ИК | КР | ИК | КР | ИК | КР | ИК | |
| 933 | 934 | 934 | 944 | 925 | 891 | |||
| 918 | 916 | 919 | 915 | 929 | ν1 | |||
| 894 | 895 | 888 | ||||||
| 866 | 855 | 867 | ||||||
| 869 | 845 | |||||||
| 837 | 838 | 840 | 840 | 838 | 830 | |||
| 814 | 815 | 815 | ||||||
| 802 | 800 | 801 | 803 | 792 | ||||
| 772 | 758 | 774 | 760 | 795 | 795 | ν3 | ||
| 747 | 746 | 767 | ||||||
| 737 | 746 | 760 | ||||||
| 680 | 682 | 682 | ||||||
| 474 | 455 | |||||||
| 417 | 417 | |||||||
| 385 | 386 | 386 | 360 | 371 | ||||
| 386 | 353 | 385 | 352 | 383 | 352 | 346 | ν2 | |
| 362 | 364 | 332 | ||||||
| 326 | 327 | 327 | ||||||
| 316 | 300 | 300 | 325 | 324 | ||||
| 320 | ν4 | |||||||
| 320 | 284 | 322 | 286 | 286 | 292 | |||
| ν2 | ||||||||
| 210 | 210 | |||||||
| 227 | 229 | R | ||||||
| 187 | ||||||||
| 189 | ||||||||
| 176 | 154 | Т | ||||||
| 154 | 157 | |||||||
| 100 | 139 | 143 | R | |||||
| 125 | 136 | R | ||||||
| R | ||||||||
| 107 | ||||||||
| 76 | 105 | Т | ||||||
| 79 | ||||||||
Представленные данные свидетельствуют о близости колебательных спектров BaMoO4 и KBaGd(MoO4)3, KBaSm(MoO4)3, α-KSm(MoO4)2, что позволяет дать удовлетворительную интерпретацию. Имеющиеся различия объяснимы изменениями в межатомных расстояниях и, как следствие, в энергиях связей Mo–O при гетеровалентном изоморфном замещении в катионных позициях. Так, границы области частот валентных колебаний групп MoO4 заметно расширяются как в высокочастотную, так и в низкочастотную стороны, а число измеренных в этой области частот втрое больше, чем в спектре BaMoO4. Увеличение числа полос связано с понижением симметрии групп MoO4, полным снятием вырождения трижды вырожденных колебаний и проявлением резонансного взаимодействия колебаний трансляционно-неэквивалентных групп MoO4.
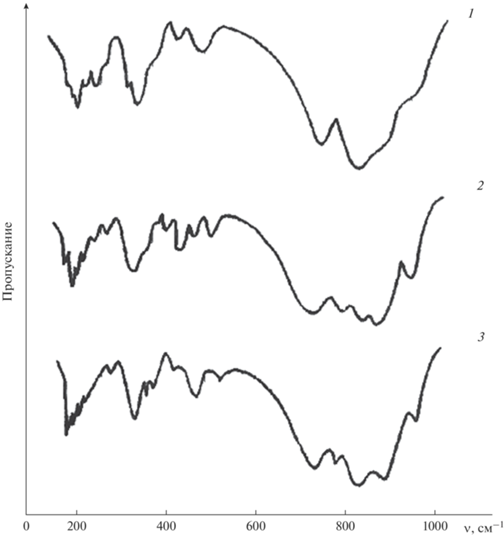
В измеренных спектрах увеличивается число либрационных колебаний MoO4-групп, активных в ИК-спектрах. Их частоты практически не меняются по ряду исследованных соединений и близки соответствующим частотам ВaMoO4. Число наблюдаемых полос трансляционных колебаний отвечает предполагаемому теорией. Соответствующие частоты в ряде случаев претерпевают закономерные изменения в ходе замещения катионов. Полученные данные свидетельствуют о том, что в трансляционных колебаниях KBaGd(MoO4)3, KBaSm(MoO4)3, α-KSm(MoO4)2 в равной степени участвуют все катионы (рис. 4). Имеющее место понижение симметрии кристаллической решетки при гетеровалентном замещении катионов в структуре шеелита определяется искажениями молибден-кислородных тетраэдров.
Образцы люминофоров KBaGd0.97Er0.01Yb0.02-(MoO4)3, KBaGd0.95Er0.01Yb0.04(MoO4), KBaGd0.90Er0.01-Yb0.09(MoO4)3 обладают способностью преобразовывать возбуждающее ИК-излучение в видимый свет (рис. 5). Ап-конверсионной люминесценцией принято называть люминесценцию, которая приводит к образованию кванта света с большей энергией, чем энергия кванта возбуждения [11]. Ап-конверсионная люминесценция в редкоземельных ионах возникает как в результате процессов, протекающих внутри одного иона, так и благодаря кооперативным межионным взаимодействиям с суммированием энергии.
Рис. 5.
Спектры люминесценции образцов люминофора KBaGd(MoO4)3:Er3+/Yb3+ с разной концентрацией ионов активаторов: KBaGd0.97Er0.01Yb0.02(MoO4)3 (1), KBaGd0.95Er0.01Yb0.04(MoO4) (2), KBaGd0.90Er0.01Yb0.09(MoO4)3 (3) (λвозб = 977 нм).
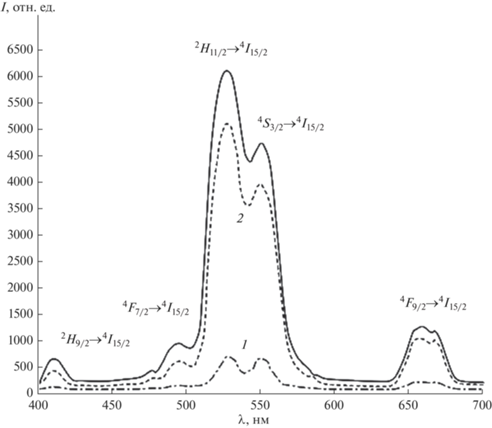
Ионы иттербия-донора обладают высоким эффективным сечением поглощения в ИК-области. Энергетические состояния иона эрбия акцептора обладают длительным временем жизни, поэтому ион-донор может безызлучательно передать на долгоживущее состояние акцептора сразу несколько поглощенных фотонов, что приведет к увеличению энергии возбужденного метастабильного состояния и, соответственно, уменьшению длины волны люминесценции KBaGd(MoO4)3:Er3+/Yb3+ [7–13, 17, 18]. Происхождение наблюдаемых полос при возбуждении (λвозб = 977 нм) в спектрах ап-конверсионной люминесценции может быть объяснено следующим образом.
После двухстадийного последовательного возбуждения ионов Er3+ до уровня 4F7/2 в результате безызлучательных релаксаций происходит заселение возбужденных уровней 2Н11/2, 4S3/2, 4F9/2, 4I9/2, что приводит к ап-конверсионной люминесценции в области 400–700 нм [7–13]. Спектр люминесценции обладает сильной полосой излучения при 525 нм, полосой средней интенсивности при 550 нм в зеленой области и двумя слабыми полосами излучения при 655 нм в красной области спектра. Полосы излучения при 525 и 550 нм в зеленой области спектра соответствуют переходам 2H11/2 → 4I15/2 и 4S3/2 → 4I15/2 в ионах Er3+, а излучение при 655 нм в красной области спектра связано с переходом 4F9/2 → 4I15/2. Полоса при 490 нм соответствует переходу 4F7/2 → 4I15/2. Полоса излучения при 410 нм обусловлена переходом 2H9/2 → 4I15/2.
Ионы-активаторы Er3+ являются центрами люминесценции люминофора, а сенсибилизирующее действие ионов Yb3+ увеличивает интенсивность ап-конверсионной люминесценции благодаря эффективной передаче энергии от Yb3+ к Er3+ и более высокому коэффициенту поглощения иттербия по сравнению с эрбием. Механизмом возбуждения 2H9/2-уровня может быть перенос энергии от возбужденного состояния Yb3+ на уровень 4F9/2 иона Er3+, поскольку разность энергий между уровнями 4F9/2 и 2H9/2 близка к энергии возбужденного иона иттербия [8–11]. Вследствие низкой заселенности уровня 4F9/2 наиболее вероятным каналом возбуждения является заселение вышележащих уровней из более заселенного 4S3/2-уровня через перенос энергии от иона Yb3+ с последующим превращением этих высоко лежащих уровней в 2H9/2 [8–13]. При переходе с высоко лежащих уровней может происходить видимая люминесценция. Более высокая интенсивность обусловлена отношением концентраций ионов Yb3+ : Er3+, равным 9 : 1 (рис. 5, спектр 3), другие соотношения концентраций ионов иттербия и эрбия являются неоптимальными. Высокое содержание ионов иттербия и низкое содержание ионов эрбия способствуют повышению интенсивности ап-конверсионной люминесценции, что обусловлено эффективным переносом энергии от иона иттербия к иону эрбия. Характер спектров связан с влиянием кристаллической решетки матрицы на штарковскую структуру основного и возбужденного уровней ионов-активаторов. Экспериментальные значения для энергетического выхода (Ben) составляют: для KBaGd0.97Er0.01Yb0.02(MoO4)3 – 0.14%, KBaGd0.95Er0.01Yb0.04(MoO4)3 – 0.19%, KBaGd0.90Er0.01Yb0.09(MoO4)3 – 0.37%. Времена жизни ап-конверсионной люминесценции ионов Er3+ в люминофоре с максимальным значением Ben = 0.37% при переходах 2H11/2 → 4I15/2 и 4S3/2 → 4I15/2 (зеленая область спектра) и 4F9/2 → 4I15/2 (красная область спектра) составили 46 ± 5 и 18 ± 3 мкс.
ЗАКЛЮЧЕНИЕ
Изучены фазовые равновесия в субсолидусной области системы K2MoO4–BaMoO4–Gd2(MoO4)3 по разрезам в интервале температур 450–800°С. Синтезирован тройной молибдат KBaGd(MoO4)3, кристаллизующийся в моноклинной сингонии (пр. гр. P21/n, Z = 9). Проведена триангуляция системы при 800°С. Получен ап-конверсионный люминофор на основе тройного молибдата, активированного ионами эрбия и иттербия KBaGd(MoO4)3:Er3+/Yb3+ при различном соотношении концентраций ионов активаторов.
Оптимизировано соотношение концентраций ионов эрбия и иттербия, высокая интенсивность обусловлена отношением концентраций ионов Yb3+ : Er3+, равным 9 : 1, другие соотношения являются неоптимальными. Люминофор KBaGd(MoO4)3:Er3+/Yb3+ может найти применение в лазерах, в преобразователях ИК-излучения в видимое, в цветных дисплеях, в биомедицинской диагностике, в оптической связи.
Список литературы
Трунов В.К., Ефремов В.А., Великодный Ю.А. Кристаллохимия и свойства двойных молибдатов и вольфраматов. Л.: Наука, 1986. 173 с.
Morozov V., Arakcheeva A., Redkin V. et al. Na2/7Gd4/7MoO4: a Modulated Scheelite-Type Structure and Condactivity Properties // Inorg. Chem. 2012. V. 51. № 9. P. 5313–5324. https://doi.org/10.1021/ic300221m
Раскина М.В., Морозов В.А., Павленко А.В. и др. Структура и люминесцентные свойства твердых растворов Sm2 – xEux(MoO4)3 // Журн. неорган. химии. 2015. Т. 60. № 1. С. 89–97. https://doi.org/10.7868/S0044457X15010122
Золотова Е.С., Рахманова М.И., Соколов В.В., Усков Е.М. Влияние висмута и кальция на интенсивность люминесцеции люминофора NaY1 – xEux(MoO4)2 // Неорган. материалы. 2011. Т. 47. № 11. С. 1368–1371.
Каминсий А.А. Спектроскопия кристаллов. М.: Наука, 1975. 255 с.
Кожевникова Н.М., Мохосоев М.В. Тройные молибдаты. Улан-Удэ: Изд-во Бурятского госуниверситета, 2000. 298 с.
Манаширов О.Я., Сатаров Д.К., Смирнов В.Б. и др. Состояние и перспективы разработок антистоксовых люминофоров для визуализации ИК-излучений в области 0.8–1.3 мкм // Неорган. материалы. 1993. Т. 29. № 10. С. 1322–1325.
Овсянкин В.В., Феофилов П.П. Кооперативная сенсибилизация люминесценции в кристаллах, активированных редкоземельными ионами // Письма в ЖЭТФ.1966. Т. 4. Вып. 11. С. 471–474.
Kuznetsov S., Ermakova Yu., Voronov V. et al. Up-conversion Quantum Yields of SrF2:Yb3+, Er3+Sub-micron Particles Prepared by Precipitation in Water Solution // J. Mater. Chem. C. 2018. V. 6. № 3. P. 598–604.
Озель Ф.Е. Материалы и устройства, использующие антистоксовые люминофоры с переносом энергии // ТИИЭР. 1973. Т. 61. № 6. С. 87–120.
Auzel F. Upconversion and Anti-Stokes Processes with f and d Ions in Solids // Chem. Rev. 2004. V. 104. № 1. P. 139–173.
Lyapin A.A., Ermakov A.S., Kuznetsov S.V. et al. Upconversion Luminescence of CaF2–SrF2–ErF3 Single Crystals upon 1.5 μm Laser Excitation // J. Phys.: Conf. Ser. 2019. V. 1410. 012086. https://doi.org/10.1088/1742-6596/1410/1/012086
Казарян А.К., Тимофеев Ю.Р., Фок М.В. Антистоксовое преобразование излучения в люминофорах с редкоземельными ионами // Тр. ФИАН. 1986. Т. 175. С. 4–65.
Евдокимов А.А., Ефремов В.А., Трунов В.К. и др. Соединения редкоземельных элементов. Молибдаты, вольфраматы. М.: Наука, 1991. 267 с.
Kozhevnikova N.M., Korsun V.P., Mursakhanova I.I., Mokhosoev M.V. Luminescence Materials Based on Re Molybdates // J. Rare Earth. 1991. V. 2. P. 845–849.
Jiang Y., Liu Y., Liu G., Dong X., Wang J., Yu W., Dong Q. Surfactant-Assisted Hydrothermal Synthesis of Octahedral Structured NaGd(MoO4)2:Eu3+/Tb3+ and Tunable Photoluminescent Properties // Opt. Mater. 2014. V. 36. P. 1865–1870. https://doi.org/10.1016/j.optmat.2014.03.043
Георгобиани А.Н., Грузинцев А.Н., Бартту К., Беналлул П. Инфракрасная люминесценция соединений Y2O2S:Er3+ и Y2O3:Er3+ // Неорган. материалы. 2004. Т. 40. № 8. С. 963–968.
Грузинцев А.Н. Антистоксовая люминесценция Y2O3:Er3+ // Неорган. материалы. 2014. Т. 50. № 1. С. 64–69. https://doi.org/10.7868/S0002337X14010084
Петров К.И., Полозникова М.Э., Шарипов Х.Т., Фомичев В.В. Колебательные спектры молибдатов и вольфраматов. Ташкент: ФАН, 1990. 135 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы