Неорганические материалы, 2022, T. 58, № 4, стр. 437-441
Синтез нанокомпозитов SrSnO3/SnO2 методом термического разложения прекурсора
А. В. Логинов 1, 2, *, А. И. Апарнев 1, Н. Ф. Уваров 1, 2
1 Новосибирский государственный технический университет
630073 Новосибирск, пр. К. Маркса, 20, Россия
2 Институт химии твердого тела и механохимии Российской академии наук
630128 Новосибирск, ул. Кутателадзе, 18, Россия
* E-mail: loginov@corp.nstu.ru
Поступила в редакцию 13.01.2022
После доработки 31.01.2022
Принята к публикации 01.02.2022
- EDN: URZAME
- DOI: 10.31857/S0002337X22040091
Аннотация
Из солянокислых растворов стронция и олова(IV) добавлением аммиака до рН 10 получен двойной гидроксид олова(IV)-стронция SrSn(OH)6, смешанный с аморфными гидратными формами диоксида олова. Методами дифференциального термического, рентгенофазового анализа и сканирующей электронной микроскопии исследованы процесс термолиза полученного образца и фазовый состав продуктов разложения. Показано, что основные стадии дегидратации завершаются при температуре около 350°С и в результате термолиза образуется рентгеноаморфный продукт, который при температуре выше 650°С переходит в нанокомпозит, состоящий из кристаллической фазы станната стронция и диоксида олова. Методом импедансометрии определены значения ионной проводимости композиционных твердых электролитов, полученных при добавлении синтезированных нанокомпозитов в ионные соединения.
ВВЕДЕНИЕ
В последние годы материалы на основе диоксида олова SnO2, допированные различными переходными и щелочноземельными металлами, вызывают повышенный интерес исследователей, что связано с множеством перспективных областей их применения. В частности, станнаты щелочноземельных металлов используются как компоненты керамических диэлектрических материалов, термостойких конденсаторов и датчиков различных газов [1–5]. Наностержни SrSnO3, полученные термолизом и гидротермальной обработкой нанопроволок из SrSn(OH)6, применяются в качестве анодного материала в литий-ионных аккумуляторах, т. к. они обладают разрядной емкостью до 200 мАч/г и улучшенной циклируемостью [6–11]. Материалы на основе SrSnO3 проявляют люминесцентные и фотокаталитические свойства, а также на его основе синтезируются керамические пигменты [12–15]. Одним из наиболее перспективных методов получения станната стронция является разложение прекурсора – смешанного гидроксида стронция и олова(IV) SrSn(OH)6.
Цель работы – синтез и исследование нанокомпозитов SrSnO3/SnO2, полученных термическим разложением двойного гидроксида SrSn(OH)6, синтезированного из растворов, содержащих хлориды олова(IV) и стронция, а также возможности использования композитов на основе SrSnO3/SnO2 в качестве оксидных гетерогенных добавок для получения композиционных твердых электролитов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовались следующие реактивы: SrCl2 · 6Н2О (ГОСТ 4140-73, квалификация “ч.”), SnCl4 · 5H2О (ТУ 2623-02-40897595-99, квалификация “ч. д. а.”), NH4OH (ГОСТ 24147-80, квалификация “ос. ч.”) (все производства ОАО “Реактив”). Для приготовления растворов использовалась дистиллированная вода, полученная с помощью системы очистки Millipore Direct-Q UV (Millipore Corp.).
Смешанный гидроксид олова-стронция состава SrSn(OH)6 был синтезирован осаждением из 1 М растворов SrCl2 · 6Н2О и SnCl4 · 5H2О раствором аммиака при рН ~ 10.5. При этом раствор аммиака добавляли с постоянной скоростью 2.5 мл/мин (дозирование реагента осуществлялось перистальтическим насосом ЛАБ-НП-1) к смеси солянокислых растворов стронция и олова(IV) при интенсивном перемешивании в течение 4 ч при комнатной температуре. Полученные осадки отделялись центрифугированием, промывались дистиллированной водой до достижения отрицательной качественной реакции на присутствие ионов Cl– в растворе и сушились при 100–110°С в течение 6 ч. Далее проводили термическую обработку порошков в муфельной печи SNOL 6,7/1300 при заданных температурах 300, 500 и 700°С в течение 4 ч.
Микроструктуру и рентгенофазовый анализ (РФА) порошков изучали методом рентгеновской дифракции на приборах Bruker D8 Advance и ДРОН-3М с использованием CuKα-излучения. Идентификацию образующихся в системе фаз проводили с помощью программы Crystallographica Search-Match, Version 2.1 и базы данных PDF4. Средний размер кристаллитов фаз оценивали по уширению рефлексов на дифрактограммах с помощью формулы Шеррера
где d – средний размер кристаллов, λ – длина волны рентгеновского излучения (1.54051 Å), β – ширина пика на половине высоты, θ – угол дифракционного пика, k = 0.9. Термический анализ высушенных порошков проводили на синхронном термоанализаторе NETZSCH Jupiter 449С STA, сопряженном с масс-спектрометром QMS 403C Aëolos (TG-QMS), в потоке аргона при температурах в диапазоне 20–1000°С со скоростью нагрева 10°С/мин. Исследования методом сканирующей электронной микроскопии (СЭМ) проведены на приборе HIТACHI TM1000, параллельно исследовался элементный состав образца с помощью энергодисперсионного анализатора ТМ-1000 Oxsford Instrument.Ионную проводимость измеряли на таблетированных образцах с серебряными электродами по двухэлектродной схеме в вакууме (5 × 10–2 мм рт. ст.) в интервале температур от 40 до 200°C на переменном токе с помощью прецизионного измерителя электрических параметров Hewlett Packard НР 4284А в области частот 20 Гц–1 МГц.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
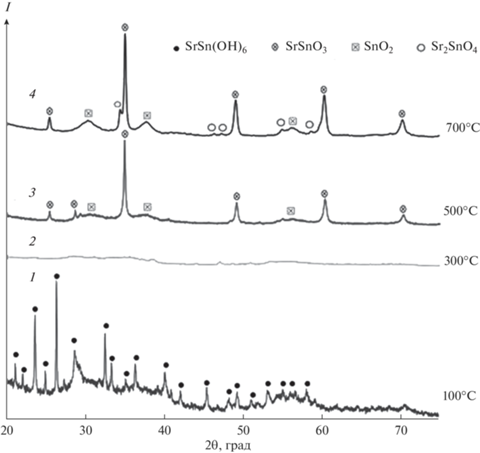
По данным РФА в свежеосажденном образце присутствует только одна кристаллическая фаза – смешанный гидроксид стронция и олова(IV) состава SrSn(OH)6 (рис. 1, дифрактограмма 1).
Процесс образования смешного гидроксида описывается уравнением реакции
(1)
$\begin{gathered} {\text{SrC}}{{{\text{l}}}_{2}} + {\text{SnC}}{{{\text{l}}}_{4}} + 6{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{OH}} \to \\ \to \,\,{\text{SrSn(OH}}{{)}_{6}} + 6{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{Cl}}. \\ \end{gathered} $Параллельно протекает реакция гидролиза хлорида олова в присутствии гидроксида аммония
(2)
$\begin{gathered} {\text{SnC}}{{{\text{l}}}_{4}} + х{{{\text{Н}}}_{{\text{2}}}}{\text{О}} + 4{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{OH}} \to \\ \to \,\,{\text{Sn}}{{{\text{О}}}_{2}}\cdotх{{{\text{Н}}}_{{\text{2}}}}{\text{О}} + 4{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{Cl}}, \\ \end{gathered} $в результате которой в образце образуется примесь гидратных форм диоксида олова.
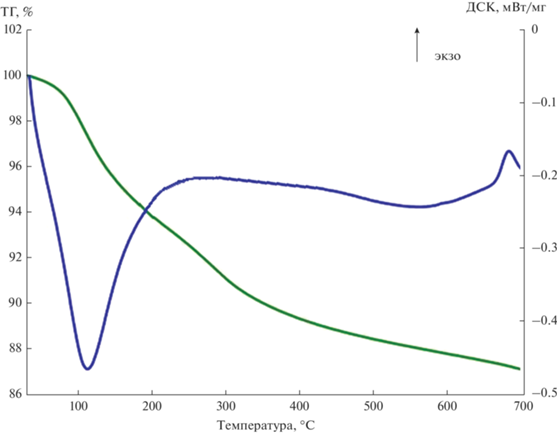
По данным дифференциальной сканирующей калориметрии (ДСК) и термогравиметрического (ТГ) анализа исходного образца (рис. 2) при нагревании на воздухе в интервале температур 100–350°C наблюдаются эндотермические эффекты, связанные с потерей массы в результате дегидратации двойного гидроксида SrSn(OH)6 и гидрата SnО2 · хН2О в соответствии с уравнениями реакций
(3)
${\text{SrSn}}{{\left( {{\text{OH}}} \right)}_{6}} \to {\text{SrSn}}{{{\text{O}}}_{3}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}},$(4)
${\text{Sn}}{{{\text{О}}}_{2}}\cdotх{{{\text{Н}}}_{{\text{2}}}}{\text{О}} \to {\text{Sn}}{{{\text{O}}}_{2}} + х{{{\text{H}}}_{{\text{2}}}}{\text{O}}.$По данным РФА, образец, полученный прогревом смешанного гидроксида при 300°С в течение 4 ч, представляет собой рентгеноаморфный продукт (рис. 1, дифрактограмма 2). В процессе нагревания образца при 500°С происходит кристаллизация – переход аморфной фазы в нанокомпозит, представляющий собой смесь нанокристаллических фаз SrSnO3 и SnO2 (рис. 1, дифрактограмма 3). Полученный станнат стронция имеет структуру перовскита, диоксид олова – касситерита, параметры их кристаллических решеток согласуются с данными PDF4 (Cards 74-1298 и 41-14455). При последующем прокаливании при 680–700°С наблюдается экзотермический эффект, который указывает на протекание процесса разложения SrSnO3 с образованием фазы SnO2 и слабо окристаллизованных частиц фазы Sr2SnO4 со структурой шпинели (Card 24-1241, PDF4) (рис. 1, дифрактограмма 4).
На СЭМ-изображениях свежеосажденного образца отчетливо видны агрегированные частицы смешанного гидроксида SrSn(OH)6 стержнеобразной формы размером до 3 мкм с высокой степенью агломерации (рис. 3а). После прокаливания до температуры 700°С частицы сохраняли стержнеобразную форму (рис. 3б, 3в). Размер стержней после прокаливания достигал 6–7 мкм, однако их диаметр слегка уменьшался, а частицы становились менее агрегированными. При проведении элементного анализа было установлено, что содержание олова на поверхности образца SrSnO3, полученного после термообработки, значительно превосходит содержание стронция (72% Sn, 28% Sr). Можно предположить, что в полученных композитах поверхность относительно крупных частиц SrSnO3 покрыта тонким слоем мелких кристаллитов диоксида олова. Это предположение подтверждается оценкой размера частиц с помощью уравнения Шеррера. В нанокомпозитах, прогретых при 700°С, размер частиц SrSnO3 и SnO2 составляет 85 и 7 нм соответственно.
Рис. 3.
СЭМ-снимки свежеосажденного SrSn(OH)6 (а), после прокаливания при 700°С агрегатов (б) и частиц (в).

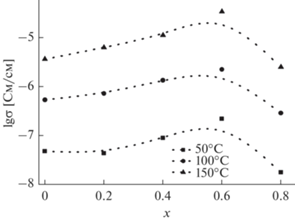
Порошки нанокомпозита SrSnO3/SnO2 были испытаны в качестве оксидных гетерогенных добавок для получения композиционных твердых электролитов на основе ионных солей. Концентрационная зависимость проводимости композитов (1 – x)CsNO2 · x(SrSnO3/SnO2) представлена на рис. 4. При увеличении концентрации добавки SrSnO3/SnO2 проводимость нитрита цезия увеличивается и достигает максимума при 60%. При дальнейшем увеличении количества добавляемого нанокомпозита SrSnO3/SnO2 наблюдается уменьшение ионной проводимости. Наличие тонкого слоя нанокристаллического диоксида олова на поверхности частиц SrSnO3 оказывает дополнительное влияние на рост проводимости за счет увеличения площади контакта фаз ионный проводник/оксид. Характер изменения проводимости типичен для композиционных твердых электролитов, ионная проводимость которых осуществляется за счет границ раздела ионная соль/оксид.
ЗАКЛЮЧЕНИЕ
Результаты исследования показали, что при осаждении смешанного гидроксида олова(IV) и стронция из солянокислых растворов получен гексагидроксостаннат(IV) стронция SrSn(OH)6 c примесью гидратных форм диоксида олова. Смешанный гидроксид SrSn(OH)6 стабилен в интервале температур 100–300°С и при термолизе образует аморфную фазу. При температуре 500°С аморфная фаза рекристаллизуется с образованием нанокомпозитов SrSnO3/SnO2. В результате термического разложения полученных образцов образуются агрегированные частицы станната стронция со стержневой морфологией размером до 7 мкм, поверхность которых покрыта мелкими частицами диоксида олова. При нагревании выше 680–700°С станнат стронция SrSnO3 частично разлагается с образованием фаз Sr2SnO4 и SnO2, т.е. образуется трехфазный нанокомпозит SrSnO3/Sr2SnO4/SnO2.
Исследована ионная проводимость композиционных твердых электролитов на основе нитрита цезия с добавкой нанокомпозита SrSnO3/SnO2, полученного термическим разложением SrSn(OH)6. Композиты состава CsNO2–(SrSnO3/SnO2) обладают повышенной ионной проводимостью, превышающей проводимость чистого нитрита цезия при 200°С.
Список литературы
Yanpei L., Jing C., Jiawen L., Yu S., Xiaofang L., Danzhen L. Hydroxide SrSn(OH)6: A New Photocatalyst for Degradation of Benzene and Rhodamine B // Appl. Catal., B. 2016. V. 182. P. 533–540. https://doi.org/10.1016/j.apcatb.2015.09.051
Stanulis A., Sakirzanovas S., Van Bael M., Kareiva A. Sol–gel (Combustion) Synthesis and Characterization of Different Alkaline Earth Metal (Ca, Sr, Ba) Stannates // J. Sol-Gel Sci. Technol. 2012. V. 64. P. 643–652. https://doi.org/10.1007/s10971-012-2896-2
Kumar A., Khan B., Yadav V., Dixit A., Kumar U., Singh M. Rietveld Refinement, Optical, Dielectric and ac Conductivity Studies of Ba-Doped SrSnO3 // J. Mater. Sci. – Mater. Electron. 2020. V. 31. P. 16838–16848. https://doi.org/10.1007/s10854-020-04240-7
Cerda J., Arbiol J., Dezanneau G., Diaz R., Morante J.R. Perovskite-Type BaSnO3 Powders for High Temperature Gas Sensor Applications // Sens. Actuators, B. 2002. V. 84. № 1. P. 21–25.
Marikutsa A., Rumyantseva M., Baranchikov A., Gaskov A. Nanocrystalline BaSnO3 as an Alternative Gas Sensor Material: Surface Reactivity and High Sensitivity to SO2 // Mater. Sci. Eng. 2015. V. 8. № 9. P. 6437–6454. https://doi.org/10.3390/ma8095311
Kamimura S., Yamada H., Xu C. Strong Reddish-Orange Light Emission from Stress-Activated Srn + 1SnnO3n + 1:Sm3+ (n = 1, 2, ∞) with Perovskite-Related Structures // Appl. Phys. Lett. 2012. V. 101. № 9. P. 091113–091115. https://doi.org/10.1063/1.4749807
Zulueta Y.A., Mut R., Kaya S., Dawson J.A., Nguyen M.T. Strontium Stannate as an Alternative Anode Material for Li-Ion Batteries // J. Phys. Chem. C. 2021. V. 125. № 27. P. 14947–14956. https://doi.org/10.1021/acs.jpcc.1c02652
Alammar T., Hamm I., Grasmik V., Wark M., Mudring A. Microwave-Assisted Synthesis of Perovskite SrSnO3 Nanocrystals in Ionic Liquids for Photocatalytic Applications // Inorg. Chem. 2017. V. 56. № 12. P. 6920. https://doi.org/10.1021/acs.inorgchem.7b00279
Loginov A.V., Aparnev A.I., Uvarov N.F. Study of Thermal Decomposition of Hexahydroxostannates(IV) MSn(OH)6, (M = Mg, Sr, Ca) // Mater. Today. 2020. V. 25. № 3. P. 477–479. https://doi.org/10.1016/j.matpr.2019.12.242
Stanulis A., Selskis A., Ramanauskas R., Beganskiene A., Kareiva A. Low temperature Synthesis and Characterization of Strontium Stannate-Titanate Ceramics // Mater. Chem. Phys. 2011. V. 130. № 3. P. 1246–1250. https://doi.org/10.1016/j.matchemphys.2011.09.005
Зима Т.М., Малыгин И.В. Гидротермальный синтез и исследование наноструктурированного диоксида олова, легированного кобальтом // Неорган. материалы. 2019. Т. 55. № 3. С. 290–297. https://doi.org/10.1134/S0002337X19020155
Yang D.Q., Zhang C., Dong L.M., Hou X.D., Zheng W.K., Xu J.Z., Ma H. Y. Synthesis and Properties of SrSn(OH)6 Nanorods and Their Flame Retardancy and Smoke Suppression Effects on Epoxy Resin // J. Coat. Technol. Res. 2019. V. 16. № 6. P. 1715–1725. https://doi.org/10.1007/s11998-019-00254-x
Hu X., Lv G., Jia Z., Jiang J., Xiao T., Yuan M., Tang Y. A General Sonochemical Approach to Rapid Synthesis of 1D Single-Crystalline MSn(OH)6 (M = Ba, Ca, Sr) Nanostructures // Appl. Surf. Sci. 2011. V. 257. № 21. P. 9008–9013. https://doi.org/10.1016/j.apsusc.2011.05.088
Dohnalova Z., Gorodylova N., Sulcova P., Vlcek M. Synthesis and Characterization of Terbium-Doped SrSnO3 Pigments // Ceram. Int. 2014. V. 40. № 8B. P. 12637–12645. https://doi.org/10.1016/j.ceramint.2014.04.110
Agafonov A.V., Grishina E.P. Nanocomposites of Inorganic Oxides with Ionic Liquids. Synthesis, Properties, Application (Review) // Russ. J. Inorg. Chem. 2019. V. 64. № 13. P. 1641–1648. https://doi.org/10.1134/S0036023619130023
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы