Журнал неорганической химии, 2019, T. 64, № 1, стр. 93-98
Фазовые равновесия в системе SrS−In2S3А. В. Кертман
1 Тюменский государственный университет
625003 Тюмень, ул. Семакова, 10, Россия
* E-mail: akertman@utmn.ru
Поступила в редакцию 05.02.2018
После доработки 04.07.2018
Принята к публикации 07.05.2018
Аннотация
Установлено, что система SrS−In2S3 эвтектического типа с инконгруэнтно плавящимся соединением состава SrIn2S4 и ограниченными областями твердых растворов на основе полиморфных модификаций In2S3. Соединение SrIn2S4 кристаллизуется в ромбической сингонии (пр. гр. Fddd) с параметрами элементарной ячейки а = 2.090, b = 2.113, c = 1.302 нм. Температура инконгруэнтного плавления SrIn2S4 составляет 1220 K, микротвердость Н = 2650 МПа. Состав эвтектики – 73 мол. % In2S3, tпл = 1170 K. Растворимость SrS в α-In2S3 при 1070 K достигает 6 мол. % SrS.
ВВЕДЕНИЕ
Сульфиды состава AIn2S4 (A – щелочноземельный металл), образующиеся в системах AS–In2S3, в последние годы вызывают повышенный интерес, так как обладают специфическими (оптическими и электрофизическими) свойствами и используются в качестве материалов инфракрасной и нелинейной оптики [1, 2].
Ранее [1, 3] были изучены фазовые равновесия в системе SrS−In2S3 в концентрационном диапазоне 50–100 мол. % In2S3. В литературе имеются сведения о том, что в системе при эквимолярном соотношении исходных сульфидов образуется соединение состава SrIn2S4, кристаллизующееся в ромбической сингонии с параметрами элементарной ячейки (э. я.): а = 2.0901(7), b = 2.1120(7), c = 1.3020(6) нм, V = 5.7474 нм3, Z = 32, пр. гр. Fddd [3]. По данным [1], соединение SrIn2S4 плавится конгруэнтно при температуре 1343 K, между фазами SrIn2S4 и In2S3 образуется эвтектика состава 73 мол. % In2S3 с температурой плавления 1223 K. Сульфид стронция SrS плавится конгруэнтно при 2590 K, кристаллизуется в кубической сингонии типа NaCl с параметром э. я. а = 0.6015 нм, пр. гр. Fm3m, микротвердость Н = 2070 МПа [4]. Температура конгруэнтного плавления In2S3, по данным разных авторов, составляет 1360 [5] и 1370 K [6].
Несмотря на многочисленные исследования, фазовая диаграмма системы In–S характеризуется противоречивой информацией по общему количеству фаз, их стехиометрии и полиморфизму [7–14].
Авторы [7, 8] указывают на низкотемпературную модификацию α-In2S3, кристаллизующуюся в кубической сингонии типа сфалерита с параметром э. я. а = 0.5360 нм, которая при 573 K переходит в β-модификацию тетрагональной сингонии с параметрами э. я. а = 0.762 и с = 3.232 нм (пр. гp. I41/amd), сохраняющуюся до 1023 K.
Согласно [9–11], In2S3 существует в низкотемпературной модификации тетрагональной сингонии, которая при 688 K распадается по твердофазной реакции In2S3 ↔ L(на основе серы) + In3 – xS4. Высокотемпературная модификация In2S3 фиксируется от 1023 K до температуры плавления. Между этими модификациями существует широкогомогенное соединение In3–xS4 с кубической структурой типа шпинели, пр. гр. Fd$\overline 3 $m.
В [12–14] описаны три полиморфные модификации In2S3. Низкотемпературная β-модификация кристаллизуется в тетрагональной сингонии с параметрами э. я. а = 0.76231(4) и с = 3.2358(3) нм, пр. гp. I41/amd. При 717 ± 5 K β-In2S3 переходит в среднетемпературную модификацию α-In2S3 кубической сингонии с параметром э. я. а = = 1.08315(2) нм, пр. гр. Fd$\overline 3 $m. При температуре 1084 K наблюдается переход α-In2S3 в высокотемпературную модификацию γ-In2S3 тригональной (гексагональной, по данным [13, 14]) сингонии с параметрами э. я. а = 0.38656(2), с = 0.91569(5) нм, γ = 120°, пр. гp. P$\overline 3 $ml [12]. В настоящей работе использованы обозначения полиморфных модификаций In2S3, принятые в [12–14].
Цель настоящей работы – изучение равновесий и построение фазовой диаграммы системы SrS−In2S3.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для построения фазовой диаграммы системы SrS−In2S3 использовали бинарные сульфиды SrS и In2S3, синтезированные по стандартным методикам [15–17] и идентифицированные при помощи химического и рентгенофазового анализа. Cульфид стронция был получен восстановлением порошка SrSO4 марки “х. ч.” в потоке водорода при 1070 K в течение 15–20 ч. Сульфид индия In2S3 синтезировали из соответствующего оксида в потоке Н2S и СS2 при 1270 K. По данным рентгенофазового анализа (РФА), синтезированные сульфиды однофазны, в пределах погрешности химического анализа (±0.2 мас. %) имеют стехиометрический состав. Полученный In2S3 кристаллизуется в среднетемпературной α-модификации кубической сингонии (рис. 1а) с параметром э. я. а = = 1.0729 нм.
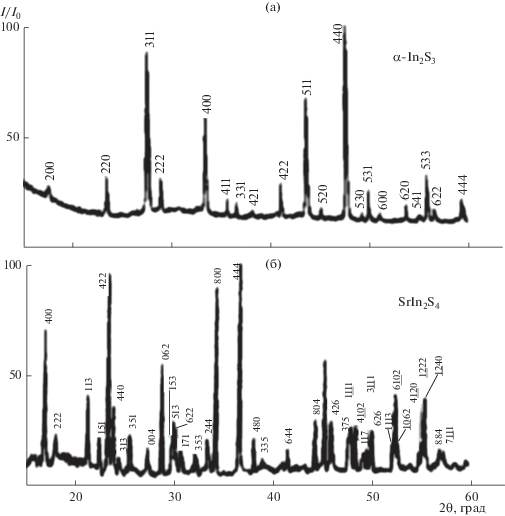
Рис. 1.
Рентгенограммы образцов состава: а – α-In2S3 (кубическая сингония), б – SrIn2S4 (ромбическая сингония), закаленных от 1070 K (дифрактометр ДРОН-3М, CuKα-излучение, Ni-фильтр).
В системе SrS−In2S3 было синтезировано 14 образцов различного химического состава. Литые образцы получали плавлением в парах серы соответствующих смесей порошков исходных сульфидов, находящихся в графитовых тиглях. Для получения гомогенных образцов использовали метод отжига и закалки. Гомогенизирующий отжиг плавленых образцов проводили в вакуумированных до остаточного давления 0.13–0.013 Па и запаянных кварцевых ампулах по двум изотермическим сечениям при температурах 1070 и 870 K. Время отжига составляло 700 и 1000 ч соответственно. Температуру отжига в муфельной печи задавали с точностью ±5 K при помощи терморегулятора “Термолюкс”. На основании результатов микроструктурного (МСА) и рентгенофазового анализа образцов в процессе отжига сделан вывод о достижении равновесного состояния образцов.
Дифференциальный термический анализ (ДТА) проводили на установке с термопарой ВР 5/20 при скорости нагрева образца 15 град/мин и нахождении пробы в вакуумированной и запаянной кварцевой ампуле с погрешностью 0.4% от измеряемой величины. Визуальный термический анализ (ВТА) выполняли на термопаре ПП-1 при нахождении пробы в молибденовом тигле. Погрешность определения температуры составляла 0.7% от измеряемой величины. Порошковые рентгенографические данные получены на рентгеновском дифрактометре ДРОН-3М в CuKα-излучении (Ni-фильтр). Параметры э. я. в отожженных образцах для веществ с кубической сингонией определены с точностью ±0.0001 нм, а с более низкой сингонией – с точностью ±0.001 нм с помощью программы POWDER2 и рентгенометрической картотеки PDF-2. МСА проводили на полированных и протравленных шлифах на металлографическом микроскопе МЕТАМ ЛВ 31, дюрометрический анализ (ДМА) – на микротвердомере ПМТ-3М методом Виккерса с погрешностью определения величины микротвердости 5–7%, нагрузка на индентор составляла 0.02 кг.
Графические построения выполнены с использованием программы Edstate 2D.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Фазовая диаграмма системы SrS−In2S3 (рис. 2) построена с применением комплекса методов физико-химического анализа и характеризуется наличием инконгруэнтно плавящегося соединения состава SrIn2S4, эвтектики между фазами SrIn2S4 и α-In2S3, ограниченной области твердого раствора на основе α-In2S3. Вследствие полиморфизма полуторного сульфида индия на представленной диаграмме возможно существование узких областей гомогенности на основе β- и γ-In2S3, которые выделены на диаграмме пунктирными линиями. Наличие полиморфных превращений β ↔ α и α ↔ γ также должно привести к реализации трехфазных равновесий, что позволяет считать данный разрез вблизи координаты In2S3 неквазибинарным.
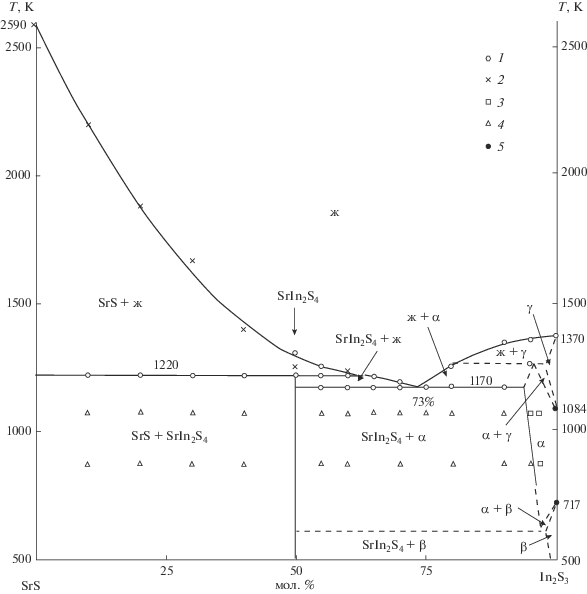
Рис. 2.
Фазовая диаграмма системы SrS–In2S3: 1 – результаты ДТА, 2 – ВТА; состояние образцов по результатам РФА, МСА, ДМА: 3 – однофазный, 4 – двухфазный, 5 – данные [12].
В системе SrS–In2S3 при эквимолярном соотношении исходных сульфидов образуется индивидуальное соединение состава SrIn2S4, что подтверждают данные рентгенофазового, микроструктурного и дюрометрического анализа. На рентгенограмме (рис. 1б) образцов состава 50 мол. % SrS−50 мол. % In2S3, отожженных и закаленных от 870 и 1070 K, наблюдаются рефлексы фазы SrIn2S4, кристаллизующейся в ромбической сингонии (пр. гр. Fddd) с параметрами а = 2.090, b = 2.113, с = 1.302 нм (рис. 3). Рефлексов фаз SrS и α-In2S3, а также непроиндицированных рефлексов не обнаружено. На микроструктуре образца данного состава наблюдали однородное светло-серое поле одной фазы без посторонних включений.
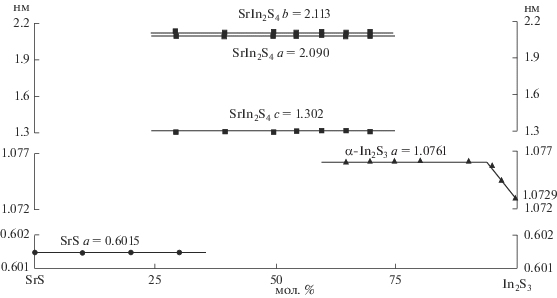
Рис. 3.
Зависимость параметров э. я. фаз от состава образцов в системе SrS–In2S3, закаленных от 1070 K. SrS – кубическая структура типа NaCl, SrIn2S4 – ромбическая структура типа EuGa2S4, α-In2S3 – кубическая структура типа шпинели.
В настоящей работе, в отличие [1], определен инконгруэнтный характер плавления соединения SrIn2S4, что подтверждается данными термического анализа, а также микроструктурой образцов из области существования фаз SrS и SrIn2S4. При МСА образца, содержащего 50 мол. % SrS и 50 мол. % In2S3, охлажденного из расплава, обнаружены микровключения фазы SrS, которые исчезают при гомогенизирующем отжиге. На шлифах образцов из области 10–40 мол. % In2S3, отожженных при 870 и 1070 K, присутствуют овальные зерна коричневого цвета фазы SrS (H = = 2070 МПа), расположенные в поле светло-серой фазы SrIn2S4 (Н = 2650 МПа, (рис. 4)). На термограммах указанных выше образцов фиксируются остановки нагрева, что, как установлено визуально при проведении ВТА, вызвано интенсивным плавлением основной части пробы. Температура начала протекания реакции инконгруэнтного плавления проб образцов, содержащих 10–50 мол. % In2S3, определенная по результатам ДТА, остается практически постоянной и составляет 1220 K. Все свойства (параметры э. я. и микротвердость) сопряженных фаз – SrS и SrIn2S4 – в области двухфазности остаются постоянными (рис. 3, 4).
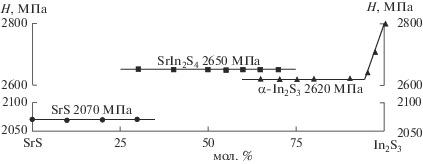
Рис. 4.
Зависимость состав–микротвердость образцов системы SrS–In2S3, закаленных от 1070 K. Нагрузка 0.020 кг.
Образование эвтектики между соединениями SrIn2S4 и α-In2S3 подтверждается характерным для эвтектических смесей видом дифференциальных термических кривых и микроструктурой образцов из области составов 55–90 мол. % In2S3. По данным МСА двухфазных образцов, состав эвтектической смеси приходится на 73 мол. % In2S3. Это подтверждается построением треугольника Таммана. Определенный нами состав эвтектической смеси в системе хорошо совпадает с литературными данными [1]. На шлифах образцов, содержащих от 55 до 70 мол. % In2S3, наблюдаются светло-серые зерна соединения SrIn2S4, микротвердость которых равна 2650 МПа (рис. 4), и эвтектика, представленная мелкодисперсной смесью кристаллов фаз, находящихся в равновесии. В образцах, содержащих 75–90 мол. % In2S3, присутствуют светло-желтые зерна твердого раствора на основе α-In2S3 (закалка от 1070 K), микротвердость которых равна 2620 МПа (рис. 4), и эвтектика. Пересечение кривых ликвидуса с линией эвтектики также происходит в интервале составов 72–74 мол. % In2S3. Температура плавления эвтектики определена на основании результатов, полученных методами ДТА и ВТА, и составляет 1170 K.
Вблизи координаты In2S3 при температурах закалки образцов обнаружена узкая область существования ограниченного твердого раствора на основе α-модификации полуторного сульфида индия. По данным МСА и РФА, при 1070 K в α-In2S3 растворяется до 6 мол. % SrS. При этом, согласно соотношению радиусов катионов r(Sr2+)/r(In3+) = 0.120/0.092 = 1.3 [18], с увеличением содержания SrS в α-In2S3 происходит закономерное увеличение параметров кубической э. я. α-In2S3 от а = 1.0729 до а = 1.0761 нм (ΔV = = +0.011 нм3) (рис. 3) и уменьшение микротвердости образцов от 2800 до 2630 МПа (ΔН = –180 МПа) (рис. 4) вследствие заполнения катионных вакансий в структуре α-In2S3. С понижением температуры растворимость SrS в α-In2S3 закономерно уменьшается и при 870 K составляет 4 мол. % SrS. Ограниченность твердого раствора подчиняется правилу Юм–Розери. Твердых растворов на основе β- и γ-In2S3 при указанных выше температурах отжига образцов не обнаружено. Для построения более точной картины фазовых равновесий вблизи координаты In2S3 и определения областей гомогенности на основе β- и γ-In2S3 требуются дополнительные исследования.
В системе также не обнаружено образования твердого раствора на основе SrS.
Ликвидус системы SrS−In2S3 состоит из трех ветвей первичной кристаллизации фаз SrS, SrIn2S4 и твердых растворов на основе α- и γ-In2S3 и построен по результатам методов ДТА и ВТА, а вблизи координаты SrS – по результатам ВТА. Температура ликвидуса определена методом ВТА. За данную величину принята температура полного плавления пробы. Экстраполяцией линии ликвидуса, нисходящей от координаты SrS, на экспериментальные данные определена фигуративная точка пересечения инконгруэнтной горизонтали с линией ликвидуса. В области концентраций 0–64 мол. % In2S3 линия ликвидуса соответствует первичному выделению кристаллов SrS, в интервале 64–73 мол. % In2S3 из расплава выделяются первичные кристаллы фазы SrIn2S4, а в области концентраций >73 мол. % In2S3 – кристаллы твердого раствора на основе In2S3.
Список литературы
Takizawa T., Kubo M., Hidaka C. // J. Cryst. Growth. 2005. V. 275. P. 433.
Moldovyan N.A. // Inorg. Mater. 1992. V. 23. № 3. P. 670.
Eisenmann B., Hofmann A. // Z. Kristallogr. 1991. V. 197. P. 167.
Кертман А.В., Краева Н.В. // Журн. неорган. химии. 2010. Т. 55. № 8. С. 1359. [Kertman A.V., Kraeva N.V. // Russ. J. Inorg. Chem. 2010. V. 55. № 8. P. 1283].
Stubbs M.X., Schule Y.A., Tornpson A.Y. et al. // J. Am. Chem. Soc. 1952. V. 74. P. 1441.
Кертман А.В. // Журн. неорган. химии. 2017. Т. 62. № 9. С. 1249. doi 10.7868/ S0044457X17090161 [Kertman A.V. // Russ. J. Inorg. Chem. 2017. V. 62. № 9. P. 1240. doi 10.1134/S003602361709008X].
Медведева 3.С. Халькогениды элементов III Б подгруппы периодической системы. М.: Наука, 1968. 216 с.
Steigmann G.A., Sutherland H.H., Goodyear J. // Acta Crystallogr. 1965. V. 19. P. 967.
Косяков А.В., Завражнов А.Ю., Наумов А.В. // Неорган. материалы. 2010. Т. 46. № 4. С. 398 [Kosyakov A.V., Zavrazhnov A.Yu., Naumov A.V. // Inorg. Mater. 2010. V. 46. № 4. P. 343].
Косяков А.В., Завражнов А.Ю., Наумов А.В., Сергеева А.В. // Вестник ВГУ. Серия: Химия, Биология, Фармация. 2009. № 2. С. 28.
Завражнов А.Ю., Наумов А.В., Аноров П.В. и др. // Неорган. материалы. 2006. Т. 42. № 12. С. 1420. [Zavrazhnov A.Yu., Naumov A.V., Anorov P.V. et al. // Inorg. Mater. 2006. V. 42. № 12. P. 1294].
Pistor P., Merino Alvarez J.M., Leon M. et al. // Acta Crystallogr. B. Struct. Sci. Cryst. Eng. Mater. 2016. V. 72. Pt. 3. P. 410. doi 10.1107/S2052520616007058
Li T., Zhang S., Meng S. et al. // Royal Soc. Chem. 2017. V. 7. P. 6457. doi 10.1039/c6ra28560k
Rodrigues-Hernandez P.E., Nieto-Zepeda K.E., Guillen-Cervantes A. et al. // Chalcogenide Letters. 2017. V. 14. № 8. P. 331.
Андреев О.В., Кертман А.В., Паршуков Н.Н. // Журн. неорган. химии. 1998. Т. 43. № 7. С. 1223 [Andreev O.V., Kertman A.V., Parshukov N.N. // Russ. J. Inorg. Chem. 1998. V. 43. № 7. P. 1127].
Русейкина А.В., Соловьев Л.А. // Журн. неорган. химии. 2016. Т. 61. № 4. С. 504. doi 10.7868/S0044457X16040164 [Ruseikina A.V., Solov’ev L.A. // Russ. J. Inorg. Chem. 2016. V. 61. № 4. P. 482. doi 10.1134/S0036023616040161].
Кертман А.В., Носов И.И., Андреев О.В. // Журн. неорган. химии. 2002. Т. 47. № 1. С. 132. [Kertman A.V., Nosov I.I., Andreev O.V. // Russ. J. Inorg. Chem. 2002. V. 47. № 1. P. 126].
Shannon R.D. // Acta Crystallogr. 1976. V. 32A. P. 751.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


