Журнал неорганической химии, 2019, T. 64, № 10, стр. 1031-1040
Синтез и строение моноядерных комплексов меди(II) с азагетероциклическими лигандами L (L = Bipy, BPA, Phen) и додекагидро-клозо-додекаборатным анионом [B12H12]2–
Е. А. Малинина 1, И. К. Кочнева 2, В. В. Авдеева 1, *, Л. В. Гоева 1, А. С. Кубасов 1, Н. Т. Кузнецов 1
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
2 Федеральная служба по интеллектуальной собственности, Федеральный институт промышленной собственности
125993 Москва, Бережковская наб., 30, корп. 1, Россия
* E-mail: avdeeva.varvara@mail.ru
Поступила в редакцию 01.04.2019
После доработки 16.04.2019
Принята к публикации 13.05.2019
Аннотация
Систематическое изучение реакций комплексообразования меди(I)/меди(II) с азагетероциклическими лигандами и кластерными анионами бора [BnHn]2– (n = 10, 12) свидетельствует о возможности синтеза моно-, би-, три-, тетраядерных и полимерных комплексных соединений меди(II). В настоящей работе изучены реакции комплексообразования меди(I) с анионом [B12H12]2– и азагетероциклическими лигандами L (L = Bipy, BPA) на воздухе в органических растворителях (CH3CN и DMF). В этих условиях происходит окисление меди(I) и в качестве конечных продуктов образуются моноядерные комплексы меди(II) с лигандами L и анионом [B12H12]2– различного состава и строения. Комплексы меди(II) получены также в системе медь(I)/серебро(I). Показано влияние условий синтеза (природа исходного клозо-додекабората, источник меди(I), наличие соединений серебра(I) в реакционном растворе) на состав и строение образующихся комплексов. Продукты реакций идентифицированы с помощью элементного и рентгеноструктурного анализа, а также ИК-спектроскопии. Методом РСА установлено строение комплексов [Ag(Bipy)2]NO3, [Cu(BPA)2Cl]Cl ⋅ DMF, [Cu(BPA)2Cl]2 ⋅ 2DMF, [Cu(BPA)2(DMF)2][B12H12] ⋅ DMF, [Cu(BPA)2][B12H12]]n и [Cu(Bipy)(DMF)4][B12H12] (CCDС № 1899332–1899337 соответственно).
ВВЕДЕНИЕ
Кластерные анионы бора [BnHn]2– (n = 10, 12) [1–3] образуют самостоятельный раздел химии бора. Изучение их свойств в процессах комплексообразования показывает, что в зависимости от условий проведения реакций, выбранного металла-комплексообразователя и лигандов кластерные анионы бора способны выступать в качестве внутрисферных лигандов [4–6], противоионов, а также участвовать в реакциях, сопровождающих комплексообразование с металлами [7, 8]: окислительно-восстановительных и реакциях замещения экзополиэдрических атомов водорода на различные функциональные группы.
Реакционная способность клозо-декаборатного аниона [B10H10]2– в реакциях комплексообразования меди(II) изучена достаточно подробно. Известно, что в реакциях комплексообразования в присутствии солей меди(II) анион [B10H10]2– участвует в окислительно-восстановительной реакции, приводя к восстановлению меди(II) до комплексов меди(I) [9]. Если в реакционном растворе присутствуют лиганды, экранирующие атом меди(II) от восстановительного действия кластерного аниона бора, то могут образоваться катионные комплексные соединения меди(II) с лигандами и клозо-декаборатным анионом в качестве противоиона [10–13]. Кроме того, реакционноспособный клозо-декаборатный анион в некоторых случаях приводит к получению замещенных производных [B10H9L]– с молекулой органического лиганда L в качестве заместителя [11, 12].
Поведение менее реакционноспособного аниона [B12H12]2– в реакциях комплексообразования меди(II) практически не изучено. В литературе имеются данные о синтезе моноядерных аквакомплексов меди(II), стабилизированных кластерным анионом бора [B12H12]2–, состава [Cu(H2O)5.5][B12H12] ⋅ ⋅ 2.5H2O и [Cu(H2O)6](H3O)2[B12H12]2 ⋅ 6H2O (смешанокатионный комплекс) [14]; комплексные соединения были получены при взаимодействии солей меди(II) c кислотой (H3O)2[B12H12]. Кроме того, описан синтез и строение полимерного комплекса меди(II) с аминогуанидином [Cu0.61H0.78Agu2][B12H12] [15]. Структура построена из комплекса [Cu(Agu)2[B12H12]]n и соли (HAgu)2[B12H12]n, так что это соединение можно рассматривать как результат изоморфного замещения ионов Н+ на ион Cu2+.
Впервые для кластерных анионов бора, например [B12H12]2–, удалось выделить трехъядерный комплекс меди(II) с 2,2'-бипиридилом состава [Cu3(Bipy)6(CO3)][B12H12]2 [16]. Комплекс получен в результате окислительно-восстановительной реакции при взаимодействии [Ag2[B12H12]] с CuCl в присутствии Bipy, показано его строение и описаны магнитные свойства.
В [17] изучены окислительно-восстановительные процессы, протекающие в системе CuI,II/[B12H12]2–/Phen в органических растворителях в присутствии 1,10-фенантролина (Phen), рассмотрены методы получения и идентификация комплексов Cu(I), Cu(II) и смешанокатионного комплекса меди(I)/меди(II). Среди комплексов меди(II) описан тетраядерный комплекс [${\text{Cu}}_{4}^{{{\text{II}}}}$(OH)4(Phen)4(DMF)2][B12H12]2, полимерный комплекс [[CuII(Phen)2][B12H12]]n и моноядерный комплекс [CuII(Phen)2Cl]2[B12H12] [17].
В настоящей работе исследованы окислительно-восстановительные процессы, протекающие в системе Cu/[B12H12]2–/L/solv (L = BPA, Bipy) в присутствии 2,2'-бипиридила (Bipy) и 2,2'-бипиридиламина (BPA), получены и охарактеризованы моноядерные комплексы меди(II) различного состава и строения с лигандами L и клозо-додекаборатным анионом в качестве противоиона.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Додекагидро-клозо-додекаборат триэтиламмония (Et3NH)2[B12H12] получали пиролизом раствора декаборана в триэтиламиноборане по методике [18].
Клозо-додекаборат цезия получали кипячением (Et3NH)2[B12H12] в водном растворе гидроксида цезия до полного удаления триэтиламина.
Клозо-додекабораты с органическими катионами (Bu3NH+, Ph4P+) синтезировали по обменной реакции между Cs2[B12H12] и соответствующими галогенидами.
Додекагидро-клозо-додекаборатокупрат(I) тетрафенилфосфония (C6H5)4P[Cu[B12H12]] получали при нагревании водной суспензии (Ph4P)2B12H12 и Cu2SO4 до 80оC в присутствии Na2SO3 [19].
Додекагидро-клозо-додекаборатодисеребро(I) [Ag2[B12H12]] и додекагидро-клозо-додекаборатоаргентат цезия Cs[Ag[B12H12]] получали по методике [20] при соотношении [B12H12]2– : Ag+ = 1 : 2 или 1 : 1 соответственно.
Нитрато-ди(2,2'-бипиридил)серебро(I) {[Ag(Bipy)2] NO3}n (1) получали в результате взаимодействия раствора нитрата серебра(I) (0.1 моль) в ацетонитриле (10 мл) c раствором Bipy (0.2 моль) в том же растворителе (10 мл). Через 15 мин после сливания растворов реагентов наблюдали образование белого осадка, который отфильтровывали, промывали водой, ацетонитрилом (2 × 10 мл) и высушивали на воздухе. Перекристаллизация конечного продукта из ацетонитрила привела к получению монокристаллов соединения 1. Выход составил ∼70%. Монокристалл 1, пригодный для РСА, получен перекристаллизацией из DMF.
[Cu(Bipy)2Cl][B12H12] (3). К раствору (Bu3NH)2[B12H12] (1 ммоль) в DMF (10 мл) добавляли CuCl (1 ммоль) и Bipy (2 ммоль), растворенные в 10 мл DMF каждый. В течение суток окраска реакционного раствора менялась с красной на зеленую. Через несколько дней из реакционного раствора выпадали кристаллы соединения 3 (зеленого цвета), которые отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. Непосредственно из реакционной массы был отобран кристалл 3 ⋅ 2DMF, подходящий для РСА. Выход составил ∼60% по бору.
[Cu(BPA)2(DMF)2][B12H12] (4). Методика 1 (селективное получение). К раствору Cs[Ag[B12H12]] (1 ммоль) в DMF (10 мл) добавляли CuCl (1 ммоль) и BPA (2 ммоль), растворенные в 10 мл DMF каждый. При смешивании компонентов наблюдали постепенное изменение окраски реакционного раствора с красной на зеленую. В течение 4–5 ч наблюдали образование кристаллического осадка зеленого цвета, который отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. В ходе реакции соединение 4 образуется селективно. Методом РСА установлено строение монокристалла 4 ⋅ DMF, выбранного непосредственно из реакционного раствора. Выход составил ∼50%.
Методика 2 (совместно с [Cu(BPA)(CO3)]2 ⋅ ⋅ 2H2O). К раствору [Ag2[B12H12]] (1 ммоль) в DMF (10 мл) добавляли CuCl (2 ммоль) и BPA (4 ммоль), растворенные в 10 мл ацетонитрила каждый. Окраска реакционного раствора постепенно менялась с красной на зеленую, в течение суток наблюдалось образование кристаллов. Образующийся кристаллический осадок отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. В ходе реакции образуется смесь [Cu(BPA)(CO3)]2 ⋅ 2H2O (темно-синие кристаллы, параметры ячейки которых соответствуют параметрам известного соединения, описанного в [11]) и комплекса 4 (зеленые кристаллы), которые разделяли механически для проведения рентгеноструктурных экспериментов. Выход соединения 4 составил ∼55% по бору.
Методика 3 (совместно с [Cu(BPA)2Cl]Cl ⋅ DMF (2)). К раствору (Bu3NH)2[B12H12] в DMF (10 мл) добавляли CuCl (2 ммоль) и BPA (4 ммоль), растворенные в 10 мл DMF каждый. Окраска реакционного раствора постепенно менялась с красной на зеленую. В течение суток наблюдалось образование кристаллов зеленого цвета, которые представляют собой смесь кристаллов 4 и [Cu(BPA)2Cl]Cl ⋅ DMF (2 ⋅ DMF). Образующийся кристаллический осадок отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. Для проведения РСА кристаллы разделяли механически. Выход 2 составил ∼65%.
[Cu(BPA)2][B12H12]n (5). К раствору Ph4P[Cu[B12H12]] (1 ммоль) в DMF или CH3CN (10 мл) приливали раствор BPA (2 ммоль) в том же растворителе (10 мл). Окраска реакционного раствора постепенно менялась на зеленую. Из реакционного раствора в течение суток наблюдали образование кристаллов зеленого цвета. Полученный кристаллический осадок 5 отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. Монокристалл 5, подходящий для РСА, был выбран непосредственно из реакционного раствора. По данной методике соединение 5 образуется селективно с выходом 82%.
[Cu(Bipy)(DMF)4][B12H12] (6). К раствору Ph4P[Cu[B12H12]] (1 ммоль) в DMF (10 мл) приливали {[Ag(Bipy)2]NO3}n (1 ммоль) в DMF (10 мл). Окраска реакционного раствора постепенно менялась на зеленую. Образующийся в течение 2–3 сут кристаллический осадок отфильтровывали, промывали на фильтре водой (2 × 5 мл) и высушивали на воздухе. В ходе реакции образуется смесь продуктов 6 (зеленые кристаллы) и {[Cu(Bipy)2]3 (CO3)}[B12H12] (7) (голубые кристаллы) [16]. Монокристаллы 6 и 7, подходящие для РСА, отобрали механически непосредственно из реакционного раствора. Параметры ячейки кристаллов 7 совпали с {[Cu(Bipy)2]3(CO3)}[B12H12], который описан нами ранее [16]. Выход соединения 6 составил <50% по бору.
Реагенты и продукты проведенных реакций представлены в табл. 1.
Таблица 1.
Схемы получения комплексов Cu(II) c анионом [B12H12]2– и L (L = Bipy, BPA, Phen)
| № реакции | Реагент | Растворитель | Продукт |
|---|---|---|---|
| L = Bipy, BPA | |||
| 1 | (Bu3NH)2[B12H12] + CuCl + 2Bipy | DMF | [Cu(Bipy)2Cl]2[B12H12] (3) |
| 2 | (Bu3NH)2[B12H12] + CuCl + 2BPA | DMF | [Cu(BPA)2(DMF)2][B12H12] (4) + + [[Cu(BPA)Cl]Cl (2) |
| 3 | Ph4P[Cu[B12H12]] + 2BPA | DMF или CH3CN | {[Cu(BPA)2][B12H12]}n (5) |
| 4 | [Ag2[B12Н12]] + 2CuCl + 4BPA | DMF/CH3CN | 4 + [Cu(BPA)(CO3)]2 [11] |
| 5 | Cs[Ag[B12H12]] + CuCl + 2BPA | DMF | 4 |
| 6 | Ph4P[Cu[B12H12]] + [Ag(Bipy)2]NO3 (1) | DMF/CH3CN | {[Cu(Bipy)2]3(CO3)}[B12H12] (7) + + [Cu(Bipy)(DMF)4][B12H12] (6) |
| L = Phen (данные [17]) | |||
| 7 | Cs[Ag[B12H12]] + CuCl + 2Phen | DMF | [Cu4(OH)4(Phen)4(DMF)2][B12H12] + + {[Cu(Phen)2][B12H12]}n |
| 8 | Ph4P[Cu[B12H12]] + 2Phen | CH3CN/CH2I2 | [CuII(Phen)3][CuI(Phen)2]2[B12H12]2 + + [Cu(Phen)3][B12H12] |
| 9 | Ph4P[Cu[B12H12]] + [Cu2(Phen)4(CO3)]Cl2 | CH3CN/CH2I2 | [Cu(Phen)2Cl]2[B12H12] |
Элементный анализ на углерод, водород и азот осуществляли на автоматическом газовом анализаторе CHNS-3 FA 1108 Elemental Analyser (Carlo Erba). Перед проведением анализа образцы высушивали до постоянной массы. Бор определяли методом атомно-абсорбционной спектроскопии на спектрофотометре Perkin–Elmer (модель 2100, CША) с электротермическим атомизатором HGA-700 [21]. Определение Cu проводили на приборе ААS-303 в пламени ацетилен-воздух. Данные элементного анализа представлены в табл. 2.
Таблица 2.
Данные элементного анализа синтезированных комплексов, %
| № комплекса | Cu | C | H | N | B |
|---|---|---|---|---|---|
| найдено/вычислено | |||||
| 1 | 22.28/22.37(Ag) | 49.14/49.81 | 3.28/3.34 | 14.44/14.52 | – |
| 3 | 16.70/16.68 | 40.98/41.01 | 5.84/5.82 | 11.01/11.04 | 17.05/17.04 |
| 4 | 9.22/9.18 | 45.11/45.13 | 6.13/6.12 | 16.15/16.19 | 18.78/18.74 |
| 5 | 11.80/11.60 | 43.76/43.85 | 5.43/5.52 | 15.27/15.34 | 23.60/23.68 |
| 6 | 9.74/9.72 | 40.42/40.41 | 7.37/7.40 | 12.83/12.85 | 19.82/19.84 |
ИК-спектры записывали на ИК-Фурье-спектрометре ИНФРАЛЮМ ФТ-02 (НПФ АП “Люмекс”) в области 4000–400 см–1 с разрешением 1 см–1. Образцы готовили в виде суспензии исследуемого вещества в вазелиновом масле (Aldrich). Данные ИК-спектроскопии представлены в табл. 3.
Таблица 3.
Максимумы некоторых полос поглощения в ИК-спектрах синтезированных комплексов (ν, см–1)
| № комплекса | ν(СН)Bipy | ν(NН)BPA | ν(ВН) | ν(C≡N) | ν(C=O)DMF | δ(BBH) | π(CH)цикла |
|---|---|---|---|---|---|---|---|
| 3 ⋅ 2DMF | 3058 | – | 2474 | 2250 | 1675 | 1059 | 771 |
| 4 ⋅ DMF | – | 3244, 3206, 3137 | 2471 | – | 1669, 1628 | 1058 | 770 |
| 5 | – | 3247, 3200, 3134 | 2468 | – | – | 1056 | 770 |
| 6 | 3080 | – | 2455 | 2250 | 1670 | 1058 | 773 |
Спектры КР записывали на ИК-спектрофотометре VERTEX 70 с приставкой RAM II FT-Raman module.
РСА. Набор дифракционных отражений для кристаллов 1–6 получен на автоматическом дифрактометре Bruker APEX2 CCD (λMoKα, графитовый монохроматор, ω–φ-сканирование). Структуры расшифрованы прямым методом с последующим расчетом разностных синтезов Фурье. Неводородные атомы уточнены в анизотропном приближении. Все атомы водорода в структурах 3 ⋅ 2DMF и 5, а также атомы водорода, связанные с атомами бора, BPA и некоординированной молекулой DMF в структуре 4 ⋅ DMF уточнены независимо в изотропном приближении; остальные атомы водорода уточнены по модели наездника с тепловыми параметрами U(H) = 1.2Uэкв (1.5Uэкв для СН3-групп) соответствующих неводородных атомов.
В элементарной ячейке 1 содержится одна молекула бипиридила, координированная атомом серебра, и два аниона ${\text{NO}}_{3}^{--}$ с заселенностью 0.5. Один из анионов уточнен в модели “жесткого тела”, второй – с ограничениями по всем длинам связей и заданием плоской геометрии. Кроме того, принято, что атомы O(1), O(2), O(3) и N(3) имеют одинаковые Uаниз. В структуре 3 ⋅ 2DMF две молекулы DMF разупорядочены по двум ориентациям каждая, различающимся поворотом вдоль двойной оси, проходящей через атомы O, N. Длина связи O(1)–C(11A) зафиксирована. Принято, что атомы C(11), С(11А), С(12), С(12А) и С(13), С(13А) попарно имеют одинаковые Uаниз. В структуре 6 одна молекула DMF разупорядочена аналогично таковым в 3, принято, что атомы C(17), С(17А), С(18), С(18А) и С(19), С(19А) попарно имеют одинаковые Uаниз. Несколько отражений с большим расхождением между наблюдаемой и вычисленной структурными амплитудами в 1, 2 ⋅ 2DMF, 3 ⋅ 2DMF и 6 исключены из уточнения.
При сборе и обработке массива отражений использованы программы APEX2, SAINT и SADABS [22]. Структура расшифрована и уточнена с помощью программ комплекса OLEX2 [23].
Основные кристаллографические данные, параметры эксперимента и характеристики уточнения структуры приведены в табл. 4, некоторые длины связей и валентные углы в комплексах 1–6 – в табл. 5 и 6. Кристаллографические данные для структур 1–6 депонированы в Кембриджском банке структурных данных (КБСД) (CCDС № 1 899 332–1 899 337). РСА проведен в ЦКП ИОНХ РАН в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Таблица 4.
Основные кристаллографические данные, параметры эксперимента и уточнения структур 1–6
| Соединение | 1 | 2 ⋅ DMF | 3 ⋅ 2DMF | 4 ⋅ DMF | 5 | 6 |
|---|---|---|---|---|---|---|
| Брутто-формула | C20H16AgN6O6 | C23H25Cl2CuN7O | C46H58B12Cl2Cu2N10O2 | C16H29B6Cu0.5N5O2 | C20H30B12CuN6 | C22H48B12CuN6O4 |
| FW | 544.25 | 549.95 | 1110.93 | 420.16 | 547.94 | 653.92 |
| T, K | 294(2) | 296(2) | 150(2) | 150(2) | 150(2) | 297(2) |
| Сингония | Моноклинная | Триклинная | Моноклинная | Моноклинная | Триклинная | Триклинная |
| Пр. гр. | C2/c | P | P21/c | P21/c | P | P |
| a, Å | 24.0862(18) | 7.0856(3) | 9.0305(4) | 10.2261(5) | 8.3668(6) | 12.4517(4) |
| b, Å | 3.7891(3) | 12.6793(5) | 14.3504(6) | 15.2774(8) | 9.9199(7) | 12.4812(4) |
| c, Å | 24.2299(18) | 15.4756(7) | 20.2446(8) | 14.3185(8) | 9.9519(12) | 14.0296(5) |
| α, град | 90 | 67.2090(10) | 90 | 90 | 111.437(3) | 113.2730(10) |
| β, град | 102.0300(10) | 77.5790(10) | 94.3120(10) | 102.3090(10) | 101.336(3) | 91.1450(10) |
| γ, град | 90 | 75.1530(10) | 90 | 90 | 110.833(2) | 117.24 |
| V, Å3 | 2162.8(3) | 1228.48(9) | 2616.10(19) | 2185.5(2) | 666.04(11) | 1726.17(10) |
| Zвыч | 4 | 2 | 2 | 4 | 1 | 2 |
| ρрасч, г/см3 | 1.6713 | 1.4866 | 1.4100 | 1.2766 | 1.3656 | 1.258 |
| μ, мм–1 | 0.982 | 1.137 | 0.965 | 0.548 | 0.845 | 0.671 |
| F(000) | 1089.0 | 567.4 | 1146.2 | 882.9 | 281.4 | 686.0 |
| Размеры кристалла, мм | 0.50 × 0.2 × × 0.12 | 0.40 × 0.28 × 0.04 | 0.20 × 0.16 × 0.08 | 0.36 × 0.12 × 0.10 | 0.20 × 0.12 × 0.08 | 0.50 × 0.40 × 0.26 |
| Интервал углов 2θ, град | 4.34–54.90 | 3.56–54.00 | 4.52–58.00 | 4.88–58.00 | 4.74–60.30 | 4.354–63.944 |
| Число отражений: измеренных независимых (N) [Rint] |
8000 2446 [0.0190], |
14 923 5305 [0.0169] |
32 529 6954 [0.0451] |
22 357 5794 [0.0499] |
9370 3905 [0.0430] |
21 600 10 857 [0.0210] |
| R1, wR2 по No | 0.0551, 0.1517 | 0.0341, 0.0929 | 0.0335, 0.0761 | 0.0446, 0.0977 | 0.0445, 0.1048 | 0.0516, 0.1550 |
| R1, wR2 по N | 0.0676, 0.1679 | 0.0408, 0.0971 | 0.0522, 0.0827 | 0.0686, 0.1076 | 0.0603, 0.1130 | 0.0709, 0.1703 |
| Δρmax /Δρmin, э/Å3 | 0.66/–0.78 | 0.84/–0.47 | 0.55/–0.43 | 0.55/–0.90 | 1.04/–0.44 | 0.65/–0.46 |
Таблица 5.
Некоторые длины связей в комплексах 2 ⋅ 2DMF и 3 ⋅ 2DMF
| Связь | d, Å | |
|---|---|---|
| 2 ⋅ 2DMF | 3 ⋅ 2DMF | |
| Cu–Cl(1) | 2.3140(7) | 2.3035(5) |
| Cu–N(1) | 1.9945(17) | 1.9785(14) |
| Cu–N(2) | 2.1741(17) | 2.1044(14) |
| Cu–N(3) | 2.0593(18) | 2.0918(14) |
| Cu–N(4) | 2.0039(17) | 1.9715(14) |
Таблица 6.
Некоторые длины связей в комплексах 4 ⋅ 2DMF, 5 и 6
| Связь | d, Å |
|---|---|
| 4 ⋅ DMF | |
| Cu–N(1)(N(1')) | 2.0044(16) |
| Cu–N(2)(N(2')) | 2.0153(15) |
| Cu–O(1)(O(1')) | 2.3643(15) |
| 5 | |
| Cu–N(1)(N(1')) | 2.0035(17) |
| Cu–N(2)(N(2')) | 1.9958(17) |
| Cu–H(1A)(H(1A')) | 2.20(17) |
| 6 | |
| Cu–N(1) | 1.9902(16) |
| Cu–N(2) | 1.9995(16) |
| Cu–O(1) | 1.9623(15) |
| Cu–O(2) | 1.9805(14) |
| Cu–O(3) | 2.4755(18) |
| Cu–O(4) | 2.3102(17) |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Изучение реакций комплексообразования меди(I) и меди(II) с клозо-додекаборатным анионом в присутствии органических лигандов L на воздухе в органических растворителях при соотношении реагентов Cu : L = 1 : 2 показывает, что наряду с моноядерными комплексами меди(II) могут образовываться би, три- и тетраядерные комплексные соединения меди(II). Схемы взаимодействий, которые протекают в системах Cu/[B12H12]2–/ L/solv, изученных в настоящей работе (L = Bipy, BPA) и описанных в литературе (L = Phen), представлены в табл. 1.
Для систем, содержащих Phen, ранее [17] было установлено, что взаимодействие Cu(I) с L в присутствии [B12H12]2– в DMF на воздухе сопровождается окислением меди(I) до меди(II), а в качестве основных продуктов образуются тетраядерный и полимерный комплексы меди(II) (табл. 1, реакция 7). При проведении реакции в системе CH3CN/CH2I2 удается замедлить процесс окисления меди(I) на воздухе, так что в качестве основных продуктов образуются моноядерные комплексы – смешанокатионный комплекс меди(I) и меди(II) [CuII(Phen)3][CuI(Phen)2]2[B12H12]2 и комплекс меди(II) [Cu(Phen)3][B12H12] (реакция 8). При направленном проведении реакции из исходного комплекса меди(II) [Cu2(CO3)(Phen)4]Cl2 в качестве основного продукта образуется моноядерный комплекс меди [Cu(Phen)2Cl]2[B12H12] (реакция 9).
В настоящей работе изучены реакции комплексообразования меди(II), протекающие в ходе окислительно-восстановительных превращений в системах, содержащих медь(I), анион [B12H12]2– и органический лиганд L, на воздухе в органических растворителях solv. Реакции проводили при варьировании источника меди(I) (CuCl или Ph4P[Cu[B12H12]]), источника кластерного аниона бора ((Bu3NH)2[B12H12], Ph4P[Cu[B12H12]], Cs[Ag[B12H12]] или [Ag2[B12Н12]]), органического лиганда (свободный лиганд L или комплекс {[Ag(Bipy)2]NO3}n). Во всех реакциях соотношение Cu : L составляло 1 : 2. Схемы проведенных реакций представлены в табл. 1 (реакции 1–6).
Ранее было показано, что использование солей серебра(I) в синтезе комплексов меди(II) благодаря сложным окислительно-восстановительным процессам (CuI → CuII, AgI → Ag0), протекающим в системе, позволяет получать нетривиальные соединения, в частности, по данной методике был получен трехъядерный комплекс меди(II) [Cu3(Bipy)6(CO3)][B12H12]2 [16].
Синтез и строение комплекса {[Ag(Bipy)2]NO3}n (1)
Для изучения реакций комплексообразования в системах медь(I)/серебро(I) в присутствии органического лиганда L предварительно синтезировали комплекс серебра(I) с Bipy:
(1)
${\text{AgN}}{{{\text{O}}}_{3}} + 2{\text{Bipy}} \to \left[ {{\text{Ag}}{{{\left( {{\text{Bipy}}} \right)}}_{2}}} \right]{\text{N}}{{{\text{O}}}_{3}}.$Комплекс 1 идентифицирован методами элементного анализа, ИК- и КР-спектроскопии, строение комплекса определено методом РСА.
На рис. 1а приведен ИК-спектр комплекса 1, из которого видно, что в области валентных колебаний ν(N=O) нитратогруппы присутствует интенсивная уширенная полоса около 1380 см–1, отражающая внешнесферное положение NO3–-группы. В спектре присутствует полный набор полос, соответствующий координированному состоянию молекул Bipy интервале 1600–700 см–1 с одновременным повышением колебательных частот ν(СС) и ν(СN), ∆ν ~ 25 см–1.
Рис. 1.
ИК-спектр 1 в области ν(NO), см–1 (а); вид спектра КР в области валентных колебаний ν(Ag–Ag), см–1 (б).
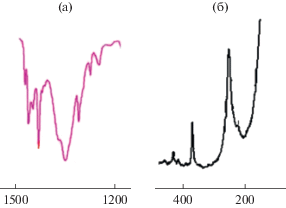
В спектре КР комплекса (рис. 1б) наблюдается узкая интенсивная полоса валентных колебаний связи металл–металл ν(Ag–Ag) при 253 см–1 с низкочастотным плечом при 237 см–1.
Пригодные для РСА монокристаллы комплекса 1 были получены перекристаллизацией из DMF. В структуре 1 (рис. 2) окружение атома серебра составляют четыре атома азота двух молекул Bipy, координационный полиэдр Ag – сильно искаженный квадрат. Длины связи Ag–N лежат в диапазоне 2.313(3)–2.320(3) Å. Катионы упакованы стопками, между которыми образуются полости, заполненные разупорядоченными нитрат-ионами. В кристалле имеются очень слабые контакты Ag…Ag (3.789(3) Å). Среднее значение этого расстояния, установленное по данным КБСД, составляет 3.026(3) Å. Между расположенными параллельно молекулами Bipy наблюдается π–π-стекинг взаимодействие с расстоянием между молекулами 3.789(3) Å и смещением между центрами гетероциклов 1.421(3) Å. За счет контактов Ag…Ag комплексные катионы [Ag(Bipy)2]+ формируют полимерную цепь. Данные РСА находятся в соответствии с результатами ИК- и КР-спектроскопии.
Рис. 2.
Строение комплекса {[Ag(Bipy)2]NO3}n (1), пунктирной линией показано расстояние между двумя молекулами Bipy.
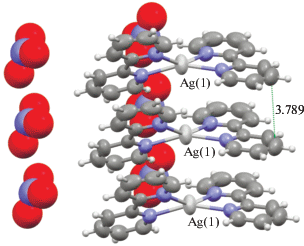
В дальнейшем комплекс 1 использовали в реакциях комплексообразования меди(II) при проведении синтезов в системе серебро(I)/медь(II).
Реакции комплексообразования меди(II) при использовании солей меди(I) в качестве исходных реагентов
В результате проведения реакций комплексообразования в системе анион [B12H12]2–/CuI/L (L = = Bipy, BPA) при соотношении металл : лиганд = = 1 : 2 установлено, что состав и строение полученных продуктов зависят от природы лиганда, меди(I) и используемого клозо-додекабората. Во всех случаях в органических растворителях протекает на воздухе окисление меди(I) до меди(II). В качестве основных продуктов реакций образуются моноядерные катионные комплексы меди(II), окружение металла в которых достраивается до КЧ = 5 или 6 присутствующими в реакционном растворе анионами хлора, CO3-группой, источником которой является CO2 воздуха, или молекулами растворителя DMF.
При взаимодействии (Bu3NH)2[B12H12] + CuCl + + 2Bipy в DMF в качестве основного продукта образуется моноядерный катионный комплекс меди(II) [Cu(Bipy)2Cl][B12H12] (3) в виде сольвата с молекулой DMF (табл. 1, реакция 1). Для BPA аналогичная реакция (реакция 2) привела к получению смеси двух моноядерных комплексов: [Cu(BPA)2(DMF)2][B12H12] (4) и [Cu(BPA)2Cl]Cl (2), выделяющихся в виде сольватов с молекулами DMF.
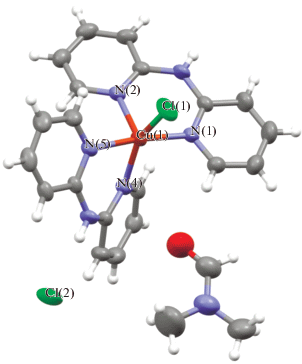
В элементарных ячейках комплексов 2 ⋅ DMF (рис. 3) и 3 ⋅ 2DMF (рис. 4) содержатся катионные комплексы меди(II) [CuL2Cl]+ (L = BPA для 2, Bipy для 3), координационные полиэдры которых представляют собой искаженную квадратную пирамиду, образованную четырьмя атомами азота двух молекул лиганда L и ионом Cl–, находящимся в экваториальной позиции. Анионную часть комплекса 2 ⋅ DMF образует хлорид-ион, комплекса 3 ⋅ 2DMF – половина аниона [B12H12]2–. Кроме того, в элементарную ячейку обоих соединений входит некоординированная молекула DMF.
В моноклинную элементарную ячейку соединения 4 · DMF (рис. 5) входят координированная атомом меди молекула BPA, координированная и сольватная молекулы DMF и половина аниона [B12H12]2–. Атом меди находится в слабоискаженном октаэдрическом окружении из четырех атомов азота двух молекул BPA и двух атомов кислорода молекул DMF.
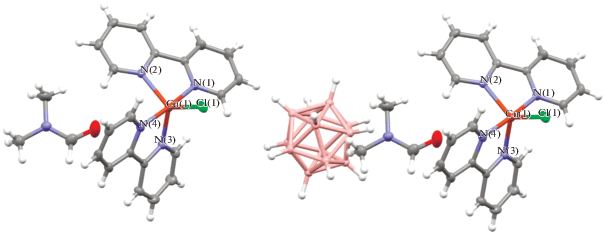
При изменении источника исходного клозо-додекабората и меди при взаимодействии купрадодекабората Ph4P[Cu[B12H12]] с органическим лигандом BPA в DMF основным продуктом является комплекс {[Cu(BPA)2][B12H12]}n (5) (табл. 1, реакция 3), имеющий полимерное строение (рис. 6). Катионная часть представляет собой комплекс меди(II), в котором медь находится в незначительно искаженном квадратном окружении, образованном четырьмя атомами азота двух молекул BPA. Две ВН-группы клозо-додекаборатных анионов через атом H(1a) достраивают координационную сферу атома меди до октаэдра, при этом образуются полимерные 1D-цепочки, связанные между собой сеткой вторичных связей (рис. 6).
Рис. 6.
Структура комплекса [Cu(BPA)2][B12H12]]n (5), пунктирными линиями показаны некоторые диводородные связи между анионом [B12H12]2– и BPA.
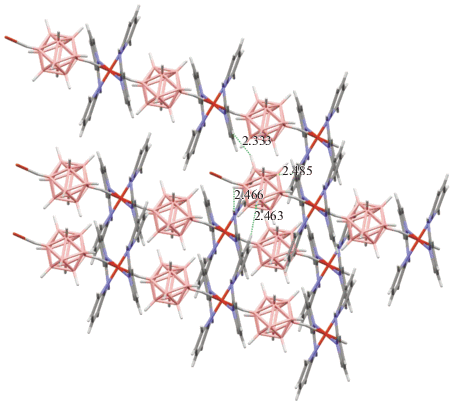
Комплексы меди(II) схожего строения получены для Phen состава {[Cu(Phen)2][B12H12]}n [17] и {[Cu(Phen)2][B10H10]}n [11]. В полученных соединениях имеются удлиненные контакты Cu…H(B) 2.85 Å, тогда как в комплексе 5 присутствует укороченный контакт Cu–H 2.20(17) Å. Такая связь между атомом водорода борного кластера и атомом меди(II) обнаружена впервые. Длина этой связи совпадает с расстояниями (B)H–Cu(I) 2.1–2.3 Å. Этот факт можно объяснить более низкой реакционной способностью клозо-додекаборатного аниона по сравнению с клозо-декаборатным, для которого подобные расстояния (B)H–Cu(II) невозможны ввиду протекания окислительно-восстановительной реакции, приводящей к восстановлению меди(II) до меди(I).
Реакции комплексообразования меди(II) в системе медь(I)/серебро(I)
Проведение реакций в системе, содержащей медь(I)/медь(II) и серебро(I), позволяет получать соединения нетривиального строения, так как наличие нескольких металлов приводит к сложным окислительно-восстановительным процессам, происходящим в реакционном растворе, что оказывает влияние на координационное окружение атомов металлов и строение образующихся продуктов.
Для BPA обнаружено, что изменение реагентов не приводит к образованию соединений, отличных от вышеописанного комплекса 4. При взаимодействии комплексов [Ag2[B12Н12]] или Cs[Ag[B12Н12]] с CuCl в присутствии BPA в ацетонитриле или смеси CH3CN/DMF обнаружено, что основным продуктом является комплекс 4, но в случае [Ag2[B12Н12]] (реакция 4) соединение 4 выпадает совместно с комплексом [Cu(BPA)(CO3)]2, описанным нами ранее [11]. В случае Cs[Ag[B12Н12]] (реакция 5) соединение 4 образуется селективно.
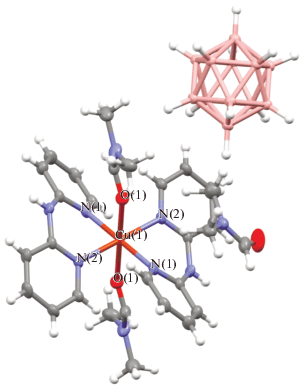
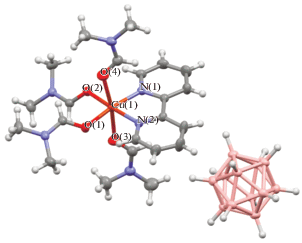
Для Bipy при проведении реакции в системе медь(I)/серебро(I) взаимодействие Ph4P[Cu[B12H12]] с предварительно синтезированным комплексом 1 дает смесь продуктов: трехъядерный комплекс меди(II) {[Cu(Bipy)2]3(CO3)}[B12H12], описанный нами ранее [16], и моноядерный комплекс 6 (табл. 1, реакция 6). Соединение 6 состоит из катионной части [Cu(Bipy)(DMF)4]2+ и двух независимых половин аниона [B12H12]2–. В отличие от описанного выше моноядерного комплекса меди(II) с BPA состава [Cu(BPA)2(DMF)2][B12H12], в окружение атома меди(II) в соединении 6 входят четыре атома кислорода молекул DMF и два атома азота молекулы Bipy (рис. 7).
Данные ИК-спектроскопии синтезированных комплексов 3–6
В ИК-спектрах комплексов 3–6 (табл. 3) присутствуют полосы валентных колебаний групп ВН с максимумами около 2450 см–1, указывающие на положение клозо-додекаборатного аниона во внешней сфере комплекса. При координации молекул азагетероциклических лигандов в спектрах соединений 3–6 наблюдается повышение значений колебательных частот ν(CN) и ν(СC) и значительное перераспределение интенсивностей полос колебаний гетероциклов в интервале 1600–700 см–1 по сравнению с таковыми в спектрах некоординированных лигандов. В ИК-спектрах соединений 4 и 5 присутствуют полосы, соответствующие валентным колебаниям NH-групп координированных молекул BPA (табл. 3). Кроме того, в спектрах соединений, содержащих координированные и некоординированные молекулы DMF, присутствуют полосы ν(CO).
ЗАКЛЮЧЕНИЕ
В работе синтезированы моноядерные комплексы меди(II) с азагетероциклическими лигандами L (L = Bipy, BPA) и клозо-додекаборатным анионом. Показано влияние исходных реагентов и условий проведения реакций на состав и строение полученных комплексов. В качестве исходных реагентов использовали соединения меди(I), некоторые реакции проводили в системе медь(I)/серебро(I). Во всех случаях происходит окисление меди(I) до комплексов меди(II). Реакции проводили при соотношении металл : лиганд = 1 : 2, поэтому в конечных комплексах, в которых КЧ атома меди было равно 5 или 6, в окружение металла входят не только молекулы органических лигандов, но также молекулы растворителей и присутствующих в реакционном растворе анионов (хлорид-ионов, CO3-группа). Получено четыре новых моноядерных комплекса меди(II) с лигандами L и анионами [B12H12]2– во внешней сфере. В полимерном комплексе [Cu(BPA)2][B12H12]]n, построенном чередованием кластерных анионов бора и моноядерного комплекса меди, обнаружены короткие контакты (B)H–Cu и разветвленная сеть водородных связей BH…HX (X = С, N) с молекулой BPA.
Список литературы
Muetterties E.L., Balthis J.H. et al. // Inorg. Chem. 1964. V. 3. P. 444.
Muetterties E.L., Knoth W.H. Polyhedral Boranes. Dekker–New York, 1968.
Greenwood N.N., Earnshaw A. Chemistry of the Elements. Butterworth-Heinemann, 1997.
Malinina E.A., Avdeeva V.V., Goeva L.V., Kuznetsov N.T. // Russ. J. Inorg. Chem. 2010. V. 55. P. 2148. https://doi.org/10.1134/S0036023610140032
Avdeeva V.V., Malinina E.A., Sivaev I.B. et al. // Crystals. 2016. V. 6. №. 5. P. 60. https://doi.org/10.3390/cryst6050060
Avdeeva V.V., Malinina E.A., Kuznetsov N.T. // Polyhedron. 2016. V. 105. P. 205. https://doi.org/10.1016/j.poly.2015.11.049
Avdeeva V.V., Malinina E.A., Kuznetsov N.T. // Russ. J. Inorg. Chem. 2017. V. 62. № 13. P. 1673. https://doi.org/10.1134/S0036023617130022
Avdeeva V.V., Polyakova I.N., Churakov A.V. et al. // Polyhedron. 2019. V. 162. P. 65. https://doi.org/10.1016/j.poly.2019.01.051
Malinina E.A., Zhizhin K.Yu., Polyakova I.N. et al. // Russ. J. Inorg. Chem. 2002. V. 47. № 8. P. 1158.
Avdeeva V.V., Dziova A.E., Polyakova I.N. et al. // Inorg. Chim. Acta. 2015. V. 430. P. 74. https://doi.org/10.1016/j.ica.2015.02.029
Dziova A.E., Avdeeva V.V., Polyakova I.N. et al. // Dokl. Chem. 2011. V. 440. P. 253. https://doi.org/10.1134/S0012500811090035
Avdeeva V.V., Dziova A.E., Polyakova I.N. et al. // Russ. J. Inorg. Chem. 2013. V. 58. P. 657. https://doi.org/10.1134/S003602361306003X
Dziova A.E., Avdeeva V.V., Polyakova I.N. et al. // Russ. J. Inorg. Chem. 2013. V. 58. P. 1527. https://doi.org/10.1134/S0036023614010045
Van N.D. Doctoral Thesis: New Salt-Like Dodecahydro-closo-Dodecaborates and Efforts for the Partial Hydroxylation of [B12H12]2– Anions. Institut für anorganische Chemie der Universitӓt, Stuttgart, 2009.
Polyakova I.N., Avdeeva V.V., Malinina E.A. et al. // Cryst. Rep. 2009. V. 54. P. 831. https://doi.org/10.1134/S1063774509050149
Malinina E.A., Kochneva I.K., Polyakova I.N. et al. // Inorg. Chim. Acta. 2018. V. 479. P. 249. https://doi.org/10.1016/j.ica.2018.04.059
Malinina E.A., Kochneva I.K., Polyakova I.N. et al. // Inorg. Chim. Acta. 2018. V. 477. P. 284. https://doi.org/10.1016/j.ica.2018.03.024
Greenwood N.N., Morris J.H. // Proc. Chem. Soc. 1963. V. 11. P. 338.
Malinina E.A., Drozdova V.V., Mustyatsa V.N. et al. // Russ. J. Inorg. Chem. 2006. V. 51. P. 1723. [Малинина Е.А., Дроздова В.В., Мустяца В.Н. и др. // Журн. неорган. химии. 2006. Т. 51. № 11. С. 1832.] https://doi.org/10.1134/S0036023606110076
Drozdova V.V., Malinina E.A., Belousova O.N. et al. // Russ. J. Inorg. Chem. 2008. V. 53. P. 1024. [Дроздова В.В., Малинина Е.А., Белоусова О.Н. и др. // Журн. неорган. химии. 2008. Т. 53. № 7. С. 1105.] https://doi.org/10.1134/S0036023608070097
Ochertyanova L.I., Mustyatsa V.N., Zhizhin K.Y. et al. // Inorg. Mater. 2004. V. 40. № 2. P. 144. [Очертянова Л.И., Мустяца В.Н., Жижин К.Ю. и др. // Неорган. материалы. 2004. Т. 40. № 2. С. 188.] https://doi.org/10.1023/B:INMA.0000016088.12295.5b
APEX2 (V. 2009, 5-1), SAINT (V7.60A), SADABS (2008/1). Bruker AXS Inc., Madison, Wisconsin, USA, 2008–2009.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии