Журнал неорганической химии, 2019, T. 64, № 11, стр. 1127-1135
Золь-гель синтез высокодисперсного карбида тантала-гафния Ta4HfC5
Е. П. Симоненко 1, *, Н. П. Симоненко 1, М. И. Петричко 2, В. Г. Севастьянов 1, Н. Т. Кузнецов 1
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
2 Институт тонких химических технологий им. М.В. Ломоносова, МИРЭА – Российский технологический университет
119571 Москва, пр-т Вернадского, 86, Россия
* E-mail: ep_simonenko@mail.ru
Поступила в редакцию 22.04.2019
После доработки 06.05.2019
Принята к публикации 13.05.2019
Аннотация
Получены порошки нанокристаллического карбида Ta4HfC5 с применением золь-гель синтеза высокодисперсного композиционного порошка состава Ta2O5–HfO2–C (прекурсоры – пентаамилоксид тантала и ацетилацетонат гафния, источник углерода – фенолформальдегидная смола) и последующего низкотемпературного карботермического синтеза (1200–1300°C, 2–4 ч, динамический вакуум). Состав исходного композиционного порошка Ta2O5–HfO2–C оптимизирован путем снижения содержания избыточного количества углерода. Определен элементный и фазовый состав полученного карбидного продукта. Показано, что при низкой температуре карботермического процесса возможен распад однофазного карбида состава Ta4HfC5 на смесь фаз карбидов тантала-гафния и гафния-тантала, однако однозначный вывод сделать невозможно из-за высокой дисперсности (размер кристаллитов составляет ~23–40 нм, размер частиц (по данным СЭМ) – ~37–45 нм). Изучено термическое поведение в токе воздуха при температуре 20–1000°C полученных высокодисперсных порошков состава Ta4HfC5; установлено влияние дисперсности образцов на положение экзотермических эффектов, связанных с окислением. Отмечено, что в качестве продукта окисления полученных порошков Ta4HfC5 помимо фазы Ta2O5 образуется сложный оксид Hf6Ta2O17.
ВВЕДЕНИЕ
Сверхтугоплавкие карбиды c температурой плавления >3000°С вызывают большой интерес, поскольку для них свойственны высокая теплопроводность, низкое давление пара [1] и хорошие механические характеристики, в частности, повышенная твердость [2].
Твердые монокарбиды металлов являются изоструктурными (кубическая гранецентрированная кристаллическая решетка), поэтому практически все карбиды металлов IV–VБ групп, за исключением VC, образуют между собой непрерывные ряды твердых растворов [3–5]. Наибольший интерес вызывает система TaC–HfC, для которой еще в 1930 г. авторы [6] установили существование экстремальной зависимости температуры плавления с максимумом для состава 4TaC · HfC (4215 K). Интерес к этой проблеме возник в 60-х годах, когда для этого состава или вблизи него были отмечены экстремумы и других свойств [3, 7–9]: электропроводности, давления пара, скорости испарения. В работе [10] подтверждена наивысшая температура плавления (3990°С) именно для состава 4TaC–HfC.
Начиная с 2000-х годов наблюдается всплеск научного и прикладного интереса к сверхтугоплавким карбидам, в том числе сложного состава, связанный, вероятно, с прогрессом в области ультравысокотемпературных керамических материалов (UHTC), перспективных для применения в наиболее термонагруженных участках гиперзвуковых летательных аппаратов [11–20].
В последние годы вновь возникла дискуссия о существовании максимума температуры плавления для состава Ta4HfC5. В работе [21] методом лазерного нагрева показано, что этот состав уступает по температуре плавления карбиду гафния (4178 ± 82 K для Ta4HfC5 по сравнению с 4232 ± 84 K для HfC). Однако в работе [22], посвященной этому вопросу, где был использован метод быстрого нагрева микросекундным импульсом электрического тока, показано, что температура плавления для обсуждаемого состава составляет 4300 ± 80 K, что существенно превышает данные [21] и подтверждает результаты [10]. Причиной ошибки в температуре плавления Ta4HfC5, полученной в [21], авторы [22] считают неправильно выбранный для этого соединения коэффициент излучения. Помимо температуры плавления состава Ta4HfC5 в [22] определена энтальпия этого процесса и теплоемкость в интервале 2000–4300 K.
Новый виток интереса к получению порошков и керамики на основе сложных карбидов в системе TaC–HfC, для которых отмечаются неплохие механические характеристики и окислительная стойкость, связан, с нашей точки зрения, с пришедшими в область бескислородной керамики (боридной, карбидной) представлениями о высокоэнтропийных сплавах [23, 24]. Для них за счет искажения кристаллической решетки из-за хаотичного распределения атомов различных металлов можно получить нехарактерно высокие для индивидуальных компонентов прочность, трещиностойкость, тепловые свойства и др.
Так, для получения керамики в системе (100 – х)TaC–хHfC (х = 20, 50 и 80 мол. %) смешанные порошки карбидов тантала и гафния спекали при температурах 2050–2450°С [25] в ходе искрового плазменного спекания (SPS). Изучены механические свойства, теплоемкость и теплопроводность изготовленных материалов, отмечена их перспективность для применения в гиперзвуковых летательных аппаратах. Метод SPS (2000–2200°С, 1 ч, вакуум) применялся также и в [26] для сравнения эффективности получения твердого раствора состава Ta4HfC5 в результате твердофазного спекания порошков TaC и HfC и реакционного спекания Ta2O5–HfO2–C.
Смешанный порошок, содержащий карбиды тантала и гафния, после их совместного помола консолидировался методом искрового плазменного спекания (1850°С, 10 мин, 60 МПа, вакуум) для получения керамических материалов состава (100 – х)TaC–xHfC, где х = 0, 20, 50, 80, 100 мол. % [27]. Термический анализ в токе воздуха таких образцов [28] показал, что твердый раствор 1TaC–1HfC обладает большей окислительной стойкостью, особенно по сравнению с индивидуальными карбидами. Для данных образцов в [29] установлена хорошая стойкость к окислению в высокоскоростной и высокоэнтальпийной струе воздуха. Наименьшая толщина окисленного слоя отмечена для твердого раствора TaC–HfC, что свидетельствует о перспективности применения таких составов для материалов, работоспособных при жестких аэродинамических нагрузках.
Твердые растворы в системе TaC–HfC–VC получали также по твердофазной реакции между соответствующими карбидами в ходе изготовления керамических материалов методом горячего прессования (1700–2000°С, 45 мин, 40 МПа) [30]. Установлено, что для состава Ta0.75Hf0.20V0.05C при некоторых условиях изготовления (1800°С, относительная плотность ~96%) вязкость разрушения превышает 5 МПа м1/2. Для последнего состава в [31] была сделана попытка изготовления монолитной керамики путем запрессовки (холодное и последующее горячее прессование, 1800°С) выкладки из волокон соответствующего состава с некоторым избытком углерода. В результате получены сетчатые пористые материалы, для которых из-за введения регулярной слабой фазы (графит) изменился характер разрушения и значительно повысился KIC (до 6.6 ± 0.4 МПа м1/2).
Сложный карбид тантала-гафния, содержащий 18 ат. % HfC, получен в [32] методом самораспространяющегося высокотемпературного синтеза с предварительной механоактивацией исходного порошка Ta–Hf–C. На основе полученного твердого раствора методами горячего прессования и искрового плазменного спекания (2000°С) изготовлены керамические материалы соответствующего состава с относительной плотностью 91–93%.
Методы синтеза, в которых металлсодержащие прекурсоры смешиваются через жидкую фазу (золь-гель технология [33–35], сольвотермический метод [36], термолиз полимерных предшественников [37, 38]), позволяют существенно снизить температуру карботермического восстановления (до 1200–1300°С) и получить целевые сложные карбиды в нанодисперсном состоянии. Синтез сложных сверхтугоплавких карбидов именно в нанокристаллическом состоянии значительно облегчает их введение в состав других, более окислительно стойких ультравысокотемпературных керамических материалов, например состава ZrB2/HfB2–SiC [39–43], а также приводит к замедлению роста зерен керамики при высокотемпературном изготовлении. Поэтому разработка методов низкотемпературного синтеза нанокристаллических карбидов тантала-гафния является важной и актуальной задачей.
Ранее нами [39] показана принципиальная возможность получения карбида тантала-гафния Ta4HfC5 с использованием золь-гель метода и последующего карботермического синтеза в условиях динамического вакуума уже при температурах ~1200–1500°C, однако при этом применялись длительные выдержки (6 ч) и присутствовал неконтролируемый избыток углерода, что с учетом наличия эвтектических составов для TaC (при температуре 3275 или 3476°С по данным [44] и [45] соответственно) и HfC (при температуре 3000 или 3180°С по данным [46] и [47] соответственно) должно отрицательно сказываться на свойствах керамических материалов на их основе.
Цель настоящей работы – изучение возможности получения карбида тантала-гафния Ta4HfC5 с применением золь-гель синтеза высокодисперсной системы Ta2O5–HfO2–C и ее последующей термической обработки при относительно низких температурах (1200–1300°С) и времени выдержки 2 и 4 ч.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Используемые реактивы: ацетилацетонат гафния [Hf(O2C5H7)4] (99%, синтезирован из HfOCl2 · ⋅ 8H2O путем взаимодействия с ацетилацетоном C5H8O2 “ч.” и 5%-ным раствором гидрата аммиака NH3 · H2O), раствор пентаамилокситантала Ta(OC5H11)5 (синтезирован в результате взаимодействия TaCl5 “ос. ч.” с амиловым спиртом “ч.” при воздействии сухого аммиака [48]), лак бакелитовый марки ЛБС-1 (раствор в 1-бутаноле).
Изменение реологических свойств коллоидного раствора во время гидролиза прекурсоров в присутствии фенолформальдегидной смолы и поликонденсации изучали с помощью ротационного вискозиметра Брукфильда Fungilab Smart L (скорость сдвига 100 об./мин, шпиндель L2).
Рентгенофазовый анализ (РФА) проводили на рентгеновском дифрактометре Bruker D8 Advance (излучение CuKα, разрешение 0.02°).
Термическое поведение продуктов в токе аргона и воздуха (250 мл/мин) в интервале температур 20–1000°С (скорость нагрева 20 град/мин) изучали с применением совмещенного ТГА/ДСК/ДТА анализатора SDT Q-600.
Сканирующая электронная микроскопия (СЭМ) выполнена на трехлучевой рабочей станции NVision 40, Carl Zeiss; элементный состав микрообластей определен с помощью приставки для энергодисперсионного анализа EDX Oxford Instrumets.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Синтез смешанного карбида тантала-гафния Ta4HfC5 осуществляли с применением гибридной методики, в соответствии с которой на первом этапе путем гидролиза тантал- и гафнийсодержащих прекурсоров в присутствии полимерного источника углерода (фенолформальдегидной смолы ЛБС-1), гелеобразования, сушки и карбонизации в условиях динамического вакуума образуется высокодисперсная химически активная система Ta2O5–HfO2–C, которая на втором этапе подвергается термической обработке при пониженном давлении (остаточное давление ~(1–5) × 10–6 атм) и температурах 1200, 1250 и 1300°С (скорость нагрева 110 град/мин) с выдержкой при максимальной температуре 2 и 4 ч.
Получение композиционного порошка Ta2O5–HfO2–C с применением золь-гель метода проводили путем добавления ацетилацетоната гафния в раствор алкоксида тантала (полное растворение) в соотношении n(Ta) : n(Hf) = 4 : 1. В полученный раствор вводили при перемешивании бутанольный раствор фенолформальдегидной смолы в количестве, рассчитанном исходя из полного протекания реакции:
Массовое содержание углерода, образующегося при пиролизе смолы, определено в результате предварительных исследований. Кроме того, поскольку при пиролизе тантал-гафнийсодержащего ксерогеля помимо углерода, источником которого является фенолформальдегидная смола, образуется еще некоторое количество углерода при термической деструкции лигандов прекурсоров, проведены предварительные эксперименты по оптимизации (уменьшению) количества вводимой смолы. В рамках экспериментов выбран необходимый избыток аморфного углерода, составляющий 20% от стехиометрического соотношения.
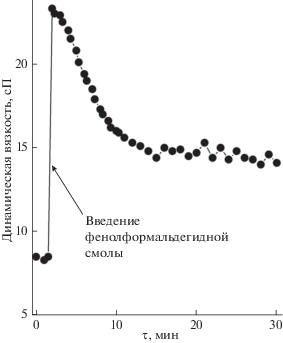
Методом ротационной вискозиметрии изучено изменение реологических свойств системы при смешении всех компонентов и гелеобразовании (рис. 1). Видно, что при введении в раствор алкоксоацетилацетонатов гафния и тантала раствора фенолформальдегидной смолы происходит скачкообразное повышение вязкости с 8.3–8.5 до 23.3 сП, что вызвано как протекающим гидролизом прекурсоров водой, содержащейся во втором растворе, и гелеобразованием за счет процессов поликонденсации, так и высаливанием полимера. При продолжении эксперимента при скорости сдвига 100 об./мин происходит снижение вязкости системы в результате разрушения некоторого количества сформировавшихся первоначально агрегатов и через ∼10–11 мин наблюдается стабилизация вязкости системы на значении 14–15 сП.
Рис. 1.
Изменение динамической вязкости системы при смешении компонентов – растворов металлсодержащих прекурсоров и фенолформальдегидной смолы.
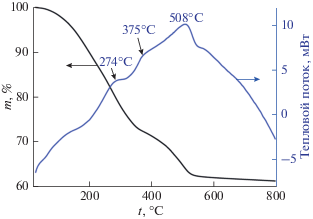
Полученный гель высушивали в роторном испарителе при температуре 50–60°С, размалывали и подвергали термической обработке в условиях динамического вакуума. Температура карбонизации выбрана на основании термического анализа в токе аргона тантал-гафний-полимерсодержащего ксерогеля, полученного после высушивания геля (рис. 2). Как видно из рис. 2, основная потеря массы образца завершается при температуре <600°С. Основываясь на этих данных, композиционный порошок Ta2O5–HfO2–C получали при температуре 600°С (выдержка в течение 2 ч в условиях динамического вакуума).
Рис. 2.
Кривые ДСК (синяя) и ТГА (черная) полученного тантал-гафний-полимерсодержащего ксерогеля в токе аргона.
Совмещенный ДСК/ДТА/ТГА подтвердил, что полученный высокодисперсный состав Ta2O5–HfO2–C содержит заданное количество углерода (рис. 3): потеря массы, соответствующая интенсивному экзотермическому эффекту с максимумом при 569°С, составляет 18%. Второй экзотермический эффект при 838°С относится к кристаллизации оксида тантала, что подтверждает рентгенограмма продукта после ДСК (рис. 4); рефлексов кристаллического HfO2 не обнаружено.
Рис. 3.
Кривые ДСК (синяя) и ТГА (черная) полученного композиционного порошка Ta2O5–HfO2–C в токе воздуха.
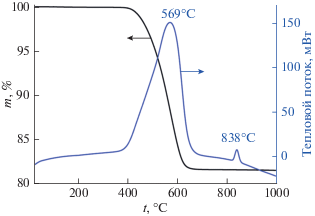
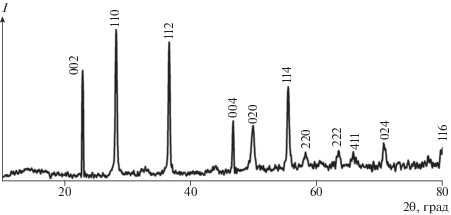
Рис. 4.
Рентгенограмма продукта, полученного в результате термического анализа полученного порошка Ta2O5–HfO2–C в токе воздуха; отмеченные индексы Миллера соответствуют фазе Ta2O5 [49].
Рентгенограмма 1, представленная на рис. 5, свидетельствует о том, что полученный при карбонизации ксерогеля композиционный порошок Ta2O5–HfO2–C является рентгеноаморфным.
Рис. 5.
Рентгенограммы композиционного порошка Ta2O5–HfO2–C (1) и полученных на его основе порошков Ta4HfC5 при температуре 1200 (2, 3), 1250 (4, 5) и 1300°С (6, 7) в течение 2 (2, 4, 6) и 4 ч (3, 5, 7); розовой штриховой линией отмечено положение наиболее интенсивного рефлекса HfO2 [50], внизу приведены рефлексы Ta4HfC5, полученные в [33].
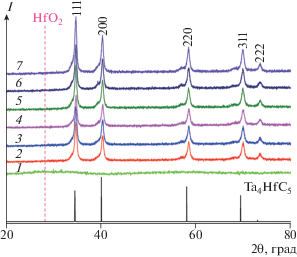
Карботермический синтез Ta4HfC5 выполнен в графитовой лодочке при пониженном давлении и температурах 1200, 1250 и 1300°С с выдержкой 2 и 4 ч. Как видно на рис. 5 (рентгенограммы 2–7), этих условий оказалось достаточно для полной конверсии оксидов тантала и гафния в кубический сложный карбид; положения уширенных рефлексов соответствуют таковым для сложного карбида тантала-гафния [33]. Однако некоторая асимметричность рефлексов и наличие невыраженных сильно уширенных гало при 2θ ~57° и 68° позволяют предположить при столь низких температурах твердофазный распад, возможность которого отмечалась в [51, 52]. Полнопрофильный анализ позволил определить средний размер кристаллитов, который для всех полученных продуктов находился в интервале 23–40 нм.
Данные СЭМ (рис. 6) подтверждают вывод о том, что синтезированные продукты являются нанодисперсными – наблюдается незначительное увеличение размера частиц с 37 ± 8 (1200°С, 2 ч) до 45 ± 11 нм (1300°С, 4 ч) по мере ужесточения режима синтеза. Выполненный EDX-анализ свидетельствует о том, что в пределах погрешности (~6%) заданное соотношение n(Ta) : n(Hf) = = 4 : 1 в полученных образцах выполняется.
Рис. 6.
Микроструктура полученных порошков состава Ta4HfC5 при различных температурах и времени выдержки карботермического синтеза.

Результаты изучения термического поведения полученных карбидов в токе воздуха (рис. 7) показали, что при температуре >800–850°C происходит полное окисление полученных нанодисперсных карбидов, что подтверждает и РФА продуктов после ДСК (рис. 8). Причем прирост массы, связанный с окислением синтезированных Ta4HfC5, начинается уже при температуре >100°C. На кривых ДСК наблюдается три перекрывающихся экзотермических эффекта с максимумами при 437–460, 567–602 и 739–753°С, которые можно отнести к окислению синтезированной карбидной фазы и имеющегося небольшого избытка углерода, заложенного при синтезе. Причем наличие двух очень близких по температурам экзотермических эффектов и двух максимумов на кривых ТГА косвенно может подтверждать то, что при карботермическом синтезе при низких температурах (1200–1300°С) возможно формирование не одного твердого раствора заданного состава, а двух твердых растворов – на основе карбида тантала и на основе карбида гафния. Вторым объяснением таких особенностей вида кривых ДСК и ТГА может быть то, что процесс окисления синтезированного карбидного продукта является двухступенчатым, вторая стадия которого затруднена диффузией кислорода через образовавшийся на поверхности частиц слой оксидов тантала и гафния. Необходимо также отметить, что по мере повышения температуры и времени карботермического синтеза Ta4HfC5 происходит смещение положения максимумов всех экзотермических эффектов на ~20–25°C для таковых в интервале температур 430–600°С и на 10–14°С – для пика с максимумом при температуре 730–760°С, что, вероятно, связано со снижением дисперсности полученного карбида.
Рис. 7.
Кривые ДСК (синие) и ТГА (черные) образцов Ta4HfC5, полученных при температуре 1200 (а) и 1300°С (б) в течение 2 ч в токе воздуха.
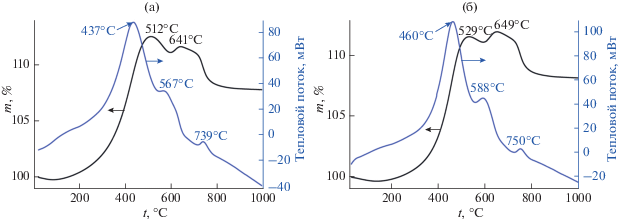
Рис. 8.
Рентгенограммы продуктов окисления в токе воздуха в интервале температур 20–1000°С образцов Ta4HfC5, полученных в результате карботермии при температуре 1200°С, 2 ч (1) и 1300°С, 4 ч (2).
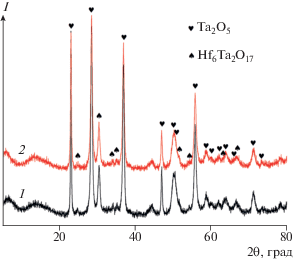
РФА (рис. 8) показал, что при окислении карбидных продуктов в результате нагрева в токе воздуха до 1000°С образуются две кристаллические фазы оксидов – Ta2O5 [49] и ~20% Hf6Ta2O17 [53]. Необходимо отметить, что фаза сложного оксида Hf6Ta2O17 не кристаллизовалась при окислении исходного порошка Ta2O5–HfO2–C (рис. 4).
ЗАКЛЮЧЕНИЕ
С применением золь-гель метода получен высокодисперсный композиционный порошок состава Ta2O5–HfO2–C. При этом в качестве прекурсоров применялся пентаамилоксид тантала и ацетилацетонат гафния, а в качестве источника углерода – фенолформальдегидная смола. Состав композиционного порошка был оптимизирован с точки зрения снижения избыточного количества углерода.
Нанокристаллические порошки сложного карбида состава Ta4HfC5 синтезированы путем относительно низкотемпературной термической обработки в вакууме полученного композиционного порошка Ta2O5–HfO2–C (при температурах 1200, 1250 и 1300°С) и достаточно коротких временах выдержки (2 и 4 ч). Установлено, что при всех режимах синтеза происходит полная конверсия оксидов тантала и гафния в карбид. На основании данных РФА и термического анализа полученных порошков Ta4HfC5 можно предположить, что при таких низких температурах карботермии возможен распад однофазной области соответствующего сложного карбида с образованием двух карбидных фаз – карбидов тантала-гафния и гафния-тантала. Однако полностью подтвердить данное утверждение не представляется возможным из-за высокой дисперсности полученного продукта – размер кристаллитов, по данным полнопрофильного анализа рентгенограмм, находится в интервале 23–40 нм, а размер частиц, по данным СЭМ, составляет 37–45 нм. При этом существует явная тенденция к повышению размера частиц и соответствующему снижению их реакционной способности при окислении в токе воздуха по мере ужесточения условий карботермического синтеза – увеличения температуры и времени выдержки.
Особенно важным с практической точки зрения является то, что при окислении полученных карбидных образцов помимо фазы оксида тантала образуется также кристаллический сложный оксид состава Hf6Ta2O17, который, как утверждается в [29], является одной из причин повышенной окислительной стойкости керамических материалов состава TaC–HfC и повышения механической прочности окисленной области этих материалов под воздействием высокоскоростных и высокоэнтальпийных потоков воздуха.
Таким образом, показано, что комбинированным методом, включающим золь-гель синтез высокодисперсного и химически активного порошка Ta2O5–HfO2–C с содержанием углерода, близким к стехиометрическому, и последующий карботермический синтез при температурах 1200–1300°C и времени выдержки 2–4 ч можно получить нанокристаллический карбид состава Ta4HfC5 с размерами частиц <50 нм без примеси оксидов металлов. Для получения однозначно однофазного карбида Ta4HfC5 можно рекомендовать повысить температуру карботермической реакции. Однако с учетом более низкого содержания углерода в исходном составе Ta2O5–HfO2–C, который в наших предыдущих исследованиях [33, 34, 48, 54] выполнял функцию матрицы, препятствующей агрегации карбидных частиц и способствующей получению более высокодисперсных частиц сверхтугоплавких карбидов, возможно значительное снижение дисперсности продуктов. Изучение термического поведения полученных высокодисперсных порошков карбидов позволяет рекомендовать использовать их не только для создания ультравысокотемпературных керамических материалов соответствующего состава Ta4HfC5, но и в качестве модифицирующих компонентов UHTC состава ZrB2(HfB2)–SiC, которые могут быть полезны:
– для ингибирования роста зерен при высокотемпературном прессовании,
– для модифицирования состава боросиликатного стекла оксидом тантала, который не только должен повышать вязкость его расплава, но и вызывать явление ликвации,
– для повышения прочности и устойчивости к уносу твердого каркаса окисленных областей материала за счет формирования фазы Hf6Ta2O17.
Список литературы
Самсонов Г.В., Виницкий И.М. Тугоплавкие соединения (справочник). М.: Металлургия, 1976. 550 с.
Казенас Е.К., Цветков Ю.В. Испарение карбидов. М.: Красанд, 2017. 800 с.
Киффер Р., Бенезовский Ф. Твердые материалы (пер. с нем.). М.: Металлургия, 1968. 384 с.
Rudy E., Nowotny H. // Monatsh. Chem. Verw. Teile anderer Wiss. 1963. B. 94. № 3. S. 507. https://doi.org/10.1007/BF00903490
Markström A., Andersson D., Frisk K. // CALPHAD. 2008. V. 32. P. 615. https://doi.org/10.1016/j.calphad.2008.07.014
Agte C., Alterthum H. // Z. Techn. Phys. 1930. № 6. S. 182.
Barantseva I.G., Paderno V.N., Paderno Yu.B. // Sov. Powder Metall. 1967. V. 6. № 2. P. 139. https://doi.org/10.1007/BF00775649
Deudmore D.L. // NASA technical note D-2512. Lewis Research Center Cleveland, Ohio, Washington D.C. 1964.
Fischer J.J. // Am. Ceram. Soc. Bull. 1964. V. 43. № 3. P. 183.
Andrievskii R.A., Strel’nikova N.S., Poltoratskii N.I. et al. // Sov. Powder Metall. 1967. V. 6. № 1. P. 65. // J. Nano Res. 2013. V. 21. P. 145.https://doi.org/10.1007/BF00773385
Arianpour F., Rezaie H.R., Golestani Fard F., et al. // J. Nano Res. 2013. V. 21. P. 145. https:///doi.org/10.4028/www.scientific.net/JNanoR.21.145.
Vorotilo S., Sidnov K., Mosyagin I.Yu. et al. // J. Alloys Compd. 2019. V. 778. P. 480. https://doi.org/10.1016/j.jallcom.2018.11.219
Wang C.R., Yang J.-M., Hoffman W. // Mater. Chem. Phys. 2002. V. 74. P. 272. https://doi.org/10.1016/S0254-0584(01)00486-2
Savino R., De Stefano Fumo M., Silvestroni L., Sciti D. // J. Eur. Ceram. Soc. 2008. V. 2. № 9. P. 1899. https://doi.org/10.1016/j.jeurceramsoc.2007.11.021
Ghaffari S.A., Faghihi-Sani M.A., Golestani-Fard F., Nojabayy M. // Int. J. Refract. Met. Hard Mater. 2013. V. 41. P. 180. https://doi.org/10.1016/j.ijrmhm.2013.03.009
Ghaffari S.A., Faghihi-Sani M.A., Golestani-Fard F., Ebrahimi S. // Ceram. Int. 2013. V. 39. P. 1985. https://doi.org/10.1016/j.ceramint.2012.08.050
Gaballa O., Cook B.A., Russell A.M. // Int. J. Refract. Metals. Hard Mater. 2013. V. 41. P. 293. https://doi.org/10.1016/j.ijrmhm.2013.04.018
Ghaffari S.A., Faghihi-Sani M.A., Golestani-Fard F., Mandal H. // J. Eur. Ceram. Soc. 2013. V. 33. P. 1479. https://doi.org/10.1016/j.jeurceramsoc.2013.01.017
Arianpour F., Golestanifard F., Rezaie H. et al. // Int. J. Refract. Met. Hard Mater. 2016. V. 56. P. 1. https://doi.org/10.1016/j.ijrmhm.2015.11.011
Zhou C., Qi Y., Cheng Y., Han W. // J. Mater. Eng. Performe. 2019. V. 28. № 1. P. 512. https://doi.org/10.1007/s11665-018-3807-7
Cedillos-Barraza O., Manara D., Boboridis K. et al. // Sci. Rep. 2016. V. 6. Article № 37962. https://doi.org/10.1038/srep37962
Savvatimskiy A.I., Onufriev S.V., Muboyadzhyan S.A. // J. Eur. Ceram. Soc. 2019. V. 39. P. 907. https://doi.org/10.1016/j.jeurceramsoc.2018.11.030
Mayrhofer P.H., Kirnbauer A., Ertelthaler Ph., Koller C.M. // Scripta Mater. 2018. V. 149. P. 93. https://doi.org/10.1016/j.scriptamat.2018.02.008
Peng C., Gao X., Wang M. et al. // Appl. Phys. Lett. 2019. V. 114. Article № 011905. https://doi.org/10.1063/1.5054954
Cedillos-Barraza O., Grasso S., Al Nasiri N. et al. // J. Eur. Ceram. Soc. 2016. V. 36. P. 1539. https://doi.org/10.1016/j.jeurceramsoc.2016.02.009
Feng L., Kim J.-M., Lee S.-H., Park S.-J. // J. Am. Ceram. Soc. 2016. V. 99. № 4. P. 1129. https://doi.org/10.1111/jace.14144
Zhang C., Gupta A., Seal S. et al. // J. Am. Ceram. Soc. 2017. P. 1. https://doi.org/10.1111/jace.14778
Zhang C., Loganathan A., Boesl B., Agarwal A. // Coatings. 2017. V. 7. Article № 111. https://doi.org/10.3390/coatings7080111
Zhang C., Boesl B., Agarwal A. // Ceram. Int. 2017. V. 43. P. 14798. https://doi.org/10.1016/j.ceramint.2017.07.227
Rezaei F., Ghassemi Kakroudi M., Shahedifar V., Pourmohammadie Vafa N. // Ceram. Int. 2017. V. 43. P. 15537. https://doi.org/10.1016/j.ceramint.2017.08.103
Shahedifar V., Ghassemi Kakroudi M. // Int. J. Refract Met. Hard Mater. 2018. V. 71. P. 15. https://doi.org/10.1016/j.ijrmhm.2017.10.025
Kurbatkina V.V., Patsera E.I., Levashov E.A., Timofeev A.N. // Ceram. Int. 2018. V. 44. P. 4320. https://doi.org/10.1016/j.ceramint.2017.12.024
Simonenko E.P., Ignatov N.A., Simonenko N.P. et al. // Russ. J. Inorg. Chem. 2011. V. 56. № 11. P. 1681. [Симоненко Е.П., Игнатов Н.А., Симоненко Н.П. и др. // Журн. неорган. химии. 2011. Т. 56. № 11. С. 1763.]https://doi.org/10.1134/S0036023611110258
Simonenko E.P., Simonenko N.P., Ezhov Yu.S. et al. // Phys. Atom. Nucl. 2015. V. 78. № 12. P. 1357. https://doi.org/10.1134/S106377881512011X
Jiang J., Wang S., Li W. // J. Am. Ceram. Soc. 2016. V. 99. P. 3198. https://doi.org/10.1111/jace.14436
Zhang J., Wang S., Li W. // Ceram. Int. 2019. V. 45. P. 1455. https://doi.org/10.1016/j.ceramint.2018.09.292
Foroughi P., Zhang C., Agarwal A., Cheng Z. // J. Am. Ceram. Soc. 2017. V. 100. № 11. P. 5056. https://doi.org/10.1111/jace.15065
Lu Y., Sun Y., Zhang T. et al. // J. Eur. Ceram. Soc. 2019. V. 39. P. 205. https://doi.org/10.1016/j.jeurceramsoc.2018.10.012
Simonenko E.P., Sevast’yanov D.V., Simonenko N.P. et al. // Russ. J. Inorg. Chem. 2013. V. 58. № 14. P. 1669. https://doi.org/10.1134/S0036023613140039
Simonenko E.P., Simonenko N.P., Gordeev A.N. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 11. P. 1484. [Симоненко Е.П., Симоненко Н.П., Гордеев А.Н. и др. // Журн. неорган. химии. 2018. Т. 63. № 11. С. 1465. https://doi.org/10.1134/Sp.0044457X1811017X]https://doi.org/10.1134/S0036023618110177
Simonenko E.P., Simonenko N.P., Gordeev A.N. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 10. P. 1345. [Симоненко Е.П., Симоненко Н.П., Гордеев А.Н. и др. // Журн. неорган. химии. 2018. Т. 63. № 10. С. 1329. https://doi.org/10.1134/S0044457X18100173]https://doi.org/10.1134/S0036023618100170
Simonenko E.P., Simonenko N.P., Gordeev A.N. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 4. P. 421. [Симоненко Е.П., Симоненко Н.П., Гордеев А.Н. и др. // Журн. неорган. химии. 2018. Т. 63. № 4. С. 393.]https://doi.org/10.1134/S0036023618040186
Simonenko E.P., Simonenko N.P., Papynov E.K. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 1. P. 1. [Симоненко Е.П., Симоненко Н.П., Папынов Е.К. и др. // Журн. неорган. химии. 2018. Т. 63. № 1. С. 3. https://doi.org/10.7868/S0044457X18010014]https://doi.org/10.1134/S0036023618010187
Kaufman L. // CALPHAD. 1991. V. 15. P. 243. https://doi.org/10.1016/0364-5916(91)90004-4
Frisk K., Fernandez Guillermet A. // J. Alloys Compd. 1996. V. 238. P. 167. https://doi.org/10.1016/0925-8388(96)02197-4
Benesovsky F., Rudy E. // Planseeberichte f. Pulvermetallurg. 1960. V. 8. P. 66.
Okamoto H. C-Hf (Carbon-Hafnium). Binary Alloy Phase Diagrams / Ed. Massalski T.B. Ohio: ASM International, Materials Park, 1990. V. 1. P. 849.
Sevast’yanov V.G., Simonenko E.P., Ignatov N.A. et al. // Inorg. Mater. 2010. V. 46. № 5. P. 495. [Севастьянов В.Г., Симоненко Е.П., Игнатов Н.А. и др. // Неорган. материалы. 2010. Т. 46. № 5. С. 563. https://doi.org/10.1134/S0002337X10050106]https://doi.org/10.1134/S0020168510050109
Hummel H.U., Fackler R., Remmert P. // Chem. Ber. 1992. V. 125. P. 551. https://doi.org/10.1002/cber.19921250304
Henderson S.J., Shebanova O., Hector A.L. et al. // Chem. Mater. 2007. V. 19. № 7. P. 1712. https://doi.org/10.1021/cm062864a
Fedorov T.F. Carbon-Hafnium-Tantalum Ternary Alloy Phase Diagram 1000C. in ASM Alloy Phase Diagrams Center, 2007.
Гусев А.И. // Журн. физ. химии. 1985. Т. 59. № 3. С. 579.
Спиридонов Ф.М., Муленкова М.Н., Цырельников В.И., Комиссарова Л.Н. // Журн. неорган. химии. 1981. Т. 26. С. 922.
Sevastyanov V.G., Simonenko E.P., Ignatov N.A. et al. // Russ. J. Inorg. Chem. 2011. V. 56. № 5. P. 661. [Севастьянов В.Г., Симоненко Е.П., Игнатов Н.А. и др. / Журн. неорган. химии. 2011. Т. 56. № 5. С. 707.]https://doi.org/10.1134/S0036023611050214
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


