Журнал неорганической химии, 2019, T. 64, № 2, стр. 201-205
Разбиение четырехкомпонентной взаимной системы Na,K||Cl,I,CrO4 и исследование ее стабильных элементов
Е. М. Егорова 1, *, С. С. Лихачева 1, И. К. Гаркушин 1
1 Самарский государственный технический университет
443100 Самара, ул. Молодогвардейская, 244, Россия
* E-mail: dvoryanova_kat@mail.ru
Поступила в редакцию 20.06.2017
После доработки 06.07.2018
Принята к публикации 16.05.2018
Аннотация
Исследование многокомпонентных солевых систем актуально в связи с широким применением нонвариантных смесей в качестве электролитических сред для выделения металлов, теплоаккумулирующих материалов. В работе проведено разбиение четырехкомпонентной взаимной системы Na,K||Cl,I,CrO4 на симплексы с использованием теории графов. Построено древо фаз системы, определены стабильные элементы. Методом дифференциального термического анализа исследован стабильный тетраэдр NaCl–KCl–KI–K2CrO4 системы Na,K||Cl,I,CrO4. В стабильном тетраэдре определены температура плавления (451°С) и содержание компонентов (экв. %) в четырехкомпонентной эвтектике (0.25% KCl + 42.40% NaCl + 30.92% KI + 26.43% K2CrO4).
ВВЕДЕНИЕ
Нонвариантные смеси на основе солей натрия, калия находят применение в качестве теплоаккумулирующих материалов, электролитов для химических источников тока и других функциональных материалов [1–5]. Информация о выявленных низкоплавких нонвариантных составах на основе солей щелочных металлов имеет также справочную ценность, так как пополняет базу данных о фазовых равновесиях в ранее не-исследованных конденсированных системах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
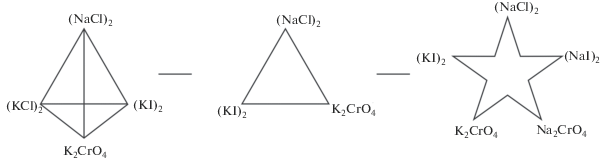
Объектом исследования является взаимная система Na,K||Cl,I,CrO4, схемы призмы составов и развертки которой представлены на рис. 1. Для изучения фазового комплекса четырехкомпонентной взаимной системы проведено разбиение на симплексы с применением теории графов [6]. Использован алгоритм разбиения полиэдров составов, разработанный авторами [7, 8] для физико-химических систем с точками нонвариантного равновесия и преобразованный в [9, 10] для систем, осложненных наличием твердых растворов различного типа. В качестве исходных данных использовали положение стабильных секущих элементов в системах меньшей размерности.
Рис. 1.
Схема призмы составов и схема развертки четырехкомпонентной взаимной системы Na,K||Cl,I,CrO4.
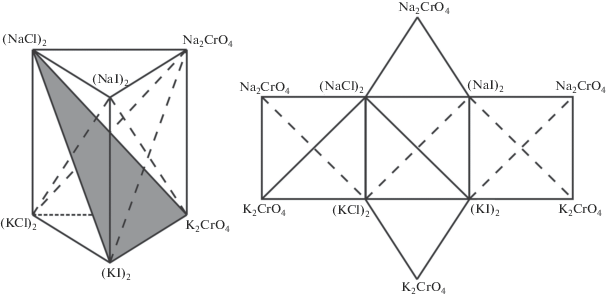
Матрица смежности четырехкомпонентной взаимной системы Na,K||Cl,I,CrO4 приведена в табл. 1. На основании данных таблицы составлено логическое выражение, представляющее собой произведение сумм индексов несмежных вершин.
Таблица 1.
Матрица смежности системы Na,K||Cl,I,CrO4
| Вещество | Индекс | X1 | X2 | X3 | X4 | X5 | X6 |
|---|---|---|---|---|---|---|---|
| NaCl | X1 | 1 | 1 | 1 | 1 | 1 | 1 |
| NaI | X2 | 1 | 1 | 0 | 1 | 1 | |
| Na2CrO4 | X3 | 1 | 0 | 1 | 1 | ||
| KCl | X4 | 1 | 1 | 1 | |||
| KI | X5 | 1 | 1 | ||||
| K2CrO4 | X6 | 1 |
Путем выписывания недостающих вершин для несвязанных графов получена совокупность симплексов:
I) X1X4X5X6 NaCl–KCl–KI–K2CrO4,
II) X1X2X3X5X6 NaCl–NaI–Na2CrO4–KI–K2CrO4.
Общие элементы каждой пары смежных симплексов образуют секущие элементы (стабильные треугольники), в нашем случае NaCl–KI–K2CrO4.
Древо фаз четырехкомпонентной взаимной системы представлено на рис. 2. Разбиение системы Na,K||Cl,I,CrO4 позволило определить, что четырехкомпонентная взаимная система состоит из стабильных тетраэдра и пентатопа, связанных стабильным секущим треугольником.
Экспериментальные исследования проводили методом дифференциального термического анализа (ДТА) на установке в стандартном исполнении. Использовали химические реактивы квалификации “х. ч.”: NaCl, KCl, KI, K2CrO4. Все исходные вещества предварительно обезвоживали, температуры плавления, полиморфного превращения (для K2CrO4 α ⇄ β 666°С) веществ соответствовали справочным данным [11, 12].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Развертка граневых элементов стабильного тетраэдра NaCl–KCl–KI–K2CrO4 и расположение политермического сечения jkl представлены на рис. 3. Данные по двух- и трехкомпонентным системам взяты из литературы: NaCl–KCl [13, 14], KCl–KI [13], KCl–K2CrO4 [14], KI–K2CrO4 [15, 16], KCl–KI–K2CrO4 [17], Na,K||Cl,I [18], Na,K||Cl,CrO4 [19]. Стабильный треугольник NaCl–KI–K2CrO4 исследован авторами [20]. Для определения характеристик эвтектической смеси в объеме кристаллизации иодида калия выбрано треугольное сечение j [70% KI + 30% NaCl] k [70% KI + 30% K2CrO4] l [70% KI + 30% KCl], в котором изучен политермический разрез YU (рис. 4). Запись кривых ДТА образцов составов, соответствующих сечению jkl, показала, что кристаллизация в тетраэдре заканчивается при температуре четырехкомпонентной эвтектики 451°C.
Рис. 3.
Развертка стабильного тетраэдра NaCl–KCl–KI–K2CrO4 и расположение политермического сечения jkl.
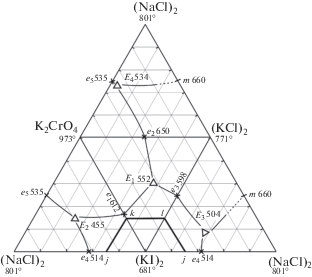
Рис. 4.
Треугольное сечение jkl и расположение разреза YU четырехкомпонентной системы NaCl–KCl–KI–K2CrO4.
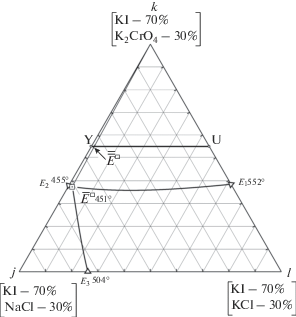
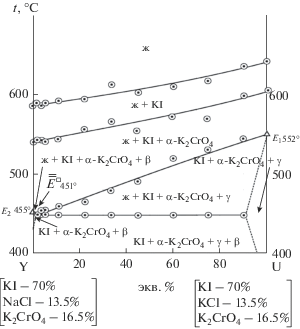
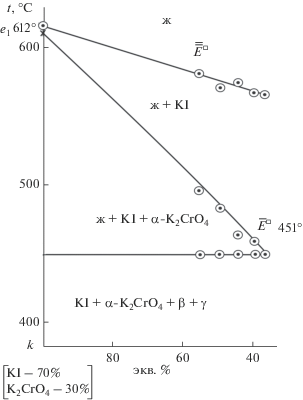
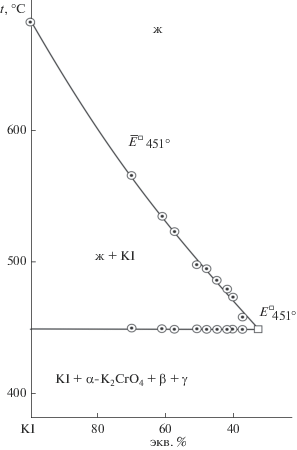
Т–х-диаграмма разреза YU представлена на рис. 5. При изучении данного разреза определено соотношение двух компонентов – хлоридов натрия и калия в четырехкомпонентной эвтектике, которое соответствует пересечению двух ветвей третичной кристаллизации и обозначено $\overline{\overline E} $◻ 451. В ходе изучения разреза, выходящего из вершины сечения k и проходящего через направление на проекцию четырехкомпонентной эвтектики $\overline{\overline E} $◻ 451, определено соотношение трех компонентов в четырехкомпонентной эвтектике – хлоридов калия, натрия и хромата калия (рис. 6). При дальнейшем изучении разреза, выходящего из вершины иодида калия и проходящего через проекцию на эвтектику $\overline Е $◻ 451 (рис. 7), определено содержание четвертого компонента – иодида калия в системе NaCl–KCl–KI–K2CrO4.
ЗАКЛЮЧЕНИЕ
В результате исследований установлено, что система относится к эвтектическому типу плавления. В эвтектике при температуре 451°С кристаллизуются 0.25% KCl + 42.40% NaCl + 30.92% KI + + 26.43% K2CrO4. Фазовые равновесия элементов стабильного тетраэдра представлены в табл. 2. Поскольку в двухкомпонентной ограняющей системе из хлоридов натрия и калия образуется непрерывный ряд твердых растворов с минимумом, в четырехкомпонентной эвтектике чистые фазы хлоридов натрия и калия не кристаллизуются. Эти фазы обозначены на рисунках: β – твердый раствор с большим содержанием хлорида натрия, γ – твердый раствор с большим содержанием хлорида калия.
Список литературы
Garkushin I.K., Gubanova T.V., Frolov E.I. et al. // Russ. J. Inorg. Chem. 2015. Т. 60. № 3. С. 324. [Гаркушин И.К., Губанова Т.В., Фролов Е.И. и др. // Журн. неорган. химии. 2015. Т. 61. № 1. С. 374.]
Ritchie A., Wilmont H. // J. Power Sources. 2006. V. 162. № 2. P. 809.
Химические источники тока. Справочник / Под ред. Коровина Н.В., Скундина А.М. М.: МЭИ, 2003. 740 с.
Garkushin I.K., Gubanova T.V., Sorokina E.I. // Russ. J. Inorg. Chem. 2013. V. 58. № 1. P. 96. [Гаркушин И.К., Губанова Т.В., Сорокина Е.И. // Журн. неорган. химии. 2013. Т. 58. № 1. С. 101.]
Chen F., Howlett P., Forsyth M. // J. Phys. Chem. 2013. V. 11. № 1. P. 105.
Сечной А.И., Гаркушин И.К., Трунин А.С. // Журн. неорган. химии. 1988. Т. 33. № 3. С. 752.
Сечной А.И., Гаркушин И.К., Трунин А.С. // Журн. неорган. химии. 1988. Т. 33. № 4. С. 1014.
Гаркушин И.К., Егорцев Г.Е., Истомова М.А. // Электрохимическая энергетика. 2009. Т. 9. № 2. С. 95.
Сечной А.И., Колосов И.Е., Гаркушин И.К. и др. // Журн. неорган. химии. 1990. Т. 35. № 4. С. 1001.
Kosmynin A.S., Garkushin I.K., Shter G.E. et al. // Thermochim. Acta. 1985. V. 93. P. 333.
Термические константы веществ. Справочник / Под ред. Глушко В.П. М.: ВИНИТИ, 1981. Вып. X. Ч. 1. 300 с.
Термические константы веществ. Справочник / Под ред. Глушко В.П. М.: ВИНИТИ, 1981. Вып. X. Ч. 2. 300 с.
Воскресенская Н.К., Евсеева Н.Н., Беруль С.И. и др. Справочник по плавкости систем из безводных неорганических солей. М.: Изд-во АН СССР, 1961. Т. 1. 845 с.
Посыпайко В.И., Алексеева Е.А. Диаграммы плавкости солевых систем. Ч. III. Двойные системы с общим катионом. М.: Металлургия, 1979. 204 с.
Игнатьева Е.О., Дворянова Е.М., Гаркушин И.К. Прогнозирование и экспериментальное исследование Т–х-диаграммы двухкомпонентной системы Na2CrO4–NaI // Тез. Докл. IХ Междунар. Курнаковского совещ. по физ.-хим. анализу. Пермь, 2010. С. 177.
Лихачева С.С., Дворянова Е.М. Фазовые равновесия в трехкомпонентной системе KCl–KI–K2CrO4 // Матер. 53 Международной научной студенческой конференции (МНСК-2015). Новосибирск. НГУ. Секция химия. С. 191.
Likhacheva S.S., Dvoryanova Е.М., Garkushin I.К. // Russ. J. Inorg. Chem. 2016. V. 61. № 1. P. 99. [Лихачева С.С., Дворянова Е.М., Гаркушин И.К. // Журн. неорган. химии. 2016. Т. 61. № 1. С. 105.]
Воскресенская Н.К., Евсеева Н.Н., Беруль С.И. и др. Справочник по плавкости систем из безводных неорганических солей. М.: Изд-во АН СССР, 1961. Т. 2. 585 с.
Кочкаров Ж.А., Гасаналиев А.М. // Изв. вузов. Химия и хим. технология. 2007. Т. 50. № 7. С. 89.
Dvoryanova Е.М., Likhacheva S.S., Garkushin I.К. et al. // Russ. J. Inorg. Chem. 2016. V. 61. № 10. P. 1321. [Дворянова Е.М., Лихачева С.С., Гаркушин И.К. и др. // Журн. неорган. химии. 2016. Т. 61. № 10. С. 1375.]
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии