Журнал неорганической химии, 2019, T. 64, № 2, стр. 196-200
Исследование системы FeS–PbS
У. А. Гасанова 1, О. М. Алиев 1, И. Б. Бахтиярлы 1, *, Ш. Г. Мамедов 1
1 Институт катализа и неорганической химии им. М. Нагиева НАН Азербайджана
Az1143 Баку, пр-т. Г. Джавида, 113, Республика Азербайджан
* E-mail: azxim@mail.ru
Поступила в редакцию 07.07.2017
После доработки 06.07.2018
Принята к публикации 20.04.2018
Аннотация
Система FeS–PbS изучена методами дифференциального термического, рентгенофазового и микроструктурного анализов и измерением микротвердости. Установлено, что система FeS–PbS является квазибинарным сечением и относится к эвтектическому типу. Координаты эвтектический точки: 45 мол. % PbS и Т = 1123 К. На основе исходных компонентов образуются узкие области растворимости.
ВВЕДЕНИЕ
Известно, что построение Т–х-фазовых диаграмм политермических сечений и проекции поверхности ликвидуса позволяет оптимизировать методики синтеза и выращивания монокристаллов. Система FeS–PbS изучена неоднократно [1–18], но данные авторов разнятся. Поэтому мы исследовали систему FeS–PbS заново.
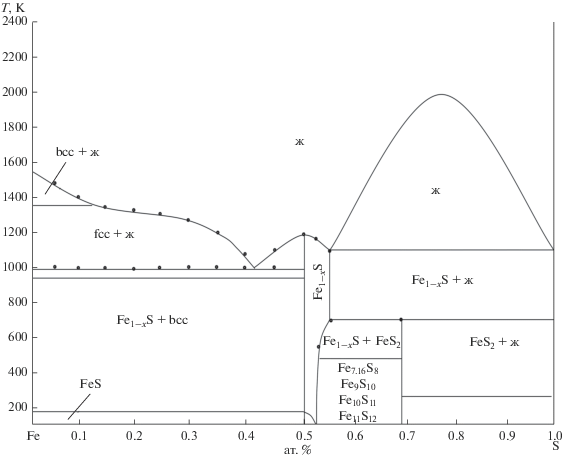
Система Fe–S также изучалась разными авторами [1, 2, 7, 16–18], однако построенные диаграммы состояния отличаются друг от друга. Наиболее приемлемой можно считать диаграмму системы Fe–S [9], для которой были учтены предыдущие исследования. По данным [9], в системе Fe–S кроме соединений FeS и FeS2 образуется ряд нестехиометрических фаз с общей формулой Fe1 –хS (рис. 1).
По данным [9–11], соединение FeS плавится конгруэнтно при 1460 К и имеет две низкотемпературные модификации с температурными переходами при 558 и 411 К [1, 2]. Соединение FeS кристаллизуется в гексагональной сингонии типа NiAs [10, 11] с параметрами элементарной ячейки a = 3.460, с = 5.681 Å, пр. гр. P63/mmc-D$\frac{4}{{6h}}.$
Соединение PbS плавится конгруэнтно при 1370 К [11] и кристаллизуется в кубической сингонии типа NaCl с параметром элементарной ячейки а = 5.935 Å, пр. гр. Fm3m. По данным [14, 15], PbS – полупроводник с шириной запрещенной зоны ∆Е = 0.42 эВ.
Квазибинарная система FeS–PbS была исследована в [19–24], однако построенные диаграммы состояния не дают полной картины фазовых равновесий и не соответствуют друг другу. Следует отметить, что во всех работах систему FeS–PbS относят к эвтектическому типу, однако ни в одной работе не приводятся данные о растворимости на основе исходных сульфидов FeS и PbS и фазовом переходе FeS. Кроме того, кривые ликвидуса системы FeS–PbS не могут быть прямолинейными, как указано в [21].
Цель настоящей работы – заново изучить фазовые равновесия в системе FeS–PbS и построить ее Т–х-диаграмму состояния.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Сульфид свинца (PbS) получали взаимодействием особо чистых элементов (Pb – 99.999%, S – 99.9999%) при температуре 1350–1400 K в толстостенных кварцевых ампулах, вакумированных до остаточного давления (≈0.1 Па). После окончания синтеза образцы PbS гомогенизировали при 1100 К в течение недели. Установлено, что PbS имеет кубическую структуру с а = 5.934 Å, что хорошо согласуется с данными [11]. FeS также синтезировали из особо чистых элементов (железо восстановленное, сера марки В-4) в вакуумированных кварцевых ампулах (≈0.1 Па). По данным рентгенофазового анализа (РФА), получена фаза сульфида железа, кристаллизующаяся в гексагональной сингонии с параметрами элементарной ячейки а = 5.965, с = 11.757 Å, z = 12, ρ = 4.84 г/см3, которые согласуются с данными [25]. Расчетные данные системы FeS–PbS представлены в табл. 1.
Таблица 1.
Расчет рентгенограмм FeS
| 2θ, град | dэксп | I/I0, % | hkl |
|---|---|---|---|
| 17.176 | 5.15858 | 3.2 | 100 |
| 18.752 | 4.72840 | 3.5 | 101 |
| 29.894 | 2.98650 | 75.4 | 110 |
| 30.436 | 2.93453 | 4.6 | 004 |
| 33.655 | 2.66088 | 75.3 | 112 |
| 35.491 | 2.52734 | 13.0 | 201 |
| 41.795 | 2.15953 | 6.9 | 203 |
| 42.230 | 2.13830 | 2.8 | 105 |
| 43.224 | 2.09139 | 100 | 114 |
| 46.469 | 1.95262 | 3.0 | 210 |
| 47.067 | 1.92920 | 8.6 | 211 |
| 52.284 | 1.74830 | 6.4 | 213 |
| 53.057 | 1.72463 | 21.1 | 300 |
| 56.143 | 1.63694 | 1.3 | 116 |
| 56.523 | 1.62682 | 2.6 | 214 |
| 61.632 | 1.50366 | 2.7 | 215 |
| 63.262 | 1.46878 | 2.3 | 008 |
| 64.295 | 1.44766 | 1.9 | 222 |
| 65.545 | 1.42304 | 1.6 | 311 |
| 69.839 | 1.34569 | 0.6 | 313 |
| 70.708 | 1.33129 | 7.4 | 224 |
Тройные сплавы, богатые FeS (> 70 мол. % FeS), синтезировали в двойных толстостенных кварцевых ампулах, так как из-за теплового расширения элементарной ячейки при охлаждении они часто растрескиваются. Максимальная температура синтеза составляла 1475 К (3 ч). Синтез продолжался не менее 8 ч. В жидком состоянии сплавы периодически перемешивали. После 40-минутного выдерживания при максимальной температуре (1475 К) образцы охлаждали со скоростью 60–65 град/ч до 1050 К и после этого закаляли в ледяной воде. Затем сплавы помещали в другую ампулу и после откачки воздуха отжигали при температуре 975–1050 К в течение недели.
Исследование сплавов проводили методами дифференциального термического (ДТА, НТР-73, хромель-алюмелевая термопара, скорость нагрева 7–10 град/мин, эталон – прокаленный Al2O3), рентгенофазового (CuКα-излучение, прибор – D2 Phaser) и микроструктурного (МСА, ПМТ-3) анализов. Травление осуществляли хромовой смесью состава (0.5 г K2Cr2O7 + 5 мл H2SO4(конц) + + 20 мл H2O). Погрешность в определении температуры плавления образцов составляла ±2К. Погрешность измерения микротвердости не превышала 3–4%, а точность вычисления параметров элементарной ячейки – ±0.001 Å.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По разрезу FeS–PbS был синтезирован 21 сплав в интервале концентрации 0–100 мол. % PbS (табл. 2). Синтез проводили из бинарных сульфидов визуально-комбинированным методом при 1350–1475 К, с последующим вибрационным перемешиванием. По предварительным результатам ДТА выбирали режим отжига; сплавы после синтеза гомогенизировали при 1050 К в течение 200 ч. Равновесие сплавов контролировали методами МСА и РФА. Литые отожженные сплавы изучали методами ДТА, РФА, МСА и измерением микротвердости.
Таблица 2.
Результаты ДТА, РФА и определения микротвердости сплавов системы FeS–PbS
| Состав, мол. % PbS | Термические эффекты, К | Микротвердость, MПa | Фазовый состав | |
|---|---|---|---|---|
| температура солидуса | температура ликвидуса | |||
| 0.0 | – | 1463 | 2500 | γ (FeS) |
| 1.0 | 430, 615, 1430 | 1460 | 2700 | γ (однофазный) |
| 3.0 | 420, 600, 1400 | 1470 | 2700 | α + γ' |
| 5.0 | 410, 570, 1350 | 1450 | – | α + γ' |
| 10 | 410, 560, 1123 | 1430 | 2700 | α + γ' |
| 15 | 410, 560, 1123 | 1420 | – | α + γ' |
| 20 | 410, 560, 1123 | 1370 | 2700 | α + γ' |
| 25 | 405, 560, 1140 | 130 | 2700 | α + γ' |
| 30 | 410, 560, 1123 | 1330 | 2700 | α + γ' |
| 35 | 408, 550, 1115 | 1230 | – | α + γ' |
| 40 | 410, 560, 1123 | 1150 | – | α + γ' |
| 45 | 410, 560, 1123 | – | Эвтектика | α + γ' |
| 50 | 410, 560, 1123 | 1160 | – | – |
| 55 | 410, 560, 1123 | 1225 | –7400 | α + γ' |
| 60 | 410, 560, 1123 | 1240 | – | – |
| 65 | 410, 1123 | 1270 | –7400 | – |
| 70 | 410, 1123 | 1300 | – | α + γ' |
| 80 | 410, 1123 | 1350 | –7400 | α + γ' |
| 90 | 410, 1123 | 1380 | –7400 | α + γ' |
| 99 | 1290 | 1388 | –7400 | γ' (однофазный) |
| 100 | – | 1388 | –7200 | PbS |
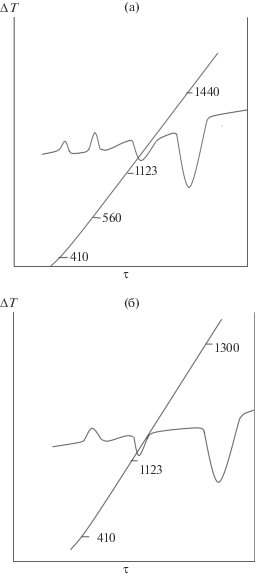
Результаты термического анализа показали, что изотермические эффекты наблюдаются на термограммах сплавов в интервале 0–70 мол. % PbS при 411 и 560 К, что, по всей вероятности, связано с полиморфным переходом α-FeS ↔ β-FeS. Термические эффекты полиморфного перехода β-FeS ↔ γ-FeS в интервале концентраций 60–98 мол. % PbS не обнаружены (рис. 2).
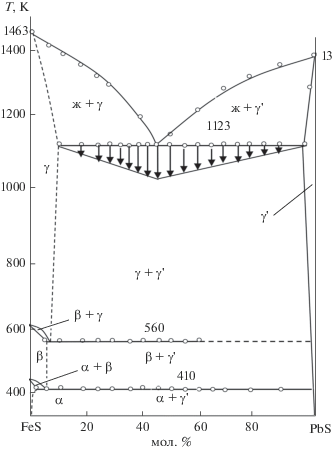
Диаграмма состояния системы FeS–PbS, построенная по полученным экспериментальным данным, приведена на рис. 3, из которого видно, что система является квазибинарным сечением и относится к эвтектическому типу.
Ликвидус системы состоит из двух ветвей первичной кристаллизации фаз γ (твердый раствор на основе γ-FeS) и γ' (твердый раствор на основе сульфида свинца). Ветви первичной кристаллизации γ- и γ'-фаз пересекаются в эвтектической точке с координатами 45 мол. % PbS и Т = 1123 К. Состав, отвечающий эвтектической точке, уточнен построением треугольника Таммана. На основе исходных компонентов образуются ограниченные области твердых растворов, доходящие до 2.0 мол. % при комнатной температуре. Причина образования ограниченной области твердых растворов в системе FeS–PbS, по-видимому, связана с различием атомных и ионных радиусов Fe(II) и Pb(II), а также с разными кристаллическими структурами FeS и PbS.
Сравнение атомных (Fe и Pb – 1.26 и 1.75 Å соответственно) и ионных (Fe2+ = 0.86 Å, Pb2+ = 1.16 Å) радиусов показывает, что атомные радиусы различаются на 28%, а ионные – на 25.86%. В результате образуются узкие области растворимости на основе сульфидов железа и свинца.
Образование ограниченных областей растворимости на основе FeS и PbS подтверждается данными измерения микротвердости и рентгенофазового анализа. При измерении микротвердости сплавов получено два ряда значений (2500–2700 и 7200–7400 МПа), относящихся к микротвердости твердых растворов: γ – на основе FeS и γ' – на основе PbS.
Следует отметить, что сплавы, содержащие более 50 мол. % FeS, хрупкие, не поддаются шлифовке и легко окисляются на воздухе.
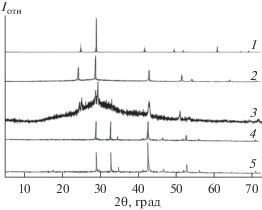
Результаты РФА (рис. 4) полностью согласуются с данными ДТА и МСА. Рентгенограмма сплава, содержащего 1.0 мол. % PbS и 2.0 мол. % FeS, полностью совпадает с рентгенограммой исходных сульфидов, что еще раз подтверждает образование узкой области растворимости на основе FeS и PbS. Параметр кубической решетки γ' твердых растворов, содержащих 2 мол. % FeS, составляет а = 5.926 Å (у чистого PbS а = 5.934 Å), а параметры элементарной ячейки FeS с ростом содержания PbS увеличиваются (а = 5.965–5.982, с = 11.757–11.762 Å).
ЗАКЛЮЧЕНИЕ
Построена Т–х-диаграмма состояния системы FeS–PbS, установлено, что она квазибинарная и относится к эвтектическому типу. Координаты эвтектической точки: 55 мол. % FeS–45 мол. % PbS, Т = 1123 К. На основе сульфида железа растворимость составляет 1.0 мол. % PbS, а на основе PbS – 2 мол. % FeS.
Список литературы
Кубашевски О. Диаграммы состояния двойных систем на основе железа / Пер. с англ. под ред. Петровой Л.А. М.: Металлургия, 1985. 184 с.
Kubaschewcki O. // ASM International / Ed. Komoto H.O. 1993. P. 364.
Gronvold F., Stolen S. // J. Chem. Thermodyn. 1992. V. 24. P. 913.
Bale C.W., Toguri J.M. // Canad. Metall. 1976. V. 15. № 1. P. 305.
Arnold R.G. // Econ. Geol. 1971. V. 66. P. 1121.
Moh.G.H., Kullerud E. Phase Relations at Low Temperatures: The Fe–S System. Carnegie Inst. Washington, 1964. V. 63. № 1. P. 207.
Kanda M., Hasegawa N., Itagaki K., Yazawa A. // Termochim. Acta. 1986. V. 109. № 1. P. 271.
Cудавцова В.С., Шаркина Н.О., Кудин В.Г. // Журн. физ. химии. 2001. Т. 75. № 4. С. 1061.
Walder P., Pelton A.D. // J. Phase Eguilibria Diffusion. 2005. V. 26. № 1. P. 23.
Sharma R., Lin J., Chang Y. // Metall. Trans. 1987. V. 18B. № 1. P. 237.
Самсонов Г.В., Дроздова С.В. Сульфиды. М.: Металлургия, 1972. 304 с.
Комарова Т.Н. // Изв. физ.-хим. Ин-та при Иркутск. ун-те. 1986. Т. 27. № 1. С. 23.
Xiu Zhilang, Liu Suwen, Xu Fengxin // J. Alloys Compd. 2008. V. 457. № 1–2. P. 9.
Власенко О.И., Левицкий С.М., Крисков Ц.А. // Физика и химия твердого тела. 2006. Т. 7. № 4. С. 660.
Угай Я.А. Введение в химию полупроводников М.: Высш. школа, 1975. 302 с.
Tikdogan E.T. // Trans. AIME. 1968. V. 242. P. 1665.
Ban-ya S., Chipman J. // Trans. AIME. 1968. V. 242. P. 940.
Mehrotra G.M., Wagner J.B. // Proc. Electrochem. Soc.1986. V. 86. P. 150.
Avetisyan K.K., Gnatishenko G.I. // Izv. Akad. Nauk Kaz. SSR. Ser. Gorn. Dela Met. Stroit. Stroim. 1956. № 6. P. 11.
Eriç H., Timuçin M. // Metallurg. Trans. B. 1981. V. 12B. P. 493.
Dutrizac J.E. // Can. J. Chem. 1980. V. 58. P. 739.
Hannu Johto, Pekka Takinen // J. Miner. Met. Mater. Soc. 2012. V. 51. P. 205.
Johto H., Taskinen P. // Proc. of the EMC. June 26–29, 2011. Düsseldorf, 2011. P. 1127.
Vargas M.B. // Metallurgia. 1979. V. 31. P. 131.
Skala R., Cisarova I., Drabek M. // Am. Mineral. 2006. V. 91. P. 917.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии