Журнал неорганической химии, 2019, T. 64, № 3, стр. 237-242
Синтез и строение фосфатов циркония и металлов (Ni, Cu, Co, Mn) в степени окисления +2
Е. А. Асабина 1, П. А. Майоров 1, В. И. Петьков 1, А. М. Ковальский 2, Е. Ю. Боровикова 3
1 Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр-т Гагарина, 23, Россия
2 Национальный исследовательский технологический университет “Московский институт стали и сплавов”,
119991 Москва, Ленинский пр-т, 4, Россия
3 Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
Поступила в редакцию 23.03.2018
После доработки 15.08.2018
Принята к публикации 23.04.2018
Аннотация
Изучено фазоообразование и строение фосфатов в системах M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = Co, Mn; M' = Ni, Cu; 0 ≤ х ≤ 2). Методами рентгенографии, электронной микроскопии, микрозондового анализа и ИК-спектроскопии изучено фазообразование сложных фосфатов, полученных золь-гель методом. Установлено образование в изученных системах ограниченных твердых растворов, кристаллизующихся в структурном типе Sc2(WO4)3. Выявлены закономерности изменения их кристаллографических характеристик от химического состава. Кристаллическая структура фосфата Mn1.2Ni0.7Zr1.3(PO4)3 уточнена методом Ритвельда по данным порошковой рентгенографии (пр. гр. P21/n, Z = 4, a = 8.8317(13), b = 8.9350(11), c = 12.4893(17) Å, β = 90.027(26)°, V = 985.55(23) Å3). Полученные данные об образовании твердых растворов M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = Co, Mn; M' = Ni, Cu) расширяют картину фазообразования известных фосфатов с октаэдро-тетраэдрическими каркасами типа {[L2(PO4)3]p–}3∞ и характеризуют общие тенденции зависимости строения фосфатов и пределов протяженности твердых растворов от разменного фактора.
ВВЕДЕНИЕ
Ортофосфаты структурных типов NaZr2(PO4)3 (NZP) [1] и Sc2(WO4)3 (SW) [2] изучаются в связи с их химической, термо-, радиационной стойкостью и регулируемым, в том числе ультрамалым, тепловым расширением. Кристаллическая структура таких соединений базируется на каркасе {[L2(PO4)3]p–}3∞, образованном объединением по вершинам LO6-октаэдров и PО4-тетраэдров. В зависимости от соединения этих фрагментов каркаса в каждом структурном типе полости заселяются катионами или остаются вакантными. Как правило, позиции каркаса заселяют небольшие по размеру высокозарядные катионы (в степенях окисления +4, +3) с преимущественно ковалентным характером связи металл–кислород. Полости структуры типа NZP с КЧ позиций 6 и 8 наиболее часто занимают низкозарядные катионы (+1, +2) средних и больших ионных радиусов. Полости структуры SW-типа могут быть заселены ионами средних и небольших радиусов, склонными к тетраэдрической координации.
Каркасные фосфаты, включающие металлы в степени окисления +2, представляют особый интерес в качестве материалов с широкими возможностями изоморфных замещений и регулирования физических свойств [3, 4]. Наиболее подробно исследовано фазообразование, строение и свойства двойных фосфатов M0.5L2(PO4)3, в которых позиции каркаса L занимают катионы Ti4+ и Zr4+, а позиции полостей M – металлы в степени окисления +2: Ni, Cu, Mg, Co, Mn, Cd, Ca, Sr, Ba [5–11]. Ранее нами изучена возможность вхождения катионов в степени окисления +2 одновременно в позиции каркаса и полостей структуры на примере твердых растворов M0.5 +xM'xZr2 –x(PO4)3 (M = = Co, Mn, Cd, Ca, Sr, Pb, Ba; M' = Mg, Co, Mn) [12–15]. В рамках настоящей работы продолжено систематическое исследование новых изоформульных рядов.
Цель работы – изучение фазоообразования и строения фосфатов в системах M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = Co, Mn; M' = Ni, Cu; 0 ≤ х ≤ 2).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Фосфаты M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = Co, Mn; M' = Ni, Cu; 0 ≤ х ≤ 2) синтезировали золь-гель методом с последующей термообработкой. Использовали следующие исходные реагенты марки “х. ч.”: CdO, MgO, CuO, Sr(NO3)2, Mn(CH3COO)2 ⋅ 4H2O, CoCl2 ⋅ 6H2O, NiCl2 ⋅ 6H2O, Pb(NO3)2, ZrOCl2 ⋅ 8H2O, NH4H2PO4. Оксиды кадмия, магния и меди предварительно растворяли в азотной кислоте, остальные реактивы – в дистиллированной воде. К стехиометрической смеси водных растворов солей металлов при перемешивании добавляли раствор дигидрофосфата аммония, взятый также в соответствии со стехиометрией фосфата. Реакционную смесь сушили при 90°С, затем диспергировали и подвергали ступенчатому отжигу при температурах 600–800°С. Отжиг чередовали с диспергированием. Рентгенофазовый анализ образцов проводили после каждой стадии отжига.
Рентгенографические исследования проводили на дифрактометре Shimadzu XRD-6000. Порошковые рентгенограммы записывали в CuKα (λ = 1.54178 Å) фильтрованном излучении в диапазоне углов 2θ от 10° до 60° с шагом сканирования 0.02°.
Рентгенограмму образца Mn1.2Ni0.7Zr1.3(PO4)3 для структурных исследований записывали в интервале углов 2θ 10°–94° с шагом 0.02° и временем выдержки в точке 15 с. Уточнение структуры фосфата проводили методом Ритвельда [16] с использованием программы Rietan-97 [17]. Аппроксимирование профилей пиков осуществляли согласно модифицированной функции псевдо-Войта (Mod-TCH pV [18]).
ИК-спектры синтезированных соединений записывали на спектрофотометре FTIR-8400 с приставкой ATR при комнатной температуре в диапазоне волновых чисел 1400−400 см–1. Образцы готовили методом осаждения тонкодисперсных пленок на подложке из KBr.
Для контроля химического состава и однородности образцов применяли электронный микрозондовый анализ. Исследования проводили на сканирующем электронном микроскопе JEOL JSM-7600F с термополевой электронной пушкой (катод Шоттки). Микроскоп оснащен системой микроанализа – энергодисперсионным спектрометром OXFORD X-Max 80 (Premium) с полупроводниковым кремний-дрейфовым детектором. Точность определения элементного состава образцов составляла 2.5 мол. %.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Согласно результатам рентгенографии и ИК-спектроскопии, в приведенных рядах фосфатов образуются ограниченные твердые растворы структурного типа SW.
Однофазные фосфаты состава Mn0.5 + xNixZr2 ‒ x(PO4)3, согласно рентгенографическим данным (рис. 1а), образуются при 0 ≤ x ≤ 0.7. В системе Mn0.5 + xCuxZr2 – x(PO4)3 твердые растворы структурного типа SW получены в интервале 0 ≤ x ≤ 0.2.
Рис. 1.
Рентгенограммы (а) и ИК-спектры (б) фосфатов Mn0.5 + xNixZr2 – x(PO4)3. Знаком 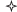 обозначены примеси.
обозначены примеси.
В системах Co0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M' = Ni, Cu) однофазные фосфаты получены при x = 0 и 0.1. Образцы составов с х > 0.1 содержали примеси фосфатов кобальта и никеля (меди).
Температура синтеза всех указанных фосфатов составляла 700°C. Рентгенограммы образцов проиндицированы в моноклинной сингонии в рамках пр. гр. P21/n.
ИК-спектры всех однофазных образцов подобны по форме и положению полос поглощения и характерны для фосфатов структурного типа вольфрамата скандия с пр. гр. P21/n (рис. 1б). Полосы поглощения в области 1270–1000 см–1 относятся к валентным асимметричным колебаниям νas, полосы при 970−930 см–1 – к валентным симметричным колебаниям νs ионов PO43–. В области 650−500 см–1 наблюдаются деформационные асимметричные колебания δas. Полосы при волновых числах ниже 500 см–1 соответствуют деформационным симметричным колебаниям δs.
Результаты электронной микроскопии и микрозондового анализа подтвердили гомогенность и химический состав синтезированных твердых растворов.
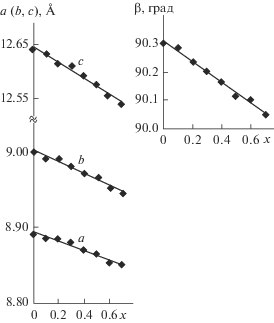
Из приведенной на рис. 2 зависимости кристаллографических характеристик твердых растворов Mn0.5 + xNixZr2 – x(PO4)3 от их химического состава видно, что с ростом х наблюдается закономерное уменьшение параметров ячейки а, b и с (а также угла моноклинности β). Уменьшение размеров ячейки связано с замещением ионов Zr4+ на небольшие ионы Ni2+ в каркасе структуры. При этом ионный радиус катионов Mn2+ невелик, чтобы рост заселенности полостей мог повлиять на размер элементарной ячейки.
Для выявления распределения катионов в степени окисления +2 в кристаллографических позициях структуры исследовано строение тройного фосфата Mn1.2Ni0.7Zr1.3(PO4)3 (х = 0.7) и установлено, что он кристаллизуется в структурном типе вольфрамата скандия.
Уточнение кристаллической структуры проведено методом Ритвельда по данным порошковой рентгенографии. В качестве исходной модели использовали координаты атомов в структуре CoMn0.5Zr1.5(PO4)3 [14]. Условия съемки и основные данные по уточнению приведены в табл. 1. Уточнение структуры проводили путем постепенного добавления уточняемых параметров при постоянном графическом моделировании фона. На рис. 3 показаны экспериментальная, вычисленная и штрих-рентгенограммы изученного фосфата. Наблюдается хорошее совпадение экспериментальной и вычисленной рентгенограмм. В уточненной модели получены положительные изотропные тепловые параметры В для всех атомов (табл. 2).
Таблица 1.
Условия съемки, параметры кристаллической решетки и результаты уточнения кристаллической структуры Mn1.2Ni0.7Zr1.3(PO4)3
| Пр. гр. | P21/n (№ 14) |
| Z | 4 |
| Интервал углов 2θ, град | 10.00−94.00 |
| Параметры ячейки: | |
| a, Å | 8.8317(13) |
| b, Å | 8.9350(11) |
| c, Å | 12.4893(17) |
| β, град | 90.027(26) |
| V, Å 3 | 985.55(23) |
| Число отражений | 889 |
| Число уточняемых параметров* | 22 + 76 |
| Факторы достоверности, %: | |
| Rwp; Rp | 3.87; 3.01 |
| S | 2.40 |
Рис. 3.
Экспериментальная (1), вычисленная (2) и разностная (3) рентгенограммы фосфата Mn1.2Ni0.7Zr1.3(PO4)3. Штрихами (4) показаны положения брегговских рефлексов.
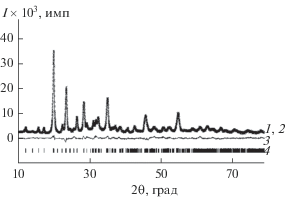
Таблица 2.
Координаты и изотропные тепловые параметры атомов в структуре Mn1.2Ni0.7Zr1.3(PO4)3
| Атом* | x | y | z | B, Å2 |
|---|---|---|---|---|
| Mn(1) | 0.7109(5) | 0.2311(4) | 0.1705(5) | 1.66(5) |
| Mn(2)** | 0.4383(8) | 0.1471(6) | 0.3134(5) | 1.89(7) |
| Zr(1) | 0.2521(4) | 0.0258(5) | 0.1269(3) | 1.12(5) |
| Ni/Zr(2)*** | 0.7462(6) | 0.0288(5) | 0.3906(7) | 1.33(5) |
| P(1) | 0.4597(7) | 0.2561(8) | 0.5033(8) | 2.97(8) |
| P(2) | 0.3974(7) | 0.3802(6) | 0.1427(8) | 2.04(7) |
| P(3) | 0.8867(8) | 0.3970(7) | 0.3564(7) | 2.62(9) |
| O(1) | 0.5712(8) | 0.3308(7) | 0.5772(9) | 2.78(11) |
| O(2) | 0.3534(8) | 0.1716(9) | 0.5693(9) | 2.73(10) |
| O(3) | 0.3829(8) | 0.3556(9) | 0.4262(9) | 1.25(8) |
| O(4) | 0.5587(7) | 0.1472(8) | 0.4351(7) | 2.26(11) |
| O(5) | 0.3764(6) | 0.2087(7) | 0.1692(8) | 1.66(9) |
| O(6) | 0.3457(9) | 0.4251(6) | 0.0315(7) | 1.23(8) |
| O(7) | 0.5608(7) | 0.4029(9) | 0.1631(8) | 2.19(10) |
| O(8) | 0.3162(8) | 0.4835(9) | 0.2267(7) | 1.56(9) |
| O(9) | 0.8279(8) | 0.2422(8) | 0.3354(6) | 1.44(9) |
| O(10) | 0.0510(7) | 0.3896(8) | 0.3691(5) | 1.75(10) |
| O(11) | 0.8101(7) | 0.4487(6) | 0.4616(9) | 1.54(8) |
| O(12) | 0.8341(6) | 0.5157(6) | 0.2683(8) | 1.39(9) |
В структуре фосфата Mn1.2Ni0.7Zr1.3(PO4)3 имеется два типа октаэдрически координированных каркасных позиций: одна заселена катионами Zr4+, а в другой статистически распределяются близкие по размерам катионы Zr4+ (r = 0.72 Å) и Ni2+ (r = 0.69 Å). Позиции тетраэдрически координированных полостей заняты ионами Mn2+ (r = = 0.66 Å).
Значения межатомных расстояний (табл. 3) в координационных полиэдрах, формирующих кристаллическую структуру изученного фосфата, согласуются с литературными данными [10–15, 19] для других фосфатов с октаэдро-тетраэдрическими каркасами. Расчет длин связей показывает, что в исследованной низкосимметричной моноклинной структуре наблюдается достаточно заметная деформация каркасообразующих полиэдров. Так, разброс межатомных расстояний в октаэдрах находится в интервале 1.96–2.15 Å, а диапазон длин связей Р–О в РО4-тетраэдрах составляет от 1.46 до 1.60 Å.
Таблица 3.
Основные межатомные расстояния в структурообразующих полиэдрах Mn1.2Ni0.7Zr1.3(PO4)3
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Mn(1)–O(2) | 1.984(10) | P(1)–O(2) | 1.460(12) |
| Mn(1)–O(7) | 2.030(8) | P(1)–O(3) | 1.476(13) |
| Mn(1)–O(12) | 2.109(7) | P(1)–O(1) | 1.506(12) |
| Mn(1)–O(9) | 2.306(9) | P(1)–O(4) | 1.561(11) |
| Mn(2)–O(4) | 1.855(10) | P(2)–O(7) | 1.479(9) |
| Mn(2)–O(5) | 1.961(11) | P(2)–O(6) | 1.516(13) |
| Mn(2)–O(3) | 2.386(11) | P(2)–O(8) | 1.571(11) |
| Mn(2)–O(12) | 2.542(9) | P(2)–O(5) | 1.579(9) |
| Zr(1)–O(8) | 1.962(9) | P(3)–O(10) | 1.461(9) |
| Zr(1)–O(5) | 2.038(8) | P(3)–O(9) | 1.501(10) |
| Zr(1)–O(3) | 2.043(9) | P(3)–O(11) | 1.548(13) |
| Zr(1)–O(10) | 2.123(8) | P(3)–O(12) | 1.597(11) |
| Zr(1)–O(11) | 2.139(11) | ||
| Zr(1)–O(1) | 2.140(8) | ||
| Ni/Zr(2)–O(6) | 2.010(11) | ||
| Ni/Zr(2)–O(4) | 2.042(9) | ||
| Ni/Zr(2)–O(2) | 2.057(9) | ||
| Ni/Zr(2)–O(12) | 2.111(12) | ||
| Ni/Zr(2)–O(7) | 2.150(9) | ||
| Ni/Zr(2)–O(9) | 2.152(9) |
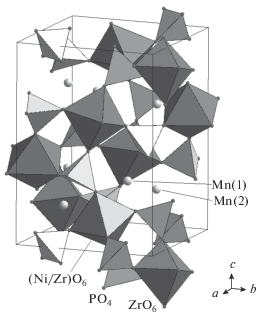
Фрагмент кристаллической структуры Mn1.2Ni0.7Zr1.3(PO4)3 представлен на рис. 4. Ее основу составляет каркас, в котором можно выделить обособленные группировки из двух разных типов октаэдров и трех РО4-тетраэдров. Колонки октаэдро-тетраэдрических группировок ориентированы поочередно в двух непересекающихся направлениях. Катионы Mn2+ располагаются в тетраэдрически координированных полостях структуры типа вольфрамата скандия.
Результаты по фазообразованию в рядах M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = Co, Mn; M' = Ni, Cu) сопоставлены с исследованными ранее аналогичными системами, включающими в позиции каркаса M' = Mg, Co, Mn [20] (табл. 4). Известно, что каркас структуры {[L2(PO4)3]p-}3∞ в определенных пределах может адаптироваться к расположенным в его полостях катионам М2+ различного размера [20]. Так, исследованные в работе фосфаты содержат в октаэдрически координированных позициях каркаса близкие по размерам ионы Zr4+ и M'2+. Включение в полости сравнительно небольших (сопоставимых по размеру с каркасобразующими ионами) катионов в степени окисления +2 обусловливает кристаллизацию этих фосфатов в структуре типа вольфрамата скандия.
Таблица 4.
Концентрационные пределы существования твердых растворов структурного типа SW в системах M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3
| M | M' | Пределы х |
|---|---|---|
| Co | Ni Mg Cu Co |
0 ≤ х ≤ 0.1 0 ≤ х ≤ 0.1 0 ≤ х ≤ 0.1 х = 0 |
| Mn | Ni Mg Cu Co Mn |
0 ≤ х ≤ 0.7 0 ≤ х ≤ 1.0 0 ≤ х ≤ 0.2 х = 0 0 ≤ х ≤ 0.35 |
С уменьшением размера катионов, занимающих полости структуры (от Mn2+ до Co2+), SW-структура становится менее устойчивой, что приводит к снижению границ х образования твердых растворов. При этом крайние члены рядов с x = 0 (M0.5Zr2(PO4)3) устойчивы, однако введение катиона в степени окисления +2 в каркас дестабилизирует структуру еще сильнее и твердые растворы в рядах Co0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 образуются лишь в очень узких пределах.
ЗАКЛЮЧЕНИЕ
Полученные результаты, касающиеся образования твердых растворов M0.5 +x${\text{M}}_{x}^{'}$Zr2 –x(PO4)3 (M = = Co, Mn; M' = Ni, Cu), расширяют картину фазообразования известных фосфатов с октаэдро-тетраэдрическими каркасами типа {[L2(PO4)3]p–}3∞ и характеризуют общие тенденции зависимости строения фосфатов и пределов протяженности твердых растворов от разменного фактора.
Список литературы
Hagman L.O., Kierkegaard P. // Acta Chem. Scand. 1968. V. 22. P. 1822. doi 10.3891/acta.chem.scand.22-1822
Ефремов B.A., Лазоряк Б.И., Трунов B.K. // Кристаллография. 1981. Т. 26. С. 72.
Pet’kov V.I., Asabina E.A., Sukhanov M.V. et al. // Chem. Eng. Trans. 2015. V. 43. P. 1825. doi 10.3303/ CET1543305
Brown J., Hirchfield D., Liu D.-M. et al. Ceramic Materials with Low Thermal Conductivity and Low Coefficients of Thermal Expansion. US Pat. 5, 102, 836 (April 7, 1992).
Pet’kov V.I., Asabina E.A. // Glass Ceram. 2004. V. 61. P. 233. doi 10.1023/B:GLAС.0000048353. 42467.0a [Петьков В.И., Асабина Е.А. // Стекло и керамика. 2004. № 7. С. 23.]
Pet’kov V.I., Kurazhkovskaya V.S., Orlova A.I., Spiridonova M.L. // Crystallogr. Rep. 2002. V. 47. № 5. P. 736. doi 10.1134/1.1509386
Pet’kov V.I., Shchelokov I.A., Asabina E.A. et al. // Russ. J. Inorg. Chem. 2006. V. 51. P. 1855. doi 10.1134/S0036023606120035 [Петьков В.И., Щелоков И.А., Асабина Е.А. и др. // Журн. неорган. химии. 2006. Т. 51. С. 1972.]
Olazcuaga R., Le Flem G., Boireau A., Soubeyroux J.L. // Adv. Mater. Res. 1994. № 1. P. 177.
El Bouari A., El Jazouli A., Dance J.M. et al. // Adv. Mater. Res. 1994. № 1. P. 173.
Asabina E.A., Orekhova N.V., Ermilova M.M. et al. // Inorg. Mater. 2015. V. 51. P. 793. doi 10.1134/S002016851508004X [Асабина Е.А., Орехова Н.В., Ермилова М.М. и др. // Неорган. материалы. 2015. Т. 51. С. 864. doi 10.7868/ S0002337X15080047]
Glukhova I.O., Asabina E.A., Pet’kov V.I. et al. // Russ. J. Inorg. Chem. 2016. V. 61. P. 681. doi 10.1134/S0036023616060085 [Глухова И.О., Асабина Е.А., Петьков В.И. и др. // Журн. неорган. химии. 2016. Т. 61. С. 717. doi 10.7868/S0044457X16060088]
Asabina E.A., Glukhova I.O., Pet’kov V.I. et al. // Russ. J. Gen. Chem. 2017. V. 87. P. 684. doi 10.1134/S1070363217040041 [Асабина Е.А., Глухова И.О., Петьков В.И. и др. // Журн. общ. химии. 2017. Т. 87. С. 550.]
Sukhanov M.V., Schelokov I.A., Pet’kov V. I. et al. // Eurasian Chem.-Tech. J. 2010. V. 12. P. 241. doi 10.18321/ectj51
Pet’kov V.I., Zhilkin E.V., Asabina E.A., Borovikova E.Yu. // Russ. J. Inorg. Chem. 2014. V. 59. P. 1087. doi 10.1134/S003602361410012X [Петьков В.И., Жилкин Е.В., Асабина Е.А. // Журн. неорган. химии. 2014. Т. 59. № 10. С. 1322.]
Asabina E., Pet’kov V., Mayorov P. et al. // Pure Appl. Chem. 2017. V. 89. № 4. doi 10.1515/pac-2016-100510.1515/pac-2016-1005
Asabina E.A., Shatunov V.E., Pet’kov V.I. et al. // Russ. J. Inorg. Chem. 2016. V. 61. P. 811. doi 10.1134/ S0036023616070020 [Асабина Е.А., Шатунов В.Е., Петьков В.И. и др. // Журн. неорган. химии. 2016. Т. 61. С. 850. doi 10.7868/S0044457X16070023]
Rietveld H.M. // Acta Crystallogr. 1967. V. 22. Pt. 1. P. 151.
Kim Y.I., Izumi F. // J. Ceram. Soc. Jpn. 1994. V. 102. P. 401.
Izumi F. // The Rietveld Method / Ed. Young R.A. Ch. 13. N.Y.: Oxford Univ. Press, 1993.
Fischer W., Singheiser L., Basu D., Dasgupta A. // Powder Diffraction. 2004. V. 19. P. 153. doi 10.1154/1.164305110.1154/1.1643051
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии