Журнал неорганической химии, 2019, T. 64, № 4, стр. 438-444
Экстракция неодима и палладия фосфорилированными тиакаликс[4]- и каликс[4]аренами из азотнокислых сред
В. Г. Торгов 1, *, С. В. Ткачев 1, Т. В. Ус 1
1 Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, пр-т академика Лаврентьева, 3, Россия
* E-mail: torgov@niic.nsc.ru
Поступила в редакцию 05.07.2018
После доработки 11.09.2018
Принята к публикации 21.09.2018
Аннотация
Проведено сопоставление раздельной и совместной экстракции неодима и палладия из азотнокислых растворов бифункциональным фосфорилированным тиакаликс[4]ареном (ТКФО) и моделирующими его монофункциональными фосфорилированным каликсареном (КФО), тиакаликсареном (ТКА) и их смесями для оценки взаимного влияния S-, PO-донорных центров экстрагентов. При этом только для ТКФО обнаружено снижение DNd: менее 0.1 по сравнению с 1.6 для КФО. Методом ЯМР на ядрах 31P{1H} и 13С{1H} показано, что уменьшение экстракции неодима ТКФО аналогично ингибированию каталитической активности ферментов (ТКФО) в присутствии эффекторов (РЗЭ) для процессов фосфорилирование–дефосфорилирование. При их координации к аллостерическому СН2P(O)R2-центру наблюдается высокая величина химсдвига (4 м.д.) сигнала 13СH2-cпейсера и образование продуктов гидролиза ТКФО (п-метилтиакаликс[4]арена и, возможно, дибутилгидроксофосфината). Результаты по экстракции смесями ТКА с КФО представляют интерес для упрощенного (Пурекс) и разрабатываемого (Карбэкс) процессов применительно к совместному извлечению неодима и палладия из азотнокислых растворов и их разделению из карбонатных растворов после реэкстракции неодима.
ВВЕДЕНИЕ
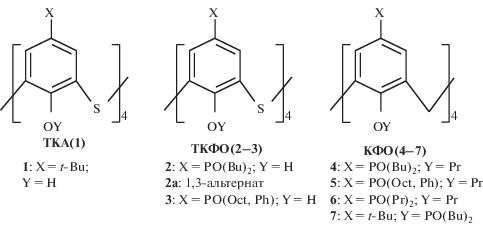
Традиционные ациклические RnХ и RnXO (X = = N, S, P) экстрагенты широко исследованы применительно к высокоактивным отходам (ВАО): нитратно-нитритным растворам переработки ядерного топлива [1] и солянокислым средам гидрохлорирования концентратов платиноидов [2]. Переход к N, S, PO-функционализированным каликс[n]аренам приводит к существенному возрастанию коэффициентов распределения (D) радиоактивных [3] и осколочных благородных [4, 5] металлов вследствие хелатообразования с двумя донорными центрами соседних фрагментов каликс[4]аренфосфиноксидов (КФО) или тиаэфиров. Для расширения возможностей разделения металлов используют молекулы бифункциональных каликс[n]аренов, содержащих в противоположных ободах РО- и S-донорные центры для отличающихся по комплексообразующей способности металлов групп А и Б. Такие экстрагенты ранее практически не применялись, вероятно, в связи с их малой доступностью. Наиболее синтетически доступны фосфорилированные в верхнем ободе тиакаликсарены (ТКА), содержащие пространственно разделенные S- и PO-донорные центры (ТКФО). Они позволяют совместить процессы извлечения из азотнокислых рафинатов ВАО актинидов-лантанидов (группа А) и осколочного палладия (группа Б). Такой подход был опробован в [6] для модельной пары европий–палладий при их совместной экстракции ТКФО из азотнокислых растворов и реэкстракции европия из группового экстракта. При количественном извлечении ионов палладия S-центрами нижнего обода молекул было обнаружено существенное снижение экстракции европия верхним ободом ТКФО по сравнению с КФО. Ранее был изучен ТКА в конформации “1,3-альтернат”, функционализированный эфирными [7] или краун-эфирными [8] атомами кислорода в верхнем и атомами азота пиридина в нижнем ободах. При совместном присутствии серебра и щелочных металлов экстракция серебра в нижний обод индуцирует [9] конформационные изменения, что снижает извлечение в верхний обод Li+, Na+, К+ и повышает экстракцию Cs+. Эти “отрицательный и положительный” аллостерические эффекты объясняются соответствием размеров “гостя” и “хозяина”. Экстракционные свойства ТКФО(2, 3) в конформации “конус” с пространственно разделенными РО- и S-центрами (рис. 1) практически не изучены. Судя по данным [6], для европия и палладия эти экстрагенты могут проявлять аллостерические свойства, отличные от свойств фосфорилированных ТКА в конформации “1,3-альтернат”, в которых мостиковые атомы серы не являются активными центрами.
Цель работы – сопоставление раздельной и совместной экстракции неодима и палладия бифункциональным ТКФО в конформации “конус”, моделирующими его монофункциональными ТКА и КФО (рис. 1) и их смесями для оценки взаимного влияния металлов и донорных центров экстрагентов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Экстрагенты и разбавители. Исследованные экстрагенты были специально синтезированы и охарактеризованы. Фрагменты донорных центров монофункциональных S- и PO-экстрагентов ТКА(1) и КФО(4–7) моделируют бифункционализированные тиакаликсарены ТКФО (2, 3) (рис. 1). В качестве разбавителя для экстракции использовали м-нитробензотрифторид (НБТФ) фирмы Rodia, для ЯМР исследований применяли 1,2-дихлорэтан (ДХЭ) “х. ч.”. Растворы экстрагентов в разбавителях (1–20 ммоль/л) готовили по точным навескам. Наименьшей растворимостью в НБТФ (1–2 ммоль/л) обладает тиакаликс[4]арен (1).
Методика работы. Растворы для экстракции получали смешением аликвотных частей растворов синтезированного комплекса K2[Pd(NO2)4] или нитрата неодима с азотной кислотой и выдерживанием их в течение недели для достижения равновесного состояния палладия в нитратно-нитритных растворах. Содержание металлов в 0.3 М HNO3 изменяли в диапазоне 1–10 ммоль/л, что близко к их содержанию в ВАО. Для проведения исследований необходимо установить наличие (или отсутствие) взаимного влияния донорных (S- и PO-) центров в ТКФО и металлов при совместной экстракции палладия и неодима. Поэтому были получены данные по совместной и раздельной экстракции палладия и неодима для одинаковых концентраций экстрагентов во всех изученных системах (ТКА, КФО, их смеси и ТКФО). Равные объемы водной и органической фаз интенсивно перемешивали в течение 30–60 мин при комнатной температуре. Аликвотную часть экстракта отбирали для промывки водными растворами или для реэкстракции неодима 2 М раствором Na2CO3 с pH 11.0. При экстракции наблюдалась нестабильность отдельных систем на основе ТКФО для концентраций неодима выше 1–6 и 0.02–0.3 ммоль/л в водной и органической фазе соответственно. Содержание металлов в азотнокислых растворах определяли ИСП АЭС (iCap-6500) и ААС (Hitachi Z-8000) методами в воздушно-ацетиленовом пламени (содержание >0.1 мкг/мл) или графитовом атомизаторе (содержание >0.001 мкг/мл).
ЯМР исследования. Спектры ЯМР 31Р{1H} и 13С{1H} сняты на спектрометре Avance 500 фирмы Bruker на частотах 202.5 и 125.8 МГц соответственно. Химсдвиги определяли методом замещения относительно 85%-ных растворов Н3РО4 и тетраметилсилана в хлороформе [10]. Для упрощения вида спектров при их регистрации подавляли спин-спиновое взаимодействие с протонами в режиме “обратной развязки с выключением”, что обеспечивало получение спектров с корректным соотношением интенсивностей. На рис. 2 схематически представлен фрагмент молекулы ТКФО(2) и дана маркировка сигналов атомов углерода при их отнесении (табл. 1, рис. 3).
Рис. 2.
Схематическое представление фрагмента молекулы ТКФО(2) и маркировка атомов во фрагменте при отнесение сигналов в табл. 1.
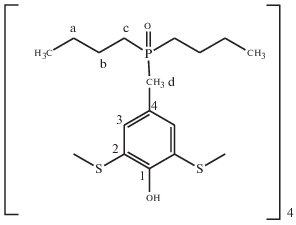
Таблица 1.
Параметры спектра ЯМР 13C{1H} раствора ТКФО(2) в дихлорэтане и предполагаемые отнесения сигналов
| Химсдвиг, м.д. |
Константа 31Р–13С, Гц |
Площадь относительно сигнала группы –СН3 | Отнесение на рис. 3 |
|---|---|---|---|
| 13.3 | – | 2.0 | –СН3 |
| 23.7 | 2.4 | 2.0 | а |
| 24.0 | 14.1 | 2.0 | b |
| 27.2 | 65.8 | 2.1 | c |
| 34.4 | 59.7 | 0.8 | d |
| 120.2 | – | 2.1 | 2 |
| 126.5 | 7.0 | 0.9 | 4 |
| 140.2 | – | 2 | 3 |
| 156.3 | – | 1.1 | 1 |
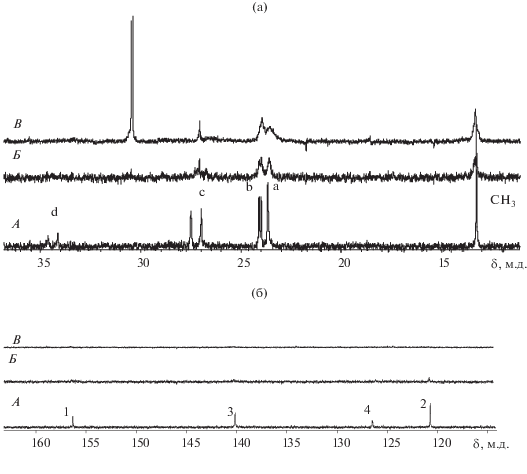
Рис. 3.
Cпектры ЯМР 13C{1H} алифатического (а) и ароматического (б) фрагментов ТКФО(2): А – исходный раствор ТКФО(2) в дихлорэтане; Б – органическая фаза после промывки экстракта неодима; В – экстракт нитрата неодима в ТКФО(2).
Для съемки ЯМР использовали образцы растворов в ДХЭ: экстрагента (10.0 ммоль/л), экстракта неодима и органической фазы после трехкратной промывки экстракта водным раствором (рН 4.0). Экстракт неодима был получен обработкой 10.0 ммоль/л раствора ТКФО(2) в ДХЭ равным объемом 0.14 М раствора нитрата неодима в 0.3 М HNO3. Содержание неодима в экстракте и органической фазе составляло соответственно 3.0 и 1.8 ммоль/л.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Раздельная экстракция неодима и палладия из азотнокислых растворов
Характер влияния строения каликc[4]аренфосфиноксидов на экстракцию неодима и европия одинаков. Величины DNd для КФО(4, 6) с “расходящейся” ориентацией РО-групп верхнего обода существенно выше таковых для КФО(7) со “сходящейся” ориентацией РО-групп нижнего обода [11]. При этом донорная способность фосфорильных атомов кислорода в КФО (4, 7) одинакова (энергии связи O1s-уровней атомов кислорода 530.3–530.4 эВ) (табл. 2). Величины отношений коэффициентов распределения РЗЭ для верхнего и нижнего ободов КФО, равные 10 для европия и 50 для неодима, указывают на локализацию РЗЭ преимущественно в верхнем ободе КФО. Поэтому эффективность извлечения РЗЭ из азотнокислых растворов связана в основном с размерами ободов в молекулах КФО. С другой стороны, согласно [12], для европия O-фосфорилирование ТКА в нижнем ободе, напротив, повышает DEu до сопоставимых величины DEu для КФО(4) с РО-группой в верхнем ободе, вероятно, вследствие хелатообразования РЗЭ с S- и PO-центрами ТКФО. Стехиометрия экстракции РЗЭ и палладия PO-каликс[4]аренами в виде моноядерных комплексов [MA3 –n(LH4 –n)m], где A = ${\text{NO}}_{3}^{ - },$ n = 0–1, m = 1–2, одинакова. Сопоставимые и невысокие величины D этих металлов недостаточны для их совместного извлечения из азотнокислых растворов.
Таблица 2.
Раздельная экстракция неодима и палладия растворами ТКА, КФО, их смесями и ТКФО в НБТФ (концентрация металлов 1.0 ммоль/л; экстрагентов – 10.0 ммоль/л)
| Экстрагент | Положение РФЭС, эВ [6] | Неодим | Палладий | ||
|---|---|---|---|---|---|
| O1s | P2p3/2 | S2p1/2 | D (R, %) | D (R, %) | |
| ТКА(1) | – | – | 163.4 | <0.01 (<1.0) | >20* (>95.0) |
| ТКФО(2) | 530.6 | 132.0 | 163.5 | <0.1 (<10.0) | >200 (>99.0) |
| ТКФО(2а) | – | – | – | <0.1 (<10.0) | – |
| ТКФО(3) | 530.7 | 132.0 | 163.4 | <0.02 (<2.0) | 1.7 (62.0) |
| КФО(4) | 530.3 | – | – | 1.6 (62.0) | 2.4 |
| КФО(4) + ТКА(1) | – | – | – | 1.4 (58.0) | >200 (>99.0) |
| КФО(5) | – | – | – | 0.08 (7.5) | 0.12 (11.0) |
| КФО(6) | 530.4 | 131.8 | – | 1.8 (64.0) | 2.4 (71.0) |
| КФО(6) + ТКА(1) | – | – | – | 1.7 (63.0) | >20* (>95.0) |
| КФО(7) | 530.4 | 131.8 | – | 0.03 (3.0) | 2.6 (72.0) |
| КФО(7) + ТКА(1) | – | – | – | 0.03 (3.0) | – |
Переход к ТКФО(2) (табл. 2) сопровождается снижением DРЗЭ на порядок по сравнению с КФО(4, 6) и не коррелирует с увеличением размеров макроцикла ТКФО(2) и донорной способностью атома кислорода PO-группы верхнего обода. Для палладия, напротив, DPd возрастает вследствие координации мостиковых атомов серы ТКФО(2). Из азотнокислых растворов палладий полностью извлекается всеми ТКА-содержащими экстрагентами (ТКА, смеси ТКА + КФО). При насыщении экстрагента образуются полиядерные формы [(PdA2)nLH4] (A = ${\text{NO}}_{3}^{ - },$ n = 1–4)], состав которых зависит от исходной концентрации палладия.
Совместная экстракция неодима и палладия
Экстракция смесями ТКА(1) с КФО(4). Коэффициенты распределения металлов из 0.3 М HNO3 при совместном присутствии палладия и неодима (европия) для ТКА(1), КФО(4, 6, 7) и их смесей в пределах погрешностей эксперимента совпадают с величинами D для индивидуальных растворов металлов (табл. 2 и 3). Оптимальной для совместного извлечения неодима (60–62%), европия (80–85%) [6] и палладия (>99%) является смесь ТКА(1) (1 ммоль/л) с КФО(4) (10 ммоль/л) в НБТФ. При одинаковых концентрациях ТКА(1) (DPd = 20) в случае смеси с КФО наблюдается возрастание DPd до 100–200. По аналогии с каликс[4]арентиаэфирами это, возможно, связано с ускоряющим действием добавок КФО на извлечение инертных форм родия и палладия из нитратно-нитритных растворов [13]. Для лабильных комплексов неодима аналогичный эффект для смесей не наблюдается. Cравнение результатов по раздельной и совместной экстракции палладия и неодима показывает, что для обоих экстрагентов, металлов и их смесей не наблюдается взаимного влияния, а извлечение металлов аддитивно с суммой величин для компонентов смеси. Поэтому смеси экстрагентов пригодны для совместного извлечения РЗЭ и палладия с отделением неодима и европия [6] при карбонатной промывке экстракта (85–100%) с потерей менее 1% палладия (табл. 3).
Таблица 3.
Поведение неодима и палладия при совместной экстракции из 0.3 М HNO3 10.0 ммоль/л растворами фосфорилированных каликс- и тиакаликсаренами в НБТФ и при карбонатной промывке экстрактов
| Экстрагент | Nd (0.5 ммоль/л) | Pd (0.5 ммоль/л) | Nd (1 ммоль/л) | Pd (1 ммоль/л) | ||||
|---|---|---|---|---|---|---|---|---|
| Rэкс, % (D) | Rпр, % | Rэкс, % (D) | Rпр, % | Rэкс, % (D) | Rпр, % | Rэкс, % (D) | Rпр, % | |
| КФО(4) | 62 (1.6) | 85 | 57 (1.3) | 94 | 59 (1.4) | 73 | 62 (1.7) | 89 |
| КФО(4)* | 83 (5.6) | 100 | 71 (2.4) | 96 | 81 (4.2) | 91 | 63 (1.7) | 90 |
| КФО(4) + ТКА(1) | 62 (1.6) | 80 | >99 (>100) | 0.9 | 58 (1.4) | 75 | >99 (200) | 0.5 |
| КФО(4) + ТКА(1)* | – | – | – | – | 82 (4.4) | 100 | 99.4(160) | 1.4 |
| ТКФО(2) | <10 (<0.1) | – | – | – | <10 (<0.1) | 20 | 99.8 (340) | 0.2 |
| ТКФО(2)* | 20 (0.25) | 35 | >99 (250) | 0.6 | 20 (0.25) | 32 | >99 (220) | 0.5 |
* Данные для европия [6].
Экстракция фосфорилированным тиакаликсареном. В отличие от каликс[4]аренфосфиноксидов, увеличение размеров верхнего обода при переходе от КФО к ТКФО для неодима, как и для европия, не приводит к ожидаемому повышению DNd. Напротив, величины DNd и DEu снижаются с 1.4–1.7 (неодим) и 4.2–5.6 (европий) для КФО(4) до 0.1–0.5 для ТКФО(2). Как и для смесей экстрагентов, DPd возрастают в случае ТКФО(2) с 1.7 до 220–340 (табл. 3). При совместной экстракции палладия и РЗЭ из азотнокислых растворов КФО(4) разделения металлов не происходит. Для ТКФО(2) вследствие ингибирования извлечения РЗЭ достигается отделение палладия от РЗЭ с коэффициентом разделения (1.5–2.2) × 103. В отличие от КФО возрастание кислотных свойств OH-группы ТКФО повышает извлечение РЗЭ и других металлов [14, 15] из слабокислых и щелочных растворов. Поэтому при карбонатной реэкстракции из экстракта ТКФО(2) в рафинат переходит только 20–35% европия и неодима (для КФО(4)–100%) и менее 1% палладия. Таким образом, в зависимости от условий в экстракте ТКФО(2) может образовываться набор комплексных форм неодима и европия. Из. азотнокислых растворов извлекаются координационные комплексы [MA3LH4)m], где m = 1, 2. Из слабокислых и щелочных растворов за счет депротонирования LH4 накапливаются смешанные формы [MA3 –n (LH4 –n)m], где A = ${\text{NO}}_{3}^{ - },$ n = 1–3, m = 1. С учетом этих данных ниже интерпретируются спектры ЯМР 13C{1H} и 31P{1H} ТКФО(2), экстрактов неодима в ТКФО(2) и органической фазы после промывки экстракта водой.
О возможном механизме ингибирования извлечения неодима. Снижение экстракции РЗЭ фосфорилированными ТКА более чем на порядок не связано с существенным уменьшением донорных свойств атомов кислорода в ТКФО(2) по сравнению с КФО(4). По данным РФЭС, для обоих экстрагентов величины энергий связи O1s фосфорильных атомов кислорода одинаковы (табл. 2). Полученные результаты не могут быть также объяснены с точки зрения образования псевдомакроциклов в обоих ободах, как это имеет место в случае “1,3-альтерната” ТКА при аллостерическом разделении серебра и щелочных металлов за счет различий в размерах ионов металлов. Координация серебра к атому азота приводит к изменению конформации бифункциональных калексаренов, что проявляется в сильном смещении сигнала протона группы –OСH2Py, ближайшего к зоне координации серебра [7, 8].
Более обоснованной для экстракции ТКФО(2) в конформации “конус” является аналогия c ингибированием каталитической активности ферментов в присутствии эффекторов (аллостерическая регуляция), в частности для процессов фосфорилирование–дефосфорилирование [16, 17]. В молекулах ТКФО активным центром (АЦ) для связывания ионов палладия являются мостиковые атомы сeры. Для РЗЭ группа –СH2–P(O)R2 верхнего обода ТКФО(2) (фермент Е) выступает также в качестве активного и аллостерического центра (АЛЦ), который пространственно отделен от АЦ для палладия. Катион неодима (ингибитор I), являющийся структурным аналогом субстрата (S), кооперативно взаимодействует с ТКФО для образования комплекса ЕI и регулирует процесс фосфорилирование–дефосфорилирование [16, 17]. При этом реакция обратимого ингибирования может протекать как без образования (Е + I → → ЕI), так и с образованием (Е + S → ЕS → E + + P)) метаболических продуктов реакции (Р) [16]. Комплексообразование нитратов РЗЭ с АЛЦ в верхнем ободе индуцирует конформационные изменения в ТКФО. Вероятно, поэтому значения DNd для экстрагента в конформациях “конус” ТКФО(2) и “1,3 альтернат” ТКФО(2а) близки и на порядок ниже таковых для КФО(4) (табл. 2). Методом ЯМР на ядрах 13С{1H} и 31Р{1H} исследовано изменение конформации ТКФО(2) при экстракции неодима за счет модификации спейсера (–СН2PO) в верхнем ободе ТКФО(2).
ЯМР характеризация процесса ингибирования извлечения неодима
ЯМР спектры ТKФО(2) в дихлорэтане. Спектры 13C{1H} алифатического и ароматического фрагментов молекулы ТKФО(2) хорошо соответствуют представленной формуле (рис. 2). Алифатическая часть спектров характеризуется наличием 4-х сигналов атомов углерода алкильных радикалов (рис. 3а), химсдвиги которых возрастают по мере сближения атомов 13C{1H} и 31P{1H} симбатно с константами их спин-спинового взаимодействия (табл. 1). Сигнал 13C{1H}-спейсера (d на рис. 3а) имеет наибольший химический сдвиг. Ароматическая часть спектров (рис. 3б) также содержит 4 сигнала. Эти результаты, как и присутствие единственного сигнала (44.4 м.д) в спектре 31P{1H} на рис. 4, свидетельствуют о чистоте исходного экстрагента (выше 97%), одинаковой симметрии атомов фосфора и высокой симметрии всей молекулы ТКФО(2).
Рис. 4.
Спектры ЯМР 31Р{1H} ТКФО(2): А – исходный раствор ТКФО(2) в дихлорэтане; Б – органическая фаза после промывки экстракта; В – экстракт нитрата неодима в ТКФО(2).
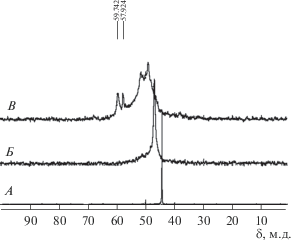
ЯМР спектры экстракта неодима. Образование комплексов, подобных фермент-cубстратным, при экстракции парамагнитного катиона Nd3+ (общая концентрация 3.0 ммоль/л) проявляется в трансформации одиночной линии фосфора в спектре ЯМР 31P{1H} (рис. 4) полушириной 15 Гц в сигнал c полушириной до 1500 Гц, состоящий из нескольких компонент. Такой спектр согласуется с присутствием в экстракте свободных молекул ТKФО(2) и набора комплексов неодима координационного [(M(NO3)3LH4)m] (сигналы 59.82 и 57.92 м.д.) и смешанного [{M(NO3)3 – n}(LH4 – n)m] (сигналы 47.03 и 44.42 м.д.) типа с различной симметрией атомов фосфора. Уширение сигнала может быть обусловлено как влиянием парамагнитного катиона, так и химическим обменом между различными формами комплексов. Кроме того, в спектре ЯМР 13C{1H} экстракта не наблюдаются сигналы 120.2–156.3 м. д. 4-х атомов углерода ароматической системы макроцикла из-за депротонирования ОН-групп нижнего обода ТКФО(2) парамагнитными катионами Nd3 + (табл. 1).
Отличительной особенностью спектра ЯМР 13CН2{1H}-спейсера является присутствие сигнала (30 м.д.), химический сдвиг которого при координации к неодиму (в отличие от алкильных атомов углерода) смещается в сторону сильного поля на 4 м.д. Высокие величины химсдвига сигнала 13CH2-спейсера и его интенсивности наблюдаются для ближайшего к неодиму атома углерода PO-аллостерического центра. Это, как и в случае координации серебра к атому азота “1,3-альтерната” [7, 8], связано с изменением конформации макроцикла вблизи центра координации. Сигналы атомов углерода бутильных групп, присоединенных к атому фосфора, уширяются, исчезают расщепления сигналов углерода на фосфоре (рис. 3а). Это также свидетельствует о координации РО-группы ТКФО к парамагнитному Nd3+ в комплексах [(M(NO3)3(LH4)m] (m = 1–2), между которыми происходит химический обмен. Присоединение к неодиму PO-групп индуцирует конформационные изменения вблизи центра координации ТКФО(2), которые катализируют реакцию гидролиза фермент-субстратного комплекса.
(1)
$\begin{gathered} {{\{ {{({\text{L}} - {\text{C}}{{{\text{H}}}_{2}} - {\text{POB}}{{{\text{u}}}_{2}})}_{2}}({\text{Nd(N}}{{{\text{O}}}_{3}}{{)}_{3}})\} }_{{\text{о }}}} + \\ {\text{ + }}\,\,{{{\text{H}}}_{{\text{2}}}}{\text{O}} \leftrightarrow {{\{ {\text{Nd(N}}{{{\text{O}}}_{3}}{{)}_{3}}\} }_{{\text{в }}}} + 2{{\{ ({\text{L}} - {\text{C}}{{{\text{H}}}_{3}})\} }_{{\text{о }}}} + \\ + \,\,2{{\{ ({\text{OH)POB}}{{{\text{u}}}_{2}}\} }_{{\text{о }}}}. \\ \end{gathered} $Одним из возможных продуктов дефосфорилирования является п-метилтиакаликс[4]арен, присутствие которого в ЯМР спектре экстракта подтверждается появлением сдвоенного сигнала метильной группы.
ЯМР спектры промытого экстракта. При обработке экстракта водными растворами (рН 4–5) координацонные комплексы [M(NO3)3(LH4)m] разрушаются с переходом неодима в рафинат (40%) и накоплением в органической фазе по схеме (2) смешанных комплексов (60%) за счет замещения нитрат-ионов на депротонированные ОН-группы нижнего обода [18]:
(2)
$\begin{gathered} {{\left\{ {{{{\left( {{\text{L}}{{{\text{H}}}_{4}}} \right)}}_{m}}({\text{Nd}}{{{\left( {{\text{N}}{{{\text{O}}}_{{\text{3}}}}} \right)}}_{3}}} \right\}}_{{\text{о }}}} + \\ + \,\,{{{\text{H}}}_{{\text{2}}}}{\text{O}} \leftrightarrow {{\left\{ {({\text{Nd}}{{{\left( {{\text{N}}{{{\text{O}}}_{{\text{3}}}}} \right)}}_{{3 - n}}}{{{\left( {{\text{L}}{{{\text{H}}}_{{4 - n}}}} \right)}}_{m}}} \right\}}_{{\text{о }}}} + \\ + \,\,n{{{\text{H}}}^{ + }},\quad\,\,\,\,n = {\text{ }}1--3. \\ \end{gathered} $Поэтому в спектре ЯМР 31P{1H} органической фазы отсутствует дублет сигналов (59.82 и 57.92 м. д.), принадлежащих координационным формам комплексов на рис. 4, и частично восстанавливается сигнал свободного ТКФO(2). Сигнал в спектре фосфора в основном становится одиночным с заметным широким пьедесталом в основании, но остается уширенным 150 Гц и смещенным в слабое поле на 3 м. д. (центр сигнала экстракта смещается в слабое поле на 7 м. д.). Это связано с присутствием в органической фазе смешанных форм комплексов неодима, и поэтому сигналы атомов углерода ароматической системы отсутствуют (рис. 3б). При промывке экстракта исходная высокая симметрия молекулы ТКФО полностью не восстанавливается. Наблюдаются сдвоенный сигнал метильной группы и смешанный сигнал α-СН2-группы (c), который походит на наложение сигнала экстракта и свободного экстрагента. Кроме того, в результате отделения координационных форм комплексов неодима при промывке водой в спектре атома углерода отсутствует смещенный сигнал d (рис. 2) атома углерода спейсера СН2-группы.
ЗАКЛЮЧЕНИЕ
Присутствие двух донорных центров в противоположных ободах тиакаликсаренов, вызывающее увеличение размеров полости и конформационной мобильности макроцикла, обусловливает возможность появления для функционализированных ТКА аллостерических эффектов [19]. Полученные результаты по совместной экстракции палладия и неодима (европия) из азотнокислых растворов показывают, что РО-группа ТКФО(2) является регулирующим центром процессов дефосфорилирования, ингибирования экстракции РЗЭ и ускорения экстракции палладия. Совокупность особенностей спектров ЯМР 13C{1H} и 31P{1H} экстрактов неодима подтверждает изменение конформации молекулы ТКФО(2) в зоне координации PO-группы к неодиму и образование продуктов дефосфорилирования. Обнаруженный аллостерический эффект для тиакаликсаренов в конформации “конус” в литературе не описан и требует специальных исследований кинетики гидролиза ТКФО.
Список литературы
Coppin G.R., Khankhasayev M.Kh. Chemical Separation Technologies and Related Methods of Nuclear Wastes Managements. Dordrecht, Netherlandes: Academ. Publ., 1999. P. 135.
Меретуков М.А., Орлов А.М. Металлургия благородных металлов (зарубежный опыт). М.: Металлургия, 1991. 415 с.
Dozol J.F., Schwing-Weill M.J., Arnaud-Neu F. et al. // Extraction and selective separation of long-lived nuclides by functionalized macrocycles. EUR 19605 EN, 2000. P. 1422.
Torgov V., Kostin G., Korda T. et al. // Solv. Extract. Ion Exchange. 2003. V. 23. № 6. P. 781. doi 10.1080/ 07366290500294970
Torgov V.G., Kostin G.A., Korda T.M. et al. // Russ. Chem. Bull. 2012. V. 61. № 7. P. 1437. [Торгов В.Г., Костин Г.А., Корда Т.М. и др. // Изв. АН. 2012. № 7. С. 1422.]
Torgov V.G., Us T.V., Lavrukhina S.A. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 6. P. 845. doi 10.1134/ S0036023617060249 [Торгов В.Г., Ус Т.В., Лаврухина С.А. и др. // Журн. неорган. химии. 2017. Т. 62. № 6. С. 868.]
Yamato T., Casas C.P., Mark R.J. et al. // J. Incl. Phenom. Macrocycl. Chem. 2006. V. 55. № 1–2. P. 31. doi 10.1007/s10847-005-9014-9
Casas C.P., Rahman S., Begum N., Xi Z., Yamato T. // J. Incl. Phenom. Macrocycl. Chem. 2008. V. 60. № 1–2. P. 173. doi 10.1007/s10847-007-9367-3
Лен Ж.М. Супрамолекулярная химия (концепции и перспективы). Новосибирск: Наука, 1998. 333 с.
IUPAC Recommendation 2001 // Pure Appl. Chem. 2001. V. 73. № 11. P. 1795.
Smirnov I.V., Karavan M.D., Efremova T.I. et al. // Radiochemistry. 2007. № 5. P. 482. doi 10.1134/ S1066362207050074 [Смирнов И.В., Караван М.Д. Ефремова Т.И. и др. // Радиохимия. 2007. Т. 49. № 5. С. 423.]
Kharchenko S., Drapailo A., Shishkina S. et al. // Supramol. Chem. 2014. V. 26. № 10–12. P. 864. http://dx.doi.org/10.1080/10610278.2014.890198.
Torgov V.G., Tatarchuk V.V., Druzhinina I.A. // Russ. J. Inorg. Chem. 2014. V. 59. № 2. P. 141. doi 10.1134/S0036023614020193 [Торгов В.Г., Татарчук В.В., Дружинина И.А. и др. // Журн. неорган. химии. 2014. Т. 59. № 2. С. 274.]
Shokova E.A., Kovalev V.V. // Russ. J. Org. Chem. 2003. V.39. № 1. P. 1 [Шокова Э.А., Ковалев В.В. // Журн. орган. химии. 2003. Т. 39. № 1. С. 13.]
Morohashi N., Narumi F., Iki N. et al. // Chem. Rev. 2006. V. 106. № 12. P. 5291. doi 10.1021/cr050565j
Северин Е.С. Биохимия. М.: Гэостар-Мед, 2003. 779 с.
Кнорре Д.Г., Мызина С.Д. Биологическая химия. Новосибирск: Изд-во СО РАН. 2012. 456 с.
Kikuchi T., Goto I., Suzuki K. et al. // Prog. Nucl. Energy. 2005. V. 47. № 1–4. P. 397. https://doi.org/10.1016/j.pnucene.2005.05.039.
Evtugyn G.A., Stoikova E.G., Shamagsumova P.V. // Russ. Chem. Rev. 2010. V. 79. № 12. P. 1071. [Евтюгин Г.А., Стойкова Е.Г., Шамагсумова Р.В. // Успехи химии. 2010. Т. 79. № 12. С. 1164.]
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии