Журнал неорганической химии, 2019, T. 64, № 6, стр. 607-612
Синтез и строение дицианоауратов органилтрифенилфосфония [Ph3PR]+[Au(CN)2]–, R = CH2С(O)Ph, CHCНMe, (CH2)4Br
В. В. Шарутин 1, *, О. К. Шарутина 1, М. А. Попкова 1
1 Национальный исследовательский Южно-Уральский государственный университет
454080 Челябинск, пр-т им. В.И. Ленина, 76, Россия
* E-mail: vvsharutin@rambler.ru
Поступила в редакцию 04.05.2018
После доработки 05.07.2018
Принята к публикации 10.07.2018
Аннотация
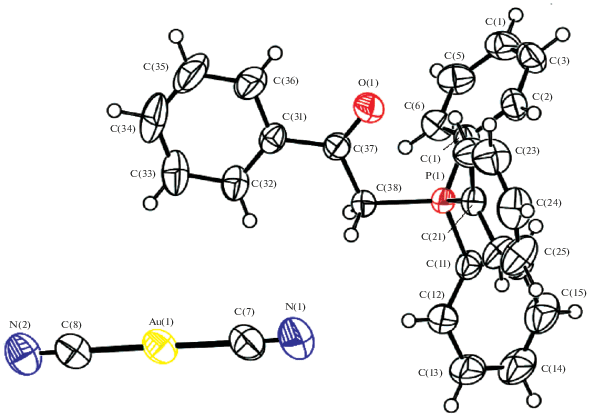
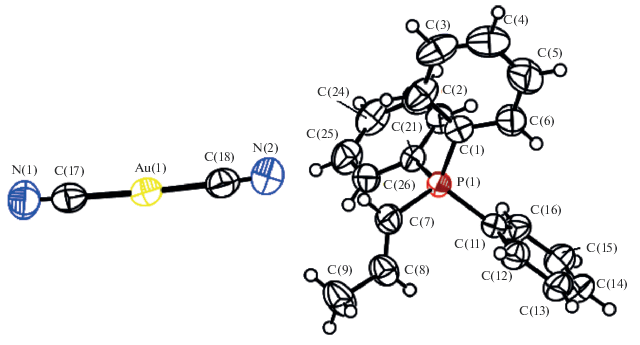
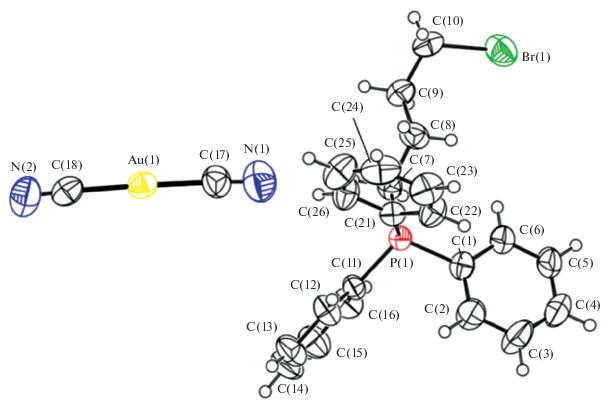
Взаимодействием дицианоаурата калия с хлоридами органилтрифенилфосфония в воде синтезированы и структурно исследованы комплексы [Ph3PR]+[Au(CN)2]–, где R = CH2C(O)Ph (I), CHCНMe (II) и (CH2)4Br (III). Атомы фосфора в катионах органилтрифенилфосфония имеют искаженную тетраэдрическую координацию: углы CPC 107.14(13)°−112.29(17)° (I), 107.38(15)°−110.84(16)° (II), 107.5(3)°−112.1(3)° (III), связи P−С 1.792(3)−1.828(3) (I), 1.768(4)−1.800(4) (II) и 1.787(5)−1.799(5) Å (III). В практически линейных анионах [Au(CN)2]− углы СAuC равны 179.38(13)° (I), 177.41(18)° (II), 178.2(3)° (III), расстояния Au−C составляют 1.967(6)−2.010(4) Å.
ВВЕДЕНИЕ
Дицианоауратные комплексы находят широкое применение в различных областях химии. Например, дицианоаурат калия использовался для получения искусственного рубинового стекла [1]. Подобные соединения золота являются действующими метаболитами некоторых лекарственных препаратов на основе Au(I) [2], применяются в качестве прекурсоров для получения магнитно- и оптически активных материалов [3]. Кроме того, было показано, что некоторые комплексы золота с олигомерными дицианоауратными анионами обладают люминесцентными свойствами [4–9]. Отметим, что к настоящему времени синтезированы и структурно охарактеризованы два дицианоауратных комплекса с тетраорганиламмонийными катионами [10] и один – с тетрафенилфосфониевым катионом [11].
В настоящей работе впервые синтезированы и структурно исследованы дицианоауратные комплексы [Ph3PR]+[Au(CN)2]–, где R = CH2C(O)Ph (I), CHCНMe (II), (CH2)4Br (III).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез [Ph3PCH2C(O)Ph]+[Au(CN)2]– (I). К водному раствору 217 мг (0.52 ммоль) хлорида трифенилбензоилметилфосфония добавляли раствор 150 мг (0.52 ммоль) дицианоаурата калия в 5 мл воды. Удаляли воду, остаток экстрагировали ацетонитрилом (3 раза по 5 мл). При медленном испарении растворителя наблюдали образование бесцветных кристаллов. Получили 312 мг (95%) комплекса I с tразл = 146°С.
ИК-спектр (ν, см−1): 3066, 3053, 3043, 3022, 2918, 2881, 2137, 1674, 1597, 1579, 1483, 1448, 1436, 1361, 1323, 1303, 1201, 1180, 1161, 1149, 1107, 1074, 1028, 987, 931, 856, 808, 779, 748, 715, 688, 615, 507, 489, 453, 439, 424.
Соединения II и III синтезировали по аналогичной методике.
[Ph3PCH=CHCH3]+[Au(CN)2]– (II) (бесцветные прозрачные кристаллы, выход 97%, tразл = = 110°С).
ИК-спектр (ν, см−1): 3082, 3057, 3024, 3007, 2916, 2214, 2156, 2141, 2100, 1649, 1614, 1587, 1485, 1438, 1375, 1338, 1315, 1255, 1184, 1163, 1112, 1026, 997, 975, 954, 839, 823, 742, 723, 684, 615, 538, 514, 501, 459, 428.
[Ph3P(CH2)4Br]$_{{\mathbf{2}}}^{{\mathbf{ + }}}$[Au(CN)2]– (III) (бесцветные прозрачные кристаллы, выход 97%, tразл = 112°С).
ИК-спектр (ν, см−1): 3080, 3057, 3022, 2966, 2933, 2897, 2873, 2808, 2218, 2140, 1963, 1901, 1818, 1587, 1483, 1456, 1435, 1435, 1332, 1313, 1280, 1242, 1226, 1186, 1114, 1070, 1026, 1012, 995, 974, 918, 848, 806, 786, 744, 727, 709, 686, 563, 526, 507, 501, 453, 426.
ИК-спектры комплексов I–III записывали на ИК-Фурье-спектрометре Shimadzu IR Affinity-1S в таблетке KBr.
РСА кристаллов I–III проводили на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0.71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [12]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [13] и OLEX2 [14]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур I−III приведены в табл. 1, основные длины связей и валентные углы − в табл. 2.
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структур I–III
| Параметр | Значение | ||
|---|---|---|---|
| I | II | III | |
| М | 630.42 | 552.35 | 647.29 |
| Сингония | Триклинная | Моноклинная | Ромбическая |
| Пр. гр. | Р$\bar {1}$ | P21/n | P212121 |
| a, Å | 9.593(8) | 10.013(5) | 8.014(5) |
| b, Å | 9.708(10) | 14.575(7) | 16.797(11) |
| c, Å | 13.762(11) | 14.618(11) | 17.544(5) |
| α, град | 98.26(5) | 90.00 | 90.00 |
| β, град | 102.00(3) | 92.16(2) | 90.00 |
| γ, град | 90.65(5) | 90.00 | 90.00 |
| V, Å3 | 1239.5(19) | 2132(2) | 2362(3) |
| Z | 2 | 4 | 4 |
| ρвыч, г/см3 | 1.689 | 1.721 | 1.821 |
| μ, мм−1 | 6.021 | 6.985 | 8.001 |
| F(000) | 612.0 | 1064.0 | 1240.0 |
| Размер кристалла, мм | 0.36 × 0.28 × 0.18 | 0.47 × 0.22 × 0.07 | 0.56 × 0.26 × 0.18 |
| Область сбора данных по 2θ, град | 6.12−61.1 | 5.6−63.12 | 6.1−47.78 |
| Интервалы индексов отражений | −13 ≤ h ≤ 13, −13 ≤ k ≤ 13, −19 ≤ l ≤ 19 | −14 ≤ h ≤ 14, −21 ≤ k ≤ 21, −21 ≤ l ≤ 21 | −9 ≤ h ≤ 9, −19 ≤ k ≤ 19, −19 ≤ l ≤ 19 |
| Измерено отражений | 76454 | 87383 | 25478 |
| Независимых отражений | 7522 (Rint = 0.0352) |
7107 (Rint = 0.0483) |
3617 (Rint = 0.0394) |
| Отражений с I > 2σ(I) | 6189 | 5065 | 3415 |
| Переменных уточнения | 298 | 245 | 263 |
| GOOF | 1.045 | 1.124 | 1.050 |
| R-факторы по F2 > 2σ(F2) | R1 = 0.0283, wR2 = 0.0666 | R1 = 0.0385, wR2 = 0.0775 | R1 = 0.0223, wR2 = 0.0552 |
| R-факторы по всем отражениям | R1 = 0.0396, wR2 = 0.0708 | R1 = 0.0669, wR2 = 0.0901 | R1 = 0.0252, wR2 = 0.0565 |
| Остаточная электронная плотность (min/max), e/A3 | 0.45/−1.49 | 0.89/−1.68 | 0.43/−0.77 |
Таблица 2.
Основные длины связей и валентные углы в структурах I−III
| Связь | d, Å | Угол | ω, град |
|---|---|---|---|
| I | |||
| Au(1)–C(7) | 2.010(4) | C(7)Au(1)C(8) | 179.38(13) |
| Au(1)–C(8) | 1.998(4) | C(1)P(1)C(38) | 109.60(12) |
| P(1)–C(1) | 1.792(3) | C(1)P(1)C(21) | 112.03(11) |
| P(1)–C(38) | 1.828(3) | C(1)P(1)C(11) | 108.16(13) |
| P(1)–C(21) | 1.806(3) | C(21)P(1)C(38) | 112.29(12) |
| P(1)–C(11) | 1.800(3) | C(11)P(1)C(38) | 107.40(12) |
| N(1)–C(7) | 1.134(5) | C(11)P(1)C(21) | 107.14(13) |
| N(2)–C(8) | 1.150(5) | C(37)C(38)P(1) | 111.92(16) |
| II | |||
| Au(1)–C(17) | 1.978(6) | C(18)Au(1)C(17) | 177.41(18) |
| Au(1)–C(18) | 1.967(6) | C(21)P(1)C(1) | 107.38(15) |
| P(1)–C(21) | 1.795(3) | C(11)P(1)C(21) | 110.84(16) |
| P(1)–C(1) | 1.800(4) | C(11)P(1)C(1) | 109.49(16) |
| P(1)–C(11) | 1.789(3) | C(7)P(1)C(21) | 108.41(18) |
| P(1)–C(7) | 1.768(4) | C(7)P(1)C(1) | 109.81(18) |
| N(1)–C(17) | 1.158(7) | C(7)P(1)C(11) | 110.83(18) |
| N(2)–C(18) | 1.165(7) | C(22)C(21)P(1) | 118.8(3) |
| III | |||
| Au(1)–C(17) | 1.967(7) | C(17)Au(1)C18 | 178.2(3) |
| Au(1)–C(18) | 1.994(7) | C(21)P(1)C7 | 107.7(3) |
| Br(1)–C(10) | 1.953(7) | C(21)P(1)C11 | 110.5(2) |
| P(1)–C(21) | 1.787(5) | C(21)P(1)C1 | 110.1(2) |
| P(1)–C(7) | 1.796(5) | C(7)P(1)C11 | 108.9(3) |
| P(1)–C(11) | 1.799(5) | C(1)P(1)C7 | 112.1(3) |
| P(1)–C(1) | 1.791(5) | C(1)P(1)C11 | 107.5(3) |
| N(1)–C(17) | 1.141(8) | C(26)C(21)P(1) | 118.6(4) |
| N(2)–C(18) | 1.113(8) | C(22)C(21)P(1) | 121.6(4) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1839771 (I), 1836099 (II), 1836088 (III); deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Комплексы I−III синтезировали из дицианоаурата калия и хлоридов органилтрифенилфосфония в воде:
Последующая перекристаллизация целевого продукта из ацетонитрила приводила к образованию устойчивых на воздухе бесцветных кристаллов.
Как известно, в ИК-спектрах как органических, так и неорганических соединений область поглощения C≡N-групп находится в узком интервале значений: 2200− 2000 см−1, что указывает на отсутствие сильного влияния окружения на колебания этих связей [15]. Поэтому цианиды легко идентифицировать по поглощению в указанной области. В спектрах соединений I−III интенсивные полосы обнаружены при 2137, 2141, 2140 см−1. Полосы поглощения связей P−СAr характеризуются областью поглощения 1450−1435 см−1 [15]. В спектрах соединений I, II и III соответствующие полосы находятся при 1437, 1538 и 1435 см−1. Кроме того, в спектре I присутствует характерная интенсивная полоса поглощения колебаний карбонильной группы С=О (1674 см−1), а в спектре II – средняя полоса поглощения С=С-связи при 1614 см−1.
По данным РСА, кристаллы I−III относятся к разным кристаллографическим системам: триклинной, моноклинной и ромбической соответственно. Кристаллы образованы катионами органилтрифенилфосфония и дицианоауратными анионами (рис. 1–3). Тетраэдрическая конфигурация катионов несколько искажена: углы при атомах фосфора CPC составляют 107.14(13)°−112.29(12)° (I), 107.38(15)°−110.84(16)° (II), 107.5(3)°−112.1(3)° (III), длины связей P−СPh (1.792(3)−1.806(3) Å (I), 1.789(3)−1.800(4) Å (II) и 1.787(5)−1.799(5) Å (III)) близки между собой. В I связь Р−С(38) (1.828(3) Å) с радикалом, содержащим электроотрицательную карбонильную группу, превышает связи с фенильными радикалами. В катионе II связь Р−С(7) с алкенильным радикалом самая короткая (1.768(4) Å). В катионе III расстояние Р−С(7) (1.796(5) Å) в пределах погрешности эксперимента совпадает с двумя из трех расстояний P−СPh.
Анионы [Au(CN)2]− практически линейны: углы СAuC равны 179.38(13)° (I), 177.41(18)° (II), 178.2(3)° (III), углы AuCN составляют 177.4(4)°, 179.6(3)°; 177.3(5)°, 178.1(5)°; 177.0(7)°, 177.4(8)° в I, II и III соответственно. Расстояния Au−C (1.998(4) и 2.010(4) в I, 1.967(6) и 1.978(6) в II, 1.967(7) и 1.994(7) Å в III) близки к сумме ковалентных радиусов указанных элементов 2.02 Å [16]. Тройные связи C≡N в цианидных лигандах равны 1.150(5) и 1.134(5) Å, 1.165(7) и 1.158(7) Å, 1.141(8) и 1.113(8) Å в I, II и III соответственно. Отметим, что во всех анионах меньшему значению связи C≡N соответствует большее расстояние Au−C.
Структурная организация кристаллов I, II и III обусловлена в основном слабыми водородными связями N⋅⋅⋅Н−С (2.50−2.68 Å).
ЗАКЛЮЧЕНИЕ
Синтезированы три новых дицианоаурата органилтрифенилфосфония реакцией обмена соответствующих солей в воде. Кристаллы, пригодные для рентгеноструктурных исследований, получены из ацетонитрила. Выявлены некоторые особенности в структурах катионов, связанные с различной природой алкильных радикалов. Варьирование расстояний Au−C и C≡N в анионах, возможно, обусловлено различными параметрами элементарных ячеек и особенностями кристаллической упаковки.
Список литературы
Wagner F.E., Haslbeck L., Stievano S. et al. // Nature. 2000. V. 407. P. 691. https://doi.org/10.1038/35037661
Shaw III C.F. // Chem. Rev. 1999. V. 99. P. 2589. doi https://doi.org/10.1021/cr980431o
Leznoff D.B., Lefebvre J. // Gold Bull. 2005. V. 38. № 2. P. 47. https://doi.org/10.1007/BF03215233
Rawashdeh-Omary M.A., Omary M.A., Patterson H.H. // J. Am. Chem. Soc. 2000. V. 122. P. 10371. https://doi.org/10.1021/ ja001545w
Rawashdeh-Omary M.A., Omary M.A., Shankle G.E. et al. // J. Phys. Chem. B. 2000. V. 104. P. 6143. https://doi.org/10.1021/ jp000563x
Assefaa Z., Haireb R.G., Sykorac R.E. // J. Solid State Chem. 2008. V. 181. P. 382. https://doi.org/10.1016/ j.jssc.2007.11.036
Colis J.C.F., Larochelle Ch., Fernández E.J. et al. // J. Phys. Chem. B. 2005. V. 109. P. 4317. https://doi.org/10.1021/ jp045868g
Assefaa Z., Kalachnikova K., Hairec R.G. et al. // J. Solid State Chem. 2007. V. 180. P. 3121. https://doi.org/10.1016/ j.jssc.2007.08.032
Roberts R.J., Le D., Leznoff D.B. // Inorg. Chem. 2017. V. 56. № 14. P. 7948. https://doi.org/10.1021/acs.inorgchem.7b00735
Cambridge Crystallographic Data Center. 2017 (deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Шарутин В.В., Попкова М.А., Тарасова Н.М. // Вестн. ЮУрГУ. Серия “Химия”. 2018. Т. 10. № 1. С. 55. https://doi.org/10.14529/chem180107
Bruker (1998). SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA.
Bruker (1998). SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Crystallogr. 2009. V. 42. P. 339. https://doi.org/10.1107/ S0021889808042726
Преч Э., Бюльманн Ф., Аффольтер К. Определение строения органических соединений. М.: Мир, 2006. 440 с.
Бацанов С.С. // Журн. неорган. химии. 1991. Т. 36. № 12. С. 3015.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии