Журнал неорганической химии, 2019, T. 64, № 7, стр. 714-726
Координационные полиэдры AlCn в структурах кристаллов
М. О. Карасев 1, *, И. Н. Карасева 1, Д. В. Пушкин 1
1 Самарский национальный исследовательский университет им. академика С.П. Королева
443086 Самара, Московское шоссе, 34, Россия
* E-mail: maxkarasev@inbox.ru
Поступила в редакцию 12.12.2018
После доработки 12.12.2018
Принята к публикации 17.12.2018
Аннотация
С помощью метода пересекающихся секторов и полиэдров Вороного–Дирихле (ПВД) проведен кристаллохимический анализ соединений, структура которых содержит координационные полиэдры AlCn. Установлено, что атомы алюминия в углеродном окружении проявляют координационные числа (КЧ) 1–7 и 10, при этом наиболее характерным КЧ атома алюминия является 4. Установлено существование единой линейной зависимости телесных углов граней ПВД, соответствующих валентным и невалентным контактам Al–C, от соответствующих межъядерных расстояний. Показано, что длина химических связей Al–C изменяется в диапазоне 1.90–2.77 Å, однако объем ПВД атома алюминия практически не зависит от его КЧ и составляет 11.4(7) Å3. Предложены критерии оценки существования кластерной связи Al–Al в структуре алюминийорганических соединений, а также проанализированы агостические взаимодействия Al···H–C.
ВВЕДЕНИЕ
Алюминийорганические соединения имеют широкое применение в органическом синтезе благодаря высокой регио- и стереоселективности карбо- и гидроалюминирования [1]. Алюминийсодержащие металлорганические каркасы используются в качестве катализаторов при синтезе спиртов и карбонильных соединений [2]. К настоящему времени установлена структура более 7500 соединений, одновременно содержащих атомы алюминия и углерода [3]. Несмотря на это, кристаллохимический анализ соединений, содержащих в своем составе координационные полиэдры (КП) AlCn, не проводился. Настоящая работа предпринята с целью установления основных закономерностей стереохимии алюминия в кристаллах, содержащих КП AlCn.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Кристаллохимический анализ проводили с помощью комплекса структурно-топологических программ TOPOS [4]. Во внимание принимались лишь те структуры, которые удовлетворяли следующим критериям: структура решена с ненулевым фактором недостоверности R ≤ 0.1, в ней определены координаты всех атомов, включая атомы водорода, а также отсутствует статистическое разупорядочение каких-либо атомов. С учетом указанных критериев объектами анализа, проводившегося с помощью полиэдров Вороного–Дирихле (ПВД), явились 224 структуры, содержащие 348 кристаллографически неэквивалентных атомов Al(III), 13 атомов Al(II) и 21 атом Al(I). Следует отметить, что нехарактерные для алюминия низшие степени окисления представлены исключительно кластерами, содержащими связи Al–Al. Полный перечень всех изученных соединений можно получить у авторов по адресу: maxkarasev@inbox.ru.
Как известно [5], ПВД атома является выпуклый многогранник, образованный в результате пересечения плоскостей, проходящих перпендикулярно через середины отрезков, соединяющих данный атом со всем его окружением. В общем случае состав ПВД некоторого атома А можно представить в виде AXiZj, где X – атомы, химически связанные с атомом А, i – его координационное число, Z – атомы, ПВД которых имеют общие грани с ПВД атома А, но не образующие с последним химических связей, j – количество атомов Z. Сумма (i + j) определяет число граней (Nf) ПВД атома А. В качестве примера рассмотрим ПВД атома алюминия в структуре Na[AlMe4] {CUVMAH} [6] (рис. 1б, табл. 1). Здесь и далее в фигурных скобках, стоящих за формулой соединения, указан буквенный код, под которым кристаллоструктурные и библиографические данные для вещества зарегистрированы в базе данных [3]. В структуре Na[AlMe4] атом алюминия имеет КЧ = 4, образуя химические связи с атомами углерода, длина которых лежит в диапазоне 1.991–2.023 Å. Однако помимо четырех сравнительно коротких связей атом алюминия образует 13 дополнительных более длинных невалентных контактов с атомами водорода (d(Al···H) = = 2.381–2.605 Å) и атомом натрия (d(Al···Na) = = 3.356 Å). Таким образом, ПВД атома Al(1) в обсуждаемой структуре имеет 17 граней.
Рис. 1.
Полиэдры Вороного–Дирихле атомов алюминия в структурах Al(CH(SiMe3)2)2(C≡CPh) {SOMCAZ} (а), Na[Al(CH3)4] {CUVMAH} (б), Al(Cp)3 {RIVNUF} (атом Al(1)) (в), Al(Np)2(PPh3–C = CH–Ph) {ANAJUV} (г), Al(Cp)3 {RIVNUF} (атом Al(2)) (д), [Al(Me3C6H2)2C6H3][B(C6F5)4] {AXUVAQ} (е), Al(CpMe3)3 {RIVPAN} (ж), [BMe(C6F5)3][Al(CpMe5)2] · CH2Cl2 {YAQDUP} (з), (C6F5)3AlAl(C5Me5) {GUHWIP} (и), Al2Me3(C6F5)3 {QEMWIO} (к), Al8Me8(CH2Ph)6 {QEHPAU} (атом Al(3)) (л), Al8Me8(CH2Ph)6 (м) (атом Al(1)) {QEHPAU}, (AlEt)7(CCH2Ph)4(C≡C–Ph)H {CUGJET} (н), [Li(C2H4N2Me2)2][Al2(CH(SiMe3)2)8Br] · 2C5H10 {WEZRAU} (о), [Li((Me2N)2C2H4)2][Al2((C(SiMe3)2)3(CH2SiMe2CHSiMe3)] {LEDYAU} (п), [Al4(C(SiMe3)3)4] · 2Me2CHOH {GASDIN} (р), (CMe3)3AlAl(C5Me5) {SEPWOA} (с), Al4(CpMe4)4 {SIXGUC} (т). Символом Np обозначен неопентил-радикал С5Н11, а символом Cp – циклопентадиенид-анион. Показаны только атомы, образующие химические связи с атомами Al. Черные кружки – атомы алюминия, белые – атомы углерода.
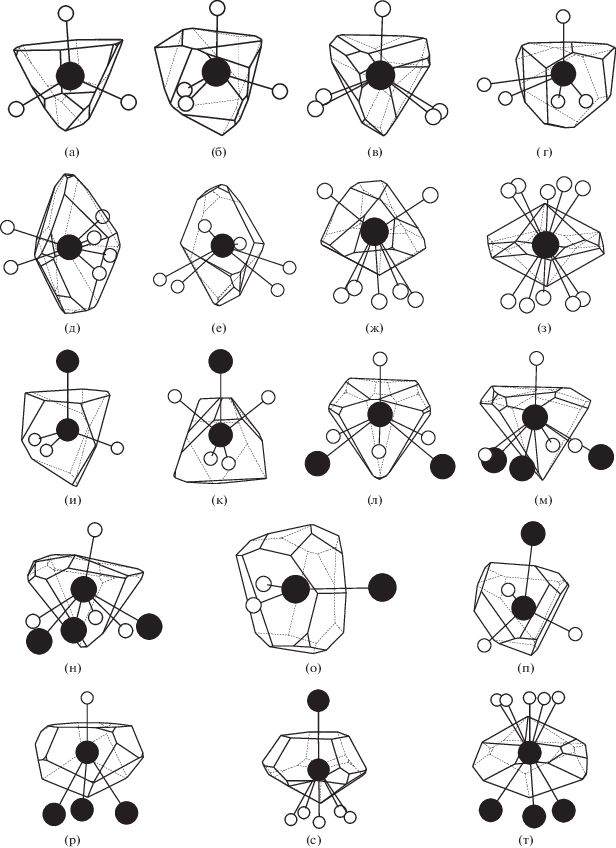
Таблица 1.
Анализ координации атомов алюминия в некоторых структурах
| Характеристики ПВД атома Al* | Величина перекрывания (Å3) двух сфер атомов Al и Х с радиусами** | Тип перекрывания Al–Х | |||||
|---|---|---|---|---|---|---|---|
| атомы окружения Х | d(Al–Х), Å | Ω(Al–Х), % | rs × rs | rs × RСД | RСД × rs | RСД × RСД | |
| Na[Al(CH3)4] {CUVMAH} [6] Центральный атом – Al(1) с КЧ = 4 |
|||||||
| C(2) × 2 | 1.991 | 16.56 | 0 | 0.0589 | 0.0105 | 0.1658 | П3 |
| C(1) × 2 | 2.023 | 15.75 | 0 | 0.0443 | 0.0041 | 0.1409 | П3 |
| #H(3) × 2 | 2.381 | 4.57 | 0 | 0.1494 | 0 | 0.3316 | П0 |
| #H(1) × 2 | 2.426 | 4.80 | 0 | 0.1728 | 0 | 0.3693 | П0 |
| #H(4) × 4 | 2.583 | 2.09 | 0 | 0.0089 | 0 | 0.0785 | П0 |
| #H(2) × 4 | 2.605 | 1.94 | 0 | 0.0008 | 0 | 0.0454 | П0 |
| Na(1) | 3.356 | 0.53 | 0 | 0 | 0 | 0 | П0 |
| [AlMe(C6F5)(μ-Me)]2 {MURQUL} [28] Центральный атом – Al(1) с КЧ = 4 + 1 |
|||||||
| C(16) | 1.934 | 15.81 | 0.0004 | 0.4654 | 0 | 0.3635 | П3 |
| C(6) | 1.993 | 19.93 | 0 | 0.6006 | 0.0005 | 0.7499 | П3 |
| C(3) | 2.096 | 10.68 | 0 | 0.3009 | 0 | 0.2985 | П2 |
| C(3) | 2.100 | 9.92 | 0 | 0.2850 | 0 | 0.2725 | П2 |
| H(2) | 2.156 | 10.33 | 0 | 0.3650 | 0 | 0.5501 | П2 |
| H(4) | 2.177 | 10.03 | 0 | 0.3132 | 0 | 0.4626 | П2 |
| #H(3) | 2.377 | 3.41 | 0 | 0.1997 | 0 | 0.5460 | П0 |
| #H(5) | 2.448 | 3.54 | 0 | 0.2712 | 0 | 1.0223 | П0 |
| #H(11) | 2.490 | 2.64 | 0 | 0.2281 | 0 | 0.9684 | П0 |
| #H(8) | 2.571 | 2.20 | 0 | 0.1229 | 0 | 0.7061 | П0 |
| #H(8) | 2.573 | 2.03 | 0 | 0.1143 | 0 | 0.6669 | П0 |
| Al(1) | 2.593 | 5.49 | 0 | 0.0408 | 0.0408 | 0.3101 | П3 |
| #F(3) | 3.097 | 2.21 | 0 | 0 | 0 | 0.1086 | П0 |
| #F(1) | 3.237 | 1.21 | 0 | 0 | 0 | 0.1923 | П0 |
| #F(1) | 3.620 | 0.51 | 0 | 0 | 0 | 0.0313 | П0 |
| #F(9) | 3.889 | 0.04 | 0 | 0 | 0 | 0.0029 | П0 |
* d(Al–Х) – расстояния между атомами, Ω(Al–Х) – телесный угол, выраженный в процентах от 4π стерадиан, под которым общая грань ПВД атомов Al и Х видна из ядра любого из них. Число симметрично равных контактов Al–Х указано как (×n). Символом # отмечены атомы Z, для которых отрезок Al⋅⋅⋅Z не пересекает соответствующую ему грань ПВД и представляющие собой неосновные или непрямые соседи [22]. ** Во всех случаях первым указан радиус сферы атома Al, вторым – атома Х. Нулевое значение указывает на отсутствие пересечения соответствующих сфер.
Для определения КЧ атомов алюминия был использован метод пересекающихся секторов [7], который однозначно и точно позволяет разделить все парные взаимодействия на сильные, соответствующие химическим связям (A–X), и слабые невалентные (A···Z) контакты. Согласно [7], типы пересечений П0 и П1 следует интерпретировать как невалентные взаимодействия A···Z, химическим связям A–X отвечают типы перекрываний П2, П3 и П4. Примеры расчета КЧ атомов Al по методу [7] представлены в табл. 1.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Согласно полученным данным, по отношению к атомам углерода атомы Al(III) в структурах кристаллов проявляют КЧ 3–7 и 10, атомы Al(II) – 2 и 3, атомы Al(I) – 1 и 5 (табл. 2). Следует отметить, что атомы алюминия, находящиеся в низших, нехарактерных степенях окисления, а также 28 атомов Al(III) с КЧ = 3 и 4 образуют 1, 2 или 3 дополнительные связи Al–Al. Состав КП таких атомов можно охарактеризовать формулой AlCnAlm, поэтому условимся далее записывать КЧ атомов алюминия, входящих в состав подобных кластеров, в виде суммы (n + m), например, КЧ атома алюминия, входящего в состав комплекса AlC4Al2, равно 4 + 2.
Таблица 2.
Характеристики ПВД атомов алюминия в окружении атомов углерода*
| Степень окисления | КЧ | КП | КТТ ПВД |
ТТВ ПВД |
Число атомов Al | Nf | Nnb | VПВД, Å3 | RСД, Å | G3 | DА, Å | Рис. ПВД** |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| III | 3 | Треугольник | – | – | 42 | 21(4) | 6 | 12.7(6) | 1.448(22) | 0.089(2) | 0.07(5) | 1а |
| 4 | Тетраэдр | 34 | {3/4} | 259 | 20(4) | 4 | 11.2(4) | 1.387(18) | 0.0087(1) | 0.05(3) | 1б | |
| 5 | Прямоугольная пирамида | 3243 | {3/6} | 2 | 25(1) | 4 | 12.1(1) | 1.423(3) | 0.090(1) | 0.06(3) | 1в | |
| Одношапочный тетраэдр | 3243 | {3/6} | 4 | 18(4) | 2.6 | 12.2(9) | 1.427(36) | 0.087(1) | 0.05(2) | 1г | ||
| 6 | Искаженный октаэдр | 46 | {3/8} | 1 | 23 | 2.8 | 13.3 | 1.471 | 0.091 | 0.05 | 1д | |
| Искаженная тригональная призма | 324252 | {3/8} | 1 | 29 | 3.8 | 12.7 | 1.446 | 0.092 | 0.02 | 1е | ||
| 7 | Одношапочная пентагональная пирамида | 314353 | {3/10} | 1 | 21 | 2 | 12.0 | 1.421 | 0.087 | 0.062 | 1ж | |
| 3242526 | {3/10} | 2 | 23(1) | 2.3 | 12.5(1) | 1.441(1) | 0.091(1) | 0.14(6) | ||||
| 10 | Пентагональная антипризма | 445462 | {3/16} | 8 | 22(3) | 1.2 | 10.91(7) | 1.379(3) | 0.090(1) | 0.01(1) | 1з | |
| Все | 320 | 20(4) | – | 11.4(7) | 1.397(29) | 0.087(2) | 0.05(3) | |||||
| 3 + 1 | Тетраэдр | 34 | {3/4} | 2 | 21(14) | 4.3 | 13.5(5) | 1.477(18) | 0.088(3) | 0.13(5) | 1и | |
| 4 + 1 | Искаженная тригональная бипирамида | 3243 | {3/6} | 16 | 19(3) | 2.8 | 11.3(6) | 1.393(26) | 0.089(1) | 0.07(5) | 1к | |
| 4 + 2 | Искаженная пентагональная пирамида | 324252 | {3/8} | 2 | 21(1) | 2.5 | 12.1(6) | 1.422(24) | 0.089(1) | 0.06(5) | 1л | |
| 4 + 3 | Трехшапочный тетраэдр | 335361 | {3/10} | 6 | 19(2) | 1.7 | 11.9(4) | 1.417(14) | 0.089(1) | 0.09(4) | 1м | |
| 324362 | {3/10} | 2 | 23(1) | 2.1 | 12.3(1) | 1.434(4) | 0.090(1) | 0.14(1) | 1н | |||
| II | 2 + 1 | Треугольник | – | – | 9 | 19(3) | 5.3 | 15.9(9) | 1.561(32) | 0.088(2) | 0.24(5) | 1о |
| 3 + 1 | Тетраэдр | 34 | {3/4} | 4 | 19(1) | 3.8 | 14.2(4) | 1.502(13) | 0.089(1) | 0.24(6) | 1п | |
| I | 1 + 3 | Тетраэдр | 34 | {3/4} | 4 | 20(1) | 4 | 18.5(1) | 1.639(4) | 0.084(1) | 0.07(1) | 1р |
| 5 + 1 | Пентагональная пирамида | 324252 | {3/8} | 2 | 24(3) | 3 | 18.1(1.5) | 1.628(44) | 0.090(3) | 0.29(6) | 1с | |
| 5 + 3 | Призма | 4454 | {3/12} | 15 | 21(1) | 1.6 | 18.8(5) | 1.649(16) | 0.090(1) | 0.18(2) | 1т | |
* КЧ – координационное число; КП – координационный полиэдр; КТТ – комбинаторно-топологический тип упрощенного ПВД, дуального КП (строчные числа указывают число вершин у грани, надстрочные – общее число граней); ТТВ – топологический тип вершин ПВД (первая цифра указывает ранг вершины, вторая – число вершин); Nf – среднее число граней ПВД; Nnb – среднее число невалентных контактов, приходящихся на одну химическую связь; VПВД – объем ПВД; RСД – радиус сферы, объем которой равен объему ПВД; G3 – безразмерная величина второго момента инерции ПВД; DA – смещение ядра атома металла из геометрического центра тяжести его ПВД. **Номер рисунка с изображением соответствующего ПВД.
Для определения формы КП атомов алюминия с КЧ > 3 использовали метод поиска изоморфизма графов реберных сеток соответствующих ПВД [8, 9]. При отнесении КП к определенному геометрическому типу в соответствии с [8, 9] рассматривали “упрощенные” ПВД, число граней которых совпадает с КЧ атомов алюминия, рассчитанным по методу пересекающихся секторов [7]. В обсуждаемых соединениях “упрощенные” ПВД атомов алюминия относятся к 10 различным комбинаторно-топологическим типам (КТТ).
На долю КП AlC3Alm (m = 0 и 1) приходится 12.6% от рассматриваемой выборки (табл. 2). Атомы алюминия, входящие в состав комплексов AlC3, имеют КП в виде тригональной пирамиды (рис. 1а). Атом алюминия выходит из плоскости, образованной тремя координированными атомами углерода, на величину δ = 0–0.45 Å. Единственным примером комплекса, содержащего атом алюминия с δ = 0, является структура (фенилэтинил)-бис(бис(триметилсилил)метил)алюминия Al(CH(SiMe3)2)2(C≡CPh) {SOMCAZ} [10], в которой атомы Al(1) занимают позиции с сайт-симметрией С2. В случае оставшегося 41 комплекса AlC3 атомы алюминия имеют сайт-симметрию С1 (39 комплексов) и С3 (2 комплекса). Подобное окружение атомов алюминия наблюдается и в случае реализации КП состава AlC2Al (рис. 1о).
Как видно из табл. 2, атомы Al(III) чаще всего координируют 4 атома углерода, образуя КП состава AlC4Alm (m = 0–3), на долю которых приходится 73.0% от исследованной выборки. Отметим, что координация четырех атомов углерода характерна исключительно для атомов Al(III) и не наблюдается для Al(II) и Al(I). Атомы алюминия, образующие тетраэдрические комплексы AlC4, занимают позиции с сайт-симметрией С1 (256 комплексов), С2, С3 и C2v (по одному комплексу). КП атомов алюминия, входящих в комплексные группировки AlC4Alm (m = 1–3), можно описать в виде образованных атомами углерода тетраэдров, на поворотных осях С2 которых располагаются дополнительные атомы алюминия (рис. 1к, 1л, 1м). Атомы Al в обсуждаемых комплексах AlC4Alm (m = = 1–3) занимают позиции с сайт-симметрией С1 (27 комплексов) и Cs (1 комплекс). Отметим, что тетраэдрическое строение имеют также комплексы алюминия с КЧ = 3+1 и 1+3 (сайт-симметрия позиций С1), в которых одна или три вершины тетраэдра заняты атомами Al (рис. 1и, 1р).
Пента- и гексакоординированные состояния атомов алюминия реализуются за счет координации π-лигандов. Так, в структуре циклопентадиенида алюминия Al(Cp)3 {RIVNUF} [11] атомы Al(1) координируют два η2- и один η1-циклопентадиенид-ион, реализуя КЧ = 5, в то время как атомы Al(2) координируют три η2-циклопентадиенид-иона, увеличивая тем самым свое КЧ до 6 (рис. 1в, 1д). Атомы Al в комплексах AlC5 и AlC6 занимают позиции с сайт-симметрией С1. Координация η5-циклопентадиенид-аниона осуществляется в комплексах AlC7, AlC10 и в кластерах AlC5Alm (m = = 1 или 5), изображенных на рис. 1ж, 1з. Например, гептакоординированный атом алюминия в структуре 1,2,4-триметилциклопентадиенида алюминия Al(1,2,4-Me3Cp) {RIVPAN} [11] координирует один η5- и два η1-1,2,4-триметилциклопентадиенид-аниона, образуя координационный полиэдр в виде пентагональной пирамиды с расщепленной вершиной (рис. 1ж). КП AlC10 наблюдаются в “сэндвичевых” структурах, в которых атомы Al координируют два η5-пентаметилциклопентадиенид-иона, располагающихся в заторможенной конформации по отношению друг к другу. Гептакоординированные атомы алюминия, а также атомы алюминия, входящие в кластеры AlC5Alm (m = 1 или 5), занимают позиции с сайт-симметрией C1, в то время как декакоординированные – С1 и Ci (по 4 комплекса на каждый тип сайт-симметрии).
В табл. 3 приведена краткая характеристика всех валентных и невалентных взаимодействий между атомами алюминия и углерода. Наглядно охарактеризовать такие взаимодействия позволяет график зависимости телесных углов (Ω), выраженных в процентах от полного телесного угла 4π стерадиан, под которыми грани ПВД “видны” из ядер атома алюминия или углерода, от соответствующих расстояний Al–C и Al···C (рис. 2). Точки на графике (рис. 2) образуют непрерывную последовательность, так что на основании значений Ω(Al–C) и d(Al–C) невозможно разделить валентные и невалентные контакты. В структуре 224 исследованных соединений ПВД всех сортов атомов алюминия в сумме образуют 7670 граней. Проведенный анализ показал, что химическим взаимодействиям Al–X отвечают 1652 грани, в том числе 1534 типа Al–C и 118 типа Al–Al. Роль атомов Z, образующих невалентные контакты с атомами Al, чаще всего играют атомы H, C и F, образуя 4856, 659 и 149 граней соответственно. Химическим связям Al–C и Al–Al отвечают грани с рангом грани (РГ) РГ = 1. Под рангом грани понимается минимальное число химических связей в структуре вещества, соединяющих два атома, ПВД которых имеют общую грань [12]. Нулевой ранг грани характеризует межмолекулярные взаимодействия. В обсуждаемой выборке ранг граней ПВД атомов Al изменяется в диапазоне от 0 до 12, за исключением РГ = 11. Химические связи Al–C в обсуждаемых соединениях лежат в диапазоне 1.90–2.77 Å, а телесные углы, отвечающие этим граням, располагаются в области от 23.4 до 3.9%. Дополнительный анализ показал, что длина связи Al–C не зависит от гибридного состояния атома углерода и составляет в среднем 2.04(9) Å. Отметим, что средняя длина связи углерод–углерод фрагмента Al–C–C закономерно изменяется в зависимости от гибридизации атома С. Так, в ряду Al–C–C, Al–C=C и Al–C≡C средние величины d(C–C) принимают значения 1.49(6), 1.36(6) и 1.20(1) Å соответственно. В то же время химическим контактам Al–Al отвечает диапазон длин связей 2.56–2.85 Å и телесных углов 16.3–2.9%.
Таблица 3.
Характеристики взаимодействий Al–E и Al···E (E = C или Al) в структуре алюминийорганических соединений
| Степень окис- ления | КЧ | Число атомов Al | Связи Al–C | Невалентные контакты Al···C | Связи Al–Al | Невалентные контакты Al···Al | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| число связей |
d(Al–C), Å | диапазон Ω(Al–C), % | число контактов |
d(Al···C), Å | Ω(Al···C), % | число связей |
d(Al–Al), Å | диапазон Ω(Al–Al), % | число контак-тов |
d(Al···Al), Å | Ω(Al···Al), % | |||||||
| диапазон | среднее | диапазон | среднее | диапазон | среднее | диапазон | среднее | |||||||||||
| III | 3 | 42 | 126 | 1.90–2.05 | 1.97(2) | 14.4–23.4 | 166 | 2.61–4.10 | 3.11(32) | <7.4 | – | – | – | – | 7 | 2.94–3.38 | 3.20(19) | <2.0 |
| 4 | 252 | 1036 | 1.90–2.46 | 2.03(6) | 3.9–22.8 | 353 | 2.60–4.34 | 3.02(27) | <5.8 | – | – | – | – | 33 | 2.81–3.46 | 3.16(20) | <3.5 | |
| 5 | 6 | 30 | 1.94–2.77 | 2.20(28) | 4.9–21.1 | 28 | 2.55–4.00 | 3.08(42) | <5.1 | – | – | – | – | – | – | – | – | |
| 6 | 2 | 12 | 1.94–2.62 | 2.26(25) | 7.4–20.8 | 22 | 2.63–4.86 | 3.38(61) | <2.7 | – | – | – | – | – | – | – | – | |
| 7 | 3 | 21 | 1.97–2.41 | 2.22(14) | 5.5–18.8 | 8 | 2.70–3.08 | 2.88(13) | <3.5 | – | – | – | – | – | – | – | – | |
| 10 | 8 | 80 | 2.11–2.18 | 2.15(12) | 8.5–9.7 | – | – | – | – | – | – | – | – | – | – | – | – | |
| Все | 320 | 1305 | 1.90–2.77 | 2.04(9) | 3.9–23.4 | 563 | 2.55–4.86 | 3.05(32) | <7.4 | – | – | – | – | 40 | 2.81–3.46 | 3.17(20) | <3.5 | |
| 3 + 1 | 2 | 6 | 1.98–2.04 | 2.01(2) | 18.1–22.5 | 9 | 2.91–2.99 | 2.96(3) | < 0.1 | 2 | 2.59–2.69 | 2.64(7) | 12.8–16.3 | – | – | – | – | |
| 4 + 1 | 16 | 64 | 1.92–2.27 | 2.04(8) | 8.3–21.6 | 29 | 2.69–4.26 | 3.03(33) | <1.3 | 16 | 2.57–2.78 | 2.64(6) | 4.1–5.9 | 5 | 2.67–3.10 | 2.85(18) | <3.6 | |
| 4 + 2 | 2 | 8 | 1.94–2.44 | 2.08(16) | 12.9–18.6 | 8 | 2.95–3.95 | 3.43(43) | <3.3 | 4 | 2.59–2.85 | 2.71(13) | 2.9–5.2 | 3 | 2.85–3.75 | 3.15(52) | <2.8 | |
| 4 + 3 | 8 | 32 | 1.93–2.38 | 2.07(10) | 13.3–18.5 | 26 | 2.96–4.01 | 3.50(37) | <2.4 | 24 | 2.58–2.85 | 2.64(9) | 2.9–5.6 | 1 | – | 3.75 | – | |
| Все | 28 | 110 | 1.92–2.44 | 2.05(9) | 8.3–22.5 | 72 | 2.69–4.26 | 3.23(41) | <3.3 | 46 | 2.57–2.85 | 2.64(7) | 2.9–16.3 | 9 | 2.67–3.75 | 2.96(34) | <3.6 | |
| II | 2 + 1 | 9 | 18 | 1.98–2.05 | 2.01(2) | 15.5–20.1 | 15 | 2.39–3.52 | 3.15(30) | <7.6 | 9 | 2.56–2.75 | 2.65(5) | 12.3–16.3 | – | – | – | – |
| 3 + 1 | 4 | 12 | 1.97–2.32 | 2.08(10) | 7.8–19.5 | 5 | 2.79–3.57 | 3.19(34) | <3.1 | 4 | 2.56–2.75 | 2.65(8) | 12.3–14.4 | – | – | – | – | |
| Все | 13 | 30 | 1.97–2.32 | 2.04(7) | 7.8–20.1 | 20 | 2.39–3.57 | 3.16(3) | <7.6 | 13 | 2.56–2.75 | 2.65(6) | 12.3–16.3 | – | – | – | – | |
| I | 1 + 3 | 4 | 4 | 2.02–2.03 | 2.03(1) | 21.0–21.3 | – | – | – | – | 12 | 2.73–2.75 | 2.74(1) | 11.0–11.9 | – | – | – | – |
| 5 + 1 | 2 | 10 | 2.16–2.22 | 2.20(2) | 8.8–9.6 | 4 | 3.63–3.91 | 3.77(12) | <1.6 | 2 | 2.59–2.69 | 2.64(7) | 12.8–16.3 | – | – | – | – | |
| 5 + 3 | 15 | 75 | 2.28–2.38 | 2.33(2) | 7.1–9.0 | – | – | – | – | 45 | 2.63–2.78 | 2.74(4) | 12.5–13.3 | – | – | – | – | |
| Все | 21 | 89 | 2.02–2.38 | 2.30(8) | 7.1–21.3 | 4 | 3.63–3.91 | 3.77(12) | <1.6 | 59 | 2.59–2.78 | 2.74(4) | 11.0–16.3 | – | – | – | – | |
Рис. 2.
Зависимость телесных углов Ω (% от 4π стерадиан) 2193 граней ПВД 348 атомов Al от межатомных расстояний Al–C и рангов, соответствующих этим граням.
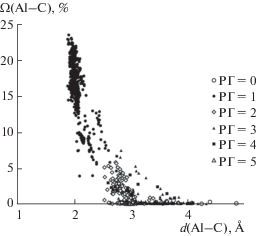
Независимо от КЧ и степени окисления атомов алюминия, а также от формы и симметрии их ПВД валентные и невалентные взаимодействия между атомами Al и C описываются единой линейной зависимостью значений телесных углов граней ПВД от соответствующих межатомных расстояний (рис. 2):
(1)
$\Omega ({\text{Al}}{\kern 1pt} --{\kern 1pt} {\text{C}}) = {\text{42}}.00\left( {{\text{33}}} \right)--{\text{13}}.0{\text{4}}\left( {{\text{13}}} \right)d({\text{Al}}{\kern 1pt} --{\kern 1pt} {\text{C}})$с коэффициентом корреляции ρ = –0.899 для 2193 граней Al–C. Как известно, наличие подобной линейной зависимости является критерием существования ближнего порядка, обусловленного химическим взаимодействием между атомами, и дает основание полагать, что взаимодействия Al–C в структуре изученных кристаллов подчиняются общей закономерности, не зависящей от валентного состояния атомов Al. Как следует из рис. 2, реализующиеся в структурах кристаллов значения d(Al–С) образуют практически непрерывную область в диапазоне 1.90–4.86 Å, при этом с ростом межатомного расстояния значения Ω(Al–С) уменьшаются от ∼2% практически до нуля.
Согласно данным табл. 3, в рассмотренных соединениях длина связи Al–C в КП AlCn изменяется более чем на 0.8 Å, однако такая вариация межатомного расстояния Al–C практически не сказывается на величине объема ПВД атома Al, который в пределах 3σ(VПВД) является константой, практически не зависящей от значения КЧ. Напротив, изменение степени окисления атома Al неминуемо сказывается на величине VПВД. Как видно из табл. 2, уменьшение степени окисления атома Al сопровождается закономерным увеличением VПВД атома алюминия, средние значения которого составляют 11.4(7), 15.4(1.2) и 18.7(6) Å3 для атомов Al(III), Al(II) и Al(I) соответственно. Факт постоянства величин VПВД и RСД в пределах одной и той же степени окисления атома Al свидетельствует в пользу модели атома как “мягкой”, обладающей способностью легко деформироваться сферы [13–15], объем которой фиксирован и зависит исключительно от степени окисления атома Al и химической природы атомов, непосредственно связанных с ним. Как было отмечено выше, в случае 28 атомов Al(III) метод пересекающихся секторов выявил помимо химических связей Al–C связи Al–Al. Из табл. 2 видно, что, несмотря на наличие таких дополнительных связей Al–Al, характеристики ПВД атомов алюминия в КП AlCnAlm в пределах погрешности совпадают с характеристиками ПВД атомов Al, установленных для КП состава AlCn.
Нецентросимметричность окружения атомов алюминия можно охарактеризовать, используя величину вектора смещения ядра атома из центра тяжести его ПВД (DA) [14]. Из приведенных в табл. 2 данных видно, что величина DA в подавляющем большинстве случаев равна нулю в пределах 2σ(DA). В пределах утроенной погрешности ненулевые значения параметр DA принимает только в случае субвалентных соединений алюминия, что, по всей видимости, вызвано наличием дополнительной связи Al–Al. В то же время комплексы Al(III) имеют ненулевое среднее значение DA только в случае КП AlC4Al3, что, вероятно, обусловлено образованием атомами Al многоцентровых двухэлектронных связей [16, 17]. В случае комплексов AlCnAlm (m = 0–3) величина вектора DA лежит в диапазоне 0–0.333 Å. Нулевые значения DA наблюдаются для четырех комплексов AlC10, в которых атомы Al имеет сайт-симметрию Сi, координируют два η5-пентаметилциклопентадиенид-аниона в [BMe(C6F5)3][Al(CpMe5)2] · ⋅ CH2Cl2 {YAQDUP} [18] и [Al(CpMe5)2][AlCpMe5Cl3] {HASPOG} [19]. Максимальное значение DA = = 0.333 Å имеет атом Al+(2) в структуре (C6F5)3AlAl(C5(CH3)5) [20], подробно обсуждаемой ниже.
Помимо вектора DA искажение ПВД описывается величиной второго момента инерции (G3) – безразмерного параметра, характеризующего степень сферичности полиэдра [21]. Для комплексов AlCnAlm (m = 0–3) величина G3 изменяется в диапазоне 0.0844–0.0925, что, согласно [21], соответствует образованию преимущественно ковалентных связей.
Наглядно охарактеризовать особенность окружения атомов алюминия в исследованных структурах позволяет (r, φ)-распределение [14], график которого для ПВД атомов Al представлен на рис. 3. На приведенных графиках ядра всех атомов Al расположены в полюсе (точка 0) полярной системы координат. Вектор DA совмещен с полярной осью абсцисс, а в случае DA = 0 с полярной осью совмещена ось z кристаллографической системы координат. В результате центр тяжести каждого ПВД лежит на горизонтальной оси справа от точки 0 или совпадает с ней. Каждой грани ПВД соответствует точка, положение которой однозначно определяется полярным радиусом r, равным по величине соответствующему межъядерному расстоянию, и полярным углом φ (угол между векторами DA и r).
Рис. 3.
Распределение (r, φ) для ПВД атомов Al, входящих в состав 348 комплексов AlIIICnAlm (а), 13 комплексов AlIICnAl (б), 21 комплекса AlICnAlm (в), 51 комплекса, в которых проявляются агостические взаимодействия Al···H–C (г). Во всех случаях черные кружки отвечают атомам С, белые кружки – атомам Al, белые квадраты – атомам Н, черные ромбы – атомам Si, черные треугольники – атомам Br (б) и F (в), белыми треугольниками обозначены атомы Н, участвующие в агостических взаимодействиях Al···H–C.
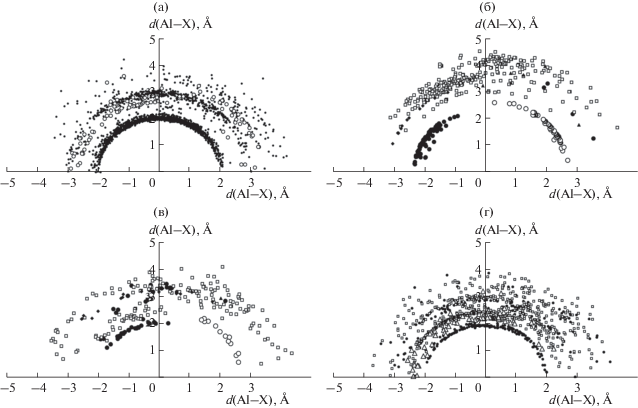
Независимо от степени окисления атомов Al на (r, φ)-распределении наблюдаются две контактные кривые, соответствующие двум координационным сферам атомов алюминия. На рис. 3а изображено (r, φ)-распределение для контактов Al–C и Al–Al в комплексах AlIIICnAlm (m = 0–3). Первая координационная сфера атомов Al3+ включает в себя валентные взаимодействия Al–C и Al–Al, которым соответствуют контактные кривые с радиусами ∼2.03(7) и 2.64(7) Å соответственно. Вторая координационная сфера представляет собой невалентные взаимодействия Al/C и Al/Al, которым отвечают контактные кривые с радиусами ∼3.08(33) и 3.24(19) Å соответственно.
Несколько иной вид имеет (r, φ)-распределение для комплексов Al2+ и Al+, изображенное на рис. 3б и 3в соответственно. В данном случае контактные кривые, отвечающие взаимодействиям Al–C и Al–Al, представлены дугами. При этом точки, характеризующие контакты Al–C, располагаются преимущественно при значениях угла φ > 90°, в то время как точки, характеризующие контакты Al–Al, лежат при значениях угла φ < < 90°. Данное обстоятельство можно объяснить исходя из направленности ковалентных связей Al–X (X = C, Al), обратившись к рис. 1с, на котором видно, что КП субвалентных атомов алюминия характеризуются асимметрией в расположении лигандов. Например, в комплексе (C6F5)3AlAl(C5Me5) {GUHWIP} [20] атом Al+(2) с одной стороны окружен атомами С-донорного лиганда (η5-C5Me5), а с диаметрально противоположной стороны – атомом Al3+(1). В комплексах Al2+ радиус C-координационной сферы равен ∼2.04(7) Å, а Al-координационной сферы – ∼2.65(6) Å. В случае комплексов одновалентного алюминия первая контактная кривая располагается на более удаленном расстоянии (2.30(8) Å), чем для комплексов Al3+ и Al2+. Вторая координационная сфера на рис. 3в характеризует кластерные связи Al–Al и имеет радиус ∼2.74(4) Å.
На (r, φ)-распределении для атомов Al2+ и Al+ (рис. 3б и 3в) наблюдается четко выраженный диффузный слой, за существование которого преимущественно отвечают внутримолекулярные контакты Al/H и Al/Si, РГ которых изменяется от 2 до 7 в случае атомов Al2+ и от 2 до 5 для атомов Al+. Следует отметить, что на рис. 3в практически полностью отсутствуют точки, соответствующие невалентным взаимодействиям Al/C, что связано со строением кластерных группировок, представленных в случае атомов Al+ тетраэдрами Al4, полностью экранированными от невалентных взаимодействий Al/C атомами лигандов, в роли которых выступают объемные группировки – η5-пентаметилциклопентадиенид-анионы и трис(триметилсилил)метил-анионы. Как видно из данных табл. 3, только в случае комплексов AlC5Al ПВД атомов Al+ имеют грани, отвечающие невалентным взаимодействиям Al/C. Данный факт связан исключительно с особенностями строения соединений. Комплексы AlC5Al не образуют компактных тетраэдрических кластеров, как в случае других производных Al+, в результате чего ПВД атомов Al+ приобретают грани, соответствующие невалентным взаимодействиям Al/C.
Интересной особенностью координационно ненасыщенных металлов в структурах кристаллов является возможность существования агостических взаимодействий M···H–C. В работах [7, 22] приведены критерии существования агостических взаимодействий, согласно которым подобные взаимодействия между атомом металла и атомом водорода, связанного с атомом углерода, реализуются если: атомы водорода имеют достаточно короткий контакт с атомом металла и являются прямыми соседями; контактам M···H–C отвечают существенно ненулевые телесные углы Ω > 5%; значения характеристик ПВД атомов М, участвующих в агостических взаимодействиях, рассчитанных с учетом и без учета атомов водорода, существенно изменяются. В изученной выборке наблюдается значительное количество “прямых” контактов Al–H (893 из 4856), которые могут соответствовать агостическим взаимодействиям Al···H–C, обусловленным ненасыщенностью валентных возможностей атомов алюминия. Среди основных граней типа Al–H встречаются 64 грани, которым соответствуют типы пересечения П2. Эти грани, согласно [7, 22], необходимо интерпретировать как агостические взаимодействия Al···H–C, соответствующие внутри- (РГ = = 2–6, 8 и 9) и межмолекулярным контактам (РГ = 0), которые можно охарактеризовать значениями d(Al–H) = 2.06–2.70 Å и Ω(Al–H) = 5.3–15.4%. В обсуждаемой выборке присутствуют 32 структуры, содержащие 51 атом алюминия, которые образуют агостические взаимодействия с атомами водорода. Последние входят в состав группировок, содержащих как sp3- (метильные и метиленовые группировки), так и sp2-гибридные атомы углерода (фенильные, винильные и аллильные фрагменты). Примером может служить структура соединения (μ4-карбидо)(μ-триизопропилфосфинимид-N,N')(μ-метил)(η5-инденил)гексаметил-три-алюминий-титан (Al3TiC)Me7(NP(i-Pr)3)(C9H7) {QORTOG} [23], в которой между атомами Н(46) метильной группировки и Al(2) реализуется агостическое взаимодействие с характеристиками d(Al–H) = 2.21 Å, Ω(Al–H) = 15.4%.
На рис. 3г представлено (r, φ)-распределение для контактов атомов алюминия, участвующих в агостических взаимодействиях Al···H–С. Из рис. 3г видно, что подавляющая часть атомов Н, вовлеченная в реализацию контактов Al···H–С, располагается между полуокружностями, отвечающими взаимодействиям Al–C и Al/H. Радиус контактной кривой, отвечающей агостическим взаимодействиям Al···H, составляет ∼2.36(21) Å.
Приведенные в табл. 3 данные свидетельствуют о неравнозначности связей Al–Al, образованных атомами алюминия в различных степенях окисления. Например, комплексы Al3+C3Al, входящие в состав двух структур, представлены биядерными кластерами (η5-пентаметилциклопентадиенил)-трис(пентафторфенил)диалюминий (C6F5)3AlAl(C5Me5) {GUHWIP} [20] и (η5-пентаметилциклопентадиенил)-три-t-бутилдиалюминий (CMe3)3AlAl(C5Me5) {SEPWOA} [24]. Кластерная связь в обсуждаемых структурах представляет собой двухэлектронную двухцентровую связь (2е2с-связь), образованную за счет неподеленной электронной пары атома Al(I) и вакантной орбитали атома Al(III) [20, 24]. Помимо кластерной связи атомы Al(III) в соединении (CMe3)3AlAl(C5Me5) образуют три связи с атомами углерода трех трет-бутильных групп, в то время как в (C6F5)3AlAl(C5Me5) такие связи реализуются с атомами углерода трех пентафторфенильных групп. В обеих структурах атом Al(I) образует связь с η5-пентаметилциклопентадиенид-анионом. Телесные углы, отвечающие взаимодействиям Al–Al в комплексах AlC3Al, лежат в диапазоне 12.8–16.3%. В то же время связям в комплексах AlC4Alm (m = 1–3), включающим в свой состав исключительно атомы Al3+, отвечают довольно низкие величины телесного угла, лежащего в диапазоне 2.9–5.9%, тогда как в комплексах, содержащих субвалентный атом алюминия, значениям Ω(Al–Al) соответствует диапазон 11.0–16.3%.
Комплексы AlC4Alm, где m = 2 или 3, входят в состав двух структур – (AlMe)8(CCH2Ph)5(C≡C–Ph) [16] {QEHPAU} и (AlEt)7(CCH2Ph)4(C≡C–Ph)H [17] {CUGJET}. В первой структуре атомы алюминия образуют кубический кластер Al8, в то время как во второй структуре кластер Al7 можно представить в виде одношапочной треугольной призмы. Образование кластеров Al8 и Al7 объясняется авторами [16, 17] возникновением многоцентровых двухэлектронных связей, подобных связям B–B в молекулах бороводородов.
В то же время вопрос о существовании кластерных связей А–А, где А = Al3+, в биядерных комплексах остается открытым. Согласно [1], биядерные комплексы Al3+ можно описать двумя способами, используя два типа связывания. Первый вариант предполагает наличие в обсуждаемых соединениях двух 2е3с-связей, реализующихся между атомами алюминия и мостиковыми атомами углерода. В таком случае кластерная связь Al–Al отсутствует. Второй вариант связывания подразумевает комбинацию одной 2е2с-связи Al–Al и одной 2е4с-связи между атомами входящих в состав 1,3-диалюминациклобутанового фрагмента.
Согласно методу пересекающихся секторов [7], комплексам AlC4Al отвечают биядерные кластеры, в которых каждый атом Al образует четыре связи с атомами углерода, при этом две связи являются концевыми и две – мостиковыми. В целом, в таком кластере два атома алюминия координируют шесть атомов углерода. На рис. 4 представлен пример такого биядерного кластера. В структуре бис(μ-t-бутилэтенилиден)тетраэтилдиалюминия [25] {UHICAQ} атомы Al образуют кластерную связь Al–Al и координируют два t-бутилэтенилиденовых монодентатных мостиковых лиганда (тип координации М2) и четыре этильных радикала, являющихся монодентатными концевыми лигандами (тип координации М1). Обозначение типов координации дано в соответствии с [26]. Согласно [26], такому комплексу соответствует кристаллохимическая формула (КХФ) А2${\text{M}}_{{\text{2}}}^{2}{\text{M}}_{4}^{1}$, где A = Al. Поскольку в подобных кластерах атомы алюминия координируют лишь С-донорные лиганды, условимся далее обозначать такие комплексы формулой Al2C6.
Рис. 4.
Молекула бис(μ-t-бутилэтенилиден)-тетраэтил-диалюминия Al2Et4(t-Bu–CH=CH)2. Большие черные кружки – атомы алюминия, белые – атомы углерода, маленькие черные кружки – атомы водорода.
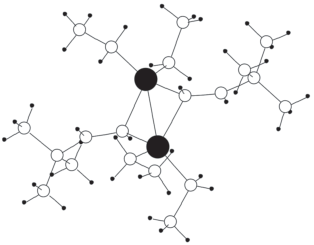
На основании кристаллохимического анализа было установлено, что из 18 комплексов Al(III)2C6, в состав 17 входят атомы Al, ПВД которых имеют общую грань, отвечающую контактам Al–Al (табл. 4). Из 17 указанных контактов Al–Al лишь 10 характеризуются типом перекрывания П3 [22], что следует рассматривать как существование химического взаимодействия между атомами алюминия. Согласно данным табл. 4, наличие или отсутствие химической связи между атомами Al(III) определяется геометрическими характеристиками четырехчленного цикла ${\text{Al}}_{2}^{{{\text{III}}}}$C2. Согласно полученным данным, кластерная связь образуется между атомами алюминия, если расстояния d(Al–Al) и d(Al–C) не превышают 2.78 и 2.22 Å соответственно. При этом величины валентных углов ∠CAlC лежат в диапазоне 97.7°–105.7°, ∠AlCAl – в диапазоне 74.9°–81.7°. Отклонение значений угла ∠CAlC в меньшую или угла ∠AlCAl в большую сторону приводит к росту расстояния d(Al–Al) и, соответственно, к невозможности образования кластера. Так, в случае структуры бис(μ2-фенилэтинилиден)-тетраметилдиалюминия Al2Me4(C≡СC6H5)2 [27] {HALWEX} значения параметров d(Al–Al) = 3.03 Å, ∠CAlC = = 88.3° и ∠AlCAl = 91.7° приводят к отсутствию общей грани ПВД у двух атомов Al, входящих в состав одного комплекса. Величина Ω(Al–Al) в кластерах Al2C6 лежит в диапазоне 4.1–5.9%. На наш взгляд, рассматриваемые в [1] модели электронного строения комплексов ${\text{Al}}_{2}^{{{\text{III}}}}$C6, следует использовать не как комбинацию, а как два самостоятельных способа описания кластерных и некластерных структур ${\text{Al}}_{2}^{{{\text{III}}}}$C6.
Таблица 4.
Некоторые характеристики комплексов Al(III)2C6*
| RefCode | Атомы Al | d(Al–Al), Å | d(Al–C), Å | ∠CAlC, град | ∠AlCAl, град | Ω(Al–Al), % | Мостиковый лиганд |
Тип перекр. Al–Al |
|---|---|---|---|---|---|---|---|---|
| BOFNOA | Al(1) | 2.669 | 2.042 | 97.7 | 81.7 75.6 |
4.1 | CH2 | П3 |
| 2.180 | ||||||||
| Al(2) | 2.039 | 98.0 | ||||||
| 2.174 | ||||||||
| DIHLAI | Al(1) | 2.784 | 2.045 | 99.8 | 80.2 | 4.1 | Cp | П3 |
| EMALIN | Al(1) | 2.664 | 2.167 | 102.8 | 77.2 | 4.6 | Ph | П3 |
| MOVZAZ | Al(2) | 2.627 | 2.016 | 102.2 | 79.2 74.9 |
5.4 | CH3 | П3 |
| 2.219 | ||||||||
| Al(3) | 2.104 | 103.6 | ||||||
| 2.095 | ||||||||
| MURQUL | Al(1) | 2.593 | 2.096 | 103.6 | 76.4 | 5.5 | CH3 | П3 |
| Al(2) | 2.587 | 2.098 | 104.2 | 75.8 | 5.9 | CH3 | П3 | |
| QACLUD | Al(1) | 2.641 | 2.135 | 103.3 | 76.7 | 5.4 | Ph–CH=C–SiMe3 | П3 |
| QEMWIO | Al(1) | 2.572 | 2.145 | 101.5 | 75.3 75.3 |
5.8 | CH3 | П3 |
| 2.127 | ||||||||
| Al(2) | 2.067 | 105.7 | ||||||
| 2.083 | ||||||||
| TPHNAL10 | Al(1) | 2.701 | 2.178 | 103.5 | 76.5 | 5.1 | Ph | П3 |
| UHICAQ | Al(1) | 2.663 | 2.104 | 101.6 | 78.5 78.3 |
4.5 | CH2 | П3 |
| 2.104 | ||||||||
| Al(2) | 2.105 | 101.2 | ||||||
| 2.117 | ||||||||
| BOCYAT | Al(1) | 2.818 | 2.129 | 98.1 | 81.9 | 2.7 | Tol | П1 |
| FIMHIU | Al(1) | 2.845 | 2.037 | 93.1 | 86.9 | 1.2 | C≡C | П1 |
| HALWEX | Al(1) | 3.030 | 2.224 | 88.3 | 91.7 | – | C≡C–Ph | – |
| HEWDAP | Al(1) | 2.833 | 2.031 | 99.5 | 80.6 | 3.1 | CH2 | П1 |
| QEWZUO | Al(2) | 2.807 | 2.449 | 89.2 | 79.8 84.2 |
3.4 | Cp | П1 |
| 2.019 | ||||||||
| Al(3) | 2.042 | 97.0 | ||||||
| 2.164 | ||||||||
| RAQXIR | Al(2) | 2.906 | 1.995 | 80.5 | 72.7 88.8 |
3.2 | Cp | П1 |
| 2.777 | ||||||||
| Al(3) | 2.155 | 97.7 | ||||||
| 2.015 | ||||||||
| VAHJIZ | Al(1) | 2.879 | 2.032 | 90.7 | 87.3 87.2 |
1.1 | C≡C | П1 |
| 2.129 | ||||||||
| Al(2) | 2.141 | 90.2 | ||||||
| 2.040 | ||||||||
| VUJJUG | Al(2) | 2.845 | 2.539 | 87.6 | 76.0 84.9 |
3.1 | Cp | П1 |
| 2.018 | ||||||||
| Al(3) | 2.037 | 97.2 | ||||||
| 2.192 |
* d(Al–Al) – расстояние между атомами алюминия, ∠CAlC – угол между мостиковыми атомами углерода и атомом алюминия, ∠AlCAl – угол между атомами алюминия и мостиковым атомом углерода, Ω(Al–Al) – телесный угол общей грани ПВД двух атомов алюминия, Cp – циклопентадиенил, Ph – фенил, Tol – толил, КХФ – кристаллохимическая формула.
ЗАКЛЮЧЕНИЕ
Использование метода разбиения кристаллического пространства с помощью ПВД атомов позволяет выявлять абсолютно все контакты между атомами в структурах кристаллов, а не только наиболее значимые, что, в частности, дало возможность охарактеризовать кластерные связи Al–Al, не характерные для трехвалентного атома алюминия.
Список литературы
Эльшенбройх К. Металлоорганическая химия. М.: БИНОМ. Лаборатория знаний, 2011. 746 с. [Elschenbroich C. Organometallchemie. Teubner Verlag, 2008.]
Aguirre-Diaz L.M., Reinares-Fisac D., Iglesias M. et al. // Coord. Chem. Rev. 2017. V. 335. № 1. P. 1. https://doi.org/10.1016/j.ccr.2016.12.003
Cambridge Structural Database System, Version 5.32 (Crystallographic Data Centre, Cambridge, 2017).
Blatov V.A., Shevchenko A.P., Serezhkin V.N. // Russ. J. Coord. Chem. 1999. Т. 25. № 7. С. 453. [Блатов В.А., Шевченко А.П., Сережкин В.Н. // Коорд. химия. 1999. Т. 25. № 7. С. 483.]
Вайнштейн Б.К., Фридкин В.М., Инденмоб В.Л. Современная кристаллография в 4-х томах. Т. 1. М.: Наука, 1979. С. 161.
Medley J.H., Fronczek F.R., Ahmad N. et al. // J. Crystallogr. Spectrosc. Res. 1985. V. 15. № 2. P. 99.
Blatova O.A., Blatov V.A., Serezhkin V.N. // Russ. J. Coord. Chem. 2000. V. 26. № 12. P. 847. [Блатова О.А., Блатов В.А., Сережкин В.Н. // Коорд. химия. 2000. Т. 26. № 12. С. 903.]
Wolf R., Hoppe R. // Z. Anorg. Allg. Chem. 1985. V. 528. № 9. P. 129. https://doi.org/10.1002/zaac.19855280914
Блатов В.А., Сережкин В.Н. // Коорд. химия. 1997. Т. 23. № 3. С. 192.
Uhl W., Er E., Hübner O., Himmel H.J. // Z. Anorg. Allg. Chem. 2008. V. 634. № 12. P. 2133. https://doi.org/10.1002/zaac.200800156
Fisher J.D., Budzelaar P.H.M., Shapiro P.J. et al. // Organometallics. 1997. V. 16. № 5. P. 871. https://doi.org/10.1021/om9610049
Shevchenko A.P., Serezhkin V.N. // Russ. J. Phys. Chem. 2004. V. 78. № 10. P. 1598. [Шевченко А.П., Сережкин В.Н. // Журн. физ. химии. 2004. Т. 78. № 10. С. 1817.]
Сережкин В.Н., Блатов В.А., Шевченко А.П. // Коорд. химия. 1995. Т. 21. № 3. С. 163.
Serezhkin V.N., Byslaev Yu.A. // Russ. J. Inorg. Chem. 1997. V. 42. № 7. P. 1064. [Сережкин В.Н., Буслаев Ю.А. // Журн. неорган. химии. 1997. Т. 42. № 7. С. 1180.]
Сережкин В.Н., Сережкина Л.Б. // Коорд. химия. 1999. Т. 25. № 3. С. 182.
Gorden J.D., Macdonald C.L.B., Cowley A.H. // Chem. Commun. 2001. V. 37 № 1. P. 75. https://doi.org/10.1039/B007341P
Schulz S., Kuczkowski A., Schuchmann D. et al. // Organometallics. 2006. V. 25. № 22. P. 5487. https://doi.org/10.1021/om060676o
Burns C.T., Shapiro P.J., Budzelaar P.H.M. et al. // Organometallics. 2000. V. 19. № 17. P. 3361. https://doi.org/10.1021/om000173x
Dohmeier C., Schnöckel H., Schneider U. et al. // Angew. Chem. Int. Ed. 1993. V. 32. № 11. P. 1655. https://doi.org/10.1002/anie.199316551
Блатов В.А., Полькин В.А., Сережкин В.Н. // Кристаллография. 1994. Т. 39. № 3. С. 457.
Serezhkin V.N., Mikhailov Yu.N., Byslaev Yu.A. // Russ. J. Inorg. Chem. 1997. V. 42. № 12. P. 1871. [Сережкин В.Н., Михайлов Ю.Н., Буслаев Ю.А. // Журн. неорган. химии. 1997. Т. 42. № 12. С. 2036.]
Kickham J.E., Guerin F., Stewart J.C. et al. // Organometallics. 2001. V. 20. № 6. P. 1175. https://doi.org/10.1021/om001047w
Uhl W., Breher F. // Organometallics. 2000. V. 19. № 22. P. 4536. https://doi.org/10.1021/om000244s
Uhl W., Breher F., Lützen A., Saak W. // Angew. Chem. Int. Ed. 2000. V. 39. № 2. P. 406.
Uhl W., Er E., Hepp A. et al. // Eur. J. Inorg. Chem. 2009. V. 2009. № 22. P. 3307. https://doi.org/10.1002/ejic.200900264
Serezhkin V.N., Vologzhanina A.V., Serezhkina L.B. et al. // Acta Crystallogr. 2009. V. 65B. № 1. P. 45. https://doi.org/10.1107/S0108768108038846
Uhl W., Breher F., Haddadpour S. et al. // Z. Anorg. Allg. Chem. 2004. V. 630. № 15. P. 1839. https://doi.org/10.1002/zaac.200400150
Hair G.S., Cowley A.H., Gorden J.D. et al. // Chem. Commun. 2003. № 3. P. 424. https://doi.org/10.1039/B210024J
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


