Журнал неорганической химии, 2019, T. 64, № 8, стр. 874-880
Термодинамические свойства моноклинной модификации ортотанталата неодима M-NdTaO4
В. Н. Гуськов 1, *, Е. Г. Сазонов 2, А. В. Тюрин 1, А. В. Гуськов 1, М. А. Рюмин 1, К. С. Гавричев 1
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
2 ООО “Технологические системы защитных покрытий”
142172 Москва, Симферопольское шоссе, 19, Россия
* E-mail: guskov@igic.ras.ru
Поступила в редакцию 25.01.2019
После доработки 04.02.2019
Принята к публикации 15.03.2019
Аннотация
Методом адиабатической калориметрии измерена изобарная теплоемкость ортотанталата неодима M-NdTaO4 в интервале температур 7–342 K. По сглаженным значениям теплоемкости рассчитаны термодинамические функции (энтропия, приращение энтальпии и приведенная энергия Гиббса) в области 0–345 K без учета вклада низкотемпературного (<8 K) магнитного превращения.
ВВЕДЕНИЕ
Ортотанталаты редкоземельных элементов – двойные высокотемпературные оксиды состава RETaO4 – характеризуются высокой плотностью, химической стабильностью, радиационной устойчивостью; проявляют интересные фотокаталитические и диэлектрические свойства, высокотемпературную ионную проводимость [1–8]. Низкая теплопроводность позволяет рассматривать ортотанталаты, в частности ортотанталат неодима, в качестве термобарьерных [9] или лазерных [10] материалов. Кристаллическая структура ортотанталатов определяется ионным радиусом редкоземельного элемента, и в ряду лантаноидов ортотанталат неодима является первым представителем, кристаллизующимся в моноклинной сингонии М (пр. гр. I2/a) типа фергюсонита, содержащей 4 формульные единицы (Z = 4) в ячейке. Это единственная низкотемпературная модификация NdTaO4, в отличие от ортотанталатов более тяжелых лантаноидов, которые в обычных условиях существуют также и в моноклинной модификации M' (пр. гр. P2/a) с Z = 2 [1]. При температурах выше ~1600 K (1330°C) М-ортотанталат неодима претерпевает обратимое фазовое превращение в тетрагональную модификацию T (пр. гр. I41/a, Z = 4), структурный тип шеелита [11]. Хотя фазовый переход M ↔ T происходит без скачкообразного изменения параметров кристаллической решетки (и его следует отнести к фазовым превращениям 2-го рода), монокристаллический М-NdTaO4 (Tпл = = 2098 K), выращенный по методу Чохральского в работе [10], несмотря на медленное охлаждение, треснул вдоль плоскости [010], что, возможно, объясняется анизотропией термического расширения. При кристаллизации тонких пленок золь-гель методом на оксиде алюминия с последующим отжигом при ~1000°C было обнаружено одновременное существование двух моноклинных (М и М ') и тетрагональной (Т ') модификаций ортотанталата неодима [12]. В работе [13] показано, что при керамическом методе синтеза однофазные образцы ортотанталата неодима могут быть получены лишь при отжиге при температурах выше 1473 K (1200°С), в противном случае наблюдается неполное взаимодействие оксидов с образованием в том числе метастабильной тетрагональной фазы Т '.
Получение однофазного и равновесного ортотанталата неодима связано с необходимостью проведения высокотемпературных обработок, а практическое использование в виде пленок, монокристаллов или компонентов, например, термобарьерных материалов требует тщательного изучения устойчивости и возможности взаимодействия с подложками или окружающей средой. Оптимальным способом предварительного анализа является термодинамическое моделирование равновесных процессов при наличии известных термодинамических характеристик участвующих веществ, в том числе изобарной теплоемкости.
Целью настоящей работы является измерение изобарной теплоемкости М-NdTaO4 и определение термодинамических функций в интервале температур 0–345 K.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Ортотанталат неодима получали методом обратного осаждения из пентахлорида тантала (99.99%) и сексвиоксида неодима (99.99%). TaCl5 растворяли в этаноле, а Nd2O3 – в соляной кислоте. Методика синтеза подробно описана в [14, 15]. Окончательный отжиг полученного ортотанталата осуществляли при температуре 1773 K (1500°С). Дифракционные исследования фазового состава и кристаллической структуры порошка проводили на дифрактометре Bruker D8 Advance (CuKα, λ = 1.5418 Å, Ni-фильтр, LYNXEYE детектор, геометрия на отражение) в интервале углов 2θ = 10°–80°. Теплоемкость измеряли автоматическим низкотемпературным калориметром АОЗТ “Термис”, описание которого приведено в работе [16]. Условия измерений описаны нами ранее в [15]. Термический анализ проведен с помощью установки синхронного термического анализа STA 449F1 Jupiter® фирмы Netzsch в атмосфере газообразного аргона высокой чистоты (99.9995%). Морфологию образцов изучали с помощью электронного микроскопа Cross Beam Zeiss NVision 40.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Для синтеза ортотанталата неодима был применен метод обратного осаждения, который позволяет не только снизить температуру взаимодействия компонентов, но и избежать возможных загрязнений [3].
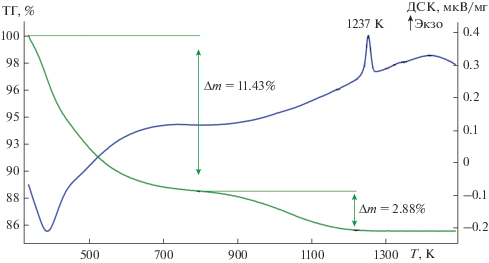
Для определения характерных температур взаимодействия компонентов осажденного и высушенного прекурсора ортотанталата неодима был выполнен его ДСК/ТГ-анализ (рис. 1). Нагревание сопровождается экзотермической потерей ∼3 молей воды на каждый моль ортотанталата в интервале температур 300–700 K; в области ~850–1225 K начинается постепенное взаимодействие компонентов с удалением еще ~1 моля H2O, приводящее к полной потере гидроксильных групп. После этого масса образца стабилизируется и наблюдается интенсивное взаимодействие компонентов, сопровождаемое экзотермическим эффектом с максимумом при 1237 K. Судя по тому, что ДСК-кривая имеет выраженный положительный наклон, взаимодействие компонентов не является полным и продолжается вплоть до температуры 1400 K (максимум на кривой ДСК). Дифракционные исследования образцов прекурсора, отожженных при 1073, 1273, 1473 K, показали, что полученные образцы не являются однофазными и содержат помимо основного компонента – M-NdTaO4 – также Nd3TaO7 и Ta2O5. Соединение Nd3TaO7 имеет структуру дефектного флюорита (веберита) с пр. гр. Cmcm [1], и его образование обусловлено, с одной стороны, высокой гомогенностью распределения исходных компонентов, а с другой – тем, что оно более устойчиво, чем ортотанталат, так как имеет бóльшую температуру плавления (~2250 и 2100 K соответственно) [17]. Таким образом, существующее предположение [3] о том, что синтез ортотанталата неодима происходит через промежуточное образование Nd3TaO7, можно считать вполне вероятным.
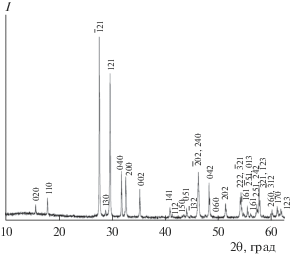
Однофазный образец M-ортотанталата неодима для дальнейших исследований был получен в результате отжига в течение 4 ч при температуре 1773 K. На дифрактограмме порошка М-NdTaO4 (рис. 2) отсутствуют посторонние рефлексы, а расчет параметров кристаллической решетки дает следующие результаты: пр. гр. I2/a, a = = 5.514(1), b = 11.238(1), c = 5.116(1) Å, β = 95.71°, V = 315.46 Å3. Эти значения хорошо совпадают с данными, полученными для монокристаллического стехиометрического M-ортотанталата неодима (a = 5.5153(8), b = 11.2388(16), c = 5.1184(7) Å, β = 95.7731(3)°, V = 315.68(13) Å3) в работе [10], а также со справочными величинами [18]. Рентгенофлюоресцентный анализ (OPTIMA-X) подтвердил отсутствие посторонних примесей и показал, что соотношение Nd : Ta = 1 : 1.049, что в пределах точности метода соответствует стехиометрии. Чтобы убедиться, что полученный образец не является наноразмерным, т.е. пригодным для термодинамических исследований, с помощью электронной микроскопии изучили морфологию синтезированного вещества (рис. 3). Основная масса образца состоит из плотных кристаллических структур с линейными размерами ~2 мкм и не является наноразмерной. Наличие мелких фрагментов, по-видимому, свидетельствует о механических напряжениях, возникающих при охлаждении, хотя это явление не характерно для фазовых превращений второго рода. Как было отмечено выше, образования трещины в монокристаллическом образце авторам [10] избежать не удалось (несмотря на медленное охлаждение) вследствие анизотропии термического расширения и, возможно, фазового превращения. Наши исследования морфологии M-ортотанталатов самария и гадолиния, полученных в аналогичных условиях, показали, что для ортотанталата самария наблюдается минимальное число мелких фрагментов [19], а в случае ортотанталата гадолиния их вообще нет [15]. Таким образом, наблюдается прямая связь термических напряжений и образования мелких фрагментов с ионным радиусом катиона ортотанталата.
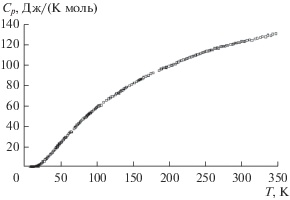
Синтезированный и охарактеризованный образец М-ортотанталата неодима был использован для измерений изобарной теплоемкости при температурах до 345 K. Для измерений низкотемпературной теплоемкости брали образец массой 4.27374 г. При расчетах использовали величину мольной массы NdTaO4, равную 389.187 г/моль, которая была вычислена с помощью справочных данных [20]. Низкотемпературная теплоемкость была измерена при температурах 7.37–341.61 K методом адиабатической калориметрии в 160 экспериментальных точках (табл. 1, рис. 4). Полученная экспериментальная зависимость Ср(Т) не имеет видимых аномалий. Температурная зависимость низкотемпературной теплоемкости M-NdTaO4 сглажена полиномом согласно алгоритму, изложенному в [21]:
(1)
$С _{р }^{0}(T) = \sum\limits_0^7 {{{A}_{j}}{{U}^{j}}} ,\,\,\,\,{\text{г д е }}\,\,\,\,U = {\text{ln}}({T \mathord{\left/ {\vphantom {T {400}}} \right. \kern-0em} {400}}).$Таблица 1.
Экспериментальная теплоемкость NdTaO4, Дж/(K моль)
| T, K | Cp | T, K | Cp | T, K | Cp | T, K | Cp |
|---|---|---|---|---|---|---|---|
| 7.37 | 0.166 | 24.96 | 4.878 | 96.52 | 56.16 | 228.75 | 106.4 |
| 8.55 | 0.241 | 26.63 | 5.820 | 98.83 | 57.46 | 231.17 | 107.1 |
| 8.83 | 0.282 | 28.45 | 7.299 | 102.19 | 59.20 | 233.07 | 107.6 |
| 9.04 | 0.291 | 29.95 | 8.189 | 108.66 | 62.58 | 235.46 | 108.2 |
| 9.26 | 0.315 | 31.65 | 9.621 | 112.11 | 64.34 | 237.41 | 108.8 |
| 9.48 | 0.327 | 33.40 | 10.67 | 115.56 | 66.03 | 239.80 | 109.5 |
| 9.82 | 0.365 | 34.98 | 12.13 | 119.02 | 67.86 | 241.74 | 109.9 |
| 10.08 | 0.3854 | 36.64 | 13.26 | 121.17 | 68.52 | 244.15 | 110.6 |
| 10.50 | 0.4235 | 38.30 | 14.86 | 126.33 | 71.26 | 246.01 | 111.1 |
| 10.77 | 0.4544 | 39.98 | 15.84 | 128.22 | 71.61 | 252.66 | 112.4 |
| 11.26 | 0.5152 | 40.02 | 15.95 | 131.80 | 73.16 | 254.49 | 112.8 |
| 11.92 | 0.5829 | 41.63 | 17.46 | 133.27 | 74.13 | 256.89 | 113.5 |
| 12.01 | 0.5988 | 43.28 | 18.51 | 136.77 | 75.74 | 258.70 | 113.4 |
| 12.27 | 0.6174 | 44.94 | 20.15 | 138.69 | 76.50 | 261.09 | 114.7 |
| 12.63 | 0.6794 | 45.69 | 20.89 | 140.26 | 77.31 | 262.88 | 115.0 |
| 12.78 | 0.7070 | 46.59 | 21.19 | 143.76 | 78.53 | 265.28 | 115.3 |
| 13.05 | 0.7387 | 48.27 | 22.86 | 147.26 | 79.88 | 269.46 | 116.1 |
| 13.37 | 0.7801 | 49.91 | 23.93 | 150.75 | 81.51 | 271.16 | 116.5 |
| 13.57 | 0.8227 | 52.42 | 26.17 | 151.02 | 81.54 | 273.60 | 116.6 |
| 13.85 | 0.8439 | 53.20 | 26.54 | 154.27 | 82.73 | 277.72 | 117.8 |
| 14.15 | 0.9012 | 54.08 | 27.68 | 157.77 | 84.40 | 279.32 | 117.8 |
| 14.41 | 0.9511 | 59.07 | 30.88 | 161.27 | 85.60 | 283.35 | 118.6 |
| 14.69 | 0.9704 | 60.73 | 32.22 | 170.27 | 88.64 | 285.85 | 118.7 |
| 14.94 | 1.032 | 62.39 | 33.73 | 177.28 | 91.17 | 287.36 | 119.0 |
| 15.53 | 1.127 | 67.44 | 36.90 | 188.34 | 94.90 | 289.87 | 119.8 |
| 15.75 | 1.174 | 69.88 | 38.51 | 191.82 | 96.14 | 291.34 | 119.9 |
| 16.14 | 1.204 | 70.85 | 39.71 | 194.29 | 96.43 | 293.87 | 120.2 |
| 16.44 | 1.270 | 72.72 | 41.13 | 195.32 | 96.91 | 295.28 | 120.4 |
| 16.62 | 1.321 | 74.81 | 42.48 | 198.65 | 97.72 | 297.85 | 121.5 |
| 17.03 | 1.459 | 76.01 | 43.49 | 201.30 | 98.73 | 299.19 | 121.6 |
| 17.50 | 1.609 | 80.23 | 46.32 | 205.22 | 99.74 | 306.21 | 122.8 |
| 17.95 | 1.718 | 83.61 | 48.07 | 209.58 | 101.0 | 309.87 | 123.2 |
| 18.38 | 1.877 | 84.85 | 48.66 | 211.43 | 101.6 | 317.21 | 124.2 |
| 18.91 | 2.057 | 85.86 | 50.02 | 213.93 | 102.4 | 319.97 | 124.7 |
| 19.29 | 2.198 | 87.09 | 50.66 | 215.79 | 102.8 | 324.49 | 125.4 |
| 20.24 | 2.491 | 88.04 | 51.24 | 218.26 | 103.6 | 327.30 | 126.3 |
| 21.61 | 3.086 | 90.21 | 52.21 | 220.13 | 104.0 | 331.72 | 126.1 |
| 21.83 | 3.226 | 90.58 | 52.38 | 222.60 | 104.8 | 334.48 | 127.4 |
| 23.29 | 3.934 | 92.77 | 54.07 | 224.44 | 105.2 | 338.89 | 127.3 |
| 23.49 | 4.019 | 94.95 | 55.20 | 226.92 | 106.0 | 341.61 | 128.5 |
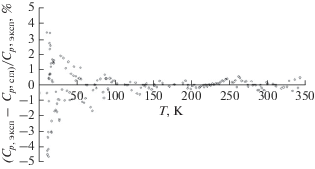
Коэффициенты сглаживающего полинома приведены в табл. 2. Разброс экспериментальных точек относительно сглаженных значений показан на рис. 5. Теплоемкость NdTaO4 экстраполирована к 0 K по уравнению Дебая (Ср = АТ 3) без учета магнитного превращения в области 0–8 K и приведена в табл. 3 курсивом. Термодинамические функции M-ортотанталата неодима, приведенные в табл. 3, рассчитаны на основании уравнения (1) также без учета вклада магнитного превращения. Это превращение не может внести заметный вклад в теплоемкость и изменение энтальпии NdTaO4, однако при расчете абсолютной энтропии влияние магнитных превращений желательно учесть. К сожалению, данные о прямых измерениях теплоемкости ортотанталата неодима ниже температуры 8 K в литературе отсутствуют, но можно ориентироваться на результаты, полученные для ортофосфата неодима, также имеющего моноклинную структуру, пр. гр. P21/n [22]. Низкотемпературное магнитное превращение из антиферромагнитного в парамагнитное состояние в области температур, близких к 0 K, увеличивает энтропию ортофосфата неодима на величину Rln(2) = 5.76 Дж/(K моль). Стандартные термодинамические свойства M-ортотанталата неодима при 298.15 K без учета низкотемпературных магнитных переходов составляют:
Таблица 2.
Коэффициенты уравнения (1) Ср = = $\sum\nolimits_0^7 {{{A}_{j}}{{U}^{j}}} ,$ где U = ln(T/400), описывающего теплоемкость М-NdTaO4
| j | Aj, Дж/(K моль) |
|---|---|
| 0 | 0.13352615 × 103 |
| 1 | 0.2615512 × 102 |
| 2 | –0.70250045 × 102 |
| 3 | –0.74650843 × 102 |
| 4 | –0.445731105 × 102 |
| 5 | –0.153991434 × 102 |
| 6 | –0.27121946 × 101 |
| 7 | –0.18730657 × 100 |
Таблица 3.
Сглаженные значения термодинамических функций моноклинной модификации NdTaO4
| T, K | $C_{p}^{0},$ Дж/(K моль) | S0, Дж/(K моль) | H0(T) – H0(0), Дж/моль |
Ф0, Дж/(K моль) |
|---|---|---|---|---|
| 1 | 0.000327 | 0.000109 | 0.0000817 | 0.0000272 |
| 2 | 0.00261 | 0.000871 | 0.00131 | 0.000218 |
| 3 | 0.00882 | 0.00294 | 0.00662 | 0.000735 |
| 4 | 0.0209 | 0.00697 | 0.0209 | 0.00174 |
| 5 | 0.0408 | 0.0136 | 0.0511 | 0.00340 |
| 6 | 0.0706 | 0.0235 | 0.106 | 0.00588 |
| 7 | 0.112 | 0.0374 | 0.196 | 0.00934 |
| 8 | 0.167 | 0.0558 | 0.335 | 0.0139 |
| 10 | 0.3770 | 0.1122 | 0.8512 | 0.02712 |
| 15 | 1.016 | 0.3795 | 4.255 | 0.09579 |
| 20 | 2.437 | 0.8395 | 12.43 | 0.2181 |
| 25 | 4.948 | 1.635 | 30.50 | 0.4151 |
| 30 | 8.251 | 2.820 | 63.25 | 0.7113 |
| 35 | 12.02 | 4.370 | 113.8 | 1.119 |
| 40 | 16.02 | 6.234 | 183.8 | 1.639 |
| 45 | 20.09 | 8.355 | 274.1 | 2.265 |
| 50 | 24.13 | 10.68 | 384.6 | 2.988 |
| 60 | 31.95 | 15.78 | 665.4 | 4.688 |
| 70 | 39.25 | 21.26 | 1022 | 6.661 |
| 80 | 46.00 | 26.95 | 1449 | 8.839 |
| 90 | 52.22 | 32.73 | 1940 | 11.17 |
| 100 | 57.96 | 38.53 | 2491 | 13.62 |
| 110 | 63.27 | 44.31 | 3098 | 16.15 |
| 120 | 68.21 | 50.03 | 3756 | 18.73 |
| 130 | 72.82 | 55.67 | 4461 | 21.36 |
| 140 | 77.14 | 61.23 | 5211 | 24.01 |
| 150 | 81.21 | 66.69 | 6003 | 26.67 |
| 160 | 85.03 | 72.06 | 6834 | 29.34 |
| 170 | 88.65 | 77.32 | 7703 | 32.01 |
| 180 | 92.07 | 82.49 | 8607 | 34.67 |
| 190 | 95.32 | 87.55 | 9544 | 37.32 |
| 200 | 98.39 | 92.52 | 10510 | 39.97 |
| 210 | 101.3 | 97.39 | 11510 | 42.58 |
| 220 | 104.1 | 102.2 | 12540 | 45.17 |
| 230 | 106.7 | 106.9 | 13590 | 47.76 |
| 240 | 109.2 | 111.5 | 14670 | 50.33 |
| 250 | 111.6 | 116.0 | 15780 | 52.84 |
| 260 | 113.9 | 120.4 | 16900 | 55.38 |
| 270 | 116.0 | 124.7 | 18050 | 57.87 |
| 280 | 118.0 | 129.0 | 19220 | 60.33 |
| 290 | 119.9 | 133.2 | 20410 | 62.77 |
| 298.15 | 121.4 | 136.5 | 21400 | 64.72 |
| 300 | 121.7 | 137.2 | 21620 | 65.17 |
| 310 | 123.4 | 141.3 | 22850 | 67.55 |
| 320 | 124.9 | 145.2 | 24090 | 69.92 |
| 330 | 126.4 | 149.1 | 25350 | 72.25 |
| 340 | 127.7 | 152.9 | 26620 | 74.57 |
| 345 | 128.3 | 154.7 | 27260 | 75.72 |
ЗАКЛЮЧЕНИЕ
Изобарная теплоемкость M-NdTaO4 впервые измерена методом адиабатической калориметрии в области температур 7.4–341.6 K и показано, что в области низких температур ортотанталат неодима не претерпевает структурных превращений. Полученные температурные зависимости изобарной теплоемкости и других термодинамических функций моноклинного М-ортотанталата неодима могут быть использованы при разработке новых материалов на его основе и термодинамическом моделировании систем с его участием.
Список литературы
Арсеньев П.А., Глушкова В.Б., Евдокимов А.А. и др. Соединения редкоземельных элементов. Цирконаты, гафнаты, ниобаты, танталаты, антимонаты. М.: Наука, 1985. 261 с.
Портной К.И., Тимофеева Н.И., Алибеков С.Е. и др. // Изв. АН СССР. Сер. Неорган. материалы. 1970. Т. 6. С. 289.
Рождественский Ф.А., Зуев М.Г., Фотиев А.А. Танталаты трехвалентных металлов. М.: Наука, 1986. 168 с.
Siqueira K.P., Carmo A P., Bell M.J.V. et al. // J. Lumin. 2016. V. 179. P. 146. https://doi.org/0.1016/j.jlumin.2016.06.054
Dias A., Siqueira K.P., Moreira R.L. // J. Alloys Compd. 2017. V. 693. P. 1243. https://doi.org/10.1016/j.jallcom.2016.10.077
Nyman M., Rodriguez M.A., Alam T.D. et al. // Chem. Mater. 2009. V. 21. P. 2201. https://doi.org/10.1021/cm9001509
Brunskova H., Mudra E., Medvecky L. et al. // Mat. Des. 2017. V. 134. P. 455. https://doi.org/10.1016/j.matdes.2017.08.068
Fujita A., Matsushita H., Katsui A. // Mater. Sci. Forum. 2007. V. 534. P. 1069. https://doi.org/10.4028/www.scientific.net/MSF.534-536.1069
Wang J., Chong X.Y., Zhou R., Feng J. // Scripta Mater. 2017. V. 126. P. 24. https://doi.org/10.1016/j.scriptamat.2016.08.019
Ning K., Zhang Q., Zhang D. et al. // J. Cryst. Growth. Des. 2014. V. 388. P. 83. https://doi.org/10.1016/j.jcrysgro.2013.10.03
Stubiĉan V.S. // J. Am. Ceram. Soc. 1964. V. 47. P. 55. https://doi.org/10.1111/j.1151-2916.1964.tb15654.x
Brunckova E., Kolev H., Kanuchova M. // Surf. Interface Anal. 2018. P. 1. https://doi.org/10.1002/sia.6583
Siqueira K.P., Dias A. // Mater. Res. 2014. V. 17 (Suppl. 1). P. 167. https://doi.org/10.1590/S1516-14392013005000189
Ryumin M.A., Sazonov E.G., Guskov V.N. et al. // Inorg. Mater. 2016. V. 52. P. 1149. [Рюмин М.А., Сазонов Е.Г., Гуськов В.Н. и др. // Неорган. материалы. 2016. Т. 52. С. 1223. https://doi.org/10.7868/S0002337X16110142]https://doi.org/10.1134/S0020168516110145
Ryumin M.A., Sazonov E.G., Guskov V.N. et al. // Inorg. Mater. 2017. V. 53. P. 728. [Рюмин М.А., Сазонов Е.Г., Гуськов В.Н. и др. // Неорган. материалы. 2017. Т. 53. С. 737. https://doi.org/10.7868/S0002337X17070120]https://doi.org/10.1134/S0020168517070147
Малышев В.В., Мильнер Г.А., Соркин Э.Л., Шибакин В.Ф. // Приборы и техника эксперимента. 1985. № 6. С. 195.
Yokogawa Y., Yoshimura M. // J. Am. Ceram. Soc. 1997. V. 80. P. 1965. https://doi.org/10.1111/j.1151-2916.1997.tb03079.x
JCPDS-ICCD PDF-2 Database #33-941.
Tyurin A.V., Khoroshilov A.V., Gus’kov V.N. et al. // Russ. J. Inorg. Chem. 2018. V. 63. P. 1599. [Тюрин А.В., Хорошилов А.В., Гуськов В.Н. и др. // Журн. неорган. химии. 2018. Т. 63. С. 1583. https://doi.org/10.1134/S0044457X18120218]https://doi.org/10.1134/S0036023618120215
https://www.nist.gov/pml/atomic-weights-and-isotopic-compositions-relativeatomic-masses
Гуревич В.М., Хлюстов В.Г. // Геохимия. 1979. № 6. С. 829.
Popa K., Jutier F., Wastin F., Konings R.J.M. // J. Chem. Thermodyn. 2006. V. 38. P. 1306. https://doi.org/10.1016/j.jct.2006.02.06
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии