Журнал неорганической химии, 2020, T. 65, № 1, стр. 40-48
Влияние природы заместителя R в карбоксилат-анионе на строение полимеров γ,γ'-дипиридила с моноядерными бензоатом и цимантренатом марганца(II)
М. А. Уварова a, А. А. Гринева a, Р. Р. Датчук a, С. Е. Нефедов a, *
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
* E-mail: snef@igic.ras.ru
Поступила в редакцию 24.07.2019
После доработки 18.08.2019
Принята к публикации 27.08.2019
Аннотация
При взаимодействии водного ацетата марганца с бензойной кислотой в метаноле получен комплекс Mn[(OOCPh]2[O(H)Me]4 (1) с высоким выходом. Медленная диффузия раствора γ,γ'-дипиридила в метаноле в метанольный раствор аддукта 1 и Mn[(OOCC5H4Mn(CO)3]2[O(H)Me]4 при соотношении реагентов 1 : 1 (комнатная температура) приводит к образованию полимеров {[(µ-γ,γ'-dipy)Mn(µ-OOCPh)]2}n (2, 2D) и {(µ-γ,γ'-dipy)2Mn2[µ-(OOCC5H4Mn(CO)3]2[η2-(OOCC5H4Mn(CO)3]2}n (3, 1D) соответственно. Полученные соединения 1–3 исследованы методами химического анализа, ИК-спектроскопии и РСА.
ВВЕДЕНИЕ
Комплексы металлов с полидентатными анионами карбоновых кислот широко используются для получения координационных полимеров (КП) различной размерности и геометрии. При этом природа заместителя в карбоксилат-анионе позволяет во многих случаях регулировать не только топологию полимера, но и спиновое состояние атомов металлов, формирующих металлокомплекс, и существенным образом влиять на физико-химические свойства образующихся материалов, в первую очередь каталитические, сорбционные, магнитные, нелинейно-оптические и др. [1–9].
Введение в такие КП высокоспиновых атомов марганца(II) позволяет ожидать значительного усиления магнитных свойств по сравнению с остальными 3d-металлами [10–13].
Ранее при изучении строения КП, образующихся в результате диффузии в раствор аддуктов переходных металлов M(OOСR)2[O(H)Me]4 (R = = Ph, (C5H4)Mn(CO)3; M = ZnII, CoII, NiII) в метаноле бидентатного γ,γ'-дипиридила в одинаковых условиях (концентрация реагентов, растворитель, температура), было показано, что их геометрия зависит от природы переходного металла и заместителя R в карбоксилат-анионах [14–16].
В продолжение проводимых исследований реакционной способности метанольных аддуктов цимантренатов и бензоатов 3d-металлов в настоящей работе изучены особенности строения КП, полученных при взаимодействии карбоксилатов MnII(OOСR)2[O(H)Me]4 (R = Ph, (C5H4)Mn(CO)3) с γ,γ'-дипиридилом.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все операции по синтезу и выделению комплексов проводили в атмосфере чистого аргона с использованием абсолютированных растворителей.
ИК-спектры кристаллических образцов регистрировали в интервале 4000–550 см–1 методом НПВО на ИК-Фурье-спектрометре Nexus фирмы Nicolet с использованием приставки MIRacle фирмы PIKETechnologies с алмазным кристаллом.
РСА кристаллов 1–3 выполнен по стандартной методике на автоматическом дифрактометре Bruker SMART Apex II, оборудованном CCD-детектором (λMo, графитовый монохроматор, ω‑сканирование).
Уточнение структур выполнено с использованием комплекса программ SHELXTL PLUS (PC версия) [17–20].
Кристаллографические данные и детали уточнения приведены в табл. 1, основные геометрические параметры изученных комплексов – в табл. 2–4. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (CCDC, № 1941030-1941032).
Таблица 1.
Кристаллографические параметры и детали уточнения структур комплексов 1–3
| Параметр | 1 | 2 | 3 |
|---|---|---|---|
| Номер CCDC | 1 941 030 | 1 941 032 | 1 941 031 |
| Брутто-формула | C18H26MnO8 | C24H18MnN2O4 | C30H24Mn3N2O12 |
| М. м. | 425.33 | 453.34 | 769.33 |
| T, K | 150(2) | 150(2) | 150(2) |
| Цвет | Бесцветный | Светло-розовый | Светло-розовый |
| Сингония | Моноклинная | Орторомбическая | Моноклинная |
| Пр. гр. | P2(1)/c | Pbcn | С2/с |
| a, Å | 9.9458(6) | 18.5885(14) | 18.9574(19) |
| b, Å | 12.2072(8) | 11.6689(9) | 11.6238(11) |
| c, Å | 8.6887(5) | 9.4326(7) | 29.888(3) |
| α, град | 90 | 90 | 90 |
| β, град | 102.3110(10) | 90 | 108.289(2) |
| γ, град | 90 | 90 | 90 |
| V, Å3 | 1030.64(11) | 2046.0(3) | 6253.3(11) |
| Z | 2 | 4 | 8 |
| ρрасч, мг/м3 | 1.371 | 1.472 | 1.634 |
| µ, мм–1 | 0.680 | 0.680 | 1.260 |
| F(000) | 446 | 932 | 3112 |
| Размеры кристалла, мм | 0.28 × 0.24 × 0.20 | 0.24 × 0.22 × 0.20 | 0.24 × 0.22 × 0.18 |
| θ-область сканирования, град | 2.68–29.99 | 2.06–30.00 | 2.26– 30.00 |
| Интервалы индексов отражений | –13 ≤ h ≤ 10, –16 ≤ k ≤ 17, –10 ≤ l ≤12 |
–25 ≤ h ≤ 26, –16 ≤ k ≤ 16, –13 ≤ l ≤ 13 |
–24 ≤ h ≤ 26, –16 ≤ k ≤ 13, –42 ≤ l ≤ 27 |
| Число отражений | 5877 | 18578 | 9120 |
| Число независимых отражений | 2637 [Rint = 0.0137] | 2987 [Rint = 0.0591] | 7155 [Rint = 0.1577] |
| GOOF | 1.007 | 1.017 | 1.009 |
| R [I > 2σ(I)] | R1 = 0.0271, wR2 = 0.0767 | R1 = 0.0380, wR2 = 0.0816 | R1 = 0.0415, wR2 = 0.1074 |
| R (по всем рефлексам) | R1 = 0.0307, wR2 = 0.0794 | R1 = 0.0675, wR2 = 0.0953 | R1 = 0.0567, wR2 = 0.1157 |
| max/min пики электронной плотности, e Å–3 | 0.456 и –0.193 | 0.402 и –0.370 | 1.161 и –0.502 |
Таблица 2
. Основные длины связей и величины валентных углов в комплексе 1
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Mn(1)–O(1) | 2.1399(8) | Mn(1)–O(1)#1 | 2.1400(8) |
| Mn(1)–O(4) | 2.1848(8) | Mn(1)–O(4)#1 | 2.1849(8) |
| Mn(1)–O(3) | 2.1938(8) | Mn(1)–O(3)#1 | 2.1939(8) |
| Угол | ω, град | Угол | ω, град |
| O(1)Mn(1)O(1)#1 | 180.0 | O(1)Mn(1)O(4) | 87.69(3) |
| O(1)#1Mn(1)O(4) | 92.31(3) | O(1)Mn(1)O(4)#1 | 92.31(3) |
| O(1)#1Mn(1)O(4)#1 | 87.69(3) | O(4)Mn(1)O(4)#1 | 180.0 |
| O(1)Mn(1)O(3) | 90.05(3) | O(1)#1Mn(1)O(3) | 89.95(3) |
| O(4)Mn(1)O(3) | 88.40(3) | O(4)#1Mn(1)O(3) | 91.60(3) |
| O(1)Mn(1)O(3)#1 | 89.95(3) | O(1)#1Mn(1)O(3)#1 | 90.05(3) |
| O(4)Mn(1)O(3)#1 | 91.60(3) | O(4)#1Mn(1)O(3)#1 | 88.40(3) |
Таблица 3.
Основные длины связей и величины валентных углов в комплексе 2
| Связь | d, Ǻ | Связь | d, Ǻ |
|---|---|---|---|
| Mn(1)–O(1)#1 | 2.1221(13) | Mn(1)–O(1) | 2.1221(12) |
| Mn(1)–O(2) | 2.1818(13) | Mn(1)–O(2)#1 | 2.1818(13) |
| Mn(1)–N(1) | 2.288(2) | Mn(1)–N(2) | 2.292(2) |
| Угол | ω, град | Угол | ω, град |
| O(1)#1Mn(1)O(1) | 172.54(7) | O(1)#1Mn(1)O(2) | 85.76(5) |
| O(1)Mn(1)O(2) | 94.07(5) | O(1)#1Mn(1)O(2)#1 | 94.07(5) |
| O(1)Mn(1)O(2)#1 | 85.76(5) | O(2)Mn(1)O(2)#1 | 177.48(7) |
| O(1)#1Mn(1)N(1) | 93.73(4) | O(1)Mn(1)N(1) | 93.73(4) |
| O(2)Mn(1)N(1) | 91.26(3) | O(2)#1Mn(1)N(1) | 91.26(3) |
| O(1)#1Mn(1)N(2) | 86.27(4) | O(1)Mn(1)N(2) | 86.27(4) |
| O(2)Mn(1)N(2) | 88.74(3) | O(2)#1Mn(1)N(2) | 88.74(3) |
| N(1)Mn(1)N(2) | 180.0 |
Таблица 4.
Основные длины связей и величины валентных углов в комплексе 3
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Mn(1)–O(2) | 2.0854(16) | Mn(1)–O(1) | 2.1066(16) |
| Mn(1)–N(2)#1 | 2.2596(17) | Mn(1)–O(3) | 2.2693(16) |
| Mn(1)–N(1) | 2.2723(17) | Mn(1)–O(4) | 2.2964(16) |
| Угол | ω, град | Угол | ω, град |
| O(2)Mn(1)O(1) | 124.58(7) | O(2)Mn(1)N(2)#1 | 86.19(6) |
| O(1)Mn(1)N(2)#1 | 90.50(6) | O(2)Mn(1)O(3) | 147.11(7) |
| O(1)Mn(1)O(3) | 87.94(6) | N(2)#1Mn(1)O(3) | 99.61(6) |
| O(2)Mn(1)N(1) | 86.01(6) | O(1)Mn(1)N(1) | 91.26(6) |
| N(2)#1Mn(1)N(1) | 171.56(6) | O(3)Mn(1)N(1) | 88.71(6) |
| O(2)Mn(1)O(4) | 90.48(7) | O(1)Mn(1)O(4) | 144.92(6) |
| N(2)#1Mn(1)O(4) | 90.64(6) | O(3)Mn(1)O(4) | 57.34(6) |
| N(1)Mn(1)O(4) | 92.66(6) |
Крайне неустойчивые на воздухе кристаллы комплекса 1 извлекали непосредственно из маточного раствора и быстро переносили на головку гониометра в ток испаряющегося жидкого азота (150 K).
Рентгеноструктурные исследования полимеров выполнены с использованием оборудования ЦКП ФМИ ИОНХ РАН, функционирующего при поддержке государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Синтез Mn(OOCPh)2[O(H)Me]4 (1). К раствору 0.3 г (1.22 ммоль) водного ацетата марганца в 15 мл метанола добавляли 0.3 г (2.45 ммоль) бензойной кислоты и перемешивали 1 ч при температуре 80°С. Полученный светло-розовый раствор концентрировали до 2 мл и выдерживали при 5°С в течение 1 сут. Образовавшиеся при этом крайне неустойчивые на воздухе бесцветные кристаллы отделяли от маточного раствора декантацией, промывали холодным гексаном и сушили в токе аргона. Выход (порошок) 68% (0.35 г).
ИК-спектр (ν, см–1): 3070 сл., 2948 сл., 2826 сл., 1676 с., 1601 ср., 1582 ср., 1324 с., 1288 с., 1101 сл., 1026 сл., 927 с., 805 с., 703 с., 665 с., 431 сл., 410 сл.
Синтез {[(µ-γ,γ'-dipy)Mn(µ-OOCPh)]2}n (2). Раствор 0.1 г (0.23 ммоль) комплекса 1 в 10 мл метанола аккуратно покрывали раствором 0.04 г (0.25 ммоль) γ,γ'-дипиридила в 5 мл метанола и оставляли при комнатной температуре на 3 сут. Образовавшиеся светло-розовые монокристаллы отделяли от маточного раствора декантацией, промывали гексаном и сушили в токе аргона. Выход 81% (0.084 г).
ИК-спектр (ν, см–1): 3068 сл., 1932 сл., 1641 ср., 1595 с., 1552 с., 1530 с., 1485 сл., 1412 сл., 1383 с., 1314 ср., 1217 ср., 1171 сл., 1151 сл., 1095 сл., 1067 ср., 1020 ср., 973 сл., 947 сл., 856 сл., 831 ср., 806 с., 718 с., 666 с., 626 с.
Синтез {(µ-γ,γ'-dipy)2Mn2[µ-(OOCC5H4Mn(CO)3]2[η2-(OOCC5H4Mn(CO)3]2}n (3). Раствор 1 г (1.4 ммоль) аддукта Mn[(OOCC5H4Mn(CO)3]2[O(H)Me]4 в 15 мл метанола аккуратно покрывали раствором 0.22 г (1.4 ммоль) γ,γ'-дипиридила в 5 мл метанола и оставляли при комнатной температуре на 3 сут. Образовавшиеся светло-розовые монокристаллы отделяли от маточного раствора декантацией, промывали гексаном и сушили в токе аргона. Выход (порошок) 92% (0.99 г).
ИК-спектр (ν, см–1): 3284 сл., 3111 сл., 2849 сл., 2359 сл., 2011 с., 1938 с., 1909 с., 1599 ср., 1531с., 1474 с., 1412 ср., 1389 с., 1354 с., 1321 с., 1222 сл., 1195 сл., 1070 сл., 1044 сл., 1025 сл., 1001сл., 966 сл., 906 сл., 855 сл., 845 сл., 806 с., 773 с.,732 сл., 662 ср., 621 с., 569 сл.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По аналогии с получением аддуктов бензоатов цинка, никеля и кобальта с метанолом реакция водного ацетата марганца с бензойной кислотой в метаноле при кипячении приводит к обмену ацетат-анионов на бензоат-анионы с образованием крайне нестабильных на воздухе бесцветных монокристаллов моноядерного комплекса Mn(OOCPh)2[O(H)Me]4 (1). Выход 68%.
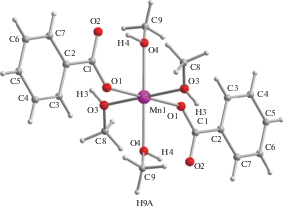
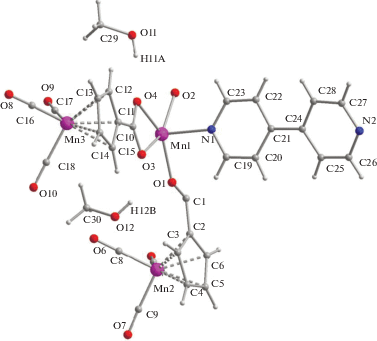
По данным РСА (табл. 1, 2, рис. 1), в центросимметричной молекуле комплекса 1 атом металла(II) находится в октаэдрическом окружении атомов кислорода, четыре из которых принадлежат координированным молекулам метилового спирта (Mn–OMeOH 2.1848(8)–2.1939(8) Å), расположенным в экваториальных позициях, а два – анионам бензойной кислоты (Mn–O 2.1399(8), 2.1400(8) Å).
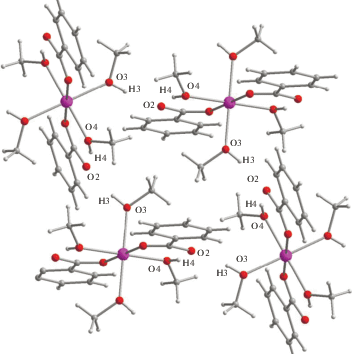
Атомы водорода Н(4) ОН-групп молекул координированного спирта образуют внутримолекулярные водородные связи с атомами О(2) анионов (О(2)…О(4) 2.625(9) Å), которые связаны также с атомами водорода Н(3) (О(2)…О(3) 2.638(9) Å) МеОН, координированного с атомом марганца другой молекулы мономера. Такая сетка межмолекулярных водородных связей приводит к формированию в кристалле 2D-полимера. Отметим, что близкое строение имеет аддукт Mn[(OOCC5H4Mn(CO)3]2[O(H)Me]4, в котором помимо двух цимантренат-анионов присутствуют также четыре координированные молекулы спирта. При этом при замене бензоат- или цимантренат-аниона на анион моноферроценкарбоновой кислоты в результате перекристаллизации из спирта получен 1D-КП с чередующимися моноядерными фрагментами Mn(FcCO2)2[(О(Н)Me]4 и биядерными фрагментами Mn2(µ-FcCO2)4 [21]. Следует отметить, что для получения безводных бензоатов марганца(II) использовали окислительно-восстановительную реакцию металлического марганца с бензойной кислотой в сольватотермических условиях, которая сопровождалась выделением водорода и с высоким выходом полимера [Mn(OOCPh)2]n, а также трехъядерного комплекса Mn3(µ-OOCPh)6(thf)4 [22].
Как и в случае изоструктурных аддуктов цинка, никеля и кобальта в тех же условиях, медленная диффузия раствора γ,γ'-дипиридила в MeOH в метанольный раствор аддукта 1 при соотношении реагентов 1 : 1 при комнатной температуре приводит к образованию монокристаллов 2D-КП {[dipyMn(µ-OOCPh)]2}n (2) светло-розового цвета. Выход 81%.
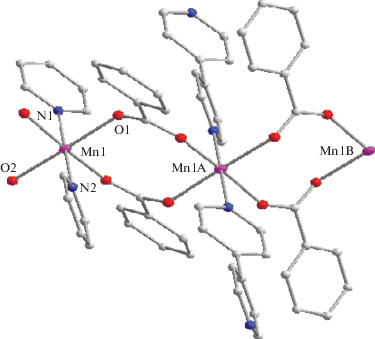
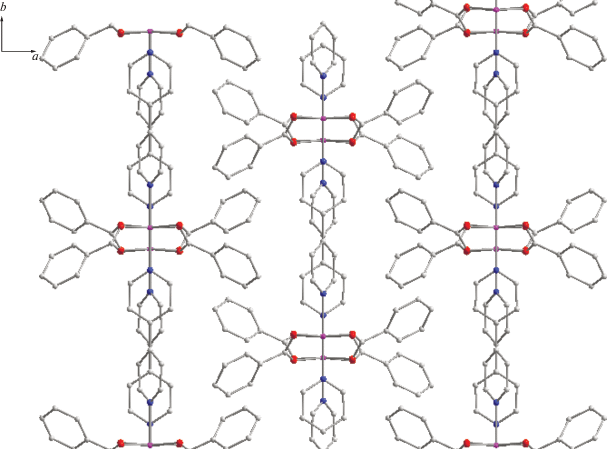
По данным РСА (табл. 1, 3, рис. 3), в полимере 2 атомы марганца образуют зигзагообразную “карбоксилатную цепь” с углом Mn(1)Mn(1A)Mn(1B) 152.5° и находятся на несвязывающем расстоянии 4.8562(9) Å, соединяясь четырьмя мостиковыми бензоат-анионами с двумя другими атомами металла (Mn–O 2.1221(13)–2.1818(13) Å). Каждый атом марганца этой цепи связан с двумя атомами азота двух противолежащих молекул дипиридила, сшивающих полимер в другом направлении (Mn–N 2.288(2)–2.292(2) Å). В итоге такие 2D-плоскости располагаются в кристаллической ячейке полимера 2 на расстоянии Mn…Mn 11.669 Å (рис. 4). Гетероциклы дипиридила развернуты друг относительно друга на угол 39.7°.
Несмотря на то, что для полимеров и комплексов металлов, имеющих большое количество координационных возможностей, в присутствии полидентатных карбоксилат-анионов можно было ожидать наличия температурно-зависимых фазовых переходов, как это наблюдалось, например, в соединениях кобальта и марганца с пивалат-анионами [23, 24], полученные в результате рентгеноструктурных исследований длины связей и величины валентных углов 2D-КП 2 при температуре 150 K близки к обнаруженным при комнатной температуре (Mn…Mn 4.876(6) Å, угол MnMnMn 153.21(2)°, Mn–O 2.129(2), 2.179(2) Å; Mn–O 2.294(4), 2.297(4) Å; угол между гетероциклами 38.8(2)°) [25].
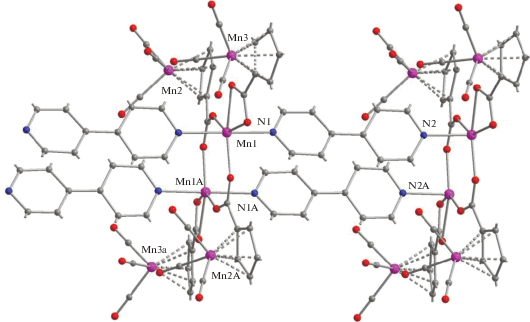
Неожиданно другой тип КП был получен при замене бензоат-аниона на более стерически нагруженный цимантренат-анион. Оказалось, что аналогичная диффузия раствора дипиридила в метаноле в метанольный раствор аддукта Mn[(OOCC5H4Mn(CO)3]2[O(H)Me]4 при комнатной температуре приводит к образованию светло-розовых монокристаллов 1D-КП {(µ-γ,γ'-dipy)2Mn2[µ-(OOCC5H4Mn(CO)3]2[η2-(OOCC5H4Mn(CO)3]2 · 2MeOH}n (3) (выход 92%). По данным РСА соединения 3 (табл. 1, 4, рис. 5, 6), в димерных фрагментах Mn2[µ-(OOCC5H4Mn(CO)3]2[η2-(OOCC5H4Mn(CO)3]2 атомы марганца(II) находятся на несвязывающем расстоянии 4.1881(6) Å и соединяются в димер двумя мостиковыми цимантренат-анионами (Mn–O 2.0854(16)–2.1066(16) Å). В димере каждый атом металла имеет искаженное октаэдрическое окружение MO4N4, дополненное двумя атомами кислорода η2-координированного цимантренат-аниона с выравненными связями M–O 2.2693(16) и 2.2964(16) Å и двумя противолежащими атомами азота, принадлежащими двум разным молекулам мостикового дипиридила, сшивающим такие димеры в линейный 1D-КП (Mn–N 2.2596(17), 2.2723(17) Å) (рис. 6).
В полимере 3 карбоксильные группы заместителей (C5H4)Mn(CO)3 димеров направлены в одну сторону, что связано со стерическими затруднениями. Атомы водорода двух сольватных молекул спирта образуют короткие связи с атомами кислорода периферийных анионов (O11…O4 2.763(7) Å, O12…O3 2.801(7) Å), гетероциклические кольца двух мостиковых дипиридилов параллельны, а угол между гетероциклами равен 30.5°.
ЗАКЛЮЧЕНИЕ
Показано, что в зависимости от природы заместителя в карбоксилат-анионе при одинаковых условиях синтеза (растворитель, температура, концентрация) и кристаллизации могут образовываться два типа полимеров: 2D, в которых атомы металлов связаны в линию карбоксилатными мостиками и каждый из них имеет по два противолежащих дипиридила (тип 1), и 1D-полимер, состоящий из димеров, каждый атом металла которых связан мостиковым бидентатным дипиридилом (тип 2).
Отметим, что, по данным CCDC, полимеры типа 1, 2 известны в координационной химии Mn(II) и γ,γ'-дипиридила. Так, образование монокристаллов КП типа 1 обнаружено в реакции перхлората марганца с 3,5-диметилбензойной кислотой в присутствии NaOH и γ,γ'-дипиридила в смеси метанол–вода [26], при использовании в аналогичной процедуре (2-бензотиазолил)тиоуксусной кислоты [27] или при взаимодействии 3,5- динитробензойной кислоты с водным раствором хлорида марганца(II) в присутствии щелочи в водно-метанольном растворе [28]. КП такого же строения получен реакцией соответствующего мета-замещенного нитробензоата марганца(II) с dipy в метаноле, в то время как для орто-замещенного комплекса в тех же условиях образуется полимер типа 2 [29]. Полимер типа 2 был синтезирован реакцией мета-толуиловой кислоты с водным ацетатом марганца в этаноле с последующей перекристаллизацией из ДМФА, причем в случае орто-метилбензойной кислоты в аналогичных условиях получен линейный полимер, в котором атомы марганца связаны с координированной молекулой воды [30, 31]. И наконец, реакция водного ацетата марганца с дипиридилом в воде также приводит к полимеру типа 2, а мета-замещенный ферроценилбензоат Mn(II), синтезированный из m-FcC6H4COONa, dipy и ацетата марганца, дает полимер [Mn(η2-OOCH4C6Fc)2(4,40-bpy)]n с геометрией “зигзаг” [32].
Отметим, что полученные полимеры растворяются в органических растворителях, что позволяет предположить возможность их модификации в реакциях с разноообразными O- и N-донорными молекулами, а также при окислении атомов металла.
Список литературы
Cook T.R., Zheng Y.-R., Stang P.J. // Chem. Rev. 2013. V. 113. P. 734. https://doi.org/10.1021/cr9601324
Leininger S., Olenyuk B., Stang P.J. // Chem. Rev. 2000. V. 100. P. 53. https://doi.org/10.1021/cr9601324
Eddaoudi M., Moler D.B., Li H.-L. et al. // Acc. Chem. Res. 2001. V. 34. P. 319. https://doi.org/10.1021/ar000034b
Dybtsev D.N., Chun H., Yoon S.H. et al. // J. Am. Chem. Soc. 2004. V. 126. P. 32. https://doi.org/10.1021/ja038678c
Li J.-R., Ma Y., McCarthy M.C. et al. // Coord. Chem. Rev. 2011. V. 55. P. 1791. https://doi.org/10.1016/j.ccr.2011.02.012
Kuppler R.J., Timmons D.J., Fang Q.-R. et al. // Coord. Chem. Rev. 2009. V. 253. P. 3042. https://doi.org/10.1016/j.ccr.2009.05.019
Han Z.-B., Lu R.-Y., Liang Y.-F. et al. // Inorg. Chem. 2012. V. 51. P. 674. https://doi.org/10.1021/ic2021929
Wu Y.-N., Li F., Zhu W. et al. // Coord. Chem. Rev. 2011. V. 50. P. 1251. https://doi.org/10.1016/j.ccr.2011.02.016
Maspoch D., Ruiz-Molina D., Veciana J. // J. Mater. Chem. 2004. V. 14. P. 2713. https://doi.org/10.1039/b407169g
Kiskin M.A., Eremenko I.L. // Russ. Chem. Rev. 2006. V. 75. P. 559. [Кискин М.А., Еременко И.Л. // Успехи химии. 2006. Т. 75. С. 627.] https://doi.org/10.1070/RC2006v075n07ABEH003636
Naiya S., Biswas S., Drew M.G.B. et al. // Inorg. Chem. 2012. V. 51. P. 5332. https://doi.org/10.1021/ic300274n
Mondal K.C., Song Y., Mukherjee P.S. // Inorg. Chem. 2007. V. 46. P. 9736. https://doi.org/10.1021/ic701018x
Seth P., Das L.K., Drew M.G.B. et al. // Eur. J. Inorg. Chem. 2012. V. 13. P. 2232. https://doi.org/10.1002/ejic.201101309
Uvarova M.A., Grineva A.A., Datchuk R.R. et al. // Russ. J. Inorg. Chem. 2018. V. 63. P. 618. [Уварова М.А., Гринева А.А., Датчук Р.Р. и др. // Журн. неорган. химии. 2018. Т. 63. № 5. С. 587.] https://doi.org/10.1134/S0036023618050108
Grineva A.A., Grechova O.D., Datchuk R.R. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 8. P. 1014. [Гринева А.А., Грехова О.Д., Датчук Р.Р. и др. // Журн. неорган. химии. 2019. Т. 64. № 8. С. 850.] https://doi.org/10.1134/S0036023619080047
Datchuk R.R. Grineva A.A., Uvarova M.A. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 10. [Датчук Р.Р., Гринева А.А., Уварова М.А. и др. // Журн. неорган. химии. 2019. Т. 64. № 10. С. 1041.]
SMART (control) and SAINT (integration) Software. Version 5.0. Bruker AXS Inc. Madison, WI, 1997.
SAINT: Area-Detector Integration Sofware. Bruker: Madison, 603, Wisconsin, USA, 2012.
Sheldrick G.M. SADABS. Program for scaling and Correction of Area Detector Data, University of Göttingen, 1997.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
Chen Z., Ma Y., Liang F. et al. // Eur. J. Inorg. Chem. 2007. P. 2040. https://doi.org/10.1002/ejic.200600868
Kornowicz A., Komorski S., Wróbel Z. et al. // Dalton Trans. 2014. V. 43. P. 3048. https://doi.org/10.1039/C3DT53211A
Amel’chenkova E.V., Denisova T.O., Nefedov S.E. // Mendeleev Commun. 2004. V. 14. № 3. P. 103. https://doi.org/10.1070/MC2004v014n03ABEH001918
Nefedov S.E., Denisova T.O. Dobrokhotova Zh.B. et al. // Russ. J. Inorg. Chem. 2006. V. 51. P. 1587. [Нефедов С.Е., Денисова Т.О., Доброхотова Ж.В. и др. // Журн. неорган. химии. 2006. Т. 51. № 10. С. 1687.] https://doi.org/10.1134/S0036023606100135
Kar P., Biswas R., Ida Y. et al. // Cryst. Growth Des. 2011. V. 11. P. 5305. https://doi.org/10.1021/cg2008649
Miao-Ling Huang // Acta Crystallogr. 2006. V. 62. P. 2075. https://doi.org/10.1107/S1600536806029527
Huang F.-P., Qing Yu, He-Dong Bian et al. // Polyhedron. 2008. V. 27. P. 3160. https://doi.org/10.1016/j.poly.2008.07.006
Wang J., Li Z.-L., Xu X.-Z. et al. // Acta Crystallogr. 2010. V. 66. P. 1187. https://doi.org/10.1107/S1600536810034495
Paramita Kar, Rituparna Biswas, Yumi Ida et al. // Cryst. Growth Des. 2011. V. 11. P. 5305. https://doi.org/10.1021/cg2008649
Wu X.-J., Chen Y.-P., Xia Z.-M. et al. // J. Mol. Struct. 2013. V. 1035. P. 318. https://doi.org/10.1016/j.molstruc.2012.10.034
Zhu H.-L., Qi J.-L., Jian-Li Lin et al. // Trans. Met. Chem. 2013. V. 38. P. 733. https://doi.org/10.1007/s11243-013-9743-3
Jinpeng L., Yinglin S., Hongwei H. et al. // J. Organomet. Chem. 2007. V. 692. P. 1584. https://doi.org/10.1016/j.jorganchem.2006.12.010
Дополнительные материалы
- скачать mnggdipy.cif
- X-Ray data
- скачать mnoocph.cif
- X-Ray data
- скачать mnphdipy.cif
- X-Ray data
Инструменты
Журнал неорганической химии