Журнал неорганической химии, 2020, T. 65, № 12, стр. 1668-1675
Термодинамические и магнитные свойства станната празеодима
А. В. Тюрин a, А. В. Хорошилов a, М. А. Рюмин a, В. Н. Гуськов a, А. В. Гуськов a, П. Г. Гагарин a, Г. Е. Никифорова a, О. Н. Кондратьева a, К. И. Печковская a, Н. Н. Ефимов a, В. М. Гуревич b, К. С. Гавричев a, *
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Институт аналитической химии и геохимии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина 19, Россия
* E-mail: gavrich@igic.ras.ru
Поступила в редакцию 25.08.2020
После доработки 03.09.2020
Принята к публикации 04.09.2020
Аннотация
Образец станната празеодима Pr2Sn2O7 был получен твердофазным взаимодействием оксидов при высокой температуре и охарактеризован методами рентгенофазового и рентгенофлуоресцентного анализов и сканирующей электронной микроскопии. Измерение теплоемкости, выполненное методами адиабатической и дифференциальной сканирующей калориметрии в диапазоне температур 7.9–1345 K, позволило определить температурные зависимости термодинамических функций Pr2Sn2O7. Намагниченность станната празеодима изучена в температурном диапазоне 2–300 K. Оценены энтальпия образования и энергия Гиббса образования Pr2Sn2O7, а также определен вид зависимости аномальной теплоемкости Шоттки.
ВВЕДЕНИЕ
Соединения с общей формулой A2В2О7 (где A = лантаноиды, B = Ti, Sn, Zr, Hf), которые имеют структуру пирохлора с кубической кристаллической решеткой (пр. гр. Fd3m), имеют целый ряд интересных физических и физико-химических свойств, что привлекло к этим соединениям большое внимание [1]. В литературе имеются обобщенные сведения о термодинамических свойствах некоторых сложных оксидов редкоземельных элементов (РЗЭ) со структурой пирохлора [2].
Станнаты РЗЭ имеют высокие температуры плавления (выше 2000°С), химическую инертность и фазовую стабильность в широком температурном диапазоне, вследствие чего они рассматриваются как перспективные материалы для термобарьерных покрытий [3].
Оксиды со структурой пирохлора продемонстрировали ряд необычных состояний, связанных с геометрической фрустрацией, таких как спиновые стекла [4], кооперативный парамагнетизм [5], спиновый лед [6–8] и лед Кагоме [9, 10].
Результаты изучения магнитных свойств и теплоемкости станната празеодима при очень низких температурах, приведенные в работах [11–14], показали, что при температуре ниже 1 K происходит изменение магнитных свойств с переходом в состояние спинового льда, которое сопровождается аномалией теплоемкости с максимумом на зависимости Сmag /T при 0.86 K [14]. Интегрирование зависимости Сmag/T позволило рассчитать величину энтропии магнитной аномалии в нулевом поле Smag = 3.1 Дж/(моль K). Авторы установили, что при наложении магнитного поля μ0H = 1T энтропия магнитной аномалии при 10 K увеличилась с 3.1 до 4.5 Дж/(моль K). В области температур выше этого превращения аномалий магнитных свойств не выявлено. Помимо наличия этого особого состояния, некоторые станнаты парамагнитных лантаноидов могут претерпевать в области низких температур магнитное упорядочение [15].
У соединений лантаноидов с неполностью заполненной f-орбиталью под действием кристаллического поля происходит расщепление электронных уровней. В результате этого некооперативного явления происходит постепенное термическое заселение возбужденных уровней, что вызывает появление аномального вклада в теплоемкость в широком температурном диапазоне, называемого аномалией Шоттки [16]. Вид аномальной кривой теплоемкости зависит от энергии и вырожденности электронных уровней.
Внимание к изучению аномальных явлений в области низких температур связано, в частности, с тем, что они вносят вклад в общее значение стандартной энтропии и приведенной энергии Гиббса соединения. Вклад в энтальпию не имеет столь значительного влияния и часто не превышает ошибки значения изменения энтальпии при стандартных условиях. Информации по изучению теплоемкости станната празеодима в области 5–300 K в литературе не обнаружено.
В области высоких температур (360–1045 K) теплоемкость станната празеодима была изучена методом дифференциальной сканирующей калориметрии (ДСК) [17]. Полученные экспериментальные данные авторы описали с использованием уравнения Майера–Келли [18] (Дж/(моль K)):
Энтальпии образования ряда станнатов РЗЭ (РЗЭ = La, Nd, Sm, Eu, Dy, Yb), полученные методом дроп-калориметрии, приведены в работе [19]. Однако для станната празеодима Pr2Sn2O7 данных по энтальпии образования не найдено.
Основной целью данного исследования было определение температурных зависимостей термодинамических функций в широком температурном диапазоне на основании измерения теплоемкости методами адиабатической и дифференциальной сканирующей калориметрии. Термодинамические величины необходимы для расчетов стабильности вещества в области, недоступной для эксперимента, и оценки взаимодействий изученных соединений с другими веществами в области высоких температур. Кроме этого, было изучено магнитное поведение станната празеодима от 2 до 300 K.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез и идентификация образцов
Образец станната празеодима Pr2Sn2O7 синтезировали по методике, описанной в [20]. В качестве исходных реагентов использовали оксид олова SnO2 (чистота 99.0%, Русхим) и предварительно прокаленный при 1273 K оксид празеодима Pr6O11 (чистота 99.9%, Химмед). Для получения станната празеодима со структурой пирохлора образец постадийно отжигали, причем на последней стадии отжиг продолжался 4 ч при 1673 K. Фазовый состав образца на разных стадиях синтеза контролировали методом рентгенофазового анализа (РФА). Исследования проводили на дифрактометре Bruker D8 Advance (CuKα-излучение, Ni-фильтр, Lynxeye-детектор, геометрия на отражение) в интервале углов 2θ = 25°–85° и шагом сканирования 0.0133°. Расчет кристаллографических параметров полученного станната празеодима проводили с помощью программного обеспечения Bruker TOPAS 4.
Химическую чистоту и соотношение катионов определяли методом рентгенофлуоресцентного анализа с помощью микрорентгенофлуоресцентного спектрометра Bruker M4 Tornado.
Морфологию синтезированного образца изучали методом растровой электронной микроскопии с помощью электронного микроскопа Carl Zeiss NVision 40.
Калориметрические измерения
Адиабатическая калориметрия. Измерение изобарной теплоемкости проводили в автоматизированной калориметрической установке БКТ-3 (АОЗТ ТЕРМИС, Менделеево Московской обл.), которая представляет собой адиабатический калориметр с дискретным вводом энергии. Для проверки надежности работы калориметра были проведены измерения теплоемкости эталонного образца бензойной кислоты марки K-2 в области 5–350 K. В результате установили, что аппаратура и методика измерений позволяют получать величины теплоемкости с погрешностью не более ±5% до 15 K, ±0.5% – от 15 до 350 K.
Дифференциальная сканирующая калориметрия. Термический анализ и измерение теплоемкости образца Pr2Sn2O7 в интервале 320–1345 K проведили на установке синхронного термического анализа STA 449F1 Jupiter® фирмы Netzsch. Калибровку по температуре и чувствительности проводили измерением плавления стандартных образцов металлов в тиглях из платины-родия с крышкой и вкладышем из Al2O3. По результатам калибровки погрешности составили 0.3 K по температуре и 0.2% по энтальпии. По результатам проверки теплоемкости сапфира максимальная погрешность (2.2% от справочных данных [21]) наблюдалась в конце температурного интервала измерений (1100–1300 K).
Более подробное описание методик калориметрических измерений приведено в работе [20].
Измерение магнитных свойств
Магнитные свойства станната празеодима были измерены в интервале температур 2–300 K с использованием PPMS-9 фирмы Quantum Design с опцией измерения намагниченности [22] в магнитном поле 1 кЭ. Измерения проводили в процессе охлаждения образца. Чтобы исключить ориентацию поликристаллов вдоль линий магнитного поля, смоченный минеральным маслом образец запаковывали в полиэтилен. Вклад минерального масла и полиэтилена учитывали при расчете магнитной восприимчивости образца.
Обработка данных по теплоемкости
В изученном диапазоне температур значения экспериментальной теплоемкости, полученные методами адиабатической и дифференциальной сканирующей калориметрии, были сглажены с использованием линейной комбинации ортонормированных полиномов [23]:
(1)
$C_{p}^{0} = \sum\limits_j^m {{{A}_{j}}{{{\left[ {1 - \exp \left( { - 0.001T} \right)} \right]}}^{j}}} ,$где Aj – коэффициент j-того члена уравнения, Т – абсолютная температура.
В области высоких температур теплоемкость, полученная методом ДСК, описана с помощью уравнения Майера–Келли [18]. При этом учитывалось, что ошибка определения теплоемкости в методе адиабатической калориметрии значительно меньше, чем при ДСК, в связи с чем значения в интервале выше 300 K были использованы как опорные при расчете теплоемкости в области высоких температур.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Описание образца Pr2Sn2O7
Изучение методом рентгеновской дифракции (рис. S1 ) показало, что синтезированный образец станната празеодима Pr2Sn2O7 при комнатной температуре имел структуру пирохлора с параметром решетки a = 10.605(1) Å, который хорошо коррелирует с литературными значениями [24–26]. Рефлексов, свидетельствующих о наличии примесных фаз, не обнаружено.
Размер частиц полученного образца, определенный по уширению рефлексов на рентгенограмме и по данным электронной микроскопии (рис. S2 ) составил более 100 нм.
Химический анализ полученного станната празеодима подтвердил, что в пределах погрешности метода соединение можно считать стехиометрическим по металлам.
Теплоемкость Pr2Sn2O7
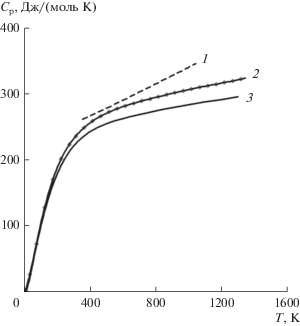
Измерение теплоемкости в области низких температур было выполнено на образце массой 0.9915 г в диапазоне 7.90–346.58 K в 112 экспериментальных точках (табл. S1 ). Для расчета мольной теплоемкости использовано значение молярной массы 631.23112 г/моль из данных [27]. Изображенная на рис. 1 температурная зависимость теплоемкости в диапазоне 7.9–346 свидетельствует об отсутствии аномалий, связанных с фазовыми превращениями.
Измерения в области высоких температур проведены методом ДСК на образце массой 69.36 мг со скоростью сканирования 20 K/мин. Температурная зависимость теплоемкости, полученная двумя методами в широком интервале температур 7.90–1345 K, была сглажена с помощью методики, описанной в [23]. Значения коэффициентов уравнения (1), описывающего теплоемкость Pr2Sn2O7, приведены в табл. S2 . Разброс экспериментальных точек относительно сглаженной кривой показан на рис. S3 . С использованием сглаженной зависимости теплоемкости рассчитаны значения энтропии, изменения энтальпии и приведенной энергии Гиббса в изученном температурном диапазоне (табл. 1).
Таблица 1.
Сглаженные значения термодинамических функций Pr2Sn2O7 в области 5–1345 К
| T, K | $C_{p}^{0}$(T), Дж/(моль K) | S0(T)*, Дж/(моль K) | H0(T) – H0(0)*, Дж/моль | Ф0(T)*, Дж/(моль К) |
|---|---|---|---|---|
| 5 | 0.169 | 0.0563 | 0.211 | 0.0141 |
| 10 | 1.350 | 0.4500 | 3.375 | 0.1125 |
| 15 | 4.556 | 1.519 | 17.09 | 0.3797 |
| 20 | 8.898 | 2.966 | 44.49 | 0.7415 |
| 25 | 13.02 | 5.385 | 99.09 | 1.421 |
| 30 | 17.56 | 8.154 | 175.4 | 2.308 |
| 35 | 22.44 | 11.22 | 275.2 | 3.359 |
| 40 | 27.62 | 14.55 | 400.3 | 4.547 |
| 45 | 33.03 | 18.12 | 551.8 | 5.854 |
| 50 | 38.62 | 21.89 | 730.9 | 7.268 |
| 60 | 50.19 | 29.94 | 1175 | 10.37 |
| 70 | 62.04 | 38.57 | 1736 | 13.77 |
| 80 | 73.92 | 47.63 | 2415 | 17.44 |
| 90 | 85.66 | 57.01 | 3214 | 21.31 |
| 100 | 97.12 | 66.64 | 4128 | 25.36 |
| 110 | 108.2 | 76.41 | 5155 | 29.55 |
| 120 | 118.9 | 86.29 | 6290 | 33.87 |
| 130 | 129.0 | 96.21 | 7530 | 38.28 |
| 140 | 138.6 | 106.1 | 8868 | 42.77 |
| 150 | 147.7 | 116.0 | 10300 | 47.33 |
| 160 | 156.3 | 125.8 | 11820 | 51.94 |
| 170 | 164.3 | 135.5 | 13430 | 56.53 |
| 180 | 171.9 | 145.1 | 15110 | 61.20 |
| 190 | 178.9 | 154.6 | 16860 | 65.88 |
| 200 | 185.5 | 164.0 | 18680 | 70.57 |
| 210 | 191.6 | 173.2 | 20569 | 75.22 |
| 220 | 197.4 | 182.2 | 22510 | 79.90 |
| 230 | 202.7 | 191.1 | 24520 | 84.50 |
| 240 | 207.7 | 199.8 | 26570 | 89.13 |
| 250 | 212.4 | 208.4 | 28670 | 93.74 |
| 260 | 216.8 | 216.8 | 30810 | 98.33 |
| 270 | 220.8 | 225.1 | 33000 | 102.9 |
| 280 | 224.6 | 233.2 | 35230 | 107.4 |
| 290 | 228.2 | 241.1 | 37490 | 111.9 |
| 298.15 | 231.0 | 247.5 | 39370 | 115.5 |
| 300 | 231.6 | 248.9 | 39790 | 116.3 |
| 310 | 234.7 | 256.6 | 42130 | 120.7 |
| 320 | 237.7 | 264.1 | 44490 | 125.0 |
| 330 | 240.5 | 271.4 | 46880 | 129.4 |
| 340 | 243.2 | 278.7 | 49300 | 133.7 |
| 350 | 245.7 | 285.7 | 51740 | 137.9 |
| 400 | 256.4 | 319.3 | 64300 | 158.5 |
| 500 | 271.5 | 378.2 | 90760 | 196.7 |
| 600 | 281.7 | 428.7 | 118400 | 231.4 |
| 700 | 289.2 | 472.7 | 147000 | 262.7 |
| 800 | 295.7 | 511.8 | 176300 | 291.4 |
| 900 | 301.8 | 546.9 | 206100 | 317.9 |
| 1000 | 307.6 | 579.0 | 236600 | 342.4 |
| 1100 | 312.8 | 608.6 | 267600 | 365.3 |
| 1200 | 317.5 | 636.0 | 299100 | 386.8 |
| 1300 | 322.5 | 661.6 | 331100 | 406.9 |
| 1345 | 325.1 | 672.7 | 345700 | 415.6 |
* Значение энтропии, изменения энтальпии и приведенной энергии Гиббса рассчитаны без учета энтропии перехода в спиновое стекло (ΔS = 3.1 Дж/(моль K)) [14].
Полученную температурную зависимость теплоемкости Pr2Sn2O7 в области 320–1345 K описали с помощью уравнения Майера–Келли [18], широко используемого в базах данных (Дж/(моль K)),
(2)
$\begin{gathered} {{C}_{p}}\left( T \right)\, = \,266.663 + 0.0451620839T - 4{\kern 1pt} 463{\kern 1pt} 149.36{{T}^{{--2}}}, \\ \left( {{{R}^{2}} = 0.999941} \right). \\ \end{gathered} $Общий вид полученной температурной зависимости станната празеодима показан на рис. 1. Там же для сопоставления приведена теплоемкость диамагнитного станната лантана [19] и данные по теплоемкости Pr2Sn2O7 из работы [17]. Анализ показал, что приведенная в [17] температурная зависимость теплоемкости в интервале температур 360–1045 K лежит выше полученных нами значений (от 6.7% при 300 K до 10.9% при 1000 K) и имеет вид прямой, не характерный для теплоемкости в этом температурном диапазоне.
Магнитная восприимчивость
Измерения магнитной восприимчивости Pr2Sn2O7 проводили в диапазоне температур 2–300 K в магнитном поле напряженностью 1000 Э в процессе охлаждения исследуемого образца. Во всем исследованном диапазоне температур зависимость магнитной восприимчивости имеет вид, характерный для парамагнетиков (рис. 2). При температуре 300 K значение χT составляет 2.67 см3 K/моль, что заметно меньше теоретической величины для двух невзаимодействующих ионов Pr3+ (3.2 см3 К/моль, 4f 2, 3H4, g = 4/5) и существенно больше теоретической величины для двух невзаимодействующих ионов Pr4+ (1.6 см3 K/моль, 4f 1, 2F5/2, g = 6/7) [28]. Такое отклонение может указывать на существование в исследуемом образце ионов празеодима в разных степенях окисления, и/или о наличии достаточно сильных антиферромагнитных взаимодействий между ионами Pr3+.
Рис. 2.
Температурная зависимость магнитной восприимчивости (1) и произведения χT (2) образца Pr2Sn2O7 в магнитном поле 1000 Э. На вставке приведена температурная зависимость обратной магнитной восприимчивости: точки – экспериментальные данные, линия – аппроксимация уравнением Кюри–Вейса.
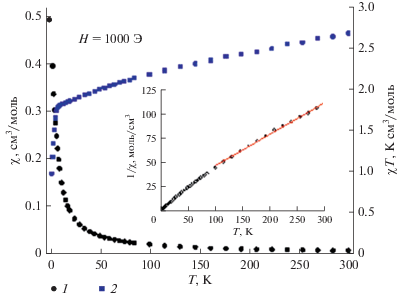
Преимущественный характер возможных магнитных взаимодействий в образце Pr2Sn2O7 можно определить, проведя аппроксимацию зависимости обратной магнитной восприимчивости от температуры уравнением закона Кюри–Вейса χ = С/(T – θ), где С – постоянная Кюри, θ – парамагнитная температура Кюри (постоянная Вейса). В результате наилучшей аппроксимации температурной зависимости обратной магнитной восприимчивости уравнением Кюри–Вейса в диапазоне температур 100–300 K (вставка на рис. 2) получены следующие параметры аппроксимации: С = 3.03 см3 K/моль, θ = –45 K. Отрицательный знак парамагнитной температуры Кюри указывает на преимущественно антиферромагнитный характер возможных магнитных взаимодействий в Pr2Sn2O7.
Предположив, что в образце сосуществуют ионы празеодима в степенях окисления Pr3+ и Pr4+, соотношение этих ионов можно оценить по формуле:
(3)
$\alpha \chi {{T}_{{{\text{теор}}\,{\text{P}}{{{\text{r}}}^{{{\text{3}} + }}}}}} + \left( {{\text{1}} - \alpha } \right)\chi {{T}_{{{\text{теор}}\,{\text{P}}{{{\text{r}}}^{{{\text{4}} + }}}}}} = \chi {{T}_{{{\text{эксп}}}}},$С другой стороны, ион Pr3+ имеет четное число f-электронов (так называемый некрамерсовский ион), и кристаллическое поле может полностью снять вырождение, что приведет к немагнитному основному состоянию, а следовательно, занижению экспериментальных значений χT по отношению к теоретической величине для Pr3+. Полагаем, что это обоснование заниженных значений χT более вероятно.
Полученные нами данные по магнитной восприимчивости Pr2Sn2O7 удовлетворительно согласуются с данными работ [13, 15].
Оценка энтальпии образования Pr2Sn2O7
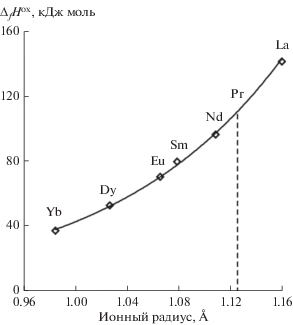
Представляет интерес оценка энтальпии образования станната празеодима. К сожалению, нам не удалось найти в литературе сведений об экспериментальном определении этой термодинамической величины, однако ее можно оценить исходя из данных для ряда станнатов лантаноидов, приведенных в [18], полагая, что в изоструктурных соединениях существует корреляция между энтальпиями образования из оксидов и радиусами иона лантаноидов, как это было показано в работе [29]. На рис. 3 построена зависимость ΔfH ox = f(Ri), в которой ионные радиусы заимствованы из работы [30] для КЧ = 8. Из этой зависимости можно оценить величину ΔfH ox (Pr2Sn2O7) = –112 ± 3 кДж/моль. Использование данных по энтальпиям образования оксидов ΔfH°(Pr2O3) = –1809.6 ± 6.7 кДж/моль [30] и ΔfH°(SnO2) = –577.6 ± 0.2 кДж/моль [18] позволяет оценить энтальпию образования станната празеодима из элементов ΔfH°(Pr2Sn2O7) = –3077 ± ± 8 кДж/моль. Энергия Гиббса образования из элементов, рассчитанная с учетом энтропии перехода в спиновый лед (Smag= 3.1 Дж/(моль K), ΔS0(Pr2Sn2O7, 298 K) = 250.6 Дж/(моль K)), составила ΔfG°(Pr2Sn2O7) = –2870 ± 10 кДж/моль. Необходимые для расчета значения энтропии Pr (73.931 Дж/(моль K)), Sn (44.141 Дж/(моль K)) и O2 (205.036 Дж/(моль K)) заимствованы из [31].
Рис. 3.
Зависимость энтальпии образования станнатов РЗЭ от ионного радиуса РЗЭ по данным работы [17].
Аномалия Шоттки
Как описано выше, теплоемкость парамагнитных соединений лантаноидов имеет аномальный вклад, связанный с расщеплением электронных уровней под действием поля кристалла, причем вид температурной зависимости аномального вклада в теплоемкость может существенно зависеть не только от свойств иона лантаноида, но и от структуры кристалла. Соответственно, и энтропия аномалии, которая рассчитывается из данных по теплоемкости, также индивидуальна для каждого соединения.
Аномальную зависимость теплоемкости соединений с f-электронами от температуры можно оценить путем расчета по частотам электронных уровней. Для различных соединений празеодима (+3) частоты электронных уровней несколько рознятся. Например, для PrPO4 одна группа уровней (3H4) лежит ниже 200 см–1, в то время как другая (3H5) – выше 2000 см–1 [32, 33], в связи с чем в области ниже 300 K теплоемкость имеет вид выраженного плавного максимума. Для оксида празеодима Pr2O3 в диапазоне ниже 1000 см–1 уровни расположены равномерно [34], и аномальная теплоемкость имеет два пологих максимума.
Вторым путем оценки аномальной теплоемкости является сопоставление теплоемкости изучаемого вещества и его диамагнитного структурного аналога (соединений La или Lu) или соединения гадолиния, у которого аномалия Шоттки фиксируется только в области ниже 20 K, по методу [34]:
(4)
${{C}_{{{\text{an}}}}}\left( T \right) = {{C}_{p}}\left( {{\text{L}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}},T} \right) - {{С}_{{{\text{lat}}}}}\left( {{\text{L}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}}} \right),$(5)
$\begin{gathered} {{С}_{{{\text{lat}}}}}\left( {{\text{L}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{7}}}}} \right) = \left( {1 - f} \right){{C}_{p}}\left( {{\text{G}}{{{\text{d}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}}} \right) + \\ + \,\,f{{C}_{p}}\left( {{\text{L}}{{{\text{a}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}}} \right). \\ \end{gathered} $Коэффициент f в уравнении (5) можно рассчитать из кристаллографических параметров
(6)
$\begin{gathered} f = \left[ {V\left( {{\text{P}}{{{\text{r}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}}} \right) - } \right. \\ \left. { - \,\,V\left( {{\text{L}}{{{\text{a}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{7}}}}} \right)} \right]/\left[ {V\left( {{\text{G}}{{{\text{d}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{7}}} \right) - V\left( {{\text{L}}{{{\text{a}}}_{{\text{2}}}}{\text{S}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{7}}}}} \right)} \right], \\ \end{gathered} $К сожалению, данных по теплоемкости станната гадолиния в области низких температур в литературе не обнаружено, в связи с чем мы провели не количественную, а качественную оценку аномалии Шоттки Pr2Sn2O7, определив разность теплоемкостей станната празеодима и станната лантана [19].
Для описания изображенной на рис. 4 температурной зависимости аномальной теплоемкости Pr2Sn2O7 в области ниже 300 K использовали аддитивный подход, представив ее как сумму от трех вкладов для энергетических уровней с частотами 50, 350 и 900 см–1. При оценке возможного вклада аномалии Шоттки использовали уравнение [16]:
(7)
$\begin{gathered} {{C}_{x}} = \frac{R}{{{{T}^{2}}}}{{\left\{ {{{\Sigma }_{i}}{{g}_{i}}{{{\left( {{{\varepsilon }_{i}}{\text{/}}kT} \right)}}^{2}}\exp \left( { - {{\varepsilon }_{i}}{\text{/}}kT} \right)} \right\}} \mathord{\left/ {\vphantom {{\left\{ {{{\Sigma }_{i}}{{g}_{i}}{{{\left( {{{\varepsilon }_{i}}{\text{/}}kT} \right)}}^{2}}\exp \left( { - {{\varepsilon }_{i}}{\text{/}}kT} \right)} \right\}} Z}} \right. \kern-0em} Z} - \\ - \,\,{{\left[ {\left\{ {{{\Sigma }_{i}}{{g}_{i}}\left( {{{\varepsilon }_{i}}{\text{/}}kT} \right)\exp \left( { - {{\varepsilon }_{i}}{\text{/}}kT} \right)} \right\}{\text{/}}Z} \right]}^{2}}, \\ \end{gathered} $Рис. 4.
Аномальная теплоемкость Pr2Sn2O7: ○ – значения, расcчитанные на 1 грамм-атом празеодима как половина разности теплоемкости станнатов празеодима и лантана; сплошная линия – сумма теплоемкостей от вкладов колебаний с частотами 50, 350 и 900 см–1. Приведенные ошибки составляют 0.5% от экспериментальных значений теплоемкости Pr2Sn2O7.
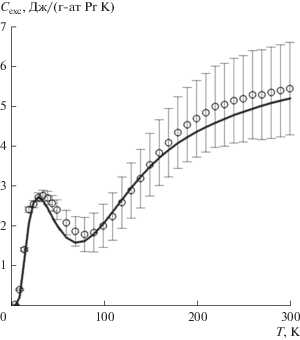
Можно видеть, что полученные модельные значения удовлетворительно коррелируют с экспериментальными данными, что позволяет отнести выявленную в области 0–300 K аномальную теплоемкость за счет аномалии Шоттки. Необходимо отметить, что у соединений празеодима помимо области спектра с относительно низкими частотами, имеется и группа частот в области выше 2000 см–1, в результате чего происходит заметный рост энтропии вещества в области высоких температур.
ЗАКЛЮЧЕНИЕ
В результате измерения теплоемкости определены температурные зависимости термодинамических свойств Pr2Sn2O7 в диапазоне 7–1345 K. В ходе анализа теплоемкости в интервале выше 7 K выявлено наличие аномалии, связанной с термическим заселением электронных уровней, расщепленных под действием кристаллического поля (аномалия Шоттки), которая характеризуется двумя плавными максимумами. В результате изучения магнитных свойств в температурном диапазоне 2–300 K показан антиферромагнитный характер возможных магнитных взаимодействий в станнате празеодима. Оценены значения энтальпии и энергии Гиббса образования Pr2Sn2O7.
Список литературы
Subramanian M.A., Aravamudan G., Subba Rao G.V. // Prog. Solid State Chem. 1983. V. 15. P. 55. https://doi.org/10.1016/0079-6786(83)90001-8
Guskov V.N., Gavrichev K.S., Gagarin P.G., Guskov A.V. // Rus. J. Inorg. Chem. 2019. V. 64. № 10. P. 1265. https://doi.org/10.1134/S0036023619100048 [Гуськов В.Н., Гавричев К.С., Гагарин П.Г., Гуськов А.В. // Журн. неорган. химии. 2019. Т. 64. № 10. С. 1072.]
Wang J., Xu F., Wheatley R.J. et al. // Mater. Des. 2015. V. 85. P. 423. https://doi.org/0.1016/j.matdes.2015.07.022
Greedan J.E., Sato M., Yan Xu, Razavi F.S. // Sol. State Commun. 1986. V. 59. № 12. P. 895. https://doi.org/10.1016/0038-1098(86)90652-6
Gardner J.S., Dunsiger S.R., Gaulin B.D. et al. // Phys. Rev. Lett. 1999. V. 82. P. 1012. https://doi.org/10.1103/PhysRevLett.82.1012
Harris M.J., Bramwell S.T., McMorrow D.F. et al. // Phys. Rev. Lett. 1997. V. 79. P. 2554. https://doi.org/10.1103/PhysRevLett.79.2554
Ramirez A.P., Hayashi A., Cava R.J. et al. // Nature. 1999. V. 399. P. 333. https://doi.org/10.1038/20619
Bramwell S.T., Gingras M.J.P. // Science. 2001. V. 294. P. 1495. https://doi.org/10.1126/science.1064761
Matsuhira K., Hiroi Z., Tayama T. et al. // J. Phys.: Condens. Matter. 2002. V. 14. P. L559. https://doi.org/10.1088/0953-8984/14/29/101
Hiroi Z., Matsuhira K., Takagi S. et al. // J. Phys. Soc. Jpn. 2003. V. 72. № 2. P. 411. https://doi.org/10.1143/JPSJ.72.411
Matsuhira K., Hinatsu Y., Tenya K. et al. // J. Phys. Soc. Jpn. 2002. V. 71. № 6. P. 1576. https://doi.org/10.1143/JPSJ.71.1576
Matsuhira K., Sekine C., Paulsen C., Hinatsu Y. // J. Magn. Magn. Mater. 2004. V. 272–276. P. e981. https://doi.org/10.1016/j.jmmm.2003.12.500
Martin N., Bonville P., Lhotel E. et al. // Phys. Rev. X. 2017. V. 7. P. 041028-1. https://doi.org/10.1103/PhysRevX.7.041028
Zhou H.D., Wiebe C.R., Janik J.A. et al. // Phys. Rev. Lett. 2008. V. 101. P. 227204-1
Blöte H.W.J., Wielinga R.F., Huiskamp W.J. // Physica. 1969. V. 43. № 4. P. 549. https://doi.org/10.1016/0031-8914(69)90187-6
Tari A. // The specific heat of matter at low temperatures. Imperial College Press, 2003. 211 p. https://doi.org/10.1142/9781860949395_0006
Denisova L.T., Irtyugo L.A., Beletskii V.V., Denisov V.M. // Phys. Sol. State. V. 58. № 7. P. 1300. [Денисова Л.Т., Иртюго Л.А., Белецкий В.В., Денисов В.М. // ФТТ. 2016. Т. 58. № 7. С. 1259].https://doi.org/10.1134/S1063783416070131
Maier C.G., Kelley K.K. // J. Am. Chem. Soc. 1932. V. 54. P. 3243. https://doi.org/10.ja-1347a029
Lian J., Helean K.B., Kennedy B.J. et al. // J. Phys. Chem. B. 2006. V. 110. P. 2343. https://doi.org/10.1021/jp055266c
Ryumin M.A., Nikiforova G.E., Tyurin A.V. et al. // Inorg. Mater. 2020. V. 56. № 1. P. 97. [Рюмин М.А., Никифорова Г.Е., Тюрин А.В. и др. // Неорган. материалы. 2020. Т. 56. № 1. С. 102.].https://doi.org/10.1134/S0020168520010148
Ditmars D.A., Ishihara S., Chang S.S. et al. // J. Res. NBS. 1982. V. 87. № 2. P. 159. https://doi.org/10.6028/jres.087.012
https://www.qdusa.com/products/ppms.html#productFeatures
Gurevich V.M., Khlyustov V.G. // Geokhimiya. 1979. № 6. P. 829. (in Russian) [Гуревич В.М., Хлюстов В.Г. // Геохимия. 1979. № 6. С. 829.]
Brisse F., Knop O. // Can. J. Chem. 1968. V. 46. № 6. P. 859. https://doi.org/10.1139/v68-148
Whinfreyd C., Eckar O., Tauber A. // J. Am. Chem. Soc. 1960. V. 82. № 11. P. 2695. https://doi.org/10.1021/ja01496a010
Kennedy B.J., Hunter B.A., Howard C.J. // J. Sol. State Chem. 1997. V. 130. P. 58. https://doi.org/10.1006/jssc.1997.7277
Wieser M.E. // Pure Appl. Chem. 2006. V. 78. № 11. P. 2051. https://doi.org/10.1351/pac2006781112051
Kahn O. Molecular magnetism. New York: VCH Publishers, 1993.
Ushakov S.V., Helean K.B., Navrotsky A. // J. Mater. Res. 2011. V. 16. P. 2623. https://doi.org/10.1557/JMR.2001.0361
Shannon R.D. // Acta Crystallogr. A. 1976. V. 32. P. 751. https://doi.org/10.1107/S0567739476001551
ttp://www.chem.msu.su/cgi-bin/tkv.p
Kowalski P.M., Beridze G., Vinograd V., Bosbach D. // J. Nuclear Mater. 2015. V. 464. P.147. https://doi.org/10.1016/j.jnucmat.2015.04.032
Thiriet C., Konings R.J.M., Javorsky P. et al. // J. Chem. Thermodyn. 2005. V. 37. P. 131. http://doi.org/101016/j.jct.2006.02.006
Gruber J.B., Justice B.H., Westrum E.F., Jr., Zandi B. // J. Chem. Thermodyn. 2002. V. 34. P. 457. https://doi.org/10.1006/jcht.2001.0860
Дополнительные материалы
- скачать ESM.docx
- Дополнительные материалы
Инструменты
Журнал неорганической химии