Журнал неорганической химии, 2020, T. 65, № 9, стр. 1168-1173
Синтез и люминесцентные свойства нанокристаллических твердых растворов (1–х)ZrO2–хEr2O3 (х = 0.015–0.5)
В. О. Веселова a, *, И. А. Юрлов b, П. А. Рябочкина b, О. В. Белова c, Т. Д. Дудкина d, А. В. Егорышева a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Национальный исследовательский Мордовский государственный университет
430005 Саранск, ул. Большевистская, 68, Россия
c Национальный исследовательский университет “Высшая школа экономики”, образовательная программа “Химия”
117312 Москва, ул. Вавилова, 7, Россия
d Национальный исследовательский ядерный университет “МИФИ”
115409 Москва, Каширское ш., 31, Россия
* E-mail: ibvarvara@yandex.ru
Поступила в редакцию 07.04.2020
После доработки 16.04.2020
Принята к публикации 27.04.2020
Аннотация
Разработан эффективный метод направленного синтеза люминесцентного материала ZrO2–Er2O3 в нанокристаллическом состоянии. Синтезированы монодисперсные образцы кубической модификации, у которых в зависимости от условий синтеза размеры частиц изменяются от 5 до 71 нм. Зарегистрированы спектры люминесценции, обусловленные переходами 4I11/2 → 4I15/2 и 4I13/2 → 4I15/2 ионов Er3+, при их возбуждении излучением с длиной волны 532 нм. При возбуждении на уровень 4I13/2 ионов Er3+ излучением с длиной волны 1550 нм зарегистрированы спектры апконверсионной люминесценции в видимой области спектра, обусловленные переходами 2H11/2, 4S3/2 → 4I15/2, 4F9/2 → 4I15/2.
ВВЕДЕНИЕ
Материалы на основе диоксида циркония находят широкое практическое применение благодаря высокой химической стабильности и биоинертности, высокому показателю преломления, а также возможности образования твердых растворов с оксидами иттрия и редкоземельных элементов. Среди различных материалов на основе диоксида циркония интерес исследователей вызывают соединения ZrO2–Y2O3–Er2O3. Их использование в качестве люминесцентных материалов обеспечивается наличием у них полос поглощения и люминесценции в видимом и ближнем ИК-диапазонах спектра. Спектрально-люминесцентные свойства объемных и наноразмерных материалов ZrO2–Y2O3–Er2O3 изучались в работах [1–6].
Наименее изученными в настоящее время остаются наноразмерные материалы ZrO2–Er2O3. Для получения высокодисперсного ZrO2 : Er3+ разные авторы использовали различные методы: соосаждение [7–9], золь-гель синтез [10, 11], сольвотермальный метод [12–14]. Однако получить ZrO2 : Er3+ с размером частиц <30 нм до сих пор не удалось. Сложность получения частиц ZrO2 : Er3+ заключается в полиморфизме диоксида циркония и зависимости фазового состава продукта от концентрации допанта [15–17].
Цель настоящей работы – разработка метода синтеза наноразмерных однофазных неагрегированных частиц твердого раствора (1–х)ZrO2–хEr2O3 (х = 0.075–0.5) в гидротермальных условиях и исследование их спектрально-люминесцентных характеристик.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для синтеза нанокристаллического оксида циркония, легированного эрбием, в качестве исходных реагентов использовали ZrOCl2 ⋅ 8H2O (Реахим, ч.), ZrO(NO3)2 ⋅ xH2O (Sigma Aldrich, 99.99%) и Er(NO3)3 ⋅ 5H2O (Acros organic, 99.9%). Для приготовления растворов точной концентрации и соблюдения рассчитанного содержания допанта в продукте предварительно определяли количество гидратных молекул воды в исходных соединениях. В случае оксихлорида циркония применяли аргентометрическое титрование по методу Мора, а для нитратов – термогравиметрический анализ свежих осадков, полученных прибавлением к растворам солей избытка аммиака.
Для синтеза в гидротермальных условиях 27 мл 0.1 мол. % водного раствора смеси солей циркония и нитрата эрбия (содержание нитрата эрбия варьировалось в пределах 1.5–50 мол. %) прикапывали при перемешивании к 23 мл 28 мас. % раствора аммиака. Полученный осадок старили в течение различного времени (5 мин–24 ч) и помещали в тефлоновый автоклав объемом 100 мл для гидротермальной обработки. Степень заполнения автоклава 50–65%. Продолжительность синтеза при температуре 110–200°С составляла 1–7 сут. Полученный продукт центрифугировали и высушивали в сушильном шкафу при 50°С.
Фазовый состав продукта определяли методом рентгенофазового анализа с помощью дифрактометра Bruker D8 Advance (CuKα-излучение, Ni-фильтр и Lynxeye детектор). Данные дифракции были собраны в диапазоне 2θ от 15° до 65° с шагом 0.02°, временем накопления 0.1 с/шаг. Идентификацию дифракционных максимумов осуществляли путем сравнения с базой данных JCPDS. Размер области когерентного рассеяния (ОКР) оценивали по формуле Шеррера. Морфологию полученных образцов изучали с помощью сканирующего электронного микроскопа Carl Zeiss NVision 40 и просвечивающего электронного микроскопа Carl Zeiss Libra 200 MC. Удельную площадь поверхности оценивали методом БЭТ с помощью анализатора АТХ-06 (Katakon, Россия) с газом-носителем – гелием марки А.
Спектры люминесценции регистрировали с помощью автоматизированной установки на базе монохроматора МДР-23. В качестве источников возбуждения использовали твердотельный лазер MGL-F-532nm-2W-11110021 на кристалле YVO4 : Nd с λизл = 532 нм и волоконный лазер Er-6.0 с λизл = = 1550 нм. В качестве приемников излучения применяли фотоэлектронный умножитель ФЭУ-79 и германиевый фотодиод ФД-7Г.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Для установления оптимальных условий синтеза было изучено влияние на фазовый состав и морфологию продукта различных условий пробоподготовки: состава прекурсоров (оксинитрат или оксихлорид циркония) и способа приготовления исходной суспензии (прямое или обратное соосаждение, время старения осадка). Оказалось, что выбор прекурсора и порядок осаждения не влияют на конечный продукт в отличие от данных [18]. Увеличение времени выдержки осадка до 24 ч также не оказало влияния на фазовый состав образцов [19]. Поэтому в дальнейшем во всех экспериментах использовали оксихлорид циркония и прикапывание раствора солей металлов к аммиаку, гидротермальной обработке подвергали свежеосажденные осадки (после 1 ч перемешивания на магнитной мешалке).
Продолжительность синтеза нанокристаллического образца ZrO2, содержащего 1.5 мол. % Er2О3, в гидротермальных условиях при температуре 110°С составила 7 сут. При меньшем времени обработки образцы содержали рентгеноаморфную фазу (рис. 1). Кристаллический образец представлял собой смесь моноклинной и кубической фаз, что соответствует фазовой диаграмме ZrO2–Er2O3 [15]. Образец состоял из неагрегированных частиц размером ~20 нм (рис. 2а), что хорошо совпало с оценкой по формуле Шеррера (19 нм).
Рис. 1.
Рентгенограммы образцов, синтезированных в течение суток при температуре 110 (1), 170 (3) и 200°С (4), а также в течение 7 сут при температуре 110°С (2). Содержание допанта 1.5 мол.%.
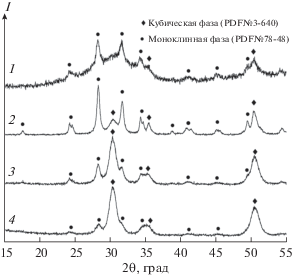
Рис. 2.
Микрофотографии образцов, синтезированных в гидротермальных условиях при 110°С, 7 сут, х = 0.015 (а) и 200°С, 24 ч, х = 0.05 (б).

Повышение температуры синтеза до 200°С позволило снизить его продолжительность до 24 ч. В этих условиях были получены образцы с преобладающей долей кубической фазы. Причем доля этой фазы увеличивалась симбатно повышению температуры синтеза (рис. 1). Технические характеристики автоклава не позволили провести синтез при температуре выше 200°С. Полученный результат свидетельствует о вероятной возможности получения кубической фазы при низком содержании допанта.
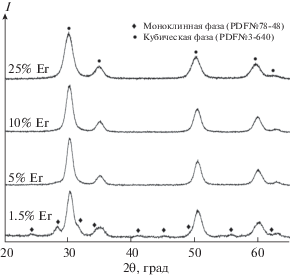
При увеличении концентрации допанта примесь моноклинной фазы исчезает (рис. 2б), при содержании допанта ≥7.5% образуется кубическая фаза (рис. 3) [20]. При 200°С (время гидротермальной обработки 24 ч) синтезирован концентрационный ряд твердых растворов (1 – х)ZrO2–хEr2O3 кубической модификации в диапазоне х = 0.075–0.5 (рис. 4).
Рис. 3.
Рентгенограмма образца с содержанием допанта 7.5%, синтезированного при 200°С в течение суток.
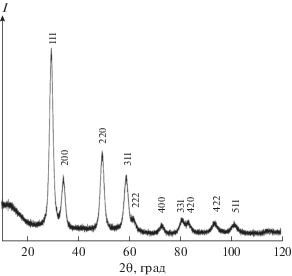
ОКР образцов, полученных в этих условиях, слабо зависит от содержания эрбия и монотонно уменьшается от 9 до 6 нм при увеличении содержания Er3+ от 5 до 35% (табл. 1). Эти данные согласуются с результатами измерения величины удельной поверхности, которая составила 90 м2/г для 7.5% Er3+ и 130 м2/г для 35% Er3+. Изменения формы частиц при повышении концентрации ионов РЗЭ не выявлено (рис. 5). На основании данных ПЭМ построены кривые распределения по размеру для образцов с различным содержанием допанта (рис. 6)
Таблица 1.
ОКР частиц образцов с различным содержанием Er2O3, отожженных при разной температуре
| Содержание Er2O3, мол. % | ОКР, нм | Модификация | |||
|---|---|---|---|---|---|
| до отжига | после отжига при t, °С | ||||
| 500 | 900 | 1200 | |||
| 5 | 9 | 9 | 13 | 25 | Смесь моноклинной и кубической |
| 7.5 | 8 | – | 13 | 51 | Кубическая |
| 15 | 7 | – | 14 | 71 | » |
| 25 | 6 | – | 12 | 36 | » |
| 35 | 6 | – | 11 | 44 | » |
| 45 | 5 | – | – | – | » |
| 50 | 5 | – | – | – | » |
Рис. 5.
Микрофотографии частиц, полученных при 200°С в течение суток, с содержанием ионов Er3+ 7.5 (а) и 35% (б).

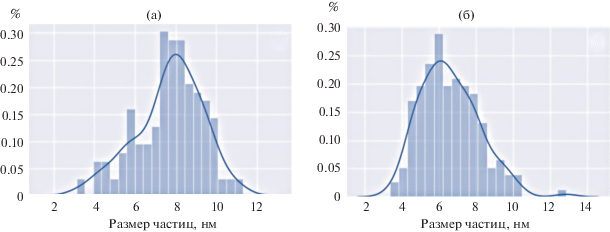
Рис. 6.
Кривые распределения частиц по размеру для образцов с содержанием допанта 7.5 (а) и 35% (б), синтезированных в стандартных условиях (сутки, 200°С).
Для исследования зависимости спектрально-люминесцентных свойств от размерного фактора необходимо синтезировать образцы с различным размером частиц [21]. Поэтому были проведены эксперименты, направленные на разработку способа контролируемого увеличения размера кристаллитов. На примере системы с 5 мол. % Er2O3 был проведен опыт с увеличением концентрации исходного раствора в пять раз. В результате получены образцы с размером 9 нм, который не отличается от размера частиц, полученных при стандартной концентрации исходного раствора. Увеличение времени гидротермальной обработки до 7 сут (t = 200°С) привело лишь к незначительному росту кристаллических зерен до 11 нм. При этом форма частиц не изменилась. Поэтому нами предложено проводить дополнительные отжиги синтезированных образцов в печи резистивного нагрева. Была проведена серия изотермических отжигов длительностью 6 ч при различной температуре. Отжиги проводили в Pt-тиглях. Зависимость размера частиц от температуры отжига для образцов с различным содержанием эрбия приведена в табл. 1. Видно, что отжиг при температуре <500°С не влияет на размер частиц. В то же время выдержка при температуре 900°С ведет к увеличению размера частиц приблизительно в два раза, а при 1200°С – в 3–7 раз. Таким образом, использование изотермических отжигов при различных температурах позволяет эффективно контролировать размер наночастиц, полученных гидротермальным способом.
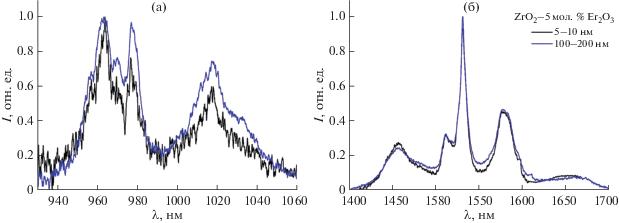
Спектры люминесценции образцов ZrO2–5 мол. % Er2O3 с различными размерами частиц показаны на рис. 7а, 7б. При возбуждении излучением с длиной волны 532 нм в спектре появляются полосы, обусловленные переходами 4I11/2 → → 4I15/2 и 4I13/2 → 4I15/2. Сравнение формы контуров спектров люминесценции для обоих переходов в образцах ZrO2–5 мол. % Er2O3 с размерами частиц от 5 до 71 нм не выявило существенных изменений.
Рис. 7.
Спектры люминесценции образцов ZrO2–5 мол. % Er2O3 с различным средним размером частиц: переход 4I11/2 → 4I15/2 (а), переход 4I13/2 → 4I15/2 (б).
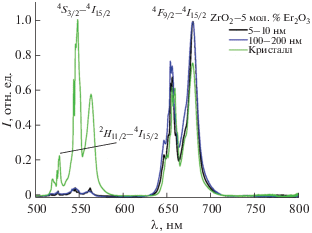
При возбуждении излучением с λ = 1550 нм в нанокристаллических образцах ZrO2–5 мол. % Er2O3 наблюдалась апконверсионная люминесценция в видимом диапазоне спектра, обусловленная переходами 2H11/2 → 4I15/2, 4S3/2 → 4I15/2, 4F9/2 → 4I15/2 ионов Er3+ с возбужденного уровня 4I13/2 (рис. 8). Аналогичные спектры также зарегистрированы для объемного кристалла ZrO2–13.4 мол. % Y2O3–0.6 мол. % Er2O3. Обнаружено совпадение формы контура спектров апконверсионной люминесценции наночастиц и объемного образца. Отличия наблюдались только в соотношении интенсивностей люминесценции в зеленой и красной областях спектра. Этот эффект может быть обусловлен различным механизмом заселения уровней 4S3/2 и 4F9/2 ионов Er3+ при их возбуждении на уровень 4I15/2 для монокристалла ZrO2–13.4 мол. % Y2O3 –0.6 мол. % Er2O3 и наночастиц ZrO2–5 мол. % Er2O3.
ЗАКЛЮЧЕНИЕ
В результате проведенного исследования разработана методика гидротермального синтеза неагрегированных нанокристаллических твердых растворов (1 – х)ZrO2 – хEr2O3 (х = 0.015–0.5) кубической модификации с размером частиц 5–9 нм. Показана эффективность дополнительного изотермического отжига для получения частиц большего размера.
Установлено, что форма спектров люминесценции, зарегистрированных для переходов 4I11/2 → 4I15/2 и 4I13/2 → 4I15/2 ионов Er3+ при возбуждении излучением с длиной волны 532 нм, а также спектров апконверсионной люминесценции с уровней 2H11/2, 4S3/2 и 4F9/2 на основной уровень 4I15/2 при возбуждении излучением с длиной волны 1550 нм не зависит от размера частиц.
Список литературы
Ryabochkina P.A., Sidorova N.V., Ushakov S.N., Lomonova E.E. // Quantum Electronics. 2014. V. 44. P. 135. https://doi.org/10.1070/QE2014v044n02ABEH015276
Wang X.V., Tan X.Y., Xu S.L. et al. // J. Lumin. 2020. V. 219. P. 116896. https://doi.org/10.1016/j.jlumin.2019.116896
Jasso G.T. Montesab E., Guzmán J.C. et al. // Ceram. Inter. 2018. V. 44. P. 154. https://doi.org//10.1016/j.ceramint.2017.09.152
Hyppänen I., Hölsä J., Kankare J. et al. // J. Lumin. 2009. V. 129. P. 1739. https://doi.org/10.1016/j.jlumin.2009.04.076
Patra A., Friend C.S., Kapoor R. et al. // J. Phys. Chem. B. 2002. V. 106. P. 1909. https://doi.org/10.1021/jp013576z
Guskov V.N., Gavrichev K.S., Gagarin P.G. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 10. P. 1265. https://doi.org/10.1134/S0036023619100048
Gagarin P.G., Tyurin A.V., Guskov V.N. et al. // Inorg. Mater. 2017. V. 53. P. 944. https://doi.org/10.1134/s0020168517090084
Maschio S., Linda B., Brückner S., Pezzotti G. // J. Ceram. Soc. Jpn. 2000. V. 108. P. 593. https://doi.org/10.2109/jcersj.108.1258_593
Li X., Lu S., Liu J. // Chin. J. Lumin. 2007. V. 28. № 3. P. 378.
Lu G., Huang Y. // Adv. Mater. Res. 2012. V. 616–618. P. 1882. https://doi.org/10.4028/www.scientific.net/AMR.616-618.1882
Durán P., Paloma Recio, José R. Jurado et al. // J. Am. Ceram. Soc. 1989. V. 72. № 11. P. 2088. https://doi.org/10.1111/j.1151-2916.1989.tb06036.x
Angeles-Chavez C., Salas P., Lopez-Luke T., de la Rosa E. // Vacuum. 2010. V. 84. № 10. P. 1226. https://doi.org/10.1016/j.vacuum.2009.10.030
Julián-López B., de la Luz V., Gonell F. et al. // J. Alloys. Compd. 2012. V. 519. P. 29. https://doi.org/10.1016/j.jallcom.2011.11.099
Gionco C., Paganini M.C., Giamello E. et al. // J. Energy Chem. 2017. V. 26. P. 270. https://doi.org/10.1016/j.jechem.2016.07.006
Duran P. // J. Am. Ceram. Soc. 1977. V. 60. P. 510. https://doi.org/10.1111/j.1151-2916.1977.tb14095.x
Jourdan J., Toffolon-Masclet C., Joubert J.M. // J. Nucl. Mater. 2010. V. 402. P. 102. https://doi.org/10.1016/j.jnucmat.2010.05.002
Glushkova V. B., Sazonova L.V. // Chem. High-Temperature Mater. 1969. P. 90. https://doi.org/10.1007/978-1-4899-4824-3_17
Коленько Ю.В., Максимов В.Д., Гаршев А.В. и др. // Журн. неорган. химии. 2004. Т. 49. № 8. P. 1237.
Murase Y., Kato E. // Nippon Kagaku Kaishi. 1978. V. 1978. № 3. P. 367.
Glushkova V.B., Hanic F., Sazonova L.V. // Ceram. Intern. 1978. V. 4. P. 176.
Ashraf S., Irfan M., Kim D. et al. // Ceram. Intern. 2014. V. 40. P. 8513. https://doi.org/10.1016/j.ceramint.2014.01.063
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии