Журнал неорганической химии, 2021, T. 66, № 1, стр. 88-96
Диаграмма твердофазных равновесий системы SnSe–Sb2Se3–Se и термодинамические свойства селенидов олова-сурьмы
Э. Н. Исмайлова a, Л. Ф. Машадиева a, Д. М. Бабанлы a, b, А. В. Шевельков c, М. Б. Бабанлы a, *
a Институт катализа и неорганической химии НАН Азербайджана
AZ-1148 Баку, пр-т Г. Джавида, 113, Азербайджан
b Азербайджанский государственный университет нефти и промышленности
AZ-1010 Баку, пр-т Азадлыг, 16/21, Азербайджан
c Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: babanlymb@gmail.com
Поступила в редакцию 06.07.2020
После доработки 31.08.2020
Принята к публикации 01.09.2020
Аннотация
Методами электродвижущих сил (ЭДС) и рентгенофазового анализа изучена система SnSe–Sb2Se3–Se, построена диаграмма твердофазных равновесий при 400 K. Из данных измерений ЭДС концентрационных цепей относительно электрода SnSe в интервале температур 300–450 K вычислены парциальные термодинамические функции SnSe в различных фазовых областях исследуемой системы. На основании этих данных с использованием соответствующих термодинамических функций SnSe и Sb2Se3 рассчитаны парциальные молярные функции олова в сплавах и стандартные термодинамические функции образования, а также стандартные энтропии соединений SnSe2, Sn2Sb6Se11, SnSb2Se4 и Sn2Sb2Se5.
ВВЕДЕНИЕ
Бинарные и тройные соединения, образующиеся в системах AIV–BV–Х (AIV = Ge, Sn, Pb; BV = Sb, Bi; X = Se, Te), относятся к числу перспективных функциональных материалов [1–5]. Многие из этих соединений, в частности тетрадимитоподобные фазы типа ${{{\text{A}}}^{{{\text{IV}}}}}{\text{B}}_{{\text{2}}}^{{\text{V}}}{\text{Т}}{{{\text{е}}}_{{\text{4}}}}$, ${{{\text{A}}}^{{{\text{IV}}}}}{\text{B}}_{{\text{4}}}^{{\text{V}}}{\text{Т}}{{{\text{е}}}_{{\text{7}}}}$, ${{{\text{A}}}^{{{\text{IV}}}}}{\text{B}}_{{\text{6}}}^{{\text{V}}}{\text{Т}}{{{\text{е}}}_{{{\text{10}}}}}$ и др., имеют высокие термоэлектрические характеристики [6–11]. Недавние исследования показали, что последние являются также трехмерными топологическими изоляторами и чрезвычайно перспективны для использования в спинтронике, квантовых вычислениях, медицине, системах безопасности и т.д. [12–19].
Для разработки методик и оптимизации условий синтеза и выращивания кристаллов многокомпонентных фаз необходимо наличие надежных данных по фазовым равновесиям в соответствующих системах и термодинамическим функциям образующихся в них фаз [20–27]. Ранее в работах [28–32] были проведены комплексные исследования фазовых равновесий в системах AIV–BV–X и термодинамических свойств образующихся в них тройных соединений и твердых растворов методом электродвижущих сил (ЭДС).
В настоящей работе представлены результаты подобного комплексного исследования системы Sn–Sb–Se в области составов SnSe–Sb2Se3–Se.
Фазовые равновесия в тройной системе Sn–Sb–Se исследовали в работах [33–37]. Построены политермические разрезы SnSe2–Sb2Se3 и SnSe–Sb2Se3, некоторые изотермические сечения фазовой диаграммы и проекция поверхности ликвидуса. Показано, что система SnSe2–Sb2Se3 имеет диаграмму состояния простого эвтектического типа [33]. Результаты работ [34–37] по системе SnSe–Sb2Se3 существенно отличаются друг от друга. Согласно [34], в системе SnSe–Sb2Se3 образуется одно конгруэнтно плавящееся тройное соединение Sn2Sb6Se11. Авторы [35] утверждают, что в данной системе образуются два соединения состава Sn2Sb6Se11 и Sn2Sb2Se5. В [36] показано образование только одного тройного соединения SnSb2Se4. Авторы работы [37] предполагают, что соединения Sn2Sb6Se11 и SnSb2Se4 лежат в области гомогенности одной фазы. К этому же заключению привело наше недавнее исследование по уточнению фазовой диаграммы системы SnSe–Sb2Se3 [38]. Было показано, что в системе SnSe–Sb2Se3 образуется тройное соединение Sn2Sb2Se5 и промежуточная γ-фаза с областью гомогенности 48–60 мол. % Sb2Se3. В эту область входят стехиометрические составы тройных соединений SnSb2Se4 и Sn2Sb6Se11, ранее указанных в [34–37].
Соединения Sn2Sb2Se5 и SnSb2Se4 кристаллизуются в орторомбической решетке [38–40].
Мы не обнаружили какие-либо данные по термодинамическим свойствам тройных соединений системы Sn–Sb–Se.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для проведения экспериментов сначала синтезировали бинарные соединения SnSe и Sb2Se3 методом прямого сплавления элементарных компонентов. Использовали олово, сурьму и селен высокой степени чистоты фирмы Evochem Advanced Materials GMBH (Германия). Синтез проводили в вакуумированных (~10–2 Па) кварцевых ампулах при температуре несколько выше (20–30 K) температур плавления синтезируемых соединений. Учитывая высокую упругость паров селена при температуре плавления SnSe, синтез этого соединения проводили в двухзонном режиме. Температура горячей зоны составляла 1200 K, холодной – 900 K, что несколько ниже температуры кипения селена (958 K) [41]. Sb2Se3 синтезировали в однозонной печи при ∼950 K. Полученные бинарные соединения идентифицировали методами ДТА (Netzsch 404 F1 Pegasus system) и РФА (дифрактометр D2 Phaser фирмы Bruker).
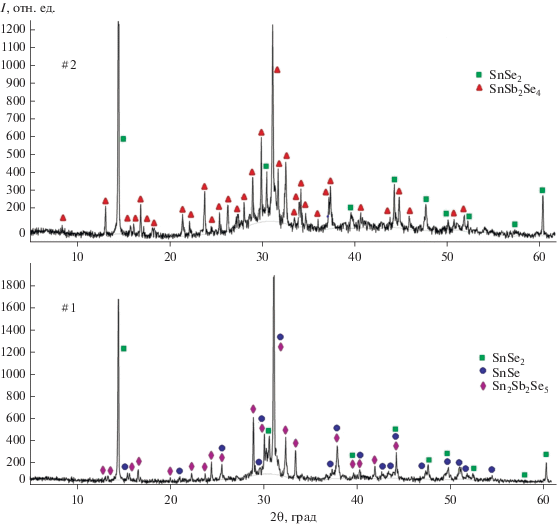
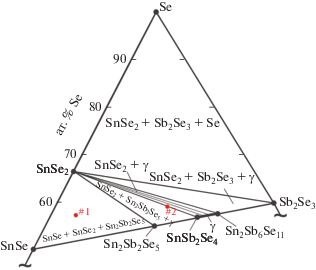
Для планирования исследований нами на основании литературных данных по фазовым равновесиям в системах Sn(Sb)–Se [42] и SnSe(SnSe2)–Sb2Se3 [33, 38] построена диаграмма твердофазных равновесий системы SnSe–Sb2Se3–Se (рис. 1). Правильность построения этой диаграммы контролировали рентгенофазовым анализом выборочных сплавов, приготовленных сплавлением синтезированных и идентифицированных бинарных соединений SnSe, Sb2Se3 и элементарного селена в условиях вакуума (10–2 Па). В качестве примера на рис. 2 приведены порошковые дифрактограммы равновесных сплавов из фазовых областей Sn2Sb2Se5 + SnSe + SnSe2 (сплав 1) и (SnSb2Se4) + + SnSe2 (сплав 2). Видно, что фазовые составы этих сплавов находятся в соответствии с фазовой диаграммой (рис. 1). Отметим, что полученная нами картина твердофазных равновесий при 400 K отличается от результатов работы [36], согласно которой в подсистеме SnSe–Sb2Se3–Se при 673.2 K образуется только одно тройное соединение SnSb2Se4, которое сосуществует с бинарными соединениями SnSe, SnSe2, Sb2Se3 и образует трехфазные области SnSe + SnSe2 + SnSb2Se4 и SnSe2 + SnSb2Se4 + Sb2Se3.
Рис. 1.
Диаграмма твердофазных равновесий системы SnSe–Sb2Se3–Se. #1 и #2 – составы образцов, порошковые дифрактограммы которых приведены на рис. 2.
Для термодинамического исследования системы SnSe–Sb2Se3–Se были составлены концентрационные цепи типа
(1)
$\left( -- \right){\text{SnSe}}\left( {{\text{тв}}} \right)\left| {{\text{жидкий электролит}},{\text{S}}{{{\text{n}}}^{{2 + }}}} \right|({\text{Sn}}\,\,{\text{в сплаве}})\left( {{\text{тв}}} \right)~\left( + \right).$Как и в работах [29, 30], концентрационные цепи относительно оловянного электрода оказались необратимыми – значения ЭДС непрерывно падали в течение опытов. По-видимому, это обусловлено химическим взаимодействием между электродами через электролит, приводящим к изменению их состава.
Правыми электродами в цепях типа (1) служили равновесные сплавы из трехфазной области SnSe + SnSe2 + Se и вдоль квазибинарного разреза SnSe–Sb2Se3 (составы 30, 35, 47, 50, 55, 62, 80 и 90 мол. % Sb2Se3 с 1 ат. % избытком селена), приготовленные вышеуказанным способом. Учитывая важность равновесности электрод-сплавов, литые образцы подвергали термическому отжигу при 750 K (500 ч) и дополнительно при 400 K (100 ч). Фазовые составы отожженных сплавов контролировали методом РФА. Электроды готовили прессованием стертых в порошок SnSе (левый электрод) и отожженных сплавов из вышеуказанных фазовых областей (правые электроды) в виде таблеток диаметром ∼5 мм и толщиной 2–3 мм на молибденовые проволоки, использованные в качестве токоотводов в электрохимической ячейке.
Электролитом служил глицериновый раствор KCl с добавлением 0.5 мас. % SnCl2. Учитывая недопустимость присутствия влаги и кислорода в электролите, глицерин (ч. д. а.) тщательно обезвоживали и обезгаживали откачкой при температуре ~400 K, использовали безводные, химически чистые соли.
Следует отметить, что метод ЭДС с глицериновым электролитом успешно применяется для термодинамического исследования бинарных и более сложных металлических, полупроводниковых и др. систем [28–32, 43–46].
Методики сборки электрохимической ячейки и измерений ЭДС подробно описаны в [43, 47]. Измерения ЭДС проводили в ячейке с инертной атмосферой с помощью высокоомного цифрового вольтметра Keithley 2100 6 1/2 Digit Multimeter в интервале температур 300–450 K.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
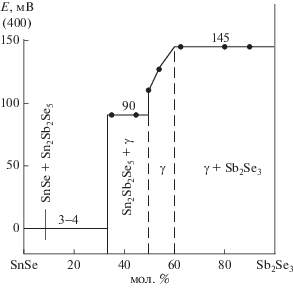
Измерения ЭДС цепей типа (1) привели к воспроизводимым результатам, находящимся в полном соответствии с диаграммой твердофазных равновесий системы SnSe–Sb2Se3–Se. В пределах каждой трехфазной области при заданной температуре численные значения ЭДС одинаковы (c точностью ±0.5 мВ) независимо от общего состава сплавов – правых электродов. Зависимость Е–х вдоль разреза SnSe–Sb2Se3 представлена на рис. 3, из которого видно, что на границе раздела двухфазных областей SnSe + Sn2Sb2Se5 и Sn2Sb2Se5 + γ ЭДС меняется скачкообразно, в пределах области гомогенности γ-фазы является функцией состава, а в двухфазных полях остается постоянной. Для всех изученных электрод-сплавов температурные зависимости ЭДС имеют линейный характер (рис. 4). Учитывая это, полученные экспериментальные данные были обработаны с помощью компьютерной программы Microsoft Office Excel 2003 методом наименьших квадратов в приближении линейной температурной зависимости ЭДС. Ход расчетов для трехфазной области γ + SnSe2 + + Sb2Se3 приведен в табл. 1. Полученные линейные уравнения представлены в табл. 2 в виде
(2)
$E = a + bT \pm t{{\left[ {\frac{{S_{E}^{2}}}{n} + \frac{{S_{E}^{2}{{{(T - \bar {T})}}^{2}}}}{{\sum {{{{({{T}_{i}} - \bar {T})}}^{2}}} }}} \right]}^{{\frac{1}{2}}}},$Рис. 4.
Зависимости ЭДС цепей типа (1) от температуры в некоторых фазовых областях системы Sn–Sb–Se: 1 – SnSe2 + Sb2Se3 + Se; 2 – γ(60 мол. % Sb2Se3) + + SnSe2 + Sb2Se3; 3 – γ(55 мол. % Sb2Se3) + SnSe2; 4 – γ(50 мол. % Sb2Se3) + SnSe2; 5 – Sn2Sb2Se5 + SnSb2Se4 + + SnSe2.
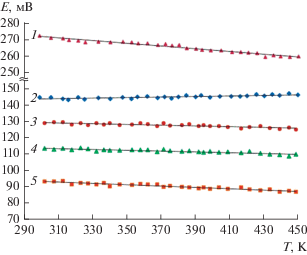
Таблица 1.
Результаты компьютерной обработки данных измерений ЭДС в фазовой области γ + SnSe2 + Sb2Se3 для получения линейного уравнения температурной зависимости ЭДС типа (2)
| Составляющие уравнения $E = a + bT \pm t{{\left[ {({{S_{E}^{2}} \mathord{\left/ {\vphantom {{S_{E}^{2}} n}} \right. \kern-0em} n}) + S_{b}^{2}{{{(T - \bar {T})}}^{2}}} \right]}^{{1/2}}}$ | |||||||
|---|---|---|---|---|---|---|---|
| Ti, K | Ei, мВ | ${{T}_{i}} - \bar {T}$ | Ei(${{T}_{i}} - \bar {T}$) | ${{({{T}_{i}} - \bar {T})}^{2}}$ | $\tilde {E}$ | ${{E}_{i}} - \tilde {E}$ | ${{({{E}_{i}} - \tilde {E})}^{2}}$ |
| 299.2 | 144.62 | –77.77 | –11247.58 | 6048.69 | 143.63 | 0.99 | 0.99 |
| 305.8 | 144.71 | –71.17 | –10299.49 | 5065.64 | 143.74 | 0.97 | 0.95 |
| 312.6 | 143.64 | –64.37 | –9246.59 | 4143.93 | 143.85 | –0.21 | 0.04 |
| 316.1 | 143.22 | –60.87 | –8718.28 | 3705.56 | 143.91 | –0.69 | 0.47 |
| 321.7 | 144.55 | –55.27 | –7989.76 | 3055.14 | 144.00 | 0.55 | 0.30 |
| 325.6 | 143.27 | –51.37 | –7360.26 | 2639.22 | 144.06 | –0.79 | 0.63 |
| 333.4 | 144.43 | –43.57 | –6293.30 | 1898.64 | 144.19 | 0.24 | 0.06 |
| 340.3 | 143.55 | –36.67 | –5264.46 | 1344.93 | 144.31 | –0.76 | 0.58 |
| 347.5 | 144.61 | –29.47 | –4262.14 | 868.68 | 144.43 | 0.18 | 0.03 |
| 352.7 | 143.68 | –24.27 | –3487.59 | 589.19 | 144.51 | –0.83 | 0.70 |
| 356.3 | 144.83 | –20.67 | –2994.12 | 427.39 | 144.57 | 0.26 | 0.07 |
| 361.8 | 145.02 | –15.17 | –2200.44 | 230.23 | 144.67 | 0.35 | 0.13 |
| 367.9 | 144.31 | –9.07 | –1309.37 | 82.33 | 144.77 | –0.46 | 0.21 |
| 372.1 | 144.96 | –4.87 | –706.44 | 23.75 | 144.84 | 0.12 | 0.02 |
| 376 | 144.14 | –0.97 | –140.30 | 0.95 | 144.90 | –0.76 | 0.58 |
| 380.2 | 144.77 | 3.23 | 467.12 | 10.41 | 144.97 | –0.20 | 0.04 |
| 384.5 | 145.81 | 7.53 | 1097.46 | 56.65 | 145.04 | 0.77 | 0.59 |
| 390 | 144.81 | 13.03 | 1886.39 | 169.69 | 145.13 | –0.32 | 0.11 |
| 393.3 | 145.92 | 16.33 | 2382.39 | 266.56 | 145.19 | 0.73 | 0.53 |
| 398.4 | 144.68 | 21.43 | 3100.01 | 459.10 | 145.27 | –0.59 | 0.35 |
| 404.3 | 145.14 | 27.33 | 3966.19 | 746.75 | 145.37 | –0.23 | 0.05 |
| 410.7 | 145.03 | 33.73 | 4891.38 | 1137.49 | 145.48 | –0.45 | 0.20 |
| 415.9 | 145.22 | 38.93 | 5652.93 | 1515.29 | 145.56 | –0.34 | 0.12 |
| 420.1 | 145.44 | 43.13 | 6272.34 | 1859.91 | 145.63 | –0.19 | 0.04 |
| 425.4 | 146.48 | 48.43 | 7093.54 | 2345.14 | 145.72 | 0.76 | 0.57 |
| 430.1 | 145.51 | 53.13 | 7730.46 | 2822.44 | 145.80 | –0.29 | 0.08 |
| 434.7 | 146.37 | 57.73 | 8449.45 | 3332.37 | 145.88 | 0.49 | 0.24 |
| 438.8 | 145.81 | 61.83 | 9014.95 | 3822.54 | 145.94 | –0.13 | 0.02 |
| 444.3 | 146.88 | 67.33 | 9888.94 | 4532.88 | 146.04 | 0.84 | 0.71 |
| 449.5 | 146.12 | 72.53 | 10597.60 | 5260.12 | 146.12 | 0.00 | 0.00 |
| $\bar {T} = 376.97$ | $\bar {E} = 144.92$ | $\sum {({{T}_{i}} - \bar {T})} $ = 971.05 | $\sum {{{{({{T}_{i}} - \bar {T})}}^{2}}} $ = 58461.60 | $\sum {{{{({{E}_{i}} - \tilde {E})}}^{2}}} $ = 9.41 | |||
Таблица 2.
Уравнения температурной зависимости ЭДС (Т = 300–450 K) для сплавов системы Sn–Sb–Se
| Фазовая область | Е, мВ = а + bТ ± 2$\tilde {S}$E(T) |
|---|---|
| SnSe2 + Sb2Se3 + Se | $296.41 - 0.0825~T \pm 2~{{\left[ {\frac{{0.49}}{{30}} + 8.4 \times {{{10}}^{{ - 6}}}{{{\left( {T - 376.97} \right)}}^{2}}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ |
| γ + SnSe2 + Sb2Se3 | $138.66 + 0.0166~T \pm 2~{{\left[ {\frac{{0.31}}{{30}} + 5.4 \times {{{10}}^{{ - 6}}}{{{\left( {T - 376.97} \right)}}^{2}}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ |
| γ + SnSe2 | $136.68 - 0.0240~T \pm 2~{{\left[ {\frac{{0.31}}{{30}} + 5.5 \times {{{10}}^{{ - 6}}}{{{\left( {T - 374.28} \right)}}^{2}}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ |
| SnSb2Se4 + SnSe2 | $121.42 - 0.0252~T \pm 2~{{\left[ {\frac{{0.33}}{{30}} + 6.0 \times {{{10}}^{{ - 6}}}{{{\left( {T - 374.28} \right)}}^{2}}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ |
| Sn2Sb2Se5 + SnSb2Se4 + SnSe2 | $105.70 - 0.0402~T \pm 2~{{\left[ {\frac{{0.30}}{{30}} + 5.4 \times {{{10}}^{{ - 6}}}{{{\left( {T - 374.28} \right)}}^{2}}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ |
Из данных табл. 2 по соотношениям [43, 44]:
Таблица 3.
Парциальные термодинамические функции SnSe в сплавах системы Sn–Sb–Se при 298.15 K
| Фазовая область | $ - \Delta {{\bar {G}}_{{{\text{SnSe}}}}}$ | $ - \Delta {{\bar {H}}_{{{\text{SnSe}}}}}$ | $\Delta {{\bar {S}}_{{{\text{SnSe}}}}}$, Дж K–1 моль–1 |
|---|---|---|---|
| кДж/моль | |||
| SnSe2 + Sb2Se3 + Se | 52.45 ± 0.10 | 57.20 ± 0.43 | –15.93 ± 1.12 |
| γ + SnSe2 + Sb2Se3 | 27.71 ± 0.08 | 26.76 ± 0.34 | 3.21 ± 0.89 |
| γ + SnSe2 | 24.99 ± 0.08 | 26.38 ± 0.34 | –4.64 ± 0.90 |
| SnSb2Se4 + SnSe2 | 21.98 ± 0.08 | 23.43 ± 0.36 | –4.85 ± 0.94 |
| Sn2Sb2Se5 + SnSb2Se4 + SnSe2 | 18.09 ± 0.08 | 20.40 ± 0.34 | –7.75 ± 0.90 |
Комбинированием данных табл. 3 с относительными парциальными термодинамическими функциями Sn в SnSe [48] (табл. 4) рассчитаны значения парциальных молярных функций олова в указанных фазовых областях, которые приведены в табл. 4.
Таблица 4.
Парциальные термодинамические функции олова в сплавах системы Sn–Sb–Se при 298.15 K
| Фазовая область | $ - \Delta {{\bar {G}}_{{{\text{Sn}}}}}$ | $ - \Delta {{\bar {H}}_{{{\text{Sn}}}}}$ | K$\Delta {{\bar {S}}_{{{\text{Sn}}}}}$, Дж К–1 моль–1 |
|---|---|---|---|
| кДж/моль | |||
| SnSe + SnSe2 [43] | 67.51 ± 0.10 | 65.00 ± 0.44 | 8.39 ± 1.16 |
| SnSe2 + Sb2Se3 + Se | 119.96 ± 0.20 | 122.20 ± 0.87 | –7.54 ± 2.28 |
| γ + SnSe2 + Sb2Se3 | 95.22 ± 0.18 | 91.76 ± 0.78 | 11.60 ± 2.05 |
| γ + SnSe2 | 92.20 ± 0.18 | 91.38 ± 0.78 | 3.76 ± 2.06 |
| SnSb2Se4 + SnSe2 | 89.49 ± 0.18 | 88.43 ± 0.80 | 3.56 ± 2.10 |
| Sn2Sb2Se5 + SnSb2Se4 + SnSe2 | 85.60 ± 0.18 | 85.40 ± 0.78 | 0.67 ± 2.06 |
Нетрудно показать, что парциальные молярные функции олова в трехфазных областях SnSe2 + Sb2Se3 + Se, γ(Sn2Sb6Se11) + SnSe2 + Sb2Se3 и Sn2Sb2Se5 + γ(SnSb2Se4) + SnSe2 являются термодинамическими функциями следующих потенциалообразующих реакций (все вещества кристаллические):
(4)
${\text{Sn}} + {\text{SnS}}{{{\text{e}}}_{2}} + 3{\text{S}}{{{\text{b}}}_{2}}{\text{S}}{{{\text{e}}}_{3}} = {\text{S}}{{{\text{n}}}_{2}}{\text{S}}{{{\text{b}}}_{6}}{\text{S}}{{{\text{e}}}_{{11}}},$(5)
${\text{Sn}} + {\text{SnS}}{{{\text{e}}}_{2}} + 2{\text{SnS}}{{{\text{b}}}_{2}}{\text{S}}{{{\text{e}}}_{4}} = 2{\text{S}}{{{\text{n}}}_{2}}{\text{S}}{{{\text{b}}}_{2}}{\text{S}}{{{\text{e}}}_{5}}.$В соответствии с этими реакциями интегральные термодинамические функции соединений SnSe2, Sn2Sb6Se11 и Sn2Sb2Se5 были вычислены по соотношениям:
(7)
$S^\circ ({\text{SnS}}{{{\text{e}}}_{2}}) = \Delta {{\bar {S}}_{{{\text{Sn}}}}} + S^\circ ({\text{Sn}}) + 2S^\circ ({\text{Se}}),$(8)
$\begin{gathered} {{\Delta }_{f}}Z({\text{S}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{b}}}_{{\text{6}}}}{\text{S}}{{{\text{e}}}_{{11}}}) = \\ = \Delta {{{\bar {Z}}}_{{{\text{Sn}}}}} + {{\Delta }_{f}}Z^\circ ({\text{SnS}}{{{\text{e}}}_{{\text{2}}}}) + 3{{\Delta }_{f}}Z^\circ ({\text{S}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{3}}}}), \\ \end{gathered} $(9)
$\begin{gathered} S^\circ ({\text{S}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{b}}}_{{\text{6}}}}{\text{S}}{{{\text{e}}}_{{{\text{11}}}}}) = \Delta {{{\bar {S}}}_{{{\text{Sn}}}}} + S^\circ ({\text{Sn}}) + \\ + \,\,S^\circ ({\text{SnS}}{{{\text{e}}}_{{\text{2}}}}) + 3S^\circ ({\text{S}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{3}}}}), \\ \end{gathered} $(10)
$\begin{gathered} {{\Delta }_{f}}Z({\text{S}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{5}}}}) = 0.5\Delta {{{\bar {Z}}}_{{{\text{Sn}}}}} + \\ + \,\,0.5{{\Delta }_{f}}Z^\circ ({\text{SnS}}{{{\text{e}}}_{{\text{2}}}}) + {{\Delta }_{f}}Z^\circ ({\text{SnS}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{4}}}}), \\ \end{gathered} $(11)
$\begin{gathered} S^\circ ({\text{S}}{{{\text{n}}}_{{\text{2}}}}{\text{S}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{5}}}}) = 0.5\Delta {{{\bar {S}}}_{{{\text{Sn}}}}} + 0.5S^\circ ({\text{Sn}}) + \\ + \,\,0.5S^\circ ({\text{SnS}}{{{\text{e}}}_{{\text{2}}}}) + S^\circ ({\text{SnS}}{{{\text{b}}}_{{\text{2}}}}{\text{S}}{{{\text{e}}}_{{\text{4}}}}). \\ \end{gathered} $В уравнениях (6), (8), (10) Z≡G, H. Стандартные интегральные термодинамические функции γ-фазы стехиометрического состава SnSb2Se4 вычислены интегрированием уравнения Гиббса–Дюгема по лучевой прямой, исходящей из вершины Sn концентрационного треугольника и проходящей через состав SnSb2Se4 [43].
При расчетах интегральных термодинамических функций тройных фаз использованы литературные данные по соответствующим термодинамическим характеристикам Sb2Se3 (табл. 5), а также значения стандартных энтропий олова (51.55 ± 0.21 Дж K–1 моль–1) и селена (42.13 ± ± 0.21 Дж K–1 моль–1), приведенные в [49]. Использованные при расчетах стандартные интегральные термодинамические функции Sb2Se3 являются взаимосогласованными и вполне надежными. Значения стандартных теплоты образования и энтропии (табл. 5), рекомендованные в различных справочниках [49–53], согласуются между собой и практически совпадают с калориметрическими данными [54], а стандартная свободная энергия образования Гиббса рассчитана нами из этих величин.
Таблица 5.
Стандартные интегральные термодинамические функции бинарных и тройных соединений в подсистеме SnSe–Sb2Se3–Se
| Соединение | –Δf G° | –Δf H° | Δf S° | S° | Источник |
|---|---|---|---|---|---|
| 298 K | |||||
| кДж/моль | Дж K– 1 моль– 1 | ||||
| Sb2Se3 | 125.9 ± 3.0 | 127.6 ± 1.3 | – | 212.1 ± 3.3 | [44–47] |
| 127.6 ± 1.1 | [48] | ||||
| SnSe2 | 120.0 ± 0.3 | 122.2 ± 0.9 | –7.5 ± 2.3 | 128.3 ± 3.0 | Наст. работа |
| 119.7 ± 0.1 | 121.3 ± 0.4 | 130.4 ± 1.7 | [43] | ||
| 119.7 + 0.2 | 124.7 + 1.2 | – | [49] | ||
| 119.0 ± 4.2 | [50] | ||||
| 110.0 | 117.2 | 111.7 | [46] | ||
| 124.7 ± 8.4 | 118.0 | [45] | |||
| 82.4 | [44] | ||||
| 91.4 | 82.4 | 119.0 ± 4.2 | [47] | ||
| Sn2Sb6Se11 | 592.9 ± 9.4 | 596.9 ± 5.2 | –13.1 ± 5.5 | 827.8 ± 15.2 | Наст. работа |
| SnSb2Se4 | 232.8 ± 3.2 | 234.9 ± 2.4 | –6.7 ± 3.9 | 306.5 ± 6.0 | Наст. работа |
| Sn2Sb2Se5 | 335.4 ± 3.4 | 338.6 ± 3.3 | –3.5 ± 6.1 | 396.8 ± 8.6 | Наст. работа |
В расчетах по соотношениям (10) и (11) использованы полученные нами данные для γ-фазы состава SnSb2Se4 (табл. 5).
Погрешности находили методом накопления ошибок.
Результаты, полученные нами для SnSe2, находятся в соответствии с данными [48, 50, 51, 54] и значительно выше величин, приведенных в [49, 52], которые, по-видимому, являются заниженными.
ЗАКЛЮЧЕНИЕ
Представлены результаты комплексного исследования твердофазных равновесий в системе SnSe–Sb2Se3–Se и термодинамических свойств промежуточных фаз методами ЭДС и РФА. Построена диаграмма твердофазных равновесий исследуемой системы при комнатной температуре, отличающаяся от результатов недавно опубликованной работы [36]. Измерением ЭДС обратимых концентрационных относительно электрода SnSe цепей в интервале температур 300–450 K получены линейные уравнения температурной зависимости ЭДС в некоторых трехфазных областях и вычислены парциальные термодинамические функции SnSe в сплавах. На основании этих данных с использованием соответствующих термодинамических функций SnSe и Sb2Se3 рассчитаны парциальные молярные функции олова в сплавах и стандартные термодинамические функции образования, а также стандартные энтропии соединений SnSe2, Sn2Sb6Se11, SnSb2Se4 и Sn2Sb2Se5. Полученные результаты для SnSe2 дополняют имеющиеся в литературе данные, а термодинамические функции тройных фаз определены нами впервые.
Список литературы
Alonso-Vante N. // Springer Inter. Publish. AG, 2018. P. 226. https://doi.org/10.1007/978-3-319-89612-0
Applications of Chalcogenides: S, Se, and Te / Ed. Ahluwalia G.K. Cham. Springer, 2016. P. 461. https://doi.org/10.1007/978-3-319-41190-3
Sanghoon X.L., Tengfei L.J., Zhang L.Y-H. Chalcogenide. From 3D to 2D and Beyond. Elsevier, 2019. P. 398. https://doi.org/10.1016/C2017-0-03585-1
Chalcogenides: Advances in Research and Applications / Ed. Nova P.W. 2018. P. 111.
Greenberg E., Hen B., Layek S. et al. // J. Phys. Rev. B. 2017. V. 95. № 6. P. 064514-5. https://doi.org/10.1103/PhysRevB.95.064514
Matsumoto R., Hou Z., Hara H. et al. // Appl. Phys. Express. 2018. V. 11. № 9. P. 093101-4. https://doi.org/10.7567/APEX.11.093101
Kosuga A., Nakai K., Matsuzawa M. et al. // J. Alloys Compd. 2015. V. 618. P. 463. https://doi.org/10.1016/j.jallcom.2014.08.183
Zemskov V.S., Shelimova L.E., Konstantinov P.P. et al. // Inorg. Mater. Appl. Res. 2013. V. 4. P. 77. https://doi.org/10.1134/S2075113313020196
Von R.F., Schilling A., Cava R.J. // J. Phys.: Condens. Matter. 2013. V. 25. № 7. P. 075804. https://doi.org/10.1088/0953-8984/25/7/075804
Quang T.V., Kim M. // J. Korean Phys. Soc. 2019. V. 74. № 3. P. 256. https://doi.org/10.3938/jkps.74.256
Kuropatwa B.A., Kleinke H. // Z. Anorg. Allg. Chem. 2012. V. 638. № 15. P. 2640. https://doi.org/10.1002/zaac.201200284
Babanly M.B., Chulkov E.V., Aliev Z.S. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 13. P. 1703. https://doi.org/10.1134/S0036023617130034
Shvets I.A., Klimovskikh I.I., Aliev Z.S. et al. // J. Phys. Rev. B. 2019. V. 100. P. 195127-5. https://doi.org/10.1103/PhysRevB.100.195127
Vergniory M.G., Menshchikova T.V., Silkin I.V. et al. // J. Phys. Rev. B. 2015. V. 92. № 4. https://doi.org/10.1103/physrevb.92.045134
Pacile D., Eremeev S.V., Caputo M. et al. // J. Phys. Stat. Sol. (RRL) - Rapid Research Letters. 2018. P. 1800341-8. https://doi.org/10.1002/pssr.201800341
Papagno M., Eremeev S., Fujii J. et al. // ACS Nano. 2016. V. 10. P. 3518. https://doi.org/10.1021/acsnano.5b07750
Hattori Y., Tokumoto Y., Kimoto K. et al. // Sci. Rep. 2020. V. 10. № 1. https://doi.org/10.1038/s41598-020-64742-6
Shvets I.A., Klimovskikh I.I., Aliev Z.S. et al. // J. Phys. Rev. B. 2017. V. 96. P. 235124 -7. https://doi.org/10.1103/physrevb.96.235124
Mal P., Bera G., Turpu G.R. et al. // J. Phys. Chem. Chem. Phys. 2019. V. 21. P. 15 030. https://doi.org/10.1039/c9cp01494b
Matsushita T., Mukai K. Chemical Thermodynamics in Materials Science: From Basics to Practical Applications. Springer, 2018. P. 257. https://doi.org/10.1007/978-981-13-0405-7
Воронин Г.Ф., Герасимов Я.И. Термодинамика и полупроводниковое материаловедение. М.: МИЭТ, 1980. С. 3–10.
Babanly M.B., Mashadiyeva L.F., Babanly D.M. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 13. P. 1649. https://doi.org/10.1134/S0036023619130035
Imamaliyeva S.Z., Babanly D.M., Tagiev D.B. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 13. P. 1703. https://doi.org/10.1134/S0036023618130041
Asadov M.M., Mustafaeva S.N., Tagiyev D.B. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 5. P. 733. https://doi.org/10.1134/S0036023620050022
Исмаилова Э.Н., Машадиева Л.Ф., Бахтиярлы И.Б. и др. // Журн. неорган. химии. 2019. Т. 64. № 6. С. 646. [Ismailova E.N., Mashadieva L.F., Bakhtiyarly I.B. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 6. P. 801. https://doi.org/10.1134/S0036023619060093]https://doi.org/10.1134/S0044457X19060096
Бахтиярлы И.Б., Курбанова Р.Д., Абдуллаева А.С. и др. // Журн. неорган. химии. 2019. Т. 64. № 7. С. 736. [Bakhtiyarly I.B., Kurbanova R.D., Abdullaeva A.S. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 7. P. 890. https://doi.org/10.1134/S0036023619070039]https://doi.org/10.1134/S0044457X19070031
Кертман А.В. // Журн. неорган. химии. 2019. Т. 64. № 1. С. 93. [Kertman A.V. // Russ. J. Inorg. Chem. 2019. V. 64. P. 130. https://doi.org/10.1134/S0036023619010133]https://doi.org/10.1134/S0044457X19010136
Гусейнов Ф.Н., Бабанлы К.Н., Алиев И.И. и др. // Журн. неорган. химии. 2012. Т. 57. № 1. С. 107. [Guseinov F.N., Babanly K.N., Aliev I.I. et al. // Russ. J. Inorg. Chem. 2012. V. 57. P. 100. https://doi.org/10.1134/S003602361201010X ]
Гусейнов Ф.Н., Сеидзаде А.Э., Юсибов Ю.А. и др. // Неорган. материалы. 2017. Т. 53. № 4. С. 347. [Guseinov F.N., Seidzade A.E., Yusibov Yu.A. et al. // Inorg. Mater. 2017. V. 53. P. 354. https://doi.org/10.1134/S0020168517040057]
Бабанлы М.Б., Гусейнов Ф.Н., Дашдыева Г.Б. и др. // Неорган. материалы. 2011. Т. 47. № 3. С. 284. [Babanly M.B., Guseinov F.N., Dashdyeva G.B. et al. // Inorg. Mater. 2011. V. 47. № 3. P. 235. https://doi.org/10.1134/S0020168511030022]
Бабанлы М.Б., Шевельков А.В., Гусейнов Ф.Н. и др. // Неорган. материалы. 2011. Т. 47. № 7. С. 796. [Babanly M.B., Shevelkov A.V., Guseinov F.N. et al. // Inorg. Mater. 2011. V. 47. № 7. P. 712. https://doi.org/10.1134/S002016851107003X]
Mansimova Sh.H., Mirzoeva R.J., Mashadiyeva L.F. et al. // J. Appl. Sol. Stat. Chem. 2018. № 4. P. 104. https://doi.org/10.18572/2619-0141-2018-4-5-104-111
Ostapyuk T.A., Yermiychuk I.M., Zmiy O.F. et al. // Chem. Met. Alloys. 2009. V. 2. P. 164. https://doi.org/10.30970/cma2.0100
Wobst W. // J. Less Common Metals. 1968. V. 14. № 1. P. 77.
Господинов Г.Г., Один И.И., Новоселова А.В. // Неорган. материалы. 1975. Т. 11. № 7. С. 1211.
Chang J., Chen S. // Metall. Mater. Trans. E. 2017. V. 4. № 2–4. P. 89. https://doi.org/10.1007/s40553-017-0110-8
Shen J., Blachnik R. // J. Therm. Acta. 2003. V. 399. № 1–2. P. 245. https://doi.org/10.1016/s0040-6031(02)00461-6
Ismailova E.N., Bakhtiyarly I.B., Babanly M.B. // J. Chem. Probl. 2020. № 2. P. 250. https://doi.org/10.32737/2221-8688-2020-2-250-256
Smith P.K., Parise J.B. // Acta Crystallogr., Sect. B. 1985. V. 41. P. 84. https://doi.org/10.1107/S0108768185001665
Mukherjee A. // Jpn. J. Appl. Physics. 1982. V. 20. P. 681.
Emsley J. The Elements, third ed. Clarendon Press, 1998.
Massalski T.B. Binary Alloys Phase Diagrams, Second Edition // ASM International. Mat. Park. Ohio, 1990.
Бабанлы М.Б., Юсибов Ю.А. Электрохимические методы в термодинамике неорганических систем. Баку: ЭЛМ, 2011. С. 306.
Морачевский А.Г., Воронин Г.Ф., Гейдерих В.А., Куценок И.Б. Электрохимические методы исследования в термодинамике металлических систем. М.: ИЦК Академкнига, 2003. С. 334.
Vassiliev V.P., Lysenko V.A. // Electrochimica Acta. 2016. V. 222. P. 1770. https://doi.org/10.1016/j.electacta.2016.11.075
Sidorko V.R., Goncharuk L.V., Antonenko R.V. // Powder Metal. Metal Ceramics. 2008. V. 47. P. 234. https://doi.org/10.1007/s11106-008-9009-3
Imamaliyeva S.Z., Musayeva S.S., Babanly D.M. et al. // Thermochimica Acta. 2019. V. 679. P. 178319-7. https://doi.org/10.1016/j.tca.2019.178319
Ismayilova E.N., Babanly D.M., Zlomanov V.P. et al. // J. New Mater. Comp. Appl. 2020. № 3.
База данных термических констант веществ / Электронная версия под ред. Йориша В.С., Юнгмана В.С. 2006. http://www.chem.msu.su/cgi-bin/tkv
Kubaschewski O., Alcock C.B., Spenser P.J. Materials Thermochemistry. 6-th ed. Pergamon Press, England. 1993. P. 363.
Barin I. Thermochemical Data of Pure Substances. Third Edition. VCH. 2008.
Герасимов Я.И., Крестовников А.Н., Горбов С.И. Химическая термодинамика в цветной металлургии. Справочник. М.: Металлургия, 1974. Т. 6. С. 312.
Howlett B.W., Misra S., Bever M. // Trans. Metall. Soc. AIME. 1964. V. 230. P. 1367.
Мелех Б.Т., Степанова Н.Б., Фомина Т.А. // Журн. физ. химии. 1971. Т. 45. С. 2018.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии