Журнал неорганической химии, 2022, T. 67, № 2, стр. 224-229
Анализ ряда трехкомпонентных систем МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs) и экспериментальное исследование трехкомпонентной системы RbF–RbBr–Rb2CrO4
А. В. Харченко a, *, Е. М. Егорова a, И. К. Гаркушин a
a Самарский государственный технический университет,
443100 Самара, ул. Молодогвардейская, 244, Россия
* E-mail: anastasya.babenko2010@yandex.ru
Поступила в редакцию 14.07.2021
После доработки 01.09.2021
Принята к публикации 17.09.2021
- EDN: CFTDOU
- DOI: 10.31857/S0044457X22020064
Аннотация
Многокомпонентные системы из галогенидов и хроматов щелочных металлов используются в качестве расплавляемых электролитов для химических источников тока, теплоаккумулирующих материалов и др. В работе объектом исследования являлась трехкомпонентная система RbF–RbBr–Rb2CrO4. Проведен анализ трехкомпонентных систем МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs) методом сравнения типа ликвидуса в рядах, образованных последовательной заменой щелочного металла в соответствии с увеличением порядкового номера в Периодической системе. Методом дифференциального термического анализа исследована система RbF–RbBr–Rb2CrO4. Изучены фазовые равновесия в системе, установлены кристаллизующиеся фазы, выявлены характеристики трехкомпонентных эвтектики и перитектики (экв. %): RbF – 39.5, RbBr – 52.0, Rb2CrO4 – 8.5, температура плавления 522°С и RbF – 19.7, RbBr – 55.0, Rb2CrO4 – 25.3, температура плавления 554°С соответственно.
ВВЕДЕНИЕ
Изучению многокомпонентных солевых систем посвящено большое количество работ разных исследователей, что позволяет накапливать и систематизировать материал о фазовых равновесиях и типах ликвидусов в системах. Анализ накопленных данных и рассмотрение объекта исследования путем построения однотипных рядов систем при замене в соли катиона или аниона в порядке размещения соответствующего элемента в Периодической системе позволяют прогнозировать характер ликвидуса неизученной системы, входящей в рассматриваемый ряд [1–7].
Предварительный теоретический анализ системы и включающих ее рядов, использование расчетных методов для прогноза характеристик нонвариантных точек [8–10], комбинация расчетного и экспериментального методов [11] позволяют минимизировать объем экспериментальных данных и, соответственно, сократить время изучения систем.
В работе объектом исследования выбрана трехкомпонентная система RbF–RbBr–Rb2CrO4, по которой информация в справочной литературе отсутствует. Данная система может выявить ценные в прикладном смысле низкоплавкие нонвариантные сплавы, перспективные для разработки расплавляемых электролитов для химических источников тока [12, 13]. Для оптимизации экспериментального исследования проведен предварительный теоретический анализ ликвидусов систем из фторидов, бромидов и хроматов s1-элементов МF–MBr–M2CrO4 (M = Li, Na, K, Rb, Cs). Массив систем представлен рядом, образованным при последовательной замене щелочного металла в порядке увеличения заряда ядра атома.
ТЕОРЕТИЧЕСКИЙ АНАЛИЗ
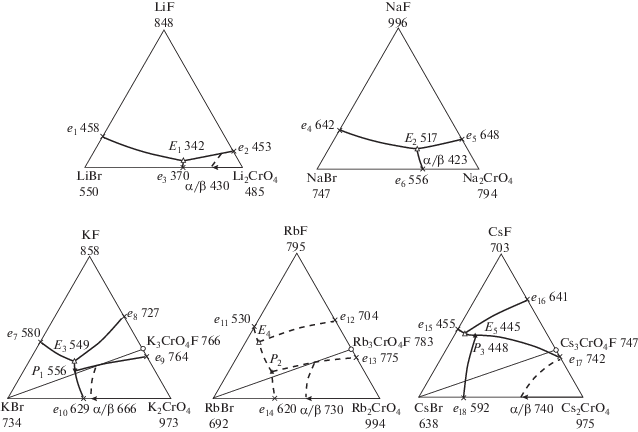
На рис. 1 представлен ряд трехкомпонентных систем МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs). Системы МF–MBr–M2CrO4 (М = Li, Na, K, Cs) исследованы ранее [14–16]. Проекция поверхности ликвидуса неизученной системы RbF–RbBr–Rb2CrO4 (наиболее вероятный вариант) нанесена пунктиром. В данном ряду систем при замене катиона щелочного металла происходит усложнение характера взаимодействия, вызванное образованием соединения конгруэнтного плавления в бинарных системах с участием солей калия, рубидия и цезия. Три системы в рассматриваемом ряду разбиты на две подсистемы (симплексы) секущей, проходящей через точку, соответствующую составу соединения. При этом в изученных ранее системах из солей калия и цезия установлено, что бинарное соединение внутри трехкомпонентной системы меняет свой характер плавления с конгруэнтного на инконгруэнтный, что приводит к образованию трехкомпонентных нонвариантных точек – эвтектики и перитектики. Аналогичный характер взаимодействия компонентов и тип лик-видуса ожидаются и в системе из солей рубидия.
Элементами огранения тройной системы являются три двухкомпонентные системы (рис. 2). Проведенный обзор литературы показал, что в системах RbF–RbBr и RbBr–Rb2CrO4 образуются эвтектики [17]. В системе RbF–Rb2CrO4 присутствует двойное соединение RbF ⋅ Rb2CrO4 конгруэнтного плавления [18]. Исходные данные по индивидуальным веществам и двухкомпонентным системам, входящим в трехкомпонентную систему, приведены в табл. 1.
Таблица 1.
Данные по индивидуальным веществам и двойным системам
| Реактив | tпл, °С | Квалификация | ТУ | |
|---|---|---|---|---|
| Индивидуальные вещества | ||||
| RbF | 795 | ч. | ТУ 6-09-04-229-83 | |
| RbBr | 692 | ч. | ТУ 6-09-3200-73 | |
| Rb2CrO4 | 994 | ч. | ТУ 6-09-3202-73 | |
| Система | Состав, экв. % | Характер точки | tпл, °С | |
| Двойные системы | ||||
| RbF–RbBr | 50 | 50 | Эвтектика | 530 |
| RbF–Rb2CrO4 | 53.8 33.3 28.2 |
46.2 66.7 71.8 |
Эвтектика Дистектика Эвтектика |
704 783 775 |
| RbBr–Rb2CrO4 | 63.0 44.0 |
37.0 56.0 |
Эвтектика Перитектика |
620 730 |
Экспериментальное исследование проводили методом дифференциального термического анализа (ДТА) [19, 20] на установке в стандартном исполнении [21, 22]. Исходные реактивы квалификации “ч.” были предварительно обезвожены. Температуры плавления веществ соответствовали справочным данным [23]. Исследования проводили в стандартных платиновых микротиглях. Составы выражены в молярных долях эквивалентов (экв. %).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
С целью подтверждения результатов прогноза и определения характеристик точек нонвариантного равновесия экспериментально исследована система RbF–RbBr–Rb2CrO4, проекция ликвидуса на треугольник составов которой представлена на рис. 2.
Для выявления точек нонвариантных равновесий в трехкомпонентной системе RbF–RbBr–Rb2CrO4 в соответствии с правилами проекционно-термографического метода [24] выбран политермический разрез A[60% RbBr + 40% RbF]–B[60% RbBr + 40% Rb2CrO4], проходящий через оба вторичных фазовых треугольника системы.
Изучение Т–х-диаграммы разреза AB позволило установить пересечение линий вторичной кристаллизации фторида рубидия и соединения Rb3CrO4F (${{\bar {E}}_{4}}$), а также пересечение линии вторичной кристаллизации бромида рубидия с линией кристаллизации соединения (${{\bar {P}}_{2}}$) и температуры плавления эвтектики (522°С) и перитектики (554°С) (рис. 3). Кроме того, установлена точка пересечения политермического разреза АВ с линией, отвечающей совместной кристаллизации полей RbBr и α-Rb2CrO4.
Изучением разрезов, выходящих из вершины RbBr и проходящих через точки пересечения ветвей вторичной кристаллизации ${{\bar {P}}_{2}}$ и ${{\bar {E}}_{4}}$ на разрезе AB, определены составы смесей, отвечающих нонвариантным равновесиям (рис. 4 и 5): Е4 522°С при содержании компонентов 39.5% RbF, 52.0% RbBr, 8.5% Rb2CrO4; температура плавления эвтектики P2 составила 554°С при содержании компонентов 19.7% RbF, 55.0% RbBr, 25.3% Rb2CrO4.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В работе впервые теоретически и экспериментально изучены фазовые равновесия в трехкомпонентной системе RbF–RbBr–Rb2CrO4. На основании анализа характера ликвидусов систем в ряду МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs) сделан качественный прогноз о наличии в системе из солей рубидия трехкомпонентных нонвариантных точек (эвтектики и перитектики), что подтверждено экспериментально методом ДТА. В системе образуются эвтектика и перитектика и кристаллизуются следующие фазы: RbF, RbBr, Rb3CrO4F, α-Rb2CrO4 и β-Rb2CrO4.
ЗАКЛЮЧЕНИЕ
Экспериментальным исследованием подтверждена топология ликвидуса трехкомпонентной системы RbF–RbBr–Rb2CrO4, полученная в результате теоретического анализа топологии ликвидусов ряда систем МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs). Треугольник составов разбивается стабильной секущей RbBr–Rb3CrO4F на два вторичных фазовых треугольника: RbF–RbBr–Rb3CrO4F и RbF–Rb2CrO4–Rb3CrO4F.
Методом ДТА определены составы и температуры плавления тройных точек нонвариантных равновесий – эвтектики и перитектики.
Анализ топологии ликвидусов ряда систем МF–MBr–M2CrO4 (М = Li, Na, K, Rb, Cs) показал, что температура плавления тройных эвтектик повышается от лития к калию и снижается к рубидию и цезию.
Список литературы
Фролов Е.И., Финогенов А.А., Гаркушин И.К. и др. // Журн. неорган. химии. 2020. Т. 65. № 3. С. 384. [Frolov E.I., Finogenov A.A., Garkushin I.K. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 3. P. 405.] https://doi.org/10.31857/S0044457X20030034
Егорцев Г.Е., Гаркушин И.К. // Журн. неорган. химии. 2008. Т. 53. № 9. С. 1596. [Egortsev G.E., Garkushin I.K. // Russ. J. Inorg. Chem. 2008. V. 53. № 9. P. 1495.]
Гаркушин И.К., Кондратюк И.М., Дворянова Е.М., Данилушкина Е.Г. Анализ, прогнозирование и экспериментальное исследование рядов систем из галогенидов щелочных и щелочноземельных элементов. Екатеринбург: УрО РАН, 2006. 148 с.
Федоров П.П. // Журн. неорган. химии. 2021. Т. 66. № 4. С. 510. [Fedorov P.P. // Russ. J. Inorg. Chem. 2021. V. 66. № 4. P. 550.] https://doi.org/10.1134/S0036023621040100
Ахмедова П.А., Гасаналиев А.М., Гаматаева Б.Ю. и др. // Журн. неорган. химии. 2017. Т. 62. № 10. С. 1393. [Akhmedova P.A., Gasanaliev A.M., Gamataeva B.Y. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 10. P. 1390.]
Ахмедова П.А., Гасаналиев А.М., Гаматаева Б.Ю. и др. // Журн. неорган. химии. 2018. Т. 63. № 6. С. 791. [Akhmedova P.A., Gasanaliev A.M., Gamataeva B.Y. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 6. P. 837.] https://doi.org/10.1134/S0036023618060025
Алиев А.Р., Ахмедов И.Р., Какагасанов М.Г. и др. // Журн. физ. химии. 2018. Т. 92. № 3. С. 403. [Aliev A.R., Akhmedov I.R., Kakagasanov M.G. et al. // Russ. J. Phys. Chem. 2018. Т. 92. № 3. С. 470.]
Трунин А.С., Будкин А.В., Мощенская Е.Ю. // Актуальные проблемы современной науки. Самара, 2003. Ч. 9. С. 44.
Mantha D., Wang T., Reddy R.G. // J. Phase Equilibria Diffusion. 2012. V. 33. № 2. P. 110. https://doi.org/10.1007/s11669-012-0005-4
Jian L.-X., Wu X.-Y., Tan Y.-Q. // J. Hunan University Natural Sci. 2014. V. 41. № 12. P. 75.
Гаркушин И.К., Губанова Т.В., Фролов Е.И., Мощенская Е.Ю. // Электрохимическая энергетика. Саратов, 2010. Т. 10. № 3. С. 147.
Masset P., Poinso J.-Y., Schoeffert S. et al. // J. Electrochem. Soc. 2005. V. 152. № 2. P. A405. https://doi.org/10.1149/1.1850861
Sveinbjörnsson D., Christiansen A.S., Viskinde R. et al. // J. Electrochem. Soc. 2014. V. 161. № 9. P. A1432. https://doi.org/10.1149/2.1061409jes
Игнатьева Е.О., Чугунова М.В. // Ашировские чтения. Самара, 2017. Т. 1. № 1-1(9). С. 109.
Игнатьева Е.О., Дворянова Е.М., Гаркушин И.К. // Конденсированные среды и межфазные границы. Воронеж, 2011. Т. 13. № 4. С. 445.
Дворянова Е.М., Игнатьева Е.О., Гаркушин И.К. // Бутлеровские сообщения. Казань, 2011. Т. 24. № 2. С. 71.
Посыпайко В.И., Алексеева Е.А. Диаграммы плавкости солевых систем. Ч. III. Двойные системы с общим катионом. М.: Металлургия, 1979. 204 с.
Воскресенская Н.К., Евсеева Н.Н., Беруль С.И., Верещатина И.П. Справочник по плавкости систем из безводных неорганических солей. М.: Изд-во АН СССР, 1961. Т.1. 845 с.
Wagner M. Thermal Analysis in Practice: Fundamental Aspects. Hanser Publications, 2018. P. 158.
Уэндландт У. Термические методы анализа. М.: Мир, 1978. 528 с.
Мощенский Ю.В. // Приборы и техника эксперимента. М.: РАН, 2003. Т. 46. № 6. С. 143.
Федотов С.В., Мощенский Ю.В. Интерфейсное программное обеспечение DSCTool. Самара: Самар. гос. техн. ун-т, 2004. 23 с.
Термические константы веществ. Справочник / Под ред. Глушко В.П. М.: ВИНИТИ, 1981. Вып. X. Ч. 1 и 2. 300 с.
Космынин А.С., Трунин А.С. Проекционно-термографический метод исследования гетерогенных равновесий в конденсированных многокомпонентных системах. Самара: Самарский гос. техн. ун-т, 2006. 183 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии