Журнал неорганической химии, 2023, T. 68, № 4, стр. 444-451
Термическая стабильность нанокристаллического сульфида цинка ZnS
С. И. Садовников a, *, С. В. Сергеева b
a Институт химии твердого тела УрО РАН
620990 Екатеринбург, ул. Первомайская, 91, Россия
b Институт металлургии УрО РАН
620016 Екатеринбург, ул. Амундсена, 101, Россия
* E-mail: sadovnikov@ihim.uran.ru
Поступила в редакцию 08.11.2022
После доработки 10.01.2023
Принята к публикации 11.01.2023
- EDN: FMNDHO
- DOI: 10.31857/S0044457X22601936
Аннотация
Нанокристаллические порошки сульфида цинка (ZnS) синтезированы химическим осаждением из водных растворов нитрата цинка и сульфида натрия в присутствии цитрата натрия или Трилона Б. Изменение концентрации реагентов в реакционных смесях позволило получить нанопорошки ZnS со средним размером частиц от 2 до 9 нм. Показано, что отжиг нанопорошков ZnS на воздухе при температуре от 280 до 530°C приводит к окислению кубического сульфида цинка до гексагонального оксида цинка. Установлено, что окисление наиболее мелких нанопорошков сульфида цинка с размером частиц 2 нм начинается при 280–330°C, а наиболее крупного нанопорошка с размером частиц 9 нм – при температуре 530°C. Выявлено, что размер частиц наиболее крупного синтезированного порошка ZnS при повышении температуры до 530°C увеличивается всего лишь с 9 до 12 нм, тогда как размер частиц наиболее мелких нанопорошков при таком же повышении температуры растет с 2 до 9 нм.
ВВЕДЕНИЕ
Низкотемпературная кубическая (пр. гр. $F\bar {4}3m$) модификация α-ZnS имеет кубическую структуру сфалерита ZnS (тип В3) и стабильна при температуре ниже 1290 K. При температуре 1293 K низкотемпературный кубический сульфид цинка переходит в высокотемпературную гексагональную (пр. гр. P63mc) модификацию β-ZnS со структурой вюрцита. В нормальных условиях крупнокристаллический (bulk) сульфид цинка является широкозонным полупроводником. Ширина запрещенной зоны Eg кубического α-ZnS составляет ~3.50–3.76 эВ, Eg гексагонального вюрцита β-ZnS составляет ~3.74–3.91 эВ [1–3]. Диаметр экситона в крупнокристаллическом (bulk) сульфиде цинка равен 4.8–5.2 нм [3]. Заметим также, что в наноразмерных частицах сульфида цинка возможна политипная структура, характерная для гексагонального вюрцита.
Сульфид цинка ZnS – один из наиболее применяемых полупроводниковых сульфидов [4, 5] наряду с сульфидами свинца, серебра, меди и кадмия. Сульфид цинка используется в усилителях и детекторах ультразвука, инфракрасных датчиках, лазерах, работающих в ближнем и среднем инфракрасном диапазонах. Особенно часто сульфид цинка применяется как люминофор при создании люминесцентных приборов, солнечных элементов, светодиодов и жидкокристаллических дисплеев [3–8]. Электронные свойства нанокристаллического сульфида цинка, как и свойства других сульфидных полупроводников, существенно отличаются от свойств крупнокристаллических аналогов [3]. Наночастицы сульфида цинка размером <10 нм синтезируют в жидких средах, включая микроэмульсии [9], в водных коллоидных растворах нитрата или сульфата цинка и сульфида натрия с применением 3-меркаптопропилтриметоксисилана как стабилизатора [10], в водных растворах нитрата цинка и сульфида натрия [11] с Трилоном Б (этилендиаминтетрауксусная кислота) в качестве стабилизатора.
Термическая стабильность размера наночастиц ZnS и их фазового состава имеет важное значение для возможного применения нанокристаллического ZnS. При нагреве нанокристаллического сульфида цинка может происходить окисление. Поэтому для расширенного применения нанокристаллического сульфида цинка нужно знать, насколько стабильны размер и фазовый состав наночастиц ZnS. В литературе такие сведения о нанокристаллическом сульфиде цинка ограничены. Поведение наночастиц ZnS рассмотрено в работе [12], где установлено, что при температуре 500°C сульфидные наночастицы полностью окисляются до оксида цинка. Влияние температуры на стабильность оптических свойств нанокомпозита PVA/ZnS рассмотрено в работе [13] и установлено, что повышение температуры отжига >300°C приводит к деградации оптических свойств указанного нанокомпозита. Поведение крупнокристаллического ZnS рассмотрено в работе [14], где установлено, что его окисление начинается при довольно высокой температуре (>610°C). В работах [15, 16] показано, что термическая стабильность нанокомпозита из наночастиц ZnS, внедренных в полимерную матрицу поливинилового спирта (ПВС), больше термической стабильности чистого ПВС.
В настоящей работе впервые изучено влияние температуры на стабильность состава наночастиц сульфида цинка, определено влияние размера наночастиц на температуру начала окисления. Изучена термическая стабильность размера наночастиц сульфида цинка с начальным размером от 2 до 9 нм, синтезированных с использованием реагентов, имеющих разную концентрацию. Выбор цитрата натрия в качестве стабилизатора связан с тем, что он является наиболее используемым и химически безвредным антиоксидантом, обеспечивающим образование единственной сульфидной фазы – в данном случае ZnS. Что касается Трилона Б, то он является универсальным комплексообразователем, способствующим получению наночастиц малого размера.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Нанокристаллические порошки сульфида цинка получали химическим осаждением из водных растворов нитрата цинка Zn(NO3)2 и сульфида натрия Na2S. В качестве комплексообразователя и стабилизатора применяли водные растворы цитрата натрия (Na3C6H5O7 ≡ Na3Cit) и динатриевой соли этилендиаминтетрауксусной кислоты (ЭДТА-H2Na2 ≡ Трилон Б). Подробно методика синтеза нанопорошков ZnS описана в работе [11].
Составы реакционных смесей приведены в табл. 1. Концентрация Zn(NO3)2 в реакционных смесях составляла 50 или 100 ммоль/л. Для равномерного распределения синтезируемых наночастиц водные растворы подвергали воздействию ультразвука с помощью ультразвукового гомогенизатора Bandelin SONOPULS HD 2070 в течение 30 мин. Синтез проводили при температуре 298–323 K, время выдержки наночастиц в реакционной смеси для образцов 1 и 2 составляло 2–3 мин, для образца 3 – 20 ч, для образца 4 – 70 ч.
Таблица 1.
Состав реакционных смесей, период решетки a и средний размер (D) частиц сульфида цинка в синтезированных нанопорошках ZnS
| № | Концентрация реагентов в реакционных смесях, ммоль/л | aB3, нм | D ± 0.5, нм (РФА) |
|||
|---|---|---|---|---|---|---|
| Zn(NO3)2 | Na2S | Na3Cit | EDTA-H2Na2 | |||
| 1* | 50 | 50 | – | – | 0.5357 | 2 |
| 2** | 100 | 100 | – | – | 0.5332 | 2.5 |
| 3* | 50 | 50 | 6.25 | – | 0.5333 | 3.5 |
| 4*** | 50 | 100 | – | 5 | 0.5395 | 9 |
Синтезированные порошки промывали методом декантации и сушили сублимационным методом в лиофильной сушилке Alpha 1-2 LDplus (Martin Christ) при температуре ледового конденсатора –55°С (218 K). Высушенные порошки нанокристаллического сульфида цинка хранили в вакуумном эксикаторе Vacuum Desiccator Sanplatec MB при остаточном давлении 13.3 Па (0.1 мм рт. ст.).
Микроструктуру, размер и элементный химический состав наночастиц ZnS в коллоидных растворах определяли методом просвечивающей электронной микроскопии (ПЭМ) на электронном микроскопе Jeol JEM-2010 с решеточным разрешением 140 пм (1.4 Å). Элементный химический состав наночастиц ZnS изучали на этом же микроскопе с использованием энергодисперсионного спектрометра Phoenix (EDAX) с Si(Li)-детектором с энергетическим разрешением 130 эВ. Для исследования коллоидные растворы наночастиц ZnS помещали на медную сетку с покрытием из коллодиевого клея. Предварительно на медную сетку наносили один или два слоя коллодиевого клея (спиртовой раствор коллоксилина). После высыхания клеевого покрытия образуется углеродсодержащая сетка с пустотами. Подробно методика ПЭМ-исследований описана в работе [17].
Для определения термической стабильности сульфида цинка навеску образца массой m помещали в муфельную печь, предварительно нагретую до требуемой температуры, выдерживали при этой температуре в атмосфере воздуха в течение 2 ч, а затем определяли величину изменения массы Δm в результате отжига.
Осажденные сульфидные порошки и те же порошки после их отжига на воздухе при разных температурах исследовали методом рентгеновской дифракции на дифрактометре Shimadzu XRD-7000 (подробно методика измерений описана в работе [18]). Окончательное уточнение структуры синтезированных сульфидных порошков проводили с помощью программного пакета X’Pert Plus [19]. Качественный и количественный фазовый состав порошков осадков оценивали с помощью программного пакета Match Version 1.10b [20].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Просвечивающая электронная микроскопия высокого разрешения (ПЭМВР) позволила оценить размер синтезированных наночастиц ZnS в реакционных смесях 1–4. На рис. 1 показаны ПЭМВР-изображения агломерированных наночастиц ZnS, полученных в реакционных смесях 1 и 3 со средним размером наночастиц от ~2 до ~4 нм соответственно. Области, выделенные на ПЭМВР-изображениях, соответствуют кубическому (пр. гр. $F\bar {4}3m$) сульфиду цинка со структурой сфалерита (α-ZnS).
Рис. 1.
ПЭМВР-изображения агломерированных нанокристаллических частиц ZnS, полученных из реакционных смесей 1 (a) и 3 (б). Выделенные области соответствуют кубическому (пр. гр. $F\bar {4}3m$) сульфиду цинка со структурой сфалерита α-ZnS, наблюдаемые межплоскостные расстояния ~0.310–0.311 нм совпадают с расстоянием между атомными плоскостями (111) кубического (пр. гр. $F\bar {4}3m$) сульфида цинка α-ZnS. Выделенные области показаны в увеличенном масштабе слева в нижних частях рисунков а, б.

Согласно результатам энергодисперсионного рентгеновского анализа, после промывки в дистиллированной воде и вакуумной сушки содержание цинка и серы в высушенных порошках сульфида цинка со средним размером частиц ~2 нм составляет 67.0 ± 0.3 мас. % Zn и 32.8 ± ± 0.3 мас. % S, со средним размером частиц ~9 нм – 67.1 ± 0.3 мас. % Zn и 32.7 ± 0.2 мас. % S, что соответствует стехиометрическому сульфиду ZnS.
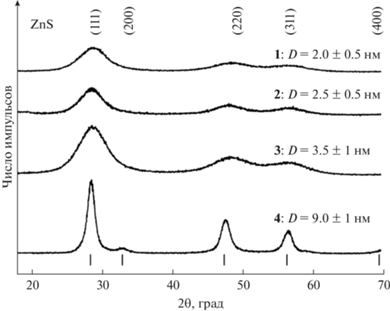
Типичные рентгенограммы синтезированных порошков сульфида цинка, осажденных из реакционных смесей 1–4 (табл. 1), показаны на рис. 2. Дифракционные отражения всех нанопорошков значительно уширены вследствие малого размера частиц ZnS. Pазмер D частиц нанопорошков ZnS, определенный по уширению дифракционных отражений, составляет от 2 до 9 нм (табл. 1). Проведенный количественный анализ и сравнение с данными [21, 22] показали, что наблюдаемый набор дифракционных отражений соответствует однофазному сульфиду цинка с кубической (пр. гр. $F\bar {4}3m$) структурой типа сфалерита. Период кристаллической решетки aB3 синтезированных нанопорошков ZnS равен ~0.5332–0.5395 нм.
Влияние температуры отжига, приводящей к изменению состава и структуры продуктов, сказывается на изменении рентгенограмм нанопорошков сульфида цинка. Как пример, на рис. 3 и 4 показано изменение рентгенограмм нанопорошков 1 и 4 сульфида цинка с наиболее мелкими и наиболее крупными наночастицами.
Рис. 3.
Изменение рентгенограмм нанокристаллического порошка 1 сульфида цинка с начальным размером наночастиц ~2 нм при увеличении температуры отжига от 180 до 530°C. Длинные черные и короткие красные штрихи показывают положения отражений кубического (пр. гр. $F\bar {4}3m$) сульфида цинка ZnS и гексагонального (пр. гр. P63mc) оксида цинка соответственно.
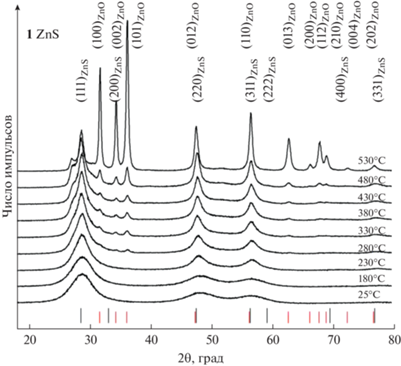
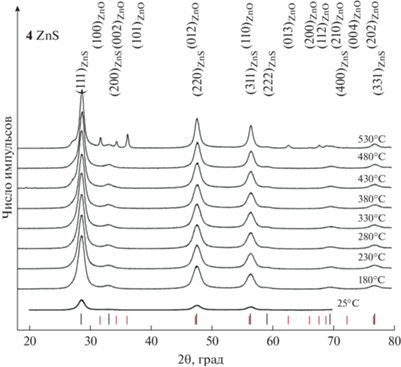
Рис. 4.
Изменение рентгенограмм нанокристаллического порошка 4 сульфида цинка с начальным размером наночастиц ~9 нм при увеличении температуры отжига от 180 до 530°C. Длинные черные и короткие красные штрихи показывают положения дифракционных отражений кубического (пр. гр. $F\bar {4}3m$) сульфида цинка ZnS и гексагонального (пр. гр. P63mc) оксида цинка соответственно.
Изменение рентгенограмм нанопорошка 1 сульфида цинка с начальным размером частиц ~2 нм при отжиге на воздухе в интервале температур от 180 до 530°C представлено на рис. 3. Размер частиц сохраняется практически неизменным при отжиге вплоть до температуры 180°C. При повышении температуры отжига до 230 и 330°C размер частиц сульфида цинка увеличивается до 3 и 5 нм соответственно. Проведенный количественный анализ и сравнение с данными [21–23] показали, что окисление нанопорошка сульфида цинка с образованием гексагонального (пр. гр. P63mc) оксида ZnO начинается при температуре отжига 280°C, когда на рентгенограмме появляются слабые дифракционные отражения (002)ZnO и (101)ZnO (рис. 3). При повышении температуры отжига >280°C количество дифракционных отражений оксида цинка и их интенсивность растут. При температуре отжига 480°C содержание оксидной фазы ZnO и размер частиц оксидной и сульфатной фаз немного увеличиваются. При температуре отжига 530°C содержание оксидной фазы достигает 21 мас. %, а размеры частиц ZnS и ZnO составляют ~10 и ~20 нм соответственно. При 530°C содержание оксидной фазы увеличивается до 30 мас. %, а размеры частиц ZnS и ZnO составляют ~20 и ~30 нм соответственно. Заметим, что на рентгенограммах нанопорошка 1, зарегистрированных после отжига при 480 и 530°C, слева от линии (111)ZnS в области углов 2θ = 27.1° присутствует линия, которую можно идентифицировать как отражение ${{\left( {100} \right)}_{{{\text{ZnS2H}}}}}$ гексагонального вюрцита ZnS со структурой 2H [24], хотя в нормальных условиях вюрцит существует при температуре >1020°C. Это может быть следствием формирования политипной структуры в наноразмерном сульфиде цинка.
Изменение рентгенограмм нанопорошка 4 сульфида цинка с начальным размером частиц ~9 нм в результате отжига на воздухе при температуре до 530°C показано на рис. 4. Размер наночастиц сохраняется практически без изменений при отжиге вплоть до температуры 380°C. При температуре отжига 430°C размер частиц увеличивается до ~10 нм. Окисление нанопорошка 4 с образованием оксида цинка начинается только при 530°C. При этой температуре отжига размер частиц ZnS увеличивается до ~12 нм, а размер частиц ZnO при 530°C составляет ~27 нм. Содержание ZnO в нанопорошке 4 при 530°C составляет 13 мас. %.
Рентгенограммы нанопорошков 2 и 3 сульфида цинка с начальным размером частиц ~2.5 и ~3.5 нм, отожженных на воздухе при температуре до 480 и 530°C соответственно, занимают промежуточное положение между рентгенограммами нанопорошков 1 и 4. Особенностью нанопорошка 2 является почти постоянный размер частиц вплоть до отжига при 430°C, тогда как в нанопорошке 3 увеличение размера частиц начинается при 280°C. Окисление нанопорошков 2 и 3 с образованием ZnO начинается при 330–380°C. Размер частиц ZnS в нанопорошке 3 при 530°C составляет ~12 нм, а размер частиц ZnO равен ~25 нм. Содержание ZnO в нанопорошке 3 при 530°C составляет 22 мас. %.
Полученные результаты показывают, что при отжиге на воздухе окисление наиболее мелких нанопорошков 1 и 2 сульфида цинка начинается при меньшей температуре (дифракционные отражения оксида цинка ZnO в образце 1 с размером частиц ~2 нм появляются уже при температуре отжига 280°C, в образце 3 с размером частиц ~3.5 нм окисление начинается при температуре отжига 330°C). Таким образом, окисление наиболее мелких нанопорошков сульфида цинка начинается при 280–330°C, а наиболее крупного нанопорошка – только при 530°C. Размер частиц наиболее крупного синтезированного порошка ZnS при повышении температуры до 530°C увеличивается всего лишь с 9 до 12 нм (на ~30%), тогда как размер частиц наиболее мелких нанопорошков при таком же повышении температуры возрастает с 2 до 9 нм, т.е. почти в 5 раз.
Настоящая работа посвящена термической стабильности наночастиц ZnS. Анализ влияния соотношения реагентов в реакционной смеси на размер наночастиц ZnS представлен в работе [11] и работах по термической стабильности и окислению сульфида свинца [25, 26].
Во всех случаях отжиг порошкообразных образцов ZnS приводит к потере массы Δm, увеличивающейся c ростом температуры отжига (рис. 5). Часть потери массы связана с окислением некоторого количества ZnS до ZnO, имеющего меньшую молекулярную массу по сравнению с ZnS. По данным рентгенофазового анализа, содержание ZnO в образцах 1, 3 и 4 после отжига при 530°C составляет 30, 22 и 13 мас. %, что соответствует убыли массы этих образцов вследствие окисления на ~5.0, ~3.6 и ~2.1 мас. %. По-видимому, остальная наблюдаемая потеря массы обусловлена в основном испарением влаги, адсорбированной нанопорошками из воздуха.
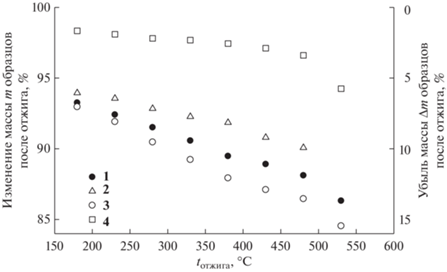
Рис. 5.
Изменение массы нанопорошков ZnS после отжига на воздухе при 180–530°C. Нумерация нанопорошков соответствует приведенной в табл. 1.
Действительно, нанопорошки очень гигроскопичны, причем их относительная влажность тем больше, чем меньше размер частиц [27, 28]. Согласно [29–31], адсорбция водяного пара из воздуха нанопорошками GaN, PbS и CdS увеличивается с уменьшением размера их частиц и ростом относительной влажности воздуха.
С учетом оценки потери массы нанопорошков при окислении ZnS до ZnO и литературных данных [29–31] по влажности и гигроскопичности сульфидных и нитридных порошков можно полагать, что потеря массы порошков сульфида цинка 1–4 связана с их относительной влажностью, составляющей от ~9–10 до ~3–4%. Судя по изменению массы, наиболее мелкие нанопорошки 1–3 с размером частиц 2.0–3.5 нм содержат больше адсорбированной влаги, тогда как в наиболее крупном нанопорошке 4 с размером частиц ~9 нм содержание адсорбированной из воздуха воды минимально. Небольшая потеря массы нанопорошков ZnS обусловлена также частичным окислением серы и удалением ее в виде газоообразного SO2, как установлено ранее при окислении нанопорошка сульфида серебра [32].
ЗАКЛЮЧЕНИЕ
Методом гидрохимического осаждения из водных растворов нитрата цинка и сульфида натрия в присутствии цитрата натрия или Трилона Б синтезированы нанокристаллические порошки кубического сульфида цинка ZnS со средним размером частиц от 2 до 9 нм. Наиболее мелкие нанопорошки ZnS с размером частиц 2–3 нм получены при синтезе из растворов нитрата цинка и сульфида натрия без комплексообразователя и стабилизатора при минимальной продолжительности осаждения 2–3 мин. Впервые изучена термическая стабильность фазового состава и размера частиц нанопорошков сульфида цинка. Отжиг нанопорошков ZnS на воздухе при температуре от 280 до 530°C приводит к изменению их фазового состава вследствие окисления кубического сульфида цинка до гексагонального оксида цинка. Окисление наиболее мелких нанопорошков сульфида цинка начинается при температуре 280–330°C, и содержание оксида цинка в этих нанопорошках при температуре отжига 530°C достигает ~30 мас. %. Наиболее крупный нанопорошок ZnS с начальным размером частиц 9 нм начинает окисляться только при 530°C. Уменьшение размера частиц ZnS до наноразмерного масштаба снижает температуру начала окисления на ~250–300°C по сравнению с крупнокристаллическим порошком сульфида цинка, начинающим окисляться при температуре ~610°C [14, 33]. В отличие от крупнокристаллических порошков ZnS, размер частиц которых при нагреве на воздухе до 600–700°C практически не меняется, размер наночастиц ZnS при нагреве до одинаковой температуры увеличивается тем больше, чем меньше исходный размер наночастиц. Различия в термическом поведении нано- и крупнокристаллических порошков ZnS на воздухе обусловлены в основном высокоразвитой поверхностью нанопорошков.
Список литературы
Kaur N., Kaur S., Singh J. et al. // J. Bioelectron. Nanotechnol. 2016. V. 1. № 1. P. 5. https://doi.org/10.13188/2475-224X.1000006
Cardona M., Harbeke G. // Phys. Rev. 1965. V. 137. № 5A. P. A1467. https://doi.org/10.1103/PhysReV.137.A1467
Sadovnikov S.I., Rempel A.A., Gusev A.I. // Russ. Chem. Rev. 2018. V. 87. № 4. P. 303. https://doi.org/10.1070/RCR4803
Fang X., Zhai T., Gautam U.K. et al. // Prog. Mater. Sci. 2011. V. 56. № 2. P. 175. https://doi.org/10.1016/j.pmatsci.2010.10.001
Wang X., Huang H., Liang B. et al. // Crit. Rev. Solid State Mater. Sci. 2013. V. 38. № 1. P. 57. https://doi.org/10.1080/10408436.2012.736887
Kryshtab T., Khomchenko V.S., Andraca-Adame J.A. et al. // J. Lumin. 2009. V. 129. № 12. P. 1677. https://doi.org/j.jlumin.2009.04.069
Ma X., Song J., Yu Z. // Thin Solid Films. 2011. V. 519. № 15. P. 5043. https://doi.org/10.1016/j.tsf.2011.01.125
Ummartyotin S., Infahsaeng Y. // Renewable Sustainable Energy Rev. 2016. V. 55. P. 17. https://doi.org/10.1016/j.rser.2015.10.120
Koroleva M.Yu., Gulyaeva E.V., Yurtov E.V. // Russ. J. Inorg. Chem. 2012. V. 57. № 3. P. 320. https://doi.org/10.1134/S0036023612030151
Kuznetsova Yu.V., Popov I.D., Rempel A.A. // AIP Conf. Proc. 2020. V. 2313. P. 030021. https://doi.org/10.1063/5.0032224
Sadovnikov S.I., Ishchenko A.V., Weinstein I.A. // J. Alloys Compd. 2020. V. 851. P. 154846. https://doi.org/10.1016/j.jallcom.2020.154846
Shanmugam N., Shanmugam C., Kannadasan N. et al. // J. Nanomater. 2013. P. 351798. https://doi.org/10.1155/2013/351798
Mohamed M.B., Abdel-Kader M.H. // Mater. Chem. Phys. 2020. V. 241. P. 122285. https://doi.org/10.1016/j.matchemphys.2019.122285
Queiroz C.A.R., Carvalho R.J., Moura F.J. // Brazil. J. Chem. Eng. 2005. V. 22. № 1. P. 127. https://doi.org/10.1590/S0104-66322005000100012
Osuntokun J., Ajibade P.A. // J. Nanomater. 2016. V. 2016. P. 3296071. https://doi.org/10.1155/2016/3296071
Osuntokun J., Ajibade P.A. // Physica B: Cond. Matter. 2016. V. 496. P. 106. https://doi.org/10.1016/j.physb.2016.05.024
Sadovnikov S.I., Gerasimov E.Yu. // Nanoscale Advances. 2019. V. 1. № 4. P. 1581. https://doi.org/10.1039/c8na00347e
Sadovnikov S.I. // Russ. J. Inorg. Chem. 2019. V. 64. № 10. P. 1309. https://doi.org/10.1134/S0036023619100115
X’Pert HighScore Plus. Version 2.2e (2.2.5). © 2009 PANalytical B. V. Almedo, the Netherlands.
Match! Version 1.10b. Phase Identification from Powder Diffraction © 2003-2010 Crystal Impact.
Van Aswegen J.T.S., Verleger H. // Die Naturwissenschafien. 1960. V. 47. № 6. P. 131. https://doi.org/10.1007/BF00628510
JCPDS card № 005-0566.
Xu Y.N., Ching W.Y. // Phys. Rev. B. 1993. V. 48. № 7. P. 4335. https://doi.org/10.1103/PhysRevB.48.4335
Ballentyne D.W.G., Roy B. // Physica. 1961. V. 27. № 3. P. 337. https://doi.org/10.1016/0031-8914(61)90106-9
Sadovnikov S.I., Kozhevnikova N.S., Rempel A.A. // Inorg. Mater. 2011. V. 47. № 8. P. 837. https://doi.org/10.1134/S0020168511080176
Sadovnikov S.I., Kozhevnikova N.S., Rempel A.A. // Russ. J. Inorg. Chem. 2011. V. 56. № 12. P. 1864. https://doi.org/10.1134/S0036023611120448
Kim S., Merkle R., Maier J. // Solid State Ionics. 2003. V. 161. № 1-2. P. 113. https://doi.org/10.1016/S0167-2738(03)00262-5
Szałaj U., Świderska Ś.A., Chodara A. et al. // Nanomaterials. 2019. V. 9. № 7. P. 1005.
Drygas M., Janik J.F., Czepirski L. // Curr. Nanosci. 2013. V. 9. № 3. P. 318. https://doi.org/10.2174/1573413711309030004
Sadovnikov S.I., Gusev A.I. // J. Alloys Compd. 2014. V. 586. P. 105. https://doi.org/10.1016/j.jallcom.2013.10.008
Bhattacharjee M., Bandyopadhyay D. // Sens. Actuators, A.: Phys. 2019. V. 285. P. 241. https://doi.org/10.1016/j.sna.2018.11.034
Sadovnikov S.I., Gusev A.I. // J. Therm. Anal. Calorim. 2018. V. 131. № 2. P. 1155. https://doi.org/10.1007/s10973-017-6691-8
Орлов А.К. // Записки Горного института. 2006. Т. 169. С. 163.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии