Журнал общей биологии, 2020, T. 81, № 4, стр. 311-320
Гипотезы и постулаты модели эволюции глобального углеродного цикла
А. А. Ивлев *
Российский государственный аграрный университет им. К.А. Тимирязева
127750 Москва, Тимирязевская ул., 49, Россия
* E-mail: aa.ivlev@list.ru
Поступила в редакцию 06.03.2020
После доработки 06.04.2020
Принята к публикации 17.04.2020
Аннотация
Ключевое представление модели глобального углеродного цикла состоит в том, что круговорот углерода сводится к переходу окисленного углерода природной углекислотно-карбонатной системы в восстановленное состояние при фотосинтезе и обратному переходу восстановленного углерода в окисленную форму при окислении осадочного органического вещества в реакции термохимической сульфатредукции. Первый переход обеспечивается энергией солнца, обратный – энергией столкновений двигающихся литосферных плит. Движение самих плит, согласно постулату, контролируется гравитационным взаимодействием Земли с другими небесными телами Солнечной системы, которое вызывает конвективные колебания магмы. В результате литосферные плиты двигаются неравномерно и появляются орогенические циклы, состоящие из короткого орогенного периода и длительного геосинклинального периода. В короткий орогенный период СО2, образующийся при окислении органического вещества, поднимается на поверхность Земли, заполняя атмосферу и гидросферу и инициируя фотосинтез. Фотосинтез развивается в геосинклинальном периоде, вследствие чего содержание СО2 падает, а кислорода увеличивается. На Земле наступает похолодание, заканчивающееся оледенением. Фотосинтез порождает на Земле климатические изменения и биотический круговорот. Благодаря участию в глобальном цикле углерода глобального фотосинтеза, проявляющегося в виде интегрированной функции ассимиляции и фотодыхания всех существовавших и существующих на Земле фотосинтезирующих организмов, включая тех, чья биомасса использовалась в пищевых цепочках, и усиливающейся оксигенации среды, происходила эволюция глобального цикла углерода и его самопроизвольное движение к экологической точке компенсации. В этой точке система глобального углеродного цикла перешла в стационарное состояние. Оно характеризуется тем, что ключевые параметры системы: содержание углекислого газа и кислорода в атмосфере и гидросфере, содержание осадочного органического вещества в земной коре, колебания уровня моря и другие связанные с ними параметры – начинают осциллировать около некоторых средних значений. Взаимообусловленность и взаимосвязанность параметров системы глобального углеродного цикла в условиях стационарности системы требуют непрерывного контроля за колебаниями многочисленных жизненно важных параметров, чтобы они не выходили за допустимые пределы, отвечающие приемлемым условиям обитания человека.
Разработанная ранее модель глобального углеродного цикла представляет собой цепь взаимообусловленных событий на планете Земля, связанных во времени и пространстве с превращениями углеродных форм (Ivlev, 2015). Использование гипотез и постулатов при создании мультифакторной модели часто становится неизбежным, поскольку не все ее аспекты оказываются в равной степени изученными и их можно аргументированно интерпретировать. При этом их использование должно быть оправдано и не должно противоречить существующим фактам и знаниям. Принимая во внимание вышесказанное, рассмотрим гипотезы и постулаты упомянутой модели.
ПОСТУЛАТ К ГЕОЛОГИЧЕСКОЙ ЧАСТИ МОДЕЛИ. ПОЧЕМУ ДВИГАЮТСЯ ЛИТОСФЕРНЫЕ ПЛИТЫ?
В настоящее время сам факт движения литосферных плит, составляющих твердую оболочку Земли, доказан экспериментально (Флинт, 1978) и лежит в основе известной геологической концепции – теории мобилизма. Причем столкновения двигающихся плит, как показано ниже, являются одним из центральных положений модели глобального цикла углерода.
Движение литосферных плит напоминает движение эскалатора. Плиты, рождаясь из мантии в зоне срединно-океанического желоба, двигаются навстречу друг другу и сталкиваются в зоне субдукции, находящейся вдоль континентальных окраин и островных дуг. Там одна из плит надвигается на другую, и нижняя плита поглощается магмой. Таким образом, зона субдукции (зона столкновения плит) является зоной сейсмической активности, зоной землетрясений, активной вулканической деятельности и горообразования. Считается, что литосферные плиты двигаются по поверхности расплавленной жидкой магмы (Jacoby, 1978; Harland et al., 1990; Fowler, 2005; Riguzzi et al., 2009).
В этом постулате остается неясным вопрос – что заставляет плиты двигаться? Обоснованным ответом на этот вопрос представляется утверждение, что плиты двигаются благодаря конвективному движению жидкой магмы (температура около 5000°С). При этом конвекция магмы находится под гравитационным воздействием небесных тел на движение Земли по околосолнечной орбите. Это воздействие проявляется в неравномерном движении литосферных плит, состоящем из короткопериодического и относительно быстрого движения, во время которого в зоне субдукции происходят частые их столкновения и выделяется большое количество энергии, а также из относительно длительного и медленного движения, при котором столкновения редки, а выделяемое количество энергии значительно меньше. Короткопериодическая фаза названа орогенным периодом, а длиннопериодическая – геосинклинальным (Руттен, 1978). Оба периода составляют орогенический цикл.
ГИПОТЕЗА ОБ ИСТОЧНИКЕ СО2, ЗАПОЛНЯЮЩЕГО СИСТЕМУ “АТМОСФЕРА–ГИДРОСФЕРА” ЗЕМЛИ В ОРОГЕННЫЙ ПЕРИОД ОРОГЕНИЧЕСКОГО ЦИКЛА
Гипотеза связана с геохимической частью модели, в которой глобальный цикл углерода представлен как петля, состоящая из окислительной и восстановительной ветвей (рис. 1). Принимается, что в круговороте углерода участвует та его часть, которая проходит через фотосинтез, а синтезируемая биомасса превращается в осадочное органическое вещество пород. Одним из участников круговорота является неорганический углерод в окисленной лабильной форме (СО2–${\text{HCO}}_{3}^{ - }$–${\text{CO}}_{3}^{ = }$). При этом между разными химическими формами углекислотно-карбонатной системы происходит химический и изотопный обмен (Ивлев, 2015). Карбонатные толщи из обмена и круговорота исключаются. Этот углерод мы называем биосферным.
Рис. 1.
Формальная схема глобального цикла углерода в виде петли. Петля имеет окислительную и восстановительную ветвь. Точка 1 соответствует фотосинтезу, т.е. переходу окисленного состояния к восстановленному; точка 2 соответствует окислению осадочного органического вещества в реакции термохимической сульфатредукции, т.е. переходу из восстановленного состояния в окисленную форму (Ivlev, 2015).
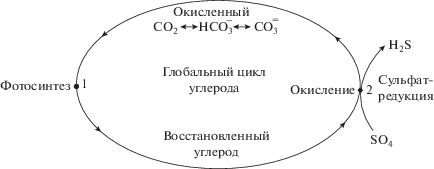
На рис. 1 точка 1 соответствует переходу из окисленного состояния углерода в восстановленное посредством фотосинтеза, точка 2 соответствует обратному переходу. Если роль и механизм фотосинтеза в точке 1 хорошо изучены, то вопрос об источнике СО2, поступающего в атмосферу и гидросферу при обратном переходе, в точке 2, и его механизм остается невыясненным. Согласно модели, переход осуществляется при окислении осадочного органического вещества в разных его формах в реакции термохимической сульфатредукции. Источником сульфатов при этом является морская вода.
Существует альтернативная точка зрения, согласно которой источником окисленного углерода в атмосфере и гидросфере является ювенильный (глубинный) СО2 (Ронов, 1976), образовавшийся из углерода тел метеоритов при образовании Земли (Галимов, 1968).
Для обоснования источника СО2, в соответствии с предложенной нами моделью, подчеркнем три принятых утверждения: 1) энергия, необходимая для протекания термохимической сульфатредукции, в которой окисляется осадочное органическое вещество, выделяется при столкновении литосферных плит в зоне субдукции; 2) в основном выделение этой энергии происходит в орогенный период циклов, поскольку именно в этот период столкновения плит происходят гораздо чаще, чем в геосинклинальный; 3) поступление СО2 в атмосферу и гидросферу связано со столкновениями, в которых одна из плит является континентальной, поскольку на ней накапливается осадочное органическое вещество.
В пользу участия термохимической сульфатредукции в образовании СО2, поступающего в атмосферу, свидетельствуют данные, полученные Маккензи и Пиготтом (Mackenzie, Pigott, 1981). Авторы изучили распространенность ряда минералов (карбонатов, гипса, пирита) и органического вещества за геологическое время, охватывающее протерозой (700 млн лет назад) и большую часть фанерозоя. Нетрудно заметить, что эти минералы потенциально являются участниками реакции сульфатредукции:
Было обнаружено, что максимумы распространенности гипса и органического вещества, которые можно отнести к субстратам реакции, соответствуют минимумам распространенности пиритов и карбонатов и наоборот. Такое распределение можно связать с периодически протекающей реакцией сульфатредукции.
Действительно, можно ожидать, что в орогенный период, когда идет интенсивное окисление органического вещества, распространенность продукта реакции, пиритов, возрастает и одновременно возрастает распространенность карбонатов, которые образуются с участием выделяющегося СО2 (рис. 2). Увеличение распространенности сульфатов можно объяснить низкой интенсивностью сульфатредукции, которая имеет место в относительно тектонически спокойном геосинклинальном периоде цикла. При этом параллельно возрастает содержание органического вещества в породах.
Рис. 2.
Синхронные изменения изотопного состава углерода морских карбонатов (а) и изотопного состава серы морских сульфатов (б) в протерозое и фанерозое (по: Mackenzie, Pigott, 1981).
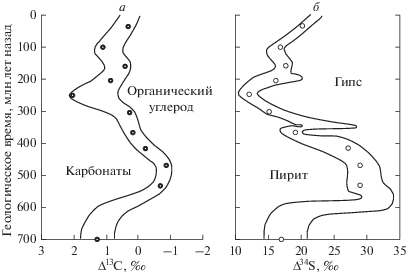
На обоснованность такого объяснения указывают результаты изучения изотопного состава углерода морских карбонатов и серы морских сульфатов (гипса) за тот же интервал времени (рис. 2). Прежде чем интерпретировать кривую, описывающую изменения изотопного состава серы, необходимо отметить, что фракционирование изотопов серы в термохимической редукции сульфатов экспериментально установлено (Nakai, Jensen, 1960; Thode et al., 1961). Кроме того, обнаружено накопление тяжелого изотопа 34S в остаточном сульфате, что свидетельствует о том, что реакция протекает с исчерпыванием, т.е. периодически. Чем больше будет исчерпывание, тем “тяжелее” будет становиться изотопный состав серы остаточного сульфата (эффект Рэлея). С точки зрения рассматриваемой модели, обогащение серы сульфатов изотопом 34S происходит в орогенный период во время интенсивной сульфатредукции. В геосинклинальный период, когда интенсивность реакции ослабевает, сера сульфатов становится обогащенной 32S относительно серы орогенного периода (рис. 2).
Почему параллельно и синхронно с изотопным составом серы меняется изотопный состав карбонатов? Ответить на этот вопрос можно следующим образом. Изотопный состав углерода морских карбонатов меняется (рис. 2), но не по причине изотопного фракционирования, сопровождающего окисление органического углерода, а из-за того, что при полном окислении органического вещества в зоне субдукции образующийся СО2 наследует изотопный состав последнего, который, как известно, значительно обогащен 12С (< –20‰) по сравнению с карбонатами морской воды (от 0 до –5‰) (Дегенс, 1974). Поэтому в орогенный период атмосфера и гидросфера Земли заполняется СО2 с относительно легким изотопным составом (Ивлев, 2015). Поступая в среду и смешиваясь с имеющимися формами неорганического углерода, он приводит к “облегчению” всего неорганического углерода. Очевидно, в геосинклинальный период изотопное смещение имеет противоположный знак.
Таким образом, синхронность изменений изотопных кривых серы и углерода морских сульфатов и карбонатов совместно с распространенностью соответствующих минералов и содержания осадочного органического углерода в породах позволяют утверждать, что источником СО2, заполняющего атмосферу и гидросферу в орогенный период, является окисление осадочного углерода в реакции термохимической сульфатредукции (Ивлев, 2019б).
В пользу обоснования связи СО2, поступающего в атмосферу и гидросферу Земли при окислении органического вещества, косвенно говорит и тот факт, что СО2, поступающий из коры в атмосферу в периоды повышенной тектонической активности, обогащен изотопом 12С (Popp et al., 1989; Derry et al., 1992; Young, 2015; Corso et al., 2018). Причиной обогащенности углерода органического вещества легким изотопом 12С относительно неорганического углерода (Дегенс, 1974) является хорошо известный изотопный эффект фотосинтеза, который обогащает биомассу, а значит и органическое вещество, изотопом 12С относительно углерода окисленных форм.
Для понимания того, как функционирует рассматриваемая модель углеродного цикла, необходимо подчеркнуть следующее. Благодаря краткости орогенного периода по сравнению с геосинклинальным, можно считать, что в орогенный период СО2 импульсно заполняет систему “атмосфера–гидросфера”, а в последующий длительный геосинклинальный период происходит постепенное исчерпание поступившего СО2 на биосинтез с последующим преобразованием “живого” вещества в осадочный органический углерод. Такая последовательность заполнения и последующего использования углекислого газа в системе “атмосфера–гидросфера” обусловливает появление изотопного эффекта исчерпывания (эффекта Рэлея), проявляющегося в постепенном обогащении углерода осадочного органического вещества от начала к концу геосинклинального периода изотопом 13С.
ПОСЛЕДОВАТЕЛЬНОСТЬ ИЗМЕНЕНИЯ КЛИМАТИЧЕСКИХ УСЛОВИЙ И БИОТИЧЕСКИЙ КРУГОВОРОТ В ОРОГЕНИЧЕСКОМ ЦИКЛЕ ЕСТЬ РЕЗУЛЬТАТ НЕРАВНОМЕРНОГО ДВИЖЕНИЯ ЛИТОСФЕРНЫХ ПЛИТ
Как было сказано, неравномерность движения литосферных плит обусловливает появление орогенических циклов, состоящих из орогенного и геосинклинального периодов. В орогенный период орогенического цикла атмосфера и гидросфера Земли заполняются углекислым газом. Поскольку СО2 является парниковым газом, поверхностная температура Земли повышается, создавая парниковый эффект. Одновременно высокие концентрации СО2 инициируют фотосинтез.
Параллельно с повышением содержания СО2 происходит падение концентрации атмосферного кислорода, накопленного благодаря фотосинтезу в предшествующий орогенический цикл. Концентрация О2 снижается, поскольку в орогенный период вместе с вулканическими эксгаляциями на поверхность Земли поступают большие массы восстановленных изверженных пород, которые используют кислород на окисление.
В последующий длительный тектонически спокойный геосинклинальный период доминирующим становится развитие фотосинтеза, чему способствуют и высокие концентрации СО2, достигнутые в орогенный период. Концентрация СО2 начинает снижаться, достигая минимума к концу геосинклинального периода. Концентрация кислорода меняется благодаря фотосинтезу противоположным образом. Она растет до максимальных значений к концу геосинклинального периода цикла.
Таким образом, из сказанного можно заключить, что начало орогенических циклов связано с интенсивным вулканизмом, магматизмом и горообразованием. На Земле возникают высокие температуры и анаэробная (или малокислородная) среда, которая характеризуется высоким отношением СО2/О2, однако к концу орогенического цикла условия меняются на противоположные. На Земле возникают низкие температуры и наступает оледенение. В атмосфере накапливается кислород. Отношение СО2/О2 становится минимальным.
Очевидно, что описанные изменения окружающей среды неизбежно должны были сказаться на эволюции биосферы. Это тем более вероятно, что орогенические циклы, особенно первые, охватывали огромные временные интервалы, порядка сотен миллионов лет (Руттен, 1978). Действительно, даже на более коротких циклах, называемых климатическими осцилляциями, охватывающих интервал от нескольких миллионов до сотен тысяч лет, исследователи установили связь видового состава организмов с условиями среды (Riding et al., 2013). Горикан с соавт. (Goričan et al., 2013), изучив распределение радиолярий, принадлежащих к 167 видам, относящихся к 69 родам и обладающих, в зависимости от условий, широким набором свойств, обнаружили смену видов и усиление их биоразнообразия при увеличении оксигенации среды. В каждом последующем цикле этот тренд воспроизводился. Проанализировав эволюцию биосферы в ходе геологического времени, Ивлев (Ivlev, 2019a) пришел к выводу, что по мере увеличения уровня оксигенации среды в сменяющих друг друга орогенических циклах, в орогенном периоде цикла при снижении концентрации кислорода и высокой концентрации СО2 видовой состав организмов смещался в сторону анаэробных и термофильных организмов. В геосинклинальном периоде циклов по мере развития фотосинтеза в атмосфере накапливался кислород, а температура снижалась. При этом видовой состав организмов смещался в сторону аэробных и холодостойких организмов. Отмечен и более высокий уровень их организации.
Наиболее драматические события в эволюции биосферы происходили при смене орогенических циклов. Это связано с резкой сменой условий среды – от аэробных и низкотемпературных условий конца геосинклинального периода к анаэробным и высокотемпературным условиям орогенного периода нового цикла. Этот переход сопровождался массовой гибелью организмов, которые не смогли адаптироваться к новым условиям. Палеонтологам известно пять больших вымираний, которые произошли в истории Земли, когда погибло до 75% существовавших видов организмов (Raup, Sepkosky, 1984; Alroy, 2008). И хотя причина, приводящая к вымираниям, во многих случаях остается невыясненной, большинство исследователей считают, что она связана с резкими изменениями условий среды, которые, как следует из модели, обусловлены сменой орогенических циклов. Повторяемость орогенических циклов и последовательность климатических и биотических событий обеспечили эволюцию и естественный отбор. Следуя этой логике, период больших массовых вымираний организмов должен соответствовать времени поступления в осадок больших масс органического вещества и времени образования толщ с богатым содержанием органического углерода (Ивлев, 2019а). Именно такие толщи стали впоследствии очагами генерации углеводородов, приведшей к образованию крупных нефтяных месторождений.
Постулируемые моделью повторяемость и периодичность климатических и биосферных событий подтверждаются многочисленными природными наблюдениями. К ним относятся свидетельства чередования следов “парникового” периода и оледенений, сопутствующие им колебания уровня моря, чередование признаков анаэробных и аэробных условий (Руттен, 1978; Флинт, 1978). Ларж с соавт. (Large et al., 2015) обнаружили длиннопериодические циклы, которым соответствовали значительные колебания содержания микроэлементов в морской воде, которые, как и орогенические циклы, начинались с активной вулканической деятельности, а заканчивались массовой гибелью организмов. Из этого можно сделать вывод, что содержание микроэлементов является одним из признаков орогенического цикла, в котором попадание микроэлементов в морскую воду происходило во время вулканических извержений. Затем концентрация микроэлементов снижалась благодаря потреблению организмами, обитающими в морской воде. Еще один аргумент в пользу существования орогенических циклов дает изучение изотопного состава углерода органического вещества. Хейс с коллегами (Hayes et al., 1989) исследовали большую коллекцию образцов органического вещества морского типа, охватывающую геологический интервал времени от неопротерозоя до конца фанерозоя, и обнаружили изотопное “утяжеление” органического вещества, приходящееся на периоды оледенения. Это и понятно, поскольку показано (Ивлев, 2015), что изотопное утяжеление связано с окончанием орогенических циклов. К этому моменту в атмосфере аккумулируется максимальное количество кислорода и соотношение СО2/О2 достигает минимума. При таком соотношении концентраций этих газов в синтез биомассы вклад фотодыхания, который сопровождается обогащением ее изотопом 13С, максимален. Поэтому органическое вещество в конце орогенического цикла оказывается обогащенным 13С.
Таким образом, наблюдаемая периодичность и повторяемость климатических и биосферных событий есть отражение постулата о существовании орогенических циклов и неравномерного движения плит. Но если рассмотреть этот постулат еще глубже, то периодичность и повторяемость климатических и биосферных процессов на Земле зависят от влияния других небесных тел на движение Земли вокруг Солнца, что обеспечивает саму неравномерность движения плит.
ПОСТУЛАТ ОБ ЭКОЛОГИЧЕСКОЙ ТОЧКЕ КОМПЕНСАЦИИ. ЭВОЛЮЦИЯ ГЛОБАЛЬНОГО ЦИКЛА УГЛЕРОДА
В рассматриваемой модели глобального цикла углерода фотосинтез является одним из основных его элементов. С фотосинтезом связано как функционирование цикла, так и его эволюция. При выяснении роли фотосинтеза в глобальном цикле углерода приходится опираться на постулат, смысл которого станет понятен после выяснения, что такое точка компенсации у индивидуального фотосинтезирующего организма.
Фотосинтез индивидуального организма включает два реципрокных процесса – ассимиляцию СО2 и фотодыхание. Это означает, что ослабление одного из них вызывает усиление другого (Andre, 2011a, b). Функционирование фотосинтеза зависит от содержания в среде углекислого газа и кислорода. Увеличение концентрации СО2 усиливает ассимиляционную функцию фотосинтеза, т.е. обеспечивает прирост биомассы. Увеличение концентрации О2 усиливает функцию фотодыхания, что снижает прирост биомассы. Может вызвать удивление, каким образом может происходить регуляция двух метаболических функций, если содержание одного газа в среде составляет 0.04%, а другого – 21%. На самом деле, регуляция определяется специфичностью фермента, которая зависит не от абсолютного содержания газов, а от их отношения. Эволюция определила то отношение этих газов, которое существует на сегодняшний день. Фермент рубиско (рибулозобисфосфат карбоксилаза/оксигеназа) обладает двойственной способностью карбоксилазы и оксигеназы, благодаря которой фотосинтезирующий организм по механизму обратной связи направляет ассимилируемый углеродный поток то на ассимиляцию, то на фотодыхание, придавая фотосинтезу осцилляционный характер (Ivlev et al., 2010). То концентрационное отношение СО2/О2, которое сегодня наблюдается у фотосинтезирующих организмов, позволяет им регулировать ассимиляцию и фотодыхание, обеспечивая фермент субстратами.
Фотосинтез в глобальном цикле углерода также имеет две функции – интегрированную функцию ассимиляции и интегрированную функцию фотодыхания, которые отражают интегральный эффект ассимиляции и фотодыхания у всех фотосинтезирующих организмов. Поэтому и фотосинтез, в отличие от фотосинтеза индивидуального организма, называется глобальным. Оба эти процесса реципрокные (Ivlev, 2016, 2020; Ивлев, 2019a).
Если считать, что количество захороненного органического вещества пропорционально количеству синтезированного “живого” вещества, то можно принять, что в те интервалы орогенических циклов, которым соответствует соотношение СО2/О2 > 1, т.е. когда превалирует ассимиляционная функция фотосинтеза, в земной коре накапливается органическое вещество, в те отрезки орогенических циклов, когда соотношение СО2/О2 < 1, аккумуляция органического вещества в коре снижается.
Очевидно, что соотношение СО2/О2 > 1 соответствует началу орогенических циклов, когда на Земле высокие температуры и анаэробная (мало кислородная) обстановка, в конце циклов СО2/О2 < 1, температура понижается и наступает оледенение. В этой связи представляют интерес оценки Толберта с соавт. (Tolbert et al., 1995), которые они сделали на основании экспериментов по газообмену у растений в закрытой камере. При содержании в камере концентрации СО2 0.022% концентрация кислорода в камере составила 23%, а при повышении концентрации СО2 до 0.035% концентрация кислорода составила 27–28%. Столь высокие концентрации кислорода соответствовали периодам оледенения, что дало основание Толберту с коллегами (Tolbert et al., 1995) и другим исследователям (Igamberdiev, Lea, 2006) говорить о том, что такие механизмы поддержания атмосферных концентраций СО2 и О2 существуют и в природе. Уместно подчеркнуть, что периодические изменения СО2/О2 и их связь с климатическими изменениями полностью соответствуют предсказаниям модели.
У каждого индивидуального фотосинтезирующего организма с ростом концентрации кислорода в среде усиливается фотодыхательная функция, что в итоге приводит к тому, что рост биомассы прекращается и остается только функция поддержания, т.е. фотодыхание полностью компенсирует рост биомассы за счет ассимиляции. Это состояние называется точкой компенсации.
В глобальном цикле углерода с каждым орогеническим циклом наступает новая ступень в оксигенации среды, т.е. средняя концентрация кислорода в новом орогеническом цикле оказывается выше, чем в предыдущем. Таким образом, разница между биомассой “живого” вещества, произведенной глобальным фотосинтезом в рассматриваемый момент геологического времени, и тем количеством восстановленного углерода, которое достигло зоны субдукции, составляет прирост осадочного органического вещества в земной коре на данный момент геологического времени. Из сказанного можно сделать вывод, что благодаря участию фотосинтеза в глобальном цикле углерода, цикл постепенно эволюционирует в сторону экологической точки компенсации. Эта эволюция происходит ступенчато, от одного орогенического цикла к другому, путем последовательного увеличения уровня оксигенации среды.
При достижении экологической точки компенсации глобальный цикл углерода переходит в стационарное состояние. Это значит, что все его характеристики начинают осциллировать около некоторых средних величин. Стационарным становится содержание осадочного органического вещества в земной коре и кислорода в атмосфере (оба – продукты глобального фотосинтеза), а также углекислого газа – субстрата глобального фотосинтеза. Мы полагаем, что достижение экологической точки компенсации произошло в миоцене, когда понижение уровня концентрации СО2 в среде привело к появлению растений с новым С4-типом ассимиляции (Cerling, 1991; Cerling et al., 1992, 1997). До этого момента колебания соотношения СО2/О2 в среде отражались на изменении соотношения вклада в биосинтез ассимиляционной и фотодыхательной функций. После достижения точки экологической компенсации колебания соотношения СО2/О2 в среде стали регулироваться изменением распространенности растений с С3- и С4-типом ассимиляции.
Представление об экологической точке компенсации позволяет по-новому взглянуть на глобальный фотосинтез с точки зрения его участия в накоплении органического вещества в земной коре и аккумуляции кислорода в атмосфере. Для этого надо представить глобальный фотосинтез как непрерывный процесс, усреднив для этого характеристики глобального фотосинтеза по орогеническим циклам. Рассмотрим, куда расходуется продукт фотосинтеза, восстановленный углерод. Сразу после образования восстановленный углерод тратится на дыхание (фотодыхание и темновое дыхание) всех организмов. После отмирания и захоронения организмов восстановленный углерод тратится на многочисленные аэробные и анаэробные окислительные процессы, сопровождающие преобразование органического вещества в осадке. На последнем завершающем этапе окисления восстановленный углерод попадает в зону субдукции, где подвергается окончательному окислению в реакции термохимической сульфатредукции. Таким образом, в восстановленном виде оказывается только углерод, который находится в земной коре на пути в зону субдукции. До момента достижения экологической точки компенсации происходило накопление осадочного органического углерода. Но с повышением концентрации кислорода наступило равенство образовавшегося при фотосинтезе восстановленного углерода и углерода, возвращаемого обратно в окисленное состояние.
Особый смысл приобретает утверждение о стационарности содержания органического вещества в земной коре. Как ясно из уравнения глобального фотосинтеза (Ivlev, 2020), в условиях стационарности содержания кислорода в атмосфере и осадочного органического вещества в земной коре оба продукта глобального фотосинтеза находятся в эквивалентных количествах. Следовательно, оценив содержание кислорода в атмосфере, можно определить количество осадочного органического вещества в земной коре (Ивлев, 2015). Следуя этой логике, можно посчитать запасы рассеянного органического вещества в коре, а через них и нефти, если принять, что определенный процент от органического вещества идет на ее образование. Для количественного расчета недостает ряда данных, из-за чего он пока невозможен. Однако существующих знаний уже достаточно, чтобы не только сказать, что нефть – это невозобновляемый ресурс, но и то, что при существующих темпах добычи нефти происходит исчерпание ее запасов, и следует уже думать, каким источником энергии ее можно заменить.
Необходимо также отметить, что стационарная система очень неустойчива и чувствительна к незначительным внешним воздействиям. Колебания жизненно важных параметров системы, приемлемых для обитания человека, таких как содержание в атмосфере кислорода и углекислого газа, поверхностная температура на Земле, колебания уровня моря, растительный покров и другие связанные с ними климатические параметры, не могут быть большими. Поэтому человечеству для выживания необходимо поддерживать стационарность системы в заданных пределах, а для этого требуется постоянный мониторинг всех параметров системы с учетом их взаимосвязанности и взаимообусловленности.
ЗАКЛЮЧЕНИЕ
Рассмотрены постулаты и гипотезы, на которых построена новая модель глобального цикла (круговорота) биосферного углерода. Этот круговорот рассматривает переход от окисленного углерода природной углекислотно-карбонатной системы (СО2–${\text{HCO}}_{3}^{ - }$–${\text{CO}}_{3}^{ = }$) в восстановленную форму путем фотосинтеза и обратный переход из восстановленной формы в окисленную путем окисления осадочного органического вещества в термохимической сульфатредукции в зоне субдукции, где происходят столкновения двигающихся плит.
Согласно одному из постулатов, круговорот углерода контролируется гравитационным взаимодействием небесных тел с Землей. Это взаимодействие передается через конвективное движение магмы, которое обусловливает неравномерное движение литосферных плит и разную частоту столкновений плит в зоне субдукции. В результате появляются орогенические циклы, состоящие из кратковременного орогенного периода и длительного геосинклинального периода. Орогенный период отвечает времени интенсивного вулканизма, магматизма и горообразования, в ходе которого атмосфера и гидросфера Земли заполняется СО2, а содержание кислорода падает, инициируется фотосинтез. Геосинклинальный период отвечает времени спокойного тектонического развития коры, времени развития фотосинтеза.
За время орогенического цикла происходит полная смена климатических условий от высокотемпературных (парникового эффекта) и анаэробных (или малокислородных) в орогенный период цикла до низкотемпературных (оледенений) и аэробных в конце геосинклинального периода цикла.
Смена климатических условий влечет за собой биотический круговорот. Общий тренд: от анаэробных (или малокислородных) и термофильных организмов в начале орогенического цикла к холодостойким и аэробным организмам в конце.
Как следствие, наиболее характерными признаками орогенических циклов являются в начале цикла интенсивный вулканизм и магматизм, в конце цикла – массовая гибель организмов и образование толщ, богатых органическим веществом. Существуют и многие другие признаки (Ivlev, 2019а), которые в данной статье не рассматриваются.
Эволюция глобального цикла углерода и достижение им экологической точки компенсации связаны с участием в нем глобального фотосинтеза. Согласно постулату, глобальный фотосинтез, как и фотосинтез индивидуального организма, обладает двумя реципрокно связанными функциями – интегрированной функцией ассимиляции и интегрированной функцией фотодыхания. Первая обеспечивает прирост общей биомассы “живого” вещества, вторая – снижает. После попадания “живого” вещества в осадок окисление продолжается. Разница между тем количеством органического вещества, которое доходит до зоны субдукции, и тем количеством восстановленного углерода, которое образуется при фотосинтезе, определяет прирост осадочного органического вещества в земной коре. При этом в соответствии с уравнением глобального фотосинтеза эквивалентное количество кислорода накапливается в атмосфере. Благодаря усилению фотодыхательной функции глобального фотосинтеза из-за эволюции фотосинтеза, прирост количества осадочного органического вещества в земной коре непрерывно уменьшается от одного орогенического цикла к другому, пока не исчезает совсем. Этот момент соответствует наступлению экологической точки компенсации. В этот момент глобальный цикл углерода переходит в стационарное состояние. Это значит, все его характеристики: содержание осадочного органического вещества в земной коре, содержание углекислого газа и кислорода в атмосфере и гидросфере – становятся стационарными и начинают осциллировать около некоторых средних значений. Стационарное состояние является неустойчивым и чувствительно даже к слабым внешним воздействиям.
Вместе с колебаниями ключевых параметров углеродного цикла в рамках принятой модели функционирования колеблются многие другие параметры, которые определяют условия обитания жизни организмов на Земле, – это поверхностная температура, уровень моря, климатические условия, распространенность на Земле и в морях разных видов растительных и животных организмов и т.д. Поэтому чтобы человек мог существовать на Земле, он должен не только постоянно контролировать эти параметры, но и поддерживать стационарность системы, влияя на параметры в допустимых пределах.
Один из выводов касается нефти как источника энергии. В условиях стационарности содержания органического вещества в земной коре, имея в виду, что нефть составляет небольшой процент от органического вещества, а также принимая во внимание все возрастающие объемы добычи, пора думать о другом источнике энергии, который мог бы ее заменить .
Роль глобального фотосинтеза формулируется в соответствующем постулате модели. Она связана со способностью глобального фотосинтеза усиливать роль фотодыхания в ответ на оксигенацию среды. В итоге углеродный цикл достигает экологической точки компенсации, т.е. состояния системы, когда количество восстановленного углерода, образованного при фотосинтезе, равно количеству углерода, окисленного в зоне субдукции.
Список литературы
Галимов Э.М., 1968. Геохимия стабильных изотопов углерода. М.: Недра. 223 с.
Дегенс Э.Т., 1974. Биогеохимия устойчивых изотопов углерода // Органическая геохимия / Под ред. Петрова А.А. Л.: Недра. С. 207–227.
Ивлев А.А., 2015. Глобальный редокс-цикл биосферного углерода. Взаимодействие фотосинтеза и движения литосферных плит. Saarbrucken: LAP Lambert Аcad. Publishing. 76 с.
Ивлев А.А., 2019а. Образование толщ, богатых органическим веществом, в свете новой модели глобального цикла углерода // Геология нефти и газа. № 5. С. 83–90.
Ивлев А.А., 2019б. О роли фотосинтеза в круговороте углерода // Океанол. исследования. Т. 47. № 4. С. 76–87.
Ронов А.Б., 1976. Вулканизм, карбонатонакопление, жизнь. Закономерности глобальной геохимии углерода // Геохимия. № 8. С. 1252–1279.
Руттен М., 1978. Происхождение жизни. М.: Мир. 471 с.
Флинт Р.В., 1978. История Земли. М.: Прогресс. 349 с.
Alroy J., 2008. Dynamics of origination and extinction in the marine fossil records // Proc. Natl. Am. Sci. USA. V. 105. Suppl. 1. P. 11536–11542.
Andre M.J., 2011a. Modelling 18O and 16O unidirectional fluxes in plants: I. Regulation of preindustrial atmosphere // BioSystems. V. 103. P. 239–251.
Andre M.J., 2011b. Modelling 18O2 and 16O2 unidirectional fluxes in plant: II. Analysis of Rubisco evolution // BioSystems. V. 103. № 2. P. 251–264.
Cerling T.E., 1991. Carbon dioxide in the atmosphere: Evidence from Cenozoic and Mesozoic paleosls // Am. J. Sci. V. 291. № 4. P. 377–400.
Cerling T.E., Wang Y., Quade J., 1992. Expansion of C4 – ecosystems as an indicator global ecological change in late Miocene // Nature. V. 361. P. 344–348.
Cerling T.E., Harris J.M., MacFadden B.J., Leakey M.J., Quade J. et al., 1997. Global vegetation change through Miocene/Pliocene boundry // Nature. V. 389. P. 153–158.
Corso J.D., Gianolla P., Rigo M., Franceschi M., Roghi G. et al., 2018. Multiple negative carbon-isotope excursion during the Carnier Pluvial Epizode // Earth Sci. Rev. V. 185. P. 732–750.
Derry L.A., Kaufman A.J., Jacobsen S.B., 1992. Sedimentary cycling and environmental change in the Late Proterozoic: Evidence from stable and radiogenic isotopes // Geochim. Cosmochim. Acta. V. 56. P. 1317–1329.
Fowler C.M.R., 2005. The Solid Earth: An Introduction to Global Geophysics. Cambridge: Cambridge Univ. Press. 206 p.
Goričan Š., Carter E.S., O’Dogherty G.L., Wever P., Paulian D. et al., 2013. Evolutionary patterns and palaeobiogeography of Pliensbachian and Toarcian (Early Jurassic) Radiolaria // Palaeogeogr. Palaeoclimatol. Palaeoecol. V. 386. P. 620–636.
Harland W.B., Armstrong R.L., Cox A.V., Craig L.E., Smith A.G., Smith D.G., 1990. A Geologic Time Scale. Cambridge: Cambridge Univ. Press. 456 p.
Hayes J.M., Popp B.N., Takigiku R., Johnson M.W., 1989. An isotopic study of biogeochemical relationships between carbonates and organic carbon in the Greenhorn Formation // Geochim. Cosm. Acta. V. 53. № 11. P. 2961–2972.
Jacoby W.R., 1978. Role of gravity in Plate Tectonics // Developments in Geotechnical Engineering. V. 14. Pt. A. P. 707–727.
Igamberdiev A.U., Lea P.J., 2006. Land plants equilibrate O2 and CO2 concentrations in the atmosphere // Photosynth. Res. V. 87. № 2. P. 177–194.
Ivlev A.A., 2015. Global redox cycle of biospheric carbon: Interaction of photosynthesisand earth crust procsess // BioSystems. V. 137. P. 1–11.
Ivlev A.A., 2016. Global redox carbon cycle and photosynthesis development // J. Ecosys. Ecograph.https://doi.org/10.4172/2157-7625.S5-003
Ivlev A.A., 2019a. The Global Carbon Cycle and the Evolution of Photosynthesis. Cambridge: Cambridge Scholars Publ. 160p.
Ivlev A.A., 2019b. Manifestations of Photosynthesis in the Evolution of the Global Carbon Cycle // Oceanogr. Fish. V. 9. № 1. P. 1–3.
Ivlev A.A., 2020. Global photosynthesis is an instrument in large natural systems studies // Geol. Earth Mar. Sci. V. 1. № 1. P. 1–4.
Ivlev A.A., Igamberdiev A.Y., Dubinsky A.Yu., 2010. Isotopic composition of carbon metabolites and metabolic oscillations in the course of photosynthesis // Biophysics. V. 49. Suppl. 1. P. 3–16.
Large R.R., Halpin J.A., Lounejeva E., Danyushevsky K.V., Maslennikov V.V. et al., 2015. Cycles of nutrient trace elements in the Phanerozoic ocean // Gondwana Res. V. 28. № 4. P. 1282–1293.
Mackenzie F.T., Pigott J.D., 1981. Tectonic controls of Phanerozoic sedimentary rock cycling // J. Geol. Soc. V. 138. P. 183–196.
Nakai N., Jensen M., 1960. Biogeochemistry of sulfur isotopes // J. Earth Sci. V. 8. P. 30−35.
Popp B.N., Takigiku R., Hayes J.M., Louda J.W., Baker E.W., 1989. The post-Paleozoic chronology and mechanism of 13C depletion in primary marine organic matter // Am. J. Sci. V. 289. P. 436–454.
Raup D.M., Sepkosky J.J., Jr., 1984. Periodicity of extinctions in the geological past // Proc. Natl. Acad. Sci. USA. V. 81. P. 801–855.
Riding J.R., Leng M.J., Kender S., Hesselbo S.P., Feist-Burkhardt S., 2013. Isotopic and palynological evidence for a new Early Yurassic environmental perturbation // Palaeogeogr. Palaeoclimatol. Palaeoecol. V. 374. P. 16–27.
Riguzzi F., Panza G., Varga P., Doglioni C., 2009. Can Earth’s rotation and tidal despinning drive plate tectonics? // Tectonophysics. V. 484. № 1–4. P. 60–73.
Thode H.G., Monster J., Dunford H.B., 1961. Sulfur isotope geochemistry // Geochim. Cosmochim. Acta. V. 25. P. 159–264.
Tolbert N.E., Benker C., Beck E., 1995. The oxygen and carbon dioxide compensation points of C3 plants: Possible role in regulating atmospheric oxygen // Proc. Natl. Acad. Sci. V. 92. P. 11230–11233.
Young G.M., 2015. Environmental upheavals of Ediacaran period and the Cambrian and “explosion” of animal life // Geosci. Front. V. 6. P. 523–615.
Дополнительные материалы отсутствуют.
Инструменты
Журнал общей биологии


