Почвоведение, 2019, № 10, стр. 1243-1258
Оценка экотоксичности почв в условиях загрязнения тяжелыми металлами
И. О. Плеханова a, *, О. А. Золотарева a, И. Д. Тарасенко a, А. С. Яковлев a
a МГУ им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: irinaoplekhanova@mail.ru
Поступила в редакцию 02.10.2018
После доработки 19.12.2018
Принята к публикации 15.02.2019
Аннотация
Экспериментально установлено, что при загрязнении почв тяжелыми металлами граничные значения концентраций металлов, выше которых выявляются признаки экотоксичности, оказались разными для тест-растения и микробного сообщества. Ингибиpование дыхания исследованных почв наблюдали пpи более высоких дозах Pb, Zn и Cd, чем уменьшение всхожести и длины проростков горчицы белой (Sinapis alba). Наиболее токсичными для растений и микроорганизмов являются соединения Cd и условия полиэлементного загрязнения. Выявлены концентрации тяжелых металлов, способные оказывать достоверное негативное воздействие на растения и почвенное микробное сообщество при разных уровнях загрязнения для дерново-подзолистой, серой лесной, чернозема выщелоченного и каштановой почв. По убыванию устойчивости к ТМ исследованные почвы можно расположить в следующий ряд: чернозем выщелоченный (Luvic Chernozem) > серая лесная (Eutric Retisol (Ochric)) > каштановая (Haplic Kastanozem) > дерново-подзолистая (Eutric Albic Retisol (Ochric)). При загрязнении почв ацетатами Pb, Zn и Cd содержание их подвижных соединений увеличивается в значительно большей степени, чем валовое содержание. Наибольшая подвижность Pb, Zn и Cd отмечается при одновременном их поступлении в почвы.
ВВЕДЕНИЕ
В настоящее время наиболее разработан санитарно-гигиенический подход к оценке качества окружающей среды, который декларирует антропоцентризм, ограничивая оценку состояния экосистемы представлениями о качестве окружающей среды как среды обитания человека. Существующая система гигиенической регламентации является единственной законодательно утвержденной базой данных для оценки и нормирования концентраций загрязняющих веществ в почвах. Недостатком этих нормативов является отсутствие учета почвенно-экологических и геохимических условий образования и функционирования почв [5, 8, 11, 16].
Многие исследователи считают, что нормативы содержания тяжелых металлов (ТМ) должны разрабатываться согласно конкретной почвенно-экологической обстановке [5, 15, 25]. Отчасти эти соображения учтены при разработке ориентировочно-допустимых концентраций (ОДК) ТМ для трех групп почв: песчаных и супесчаных, суглинистых и глинистых, близких к нейтральным и нейтральным суглинистым и глинистым [ГН 2.1.7.2042-06]. Отсутствие дифференциации нормативов по природно-климатическим зонам и видам хозяйственного использования ограничивает возможности объективной оценки уровней загрязнения почв. Целью экологического нормирования является разработка научно обоснованных критериев и норм предельно допустимых концентраций (ПДК), охватывающих все виды вредных воздействий на окружающую среду и почвы различного хозяйственного назначения. Токсическое действие загрязняющих веществ зависит от конкретной биогеохимической обстановки, поскольку существует перенос этих веществ между всеми компонентами окружающей среды, включая почву, растения, почвенных животных, микроорганизмы и воздух.
Система ПДК, основанная на дифференцированном изучении аналитическими методами отдельных веществ, не всегда отвечает современным принципам системности в экологии и не может в полной мере обеспечить сохранение приемлемого уровня экологической безопасности. Часто в окружающую среду поступает несколько загрязняющих веществ и идентифицировать каждое из них трудно, при этом может наблюдаться эффект синергического действия. В этом случае необходимо привлекать методы биотестирования и изучать отклик биологических систем с помощью анализа зависимости доза–эффект [2, 6, 25].
Пределом допустимой концентрации загрязняющих веществ в почвах является уровень, при котором начинает изменяться количество и качество вновь создаваемого живого вещества, то есть биологическая продукция [8]. Этот уровень загрязнения почвы прямо или косвенно влияет на контактирующие сопредельные среды, что необходимо учитывать при разработке показателей экологического нормирования для реальных почв.
В настоящее время не существует общепринятой и проработанной теории экологического нормирования. Вместе с тем в последние десятилетия сделан существенный вклад в разработку этой концепции: формируются основные подходы, принципы экологического контроля, предложены различные критерии для оценки качества водных и наземных экосистем, которые базируются на биотической концепции контроля качества природной среды [6, 8, 12, 25, 29, 30 ] . Следует отметить, что выбор критериев для оценки экологического состояния почв является ключевым, поскольку определяет качество среды обитания, оцениваемое по показателям жизнедеятельности биологических систем. Если выбранные показатели удовлетворяют установленным критериям, то уровень антропогенной нагрузки можно считать приемлемым (допустимым). Почвенные характеристики должны рассматриваться в качестве основных оценочных критериев состояния экосистемы, поскольку они определяют функционирование растений, комплекса почвенных микроорганизмов и животных, а также качество природных вод. Эти критерии должны включать характеристику химических, физических и биологических свойств почв, в том числе определение форм соединений металлов в почвах, что необходимо для оценки их влияния на окружающую среду, а также устойчивость почв к загрязнению ТМ. В своей работе Глазовская [8] отмечает, что основным показателем устойчивости почв к различным химическим воздействиям должно быть ее эколого-геохимическое состояние, обеспечивающее нормальное функционирование присущих данной биогеоценотической системе совокупностей живых организмов и качество создаваемой биологической продукции. Все почвы обладают способностью сохранять и поддерживать в определенном диапазоне значений свои свойства при различных внешних воздействиях. Это уникальное свойство почв зависит от их буферности, которая определяется такими химическими, физическими и биологическими параметрами, как кислотность, гранулометрический и минералогический состав, содержание гумуса, состав обменных катионов и др., которые определяют реакцию почв на загрязнение и возможность осуществления экологических функций. Показателями нормального функционирования почвы как биокосной системы являются биологическая продуктивность и качество создаваемой биологической продукции [8].
Одним из интегральных показателей загрязнения почвы является ее фитотоксичность (свойство почвы подавлять рост и развитие высших растений). Этот показатель характеризует границу, определяющую изменение продуктивности экосистемы, что является одним из основных критериев качества почв.
Цель работы – оценка экологического состояния зональных почв: дерново-подзолистой, серой лесной, чернозема выщелоченного и каштановой – при искусственном загрязнении соединениями Zn, Pb, Cd при раздельном и совместном их поступлении в почвы по показателям состояния ТМ, микробиологической активности и фитотоксичности почв.
ОБЪЕКТЫ И МЕТОДЫ
Исследовали пробы из пахотных горизонтов почв: дерново-подзолистой (Eutric Albic Retisol (Loamic, Aric, Cutanic, Differentic, Ochric)) (Московская область), серой лесной (Eutric Retisol (Loamic, Aric, Cutanic, Ochric)) (Тульская область), чернозема выщелоченного (Luvic Chernozem (Laomic, Aric, Pachic)) (Липецкая область) и каштановой (Haplic Kastanozem (Loamic, Aric)) (Волгоградская область).
Основные химические свойства исследуемых почв показаны в табл. 1. Содержание органического вещества в образцах почв определяли по методу Тюрина в модификации Никитина со спектрофотометрическим окончанием, рН водной и солевой вытяжек – потенциометрически, гидролитическую кислотность – путем вытеснения 1 M раствором СН3СООNa [1].
Таблица 1.
Показатели химических свойств почв
| Почва | Cорг, % | рН | Сумма обменных оснований | Гидролитическая кислотность | |
|---|---|---|---|---|---|
| KCl | H2O | ||||
| смоль(экв)/кг | |||||
| Дерново-подзолистая | 1.3 | 5.2 | 6.4 | 16 | 1.9 |
| Серая лесная | 2.9 | 5.7 | 6.7 | 15 | 3.2 |
| Чернозем выщелоченный | 3.9 | 5.9 | 6.8 | 28 | 3.0 |
| Каштановая | 1.45 | 6.8 | 7.7 | 17 | 1.3 |
Исследуемые почвы характеризуются слабокислой и близкой к нейтральной реакцией среды. Для каштановой почвы pH имеет щелочное значение, возможно, связанное с некоторым засолением. Значения рНКСl серой лесной почвы, каштановой и чернозема >5.5, а дерново-подзолистой <5.5, следовательно, первые три почвы относятся к группе с нейтральной реакцией среды и суглинистым гранулометрическим составом, а дерново-подзолистая почва – к группе со слабокислой реакцией среды и суглинистым гранулометрическим составом, что определяет их разную устойчивость к ТМ и различные значения ОДК [8, 11, 14]. В градациях ОДК не учитывается содержание гумуса, однако следует отметить, что в дерново-подзолистой и каштановой почвах содержание органического вещества в 2–3 раза меньше, чем в черноземе и серой лесной почве.
Валовое содержание ТМ в почвах определяли после разложения их царской водкой (HCl + + HNO3 в соотношении 3 : 1) [20]. Содержание ТМ исследовали в 1 M азотнокислой и ацетатно-аммонийной вытяжках с рН 4.8. Водную вытяжку готовили в соотношении почва : вода 1 : 10, фильтровали и концентрировали упариванием в 50 раз. Определение содержания ТМ в вытяжках проводили на атомно-абсорбционном спектрофотометре AAS-3 в пламени ацетилен–воздух с использованием дейтеpиевого корректора фона и методом атомно-эмиссионной спектроскопии с индуктивно связанной плазмой на приборе Agilent ICP-MS 7100a.
Чернозем характеризуется значительной мощностью гумусового горизонта, высоким содержанием Сорг и илистой фракции, большой емкостью поглощения, что свидетельствует о высокой буферности этой почвы по отношению к ТМ [14, 15]. Отмечается больший показатель суммы обменных оснований в черноземе по сравнению с остальными почвами.
Дерново-подзолистая почва характеризуется более низким естественным плодородием, большей кислотностью и меньшей гумусированностью, а также более низкой буферностью по сравнению с другими почвами. С учетом этих свойств уровни ОДК, используемые для оценки дерново-подзолистой почвы, в 2 раза ниже, чем для нейтральных почв [ГН 2.1.7.2042-06] (табл. 2).
Таблица 2.
Уровни ОДК и дозы тяжелых металлов, вносимые в почвы, мг/кг
| Элемент | Кратность ОДК | ||||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 5 | 10 | |
| Серая лесная, каштановая почвы и чернозем выщелоченный | |||||
| Pb | 130 | 260 | 390 | 650 | 1300 |
| Zn | 220 | 440 | 660 | 1100 | 2200 |
| Cd | 2 | 4 | 6 | 10 | 20 |
| Дерново-подзолистая почва | |||||
| Pb | 65 | 130 | 195 | 325 | 650 |
| Zn | 110 | 220 | 330 | 550 | 1100 |
| Cd | 1 | 2 | 3 | 5 | 10 |
В почвы вносили водный раствор уксуснокислых солей ТМ из расчета следующих доз 1 ОДК, 2 ОДК, 3 ОДК, 5 ОДК, 10 ОДК для Pb, Zn, Cd. Для варианта с комплексным загрязнением вносили одновременно раствор смеси всех трех металлов в дозах от 1 до 10 ОДК. Соли уксусной кислоты были выбраны для опыта в связи с их хорошей растворимостью, что способствует быстрому взаимодействию с почвенными компонентами, гидролиз этих солей не сопровождается резким сдвигом рН в область кислой реакции среды. Ацетат-ионы являются естественным продуктом метаболизма растений и незначительно изменяют питательный режим почв. При техногенном загрязнении в почву поступают различные соединения ТМ, отличающиеся химическими свойствами, причем доля труднорастворимых соединений значительно больше. Однако вблизи текстильных и химических предприятий по выработке пластических масс, синтетических волокон и ацетилцеллюлозы значительна эмиссия ацетатов ТМ.
В вегетационные сосуды с массой почвы 500 г высаживали одинаковые по размеру семена горчицы белой (Sinapis alba) и семена овса (Avena sp.) по 30 шт. на сосуд. Продолжительность вегетационных опытов составляла 40 дней. Предварительно почвы инкубировали в течение 14 дней при влажности равной 60% предельной влагоемкости (ПВ). Опыты проводили в трех повторностях.
Для изучения динамики развития тест-культур определяли всхожесть семян, энергию прорастания, длину корней и проростков. Уровень фитототоксичности почв отмечали при концентрации ТМ, вызывающей подавление роста и развития растений на 20% от контроля.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Валовое содержание элементов в незагрязненных почвах находится в пределах типичных колебаний содержания микроэлементов [6, 19]. Содержание цинка в дерново-подзолистой почве и черноземе выщелоченном выше кларка по Виноградову (табл. 3), что соответствует современной тенденции накопления этого элемента в почвах [3, 16].
Таблица 3.
Валовое содержание ТМ в почвах опыта (мг/кг) и коэффициент концентрации ТМ (Кс) относительно контроля
| Вариант | Zn | Кс | Pb | Кс | Cd | Кс |
|---|---|---|---|---|---|---|
| Дерново-подзолистая почва | ||||||
| Контроль | 56 ± 2 | 1 | 9.4 ± 0.5 | 1 | 0.12 ± 0.2 | 1 |
| 1 ОДК | 166 | 2.9 | 74 | 7.9 | 1.12 | 9.3 |
| 2 ОДК | 276 | 4.9 | 139 | 14.4 | 2.12 | 17.7 |
| 3 ОДК | 386 | 6.9 | 204 | 21.3 | 3.12 | 26 |
| 5 ОДК | 606 | 10.8 | 334 | 35.1 | 5.12 | 42.7 |
| 10 ОДК | 1156 | 20.5 | 659 | 70. | 10.12 | 84.3 |
| Серая лесная почва | ||||||
| Контроль | 47.5 ± 0.9 | 1 | 10.5 ± 0.4 | 1 | 0.2 ± 0.03 | 1 |
| 1 ОДК | 267 | 5.6 | 140 | 13.4 | 2.2 | 11 |
| 2 ОДК | 487 | 10.3 | 270 | 25.8 | 4.2 | 21 |
| 3 ОДК | 707 | 14.9 | 400 | 38.1 | 6.2 | 31 |
| 5 ОДК | 1147 | 24.2 | 660 | 62.9 | 10.2 | 51 |
| 10 ОДК | 2247 | 47.3 | 1310 | 124.8 | 20.2 | 101 |
| Чернозем выщелоченный | ||||||
| Контроль | 71 ± 1.8 | 1 | 25.7 ± 1.5 | 1 | 0.28 ± 0.03 | 1 |
| 1 ОДК | 291 | 4.1 | 155 | 6 | 2.28 | 8.1 |
| 2 ОДК | 511 | 7.2 | 285 | 11.1 | 4.28 | 15.3 |
| 3 ОДК | 731 | 10.3 | 415 | 16.2 | 6.28 | 22.4 |
| 5 ОДК | 1171 | 16.5 | 675 | 26.3 | 10.28 | 36.7 |
| 10 ОДК | 2271 | 32 | 2225 | 86.6 | 20.28 | 72.4 |
| Каштановая почва | ||||||
| Контроль | 48.8 ± 1.5 | 1 | 15.5 ± 1.2 | 1 | 0.13 ± 0.02 | 1 |
| 1 ОДК | 266 | 5.5 | 145 | 9.4 | 2.13 | 16.4 |
| 2 ОДК | 486 | 9.9 | 275 | 17.8 | 4.13 | 31.8 |
| 3 ОДК | 706 | 14.5 | 405 | 26.2 | 6.13 | 47.1 |
| 5 ОДК | 1146 | 23.5 | 665 | 42.9 | 10.13 | 77.9 |
| 10 ОДК | 2246 | 46 | 1315 | 85 | 20.13 | 154.8 |
Валовое содержание ТМ определяют для оценки уровней загрязнения почв с целью сравнения с фоновым, эталонным содержанием или с ПДК [ГН 2.1.7.2041-06, 8, 13, 16, 22]. Как правило, одного этого показателя бывает недостаточно, так как ряд ПДК разработан только для подвижных соединений, которые извлекают ацетатно-аммонийным буфером (ААБ) с рН 4.8. Эта вытяжка широко используется в агрохимии для определения доступных для растений соединений микроэлементов и ТМ. По мнению многих исследователей, степень загрязнения почв ТМ правильнее оценивать по содержанию их наиболее подвижных и доступных растениям форм [13, 15, 16, 19]. По валовому содержанию ТМ в почве не всегда можно судить об экологической ситуации и влиянии загрязняющих веществ на растения. Если содержание ТМ превышает фоновый уровень в 2–3 раза, такие почвы не всегда можно отнести к загрязненным. Влияние на компоненты природной среды зависит от исходного содержания ТМ, которое может быть низким, и тогда это влияние может дать положительный эффект, или повышенным, и тогда могут возникать негативные последствия для живых организмов и качества сопредельных сред. Кроме того, реакция почвы на загрязнение сильно зависит от свойств почвы. В процессе жизнедеятельности растения контактируют в основном с доступными соединениями ТМ, количество которых тесно связано с буферностью почв [14, 15], которая определяется кислотностью, содержанием органического вещества, составом обменных катионов и анионов, а также гранулометрическим и минералогическим составом.
При внесении в дерново-подзолистую почву Zn, Pb и Cd в дозе, равной 1ОДК, их содержание относительно фона увеличилось в 3, 8 и 9 раз соответственно. Для серой лесной, чернозема и каштановой почв эти коэффициенты были выше, то есть допустимые концентрации перечисленных элементов превышали фоновое содержание в 5–10 раз. При искусственном загрязнении почв соединениями Pb, Zn и Cd увеличивается не только общее содержание этих металлов в почвах, но изменяется соотношение между формами соединений. Например, при внесении максимальной дозы Zn его общее содержание увеличилось в 20 раз, а содержание подвижных соединений увеличилась в 211 раз по сравнению с контрольными пробами (табл. 4). Значительно увеличилась подвижность соединений Pb, Zn и Cd во всех почвах при загрязнении, но наибольшие изменения произошли при комплексном загрязнении тремя металлами одновременно. Вероятно, это связано с увеличением конкуренции ионов металлов за реакционные центры. Использованные экстрагенты не являются селективными, что не позволяет судить о преимущественном поглощении ТМ определенными компонентами почв. Однако способность соединений Pb к образованию прочных комплексных соединений с органическим веществом позволяет предположить, что именно эти позиции в большей степени заняты ионами Pb [16, 18, 20, 21].
Таблица 4.
Содержание кислоторастворимых и подвижных соединений ТМ в почвах опыта (над чертой – мг/кг воздушно-сухой почвы; под чертой – % от валового содержания; среднее значение ± стандартная ошибка) и коэффициент концентрации ТМ (Кс) относительно контроля
| Вариант | Zn | Pb | Cd | ||||||||
| AAБ | Кс | 1 М НNO3 |
Кс | AAБ | Кс | 1 М НNO3 | Кс | AAБ | 1 М НNO3 |
Кс | |
| Дерново-подзолистая почва | |||||||||||
| Контроль | $\frac{{2.1 \pm 0.043}}{{4 \pm 0.12}}$ | 1 | $\frac{{4.5 \pm 0.11}}{{8 \pm 0.19}}$ | 1 | $\frac{{0.6 \pm {\text{0}}{\text{.20}}}}{{5.5 \pm {\text{ 0}}{\text{.15}}}}$ | 1 | $\frac{{1.2 \pm 0.08}}{{20 \pm 1.11}}$ | 1 | 0.02 | $\frac{{0.03 \pm 0.028}}{{16 \pm 1.17}}$ | 1 |
| 1 ОДК | $\frac{{55 \pm 2.1}}{{33 \pm 1.1}}$ | 26 | $\frac{{70 \pm 2.45}}{{42 \pm 1.47}}$ | 15.5 | $\frac{{10 \pm 1.12}}{{14 \pm 1.18}}$ | 16.6 | $\frac{{28 \pm 1.12}}{{39 \pm 2.22}}$ | 23.3 | $\frac{{0.35 \pm 0.005}}{{31 \pm 1.12}}$ | $\frac{{0.6 \pm 0.02}}{{53 \pm 1.41}}$ | 20 |
| 2 ОДК | $\frac{{118 \pm 4.11}}{{43 \pm 1.22}}$ | 29.5 | $\frac{{145 \pm 3.12}}{{52 \pm 1.33}}$ | 32.2 | $\frac{{34 \pm 2.45}}{{25 \pm 1.35}}$ | 56.7 | $\frac{{55 \pm 2.43}}{{41 \pm 1.42}}$ | 45.8 | $\frac{{0.8 \pm 0.006}}{{38 \pm 1.88}}$ | $\frac{{1.2 \pm 0.01}}{{57 \pm 2.32}}$ | 60 |
| 3 ОДК | $\frac{{207 \pm 5.72}}{{53 \pm 1.48}}$ | 51.7 | $\frac{{277 \pm 6.14}}{{71 \pm 2.31}}$ | 61.6 | $\frac{{73 \pm 2.41}}{{36 \pm 1.42}}$ | 121.6 | $\frac{{113 \pm 2.43}}{{56 \pm 1.33}}$ | 94.2 | $\frac{{1.5 \pm 0.035}}{{48 \pm 1.42}}$ | $\frac{{2 \pm 0.02}}{{64 \pm 2.32}}$ | 100 |
| 5 ОДК | $\frac{{374 \pm 6.53}}{{62 \pm 2.11}}$ | 93.5 | $\frac{{437 \pm 7.33}}{{72 \pm 2.41}}$ | 97.1 | $\frac{{121 \pm 3.43}}{{37 \pm 1.22}}$ | 201.6 | $\frac{{210 \pm 3.41}}{{64 \pm 1.42}}$ | 175 | $\frac{{3 \pm 1.22}}{{58 \pm 1.43}}$ | $\frac{{3.6 \pm 0.022}}{{70 \pm 3.41}}$ | 180 |
| 10 ОДК | $\frac{{845 \pm 7.22}}{{73 \pm 2.12}}$ | 211.2 | $\frac{{964 \pm 6.28}}{{83 \pm 1.35}}$ | 214.2 | $\frac{{241 \pm 4.22}}{{52 \pm 1.26}}$ | 401 | $\frac{{459 \pm 4.42}}{{70 \pm 2.43}}$ | 382.5 | $\frac{{6.9 \pm 0.01}}{{~68 \pm 2.32}}$ | $\frac{{9.3 \pm 0.22}}{{92 \pm 2.43}}$ | 465 |
| Полиэлементное загрязнение | |||||||||||
| 1 ОДК | $\frac{{69 \pm 1.88}}{{41 \pm 1.11}}$ | 32.8 | $\frac{{106 \pm 3.42}}{{63 \pm 2.11}}$ | 23.5 | $\frac{{24 \pm 1.11}}{{34 \pm 1.88}}$ | 40 | $\frac{{45 \pm 2.02}}{{64 \pm 2.56}}$ | 37.5 | $\frac{{0.4 \pm 0.002}}{{36 \pm 1.42}}$ | $\frac{{0.7 \pm 0.003}}{{63 \pm 1.43}}$ | 35 |
| 2 ОДК | $\frac{{128 \pm 3.22}}{{46 \pm 1.17}}$ | 61 | $\frac{{187 \pm 4.22}}{{67 \pm 1.88}}$ | 41.5 | $\frac{{55 \pm 2.12}}{{41 \pm 1.92}}$ | 91.7 | $\frac{{77 \pm 2.71}}{{57 \pm 1.93}}$ | 64.2 | $\frac{{0.9 \pm 0.005}}{{43 \pm 1.51}}$ | $\frac{{1.5 \pm 0.13}}{{70 \pm 2.11}}$ | 75 |
| 3 ОДК | $\frac{{196 \pm 4.22}}{{51 \pm 1.18}}$ | 93.3 | $\frac{{274 \pm 5.33}}{{71 \pm 2.13}}$ | 60.9 | $\frac{{99 \pm 3.42}}{{49 \pm 2.11}}$ | 165 | $\frac{{129 \pm 3.42}}{{64 \pm 2.11}}$ | 107.5 | $\frac{{1.7 \pm 0.01}}{{55 \pm 1.88}}$ | $\frac{{2.4 \pm 0.18}}{{77 \pm 2.17}}$ | 120 |
| 5 ОДК | $\frac{{395 \pm 7.12}}{{65 \pm 1.42}}$ | 188 | $\frac{{469 \pm 6.11}}{{77 \pm 2.35}}$ | 104.2 | $\frac{{186 \pm 4.55}}{{56 \pm 2.18}}$ | 310 | $\frac{{221 \pm 4.15}}{{67 \pm 2.22}}$ | 184.1 | $\frac{{3.3{\text{ }} \pm 0.01}}{{65 \pm 1.93}}$ | $\frac{{4 \pm 0.28}}{{78 \pm 2.19}}$ | 200 |
| 10 ОДК | $\frac{{882 \pm 10.11}}{{76 \pm 2.11}}$ | 420 | $\frac{{1011 \pm 13.8}}{{87 \pm 3.31}}$ | 224.7 | $\frac{{426 \pm 6.33}}{{65 \pm 3.13}}$ | 710 | $\frac{{510 \pm 7.14}}{{78 \pm 2.33}}$ | 425 | $\frac{{7.6 \pm 0.08}}{{75 \pm 2.1}}$ | $\frac{{9.5 \pm 0.37}}{{94 \pm 2.32}}$ | 475 |
| Вариант | Zn | Pb | Cd | ||||||||
| AAБ | Кс | 1 М НNO3 |
Кс | AAБ | Кс | 1 М НNO3 |
Кс | AAБ | 1 М НNO3 |
Кс | |
| Серая лесная почва | |||||||||||
| Контроль | $\frac{{1.7 \pm 0.021}}{{3.3 \pm 0.032}}$ | 1 | $\frac{{6.8 \pm 0.21}}{{14 \pm 0.82}}$ | 1 | $\frac{{1 \pm 0.02}}{{9 \pm 1.33}}$ | 1 | $\frac{{3 \pm 0.02}}{{27 \pm 1.17}}$ | 1 | 0.02 | $\frac{{0.022 \pm 0.0004}}{{11 \pm 0.2}}$ | 1 |
| 1 ОДК | $\frac{{64 \pm 2.12}}{{24 \pm 1.22}}$ | 37.6 | $\frac{{105 \pm 3.11}}{{39 \pm 1.25}}$ | 21.3 | $\frac{{29 \pm 1.23}}{{20 \pm 1.11}}$ | 29 | $\frac{{55 \pm 2.42}}{{39 \pm 2.88}}$ | 18.3 | $\frac{{0.5 \pm 0.03}}{{23 \pm 1.11}}$ | $\frac{{0.6 \pm 0.03}}{{27 \pm 1.1}}$ | 27 |
| 2 ОДК | $\frac{{145 \pm 3.72}}{{30 \pm 1.11}}$ | 85.3 | $\frac{{200 \pm 3.88}}{{41 \pm 1.17}}$ | 29.4 | $\frac{{54 \pm 1.83}}{{20 \pm 0.99}}$ | 54 | $\frac{{114 \pm 4.1}}{{42 \pm 1.35}}$ | 38 | $\frac{{1 \pm 0.022}}{{24 \pm 1.23}}$ | $\frac{{1.2 \pm 0.033}}{{29 \pm 1.42}}$ | 54.5 |
| 3 ОДК | $\frac{{288 \pm 4.12}}{{41 \pm 1.14}}$ | 169.4 | $\frac{{327 \pm 5.13}}{{47 \pm 1.17}}$ | 48.1 | $\frac{{125 \pm 2.88}}{{31 \pm 1.11}}$ | 125 | $\frac{{200 \pm 4.12}}{{50 \pm 1.82}}$ | 66.7 | $\frac{{2 \pm 0.02}}{{32 \pm 1.23}}$ | $\frac{{2.4 \pm 0.03}}{{39 \pm 1.28}}$ | 109 |
| 5 ОДК | $\frac{{490 \pm 5.32}}{{43 \pm 2.32}}$ | 288.2 | $\frac{{591 \pm 6.13}}{{52 \pm 2.42}}$ | 86.9 | $\frac{{195 \pm 3.11}}{{30 \pm 1.41}}$ | 195 | $\frac{{330 \pm 5.22}}{{50 \pm 1.92}}$ | 110 | $\frac{{3.4 \pm 0.02}}{{33 \pm 1.42}}$ | $\frac{{5 \pm 0.021}}{{49 \pm 1.33}}$ | 227 |
| 10 ОДК | $\frac{{1133 \pm 9.33}}{{51 \pm 2.41}}$ | 666.5 | $\frac{{1750 \pm 14.12}}{{78 \pm 3.13}}$ | 257.4 | $\frac{{650 \pm 8.72}}{{49 \pm 2.33}}$ | 650 | $\frac{{801 \pm 10.12}}{{61 \pm 2.11}}$ | 267 | $\frac{{9.2 \pm 0.21}}{{46 \pm 1.58}}$ | $\frac{{13 \pm 0.82}}{{64 \pm 2.11}}$ | 591 |
| Полиэлементное загрязнение | |||||||||||
| 1 ОДК | $\frac{{75 \pm 2.33}}{{28 \pm 1.12}}$ | 44.1 | $\frac{{141 \pm 3.99}}{{53 \pm 2.22}}$ | 20.7 | $\frac{{34 \pm 2.11}}{{24 \pm 1.11}}$ | 34 | $\frac{{69 \pm 1.11}}{{49 \pm 0.82}}$ | 23 | $\frac{{0.6 \pm 0.02}}{{27 \pm 1.13}}$ | $\frac{{1.1 \pm 0.033}}{{45 \pm 1.42}}$ | 50 |
| 2 ОДК | $\frac{{186 \pm 4.22}}{{38 \pm 1.33}}$ | 109.4 | $\frac{{277 \pm 5.33}}{{57 \pm 2.18}}$ | 40.7 | $\frac{{81 \pm 2.31}}{{30 \pm 1.11}}$ | 81 | $\frac{{109 \pm 1.32}}{{40 \pm 0.72}}$ | 36.3 | $\frac{{1.4 \pm 0.022}}{{33 \pm 1.11}}$ | $\frac{{2.3 \pm 0.011}}{{54 \pm 2.12}}$ | 104 |
| 3 ОДК | $\frac{{301 \pm 5.78}}{{43 \pm 1.72}}$ | 177 | $\frac{{422 \pm 3.42}}{{60 \pm 1.93}}$ | 62 | $\frac{{148 \pm 4.22}}{{37 \pm 1.12}}$ | 148 | $\frac{{198 \pm 4.13}}{{50 \pm 1.28}}$ | 66 | $\frac{{2.2 \pm 0.011}}{{35 \pm 1.42}}$ | $\frac{{3.4 \pm 0.012}}{{55 \pm 1.89}}$ | 154 |
| 5 ОДК | $\frac{{529 \pm 8.13}}{{46 \pm 1.88}}$ | 311.2 | $\frac{{723 \pm 9.42}}{{63 \pm 2.32}}$ | 106 | $\frac{{244 \pm 2.43}}{{37 \pm 0.88}}$ | 244 | $\frac{{357 \pm 3.23}}{{54 \pm 1.88}}$ | 119 | $\frac{{4 \pm 0.33}}{{39 \pm 1.11}}$ | $\frac{{5.8 \pm 0.1}}{{57 \pm 1.1}}$ | 263.6 |
| 10 ОДК | $\frac{{1490 \pm 17.22}}{{66 \pm 2.72}}$ | 876 | $\frac{{1790 \pm 13.88}}{{80 \pm 3.15}}$ | 263 | $\frac{{765 \pm 5.23}}{{58 \pm 1.22}}$ | 765 | $\frac{{911 \pm 9.11}}{{70 \pm 2.33}}$ | 303.7 | $\frac{{13.1 \pm 0.82}}{{64 \pm 1.32}}$ | $\frac{{17 \pm 0.32}}{{84 \pm 2.8}}$ | 772.7 |
| Вариант | Zn | Pb | Cd | ||||||||
| AAБ | Кс | 1 М НNO3 |
Кс | AAБ | Кс | 1 М НNO3 |
Кс | AAБ | 1 М НNO3 |
Кс | |
| Чернозем выщелоченный | |||||||||||
| Контроль | $\frac{{1.2 \pm 0.023}}{{2.1 \pm 0.11}}$ | 1 | $\frac{{6.2 \pm 0.03}}{{11 \pm 0.08}}$ | 1 | $\frac{{0.5 \pm 0.002}}{{1.9 \pm 0.012}}$ | 1 | $\frac{{3 \pm 0.012}}{{12 \pm 0.11}}$ | 1 | 0.01 | $\frac{{0.012 \pm 0.00}}{{4 \pm 0.022}}$ | 1 |
| 1 ОДК | $\frac{{111 \pm 5.42}}{{38 \pm 1.18}}$ | 92.5 | $\frac{{138 \pm 5.85}}{{47 \pm 1.17}}$ | 22.2 | $\frac{{15 \pm 0.72}}{{10 \pm 0.62}}$ | 30 | $\frac{{38 \pm 0.82}}{{24 \pm }}$ | 12.7 | $\frac{{0.8 \pm 0.001}}{{35 \pm 0.92}}$ | $\frac{{1 \pm 0.001}}{{44 \pm 2.13}}$ | 66.7 |
| 2 ОДК | $\frac{{224 \pm 7.33}}{{44 \pm 1.32}}$ | 186.7 | $\frac{{245 \pm 6.33}}{{48 \pm 1.21}}$ | 39.5 | $\frac{{65 \pm 2.41}}{{23 \pm 1.32}}$ | 130 | $\frac{{97 \pm 3.41}}{{34 \pm 1.35}}$ | 32.3 | $\frac{{1.6 \pm 0.002}}{{37 \pm 1.12}}$ | $\frac{{2 \pm 0.041}}{{47 \pm 2.45}}$ | 167 |
| 3 ОДК | $\frac{{357 \pm 8.28}}{{49 \pm 1.41}}$ | 297.5 | $\frac{{397 \pm 7.22}}{{54 \pm 1.42}}$ | 64 | $\frac{{108 \pm 2.82}}{{26 \pm 0.92}}$ | 216 | $\frac{{165 \pm 4.22}}{{40 \pm 1.37}}$ | 55 | $\frac{{2.4 \pm 0.002}}{{38 \pm 1.11}}$ | $\frac{{3 \pm 0.022}}{{48 \pm 1.88}}$ | 250 |
| 5 ОДК | $\frac{{612 \pm 9.15}}{{52 \pm 1.62}}$ | 510 | $\frac{{645 \pm 8.13}}{{55 \pm 1.49}}$ | 104 | $\frac{{203 \pm 3.11}}{{30 \pm 1.17}}$ | 406 | $\frac{{313 \pm 4.55}}{{46 \pm 1.45}}$ | 104 | $\frac{{4.1 \pm 0.08}}{{40 \pm 1.15}}$ | $\frac{{4.9 \pm 0.012}}{{48 \pm 1.55}}$ | 408 |
| 10 ОДК | $\frac{{1508 \pm 13.44}}{{66 \pm 1.72}}$ | 1256 | $\frac{{1649 \pm 21.82}}{{73 \pm 1.61}}$ | 266 | $\frac{{499 \pm 4.82}}{{38 \pm 1.21}}$ | 998 | $\frac{{699 \pm 10.2}}{{53 \pm 2.12}}$ | 233 | $\frac{{11 \pm 0.82}}{{54 \pm 2.12}}$ | $\frac{{14.9 \pm 0.75}}{{73 \pm 1.82}}$ | 1242 |
| Полиэлементное загрязнение | |||||||||||
| 1 ОДК | $\frac{{114 \pm 5.32}}{{39 \pm 1.21}}$ | 95 | $\frac{{148 \pm 8.35}}{{51 \pm 1.22}}$ | 23.9 | $\frac{{40 \pm 2.13}}{{26 \pm 1.18}}$ | 80 | $\frac{{72 \pm 2.28}}{{46 \pm 1.82}}$ | 24 | $\frac{{0.9 \pm 0.001}}{{39 \pm 1.13}}$ | $\frac{{1.2 \pm 0.035}}{{52 \pm 1.43}}$ | 100 |
| 2 ОДК | $\frac{{253 \pm 6.88}}{{49 \pm 1.22}}$ | 211 | $\frac{{294 \pm 10.22}}{{57 \pm 2.41}}$ | 47.4 | $\frac{{100 \pm 3.45}}{{35 \pm 1.42}}$ | 200 | $\frac{{147 \pm 4.28}}{{51 \pm 2.17}}$ | 49 | $\frac{{1.8 \pm 0.05}}{{42 \pm 1.21}}$ | $\frac{{2.6 \pm 0.022}}{{60 \pm 1.65}}$ | 217 |
| 3 ОДК | $\frac{{391 \pm 8.22}}{{53 \pm 1.83}}$ | 326 | $\frac{{434 \pm 12.21}}{{59 \pm 1.75}}$ | 70 | $\frac{{156 \pm 4.28}}{{37 \pm 1.45}}$ | 312 | $\frac{{218 \pm 5.25}}{{52 \pm 1.89}}$ | 72.7 | $\frac{{2.8 \pm 0.12}}{{45 \pm 1.43}}$ | $\frac{{3.9 \pm 0.058}}{{62 \pm 1.98}}$ | 325 |
| 5 ОДК | $\frac{{662 \pm 10.17}}{{56 \pm 1.75}}$ | 552 | $\frac{{724 \pm 16.33~}}{{62 \pm 2.33}}$ | 122 | $\frac{{279 \pm 3.48}}{{41 \pm 1.28}}$ | 558 | $\frac{{360 \pm 6.12}}{{53 \pm 1.85}}$ | 120 | $\frac{{4.8 \pm 0.15}}{{47 \pm 1.42}}$ | $\frac{{6.5 \pm 0.082~}}{{63 \pm 2.11}}$ | 542 |
| 10 ОДК | $\frac{{1754 \pm 19.33}}{{77 \pm 2.22}}$ | 1462 | $\frac{{1835 \pm 33.44}}{{81 \pm 3.35}}$ | 296 | $\frac{{669 \pm 6.33}}{{50 \pm 1.24}}$ | 1338 | $\frac{{810 \pm 9.12}}{{61 \pm 1.65}}$ | 270 | $\frac{{15.8 \pm 0.53}}{{78 \pm 2.21}}$ | $\frac{{17.6 \pm 0.73~}}{{87 \pm 2.22}}$ | 1467 |
| Вариант | Zn | Pb | Cd | Вариант | Zn | Pb | Cd | Вариант | Zn | Pb | Cd |
| AAБ | Кс | 1 М НNO3 |
AAБ | Кс | 1 М НNO3 |
AAБ | Кс | 1 М НNO3 |
|||
| Каштановая почва | |||||||||||
| Контроль | $\frac{{1.4 \pm 0.01}}{{13 \pm 0.017}}$ | 1 | $\frac{{8.3 \pm 0.56}}{{17 \pm 1.11}}$ | 1 | $\frac{{0.6 \pm 0.001}}{{3.9 \pm 0.03}}$ | 1 | $\frac{{2.5 \pm 0.021}}{{18 \pm 0.32}}$ | 1 | 0.009 | $\frac{{0.02 \pm 0.00001}}{{15 \pm 0.02}}$ | 1 |
| 1 ОДК | $\frac{{124 \pm 4.21}}{{46 \pm 2.33}}$ | 88.6 | $\frac{{148 \pm 2.28}}{{55 \pm 1.11}}$ | 17.8 | $\frac{{30 \pm 0.89}}{{21 \pm 0.92}}$ | 50 | $\frac{{59 \pm 1.42}}{{41 \pm 1.28}}$ | 23.6 | $\frac{{0.7 \pm 0.012}}{{33 \pm 1.55}}$ | $\frac{{1.2 \pm 0.0009}}{{56 \pm 1.35}}$ | 60 |
| 2 ОДК | $\frac{{257 \pm 5.42}}{{53 \pm 4.45}}$ | 183.6 | $\frac{{301 \pm 3.45}}{{62 \pm 2.41}}$ | 36.3 | $\frac{{85 \pm 2.13}}{{31 \pm 1.28}}$ | 142 | $\frac{{167 \pm 4.23}}{{61 \pm 1.42}}$ | 66.8 | $\frac{{2.1 \pm 0.033}}{{51 \pm 1.12}}$ | $\frac{{2.7 \pm 0.01}}{{65 \pm 2.43}}$ | 135 |
| 3 ОДК | $\frac{{411 \pm 6.82}}{{58 \pm 1.89}}$ | 294 | $\frac{{519 \pm 5.22}}{{73 \pm 1.82}}$ | 62.5 | $\frac{{210 \pm 5.32}}{{52 \pm 2.32}}$ | 350 | $\frac{{257 \pm 3.42}}{{64 \pm 2.12}}$ | 103 | $\frac{{3.7 \pm 0.022}}{{60 \pm 1.22}}$ | $\frac{{4.3 \pm 0.02}}{{70 \pm 1.88}}$ | 215 |
| 5 ОДК | $\frac{{716 \pm 9.13}}{{62 \pm 3.62}}$ | 511 | $\frac{{950 \pm 18.33}}{{83 \pm 2.11}}$ | 114.5 | $\frac{{368 \pm 5.32}}{{55 \pm 2.13}}$ | 613 | $\frac{{451 \pm 4.15}}{{68 \pm 2.18}}$ | 180 | $\frac{{6.9 \pm 0.042}}{{67 \pm 1.42}}$ | $\frac{{7.3 \pm 0.56}}{{72 \pm 3.21}}$ | 365 |
| 10 ОДК | $\frac{{1839 \pm 19.44}}{{82 \pm 2.42}}$ | 1314 | $\frac{{2012 \pm 50.22}}{{90 \pm 2.21}}$ | 242 | $\frac{{824 \pm 8.32}}{{63 \pm 2.32}}$ | 1373 | $\frac{{909 \pm 8.12}}{{69 \pm 2.17}}$ | 363 | $\frac{{15 \pm 0.12}}{{74 \pm 1.88}}$ | $\frac{{15.4 \pm 0.82}}{{76 \pm 2.82}}$ | 770 |
| Полиэлементное загрязнение | |||||||||||
| 1 ОДК | $\frac{{181 \pm 5.4}}{{67 \pm 2.00}}$ | 129 | $\frac{{211 \pm 6.23}}{{79 \pm 2.28}}$ | 25.4 | $\frac{{88 \pm 2.22}}{{47 \pm 2.17}}$ | 146 | $\frac{{94 \pm 2.88}}{{65 \pm 1.88}}$ | 37.6 | $\frac{{1.1 \pm 0.001}}{{52 \pm 2.32}}$ | $\frac{{1.4 \pm 0.007}}{{66 \pm 2.63}}$ | 70 |
| 2 ОДК | $\frac{{329 \pm 7.3}}{{68 \pm 2.12}}$ | 235 | $\frac{{382 \pm 7.11}}{{78 \pm 2.46}}$ | 46 | $\frac{{155 \pm 4.12}}{{56 \pm 1.6}}$ | 258 | $\frac{{184 \pm 3.42}}{{67 \pm 2.12}}$ | 73.6 | $\frac{{2.5 \pm 0.05}}{{60 \pm 1.98}}$ | $\frac{{3 \pm 0.12}}{{73 \pm 2.92}}$ | 150 |
| 3 ОДК | $\frac{{529 \pm 8.6}}{{75 \pm 2.13}}$ | 378 | $\frac{{561 \pm 5.32}}{{79 \pm 2.55}}$ | 67.6 | $\frac{{256 \pm 5.26}}{{63 \pm 2.45}}$ | 427 | $\frac{{284 \pm 5.12}}{{70 \pm 2.42}}$ | 113.6 | $\frac{{4 \pm 0.12}}{{65 \pm 2.33}}$ | $\frac{{4.8 \pm 0.28}}{{78 \pm 2.55}}$ | 240 |
| 5 ОДК | $\frac{{900 \pm 10.25}}{{78 \pm 2.25}}$ | 643 | $\frac{{928 \pm 8.43}}{{81 \pm 2.82}}$ | 111.8 | $\frac{{441 \pm 8.42}}{{66 \pm 2.52}}$ | 735 | $\frac{{482 \pm 7.43}}{{72 \pm 2.39}}$ | 192.8 | $\frac{{7.3 \pm 0.21}}{{72 \pm 2.45}}$ | $\frac{{8.1 \pm 0.32}}{{80 \pm 3.12}}$ | 405 |
| 10 ОДК | $\frac{{1889 \pm 21.22}}{{84 \pm 2.35}}$ | 1349 | $\frac{{2047 \pm 42.45}}{{91 \pm 2.36}}$ | 246.6 | $\frac{{956 \pm 10.13}}{{73 \pm 2.44}}$ | 1593 | $\frac{{1023 \pm 12.45}}{{78 \pm 2.21}}$ | 409 | $\frac{{16.2 \pm 0.56}}{{80 \pm 2.62}}$ | $\frac{{18 \pm 0.89}}{{89 \pm 3.03}}$ | 900 |
Следует отметить, что доля подвижных соединений в загрязненной дерново-подзолистой почве была больше, чем в серой лесной почве, несмотря на более низкое общее содержание ТМ. Доля подвижных соединений в каштановой почве была выше, чем в черноземе, при одинаковом уровне загрязнения этих почв, что свидетельствует о большей устойчивости чернозема к ТМ.
Сравнение содержания подвижных соединений ТМ с ПДК показало, что для всех почв при уровне загрязнения 1 ОДК количество подвижных соединений ТМ превышает этот показатель в 2.5–5 раз. ОДК для валового содержания элементов разработаны с учетом почвенных свойств и логично ожидать, что при валовом содержании 1 ОДК ТМ, содержание подвижных соединений будет равным 1 ПДК. Несоответствие этих показателей для всех ТМ в исследованных почвах свидетельствует о том, что и для подвижных соединений ТМ нормативное содержание зависит от свойств почв. Известно, что токсичность ТМ непосредственно связана с их биологической доступностью почвенным организмам, которая определяется пулом загрязняющих веществ, способных переходить в почвенный раствор. Корневая система растений способна усваивать не только растворимые в воде соединения, но и более прочно связанные, как за счет растворения их корневыми выделениями растений [23], так и в результате адсорбции и избирательного поглощения клеточными стенками [28].
С ростом дозы загрязняющего вещества для всех почв отмечается увеличение подвижности соединений элементов, входящих в его состав, а также доля от валового содержания и, следовательно, растет опасность загрязнения почв и сопредельных сред. Причем соединения Zn и Cd в исследованных почвах более подвижны, чем соединения Pb, что вероятно связано с их более низким сродством к органическому веществу и более высокой растворимостью их соединений. Соединения Pb менее подвижны в почвах вследствие сорбции твердой фазой почвы, образования прочных комплексных соединений с органическим веществом, а также образования труднорастворимых соединений. Несмотря на меньшую подвижность этого элемента, превышение ПДК для подвижных соединений отмечается даже при минимальном уровне загрязнения.
Подвижность Cd, как и других ТМ, в значительной степени зависит от pH, содержания и состава глинистых минералов. В дерново-подзолистой почве со слабокислой реакцией среды подвижность Cd выше, чем в черноземе выщелоченном, серой лесной и каштановой почвах, которые имеют нейтральную и слабощелочную реакцию и большее содержание илистой фракции. Несмотря на низкое содержание в почве, доля Cd, переходящего в вытяжку ААБ, больше, чем Zn и Pb. С увеличением концентрации содержание подвижных форм Cd быстро возрастает.
Следует отметить, что наибольшая подвижность Pb, Zn и Cd отмечается при комплексном загрязнении почв ТМ. Этот факт следует учитывать, так как на практике чаще всего наблюдается полиэлементное загрязнение почв как в случае промышленного, так и транспортного загрязнения.
Основой для ландшафтно-геохимической оценки загрязнения почв является коэффициент аномалии – отношение среднего содержания металла в загрязненной почве к его фоновому содержанию или местному геохимическому фону [11, 13, 22]. Эти коэффициенты (Кc) были рассчитаны для валового содержания (табл. 3), подвижных и кислоторастворимых соединений в загрязненных почвах (табл. 4). Полученные значения чрезвычайно контрастно отражают различия между загрязненными и незагрязненными почвами. При дозе, равной 1 ОДК, валовое содержание Zn в дерново-подзолистой почве увеличилось в 2.9 раза, а содержание подвижных и кислоторастворимых соединений возросло в 13.7 и 15.5 раз соответственно. Еще более значительное увеличение подвижности металлов наблюдалось с ростом уровня загрязнения почв. Кроме того, при полиэлементном загрязнении почв коэффициенты концентрации подвижных и кислоторастворимых соединений ТМ в 1.5–2 раза выше, чем при монометалльном.
Таким образом, при загрязнении почв наблюдается резкое увеличение подвижности ТМ, которое является наиболее чувствительным диагностическим признаком загрязнения почв. Это подтверждается сравнением значений коэффициентов концентрации металлов для валового содержания и для подвижных соединений. Масштабы изменения подвижности элементов различны, что приводит к изменению соотношения между массами отдельных элементов как в твердой, так и в жидкой фазах почв. Такая перестройка состояния ТМ, несомненно, приведет к изменению их поглощения растениями. Следует отметить, что при полиэлементном загрязнении разница между содержанием подвижных соединений в загрязненных и незагрязненных почвах значительно возрастает.
Для оценки уровня загрязнения почв используют разные показатели: один из них – доля подвижных соединений от валового содержания. Для фоновых почв эта доля составляет 2–10%, при уровне загрязнения, равном 1 ОДК, 15–30%, для комплексного загрязнения этот показатель увеличивается до 30–40%. При дозе ТМ, равной 10 ОДК, в группу подвижных соединений переходит от 50 до 70% от валового содержания. С увеличением уровня загрязнения растет и доля кислоторастворимых соединений, которая достигает 70–90% при максимальном уровне загрязнения.
Для оценки экологического состояния загрязненных почв предлагаются различные показатели. Например, коэффициент подвижности металлов, показывающий соотношение непрочносвязанных и прочносвязанных соединений ТМ [18]. Предлагается [17] использовать коэффициент защитных свойств почв (КЗ) по отношению к ТМ, который показывает, какая доля металла от его валового содержания в почве находится в недоступной для растений форме:
На примере исследованных почв коэффициент защитных свойств с увеличением уровня загрязнения почв уменьшается от 80–90 до 10–15%.
Все предложенные показатели уровня загрязнения почв являются чувствительными, они объективно отражают изменения в состоянии ТМ в почвах и могут являться характеристикой уровня загрязнения почв. Однако большое разнообразие почвенных свойств, взаимное влияние соединений металлов друг на друга и взаимодействие с компонентами окружающей среды усложняют процедуру нормирования.
Наибольшей миграционной способностью обладают растворимые в воде соединения ТМ, поэтому для определения возможностей миграции элементов из загрязненных почв в открытые водоемы или грунтовые воды необходимо использовать информацию о содержании элементов в водной вытяжке из почв, или в почвенном растворе. Результаты опыта показали, что, несмотря на высокий уровень загрязнения почв, в водную вытяжку переходит лишь незначительная часть ТМ в соответствии с растворимостью их соединений и константами устойчивости комплексов [7, 16] (табл. 5). Это явление связано с тем, что ТМ прочно сорбируются минеральными и органическими компонентами почв, а также находятся в форме малорастворимых соединений. С увеличением уровня загрязнения почв увеличивается и концентрация загрязняющих веществ, способных переходить в водные среды. Коэффициенты корреляции между валовым содержанием ТМ и их содержанием в водных вытяжках достаточно высоки и равны 0.90–0.96. В реальных условиях миграция ТМ в водные среды может происходить более интенсивно за счет поверхностного и латерального стока, а также при изменении условий увлажнения и снижении окислительно-восстановительного потенциала [4, 21, 26].
Таблица 5.
Содержание Pb, Zn и Cd в водных вытяжках из почв, мг/л
| Вариант | Pb | Zn | Cd |
|---|---|---|---|
| Дерново-подзолистая почва | |||
| Контроль | $\frac{{0.004}}{{0.001}}$ | $\frac{{0.137}}{{0.005}}$ | $\frac{{0.002}}{{0.001}}$ |
| 1 ОДК | $\frac{{0.018}}{{0.001}}$ | $\frac{{0.253}}{{0.012}}$ | $\frac{{0.008}}{{0.001}}$ |
| 5 ОДК | $\frac{{0.037}}{{0.007}}$ | $\frac{{0.430}}{{0.022}}$ | $\frac{{0.016}}{{0.001}}$ |
| 10 ОДК | $\frac{{0.042}}{{0.003}}$ | $\frac{{0.486}}{{0.034}}$ | $\frac{{0.023}}{{0.002}}$ |
| Серая лесная почва | |||
| Контроль | $\frac{{0.003}}{{0.001}}$ | $\frac{{0.107}}{{0.012}}$ | $\frac{{0.008}}{{0.003}}$ |
| 1 ОДК | $\frac{{0.009}}{{0.002}}$ | $\frac{{0.230}}{{0.016}}$ | $\frac{{0.009}}{{0.001}}$ |
| 5 ОДК | $\frac{{0.012}}{{0.002}}$ | $\frac{{0.313}}{{0.017}}$ | $\frac{{0.011}}{{0.001}}$ |
| 10 ОДК | $\frac{{0.032}}{{0.003}}$ | $\frac{{0.373}}{{0.046}}$ | $\frac{{0.018}}{{0.002}}$ |
| Чернозем выщелоченный | |||
| Контроль | $\frac{{0.002}}{{0.001}}$ | $\frac{{0.083}}{{0.009}}$ | $\frac{{0.001}}{{0.000}}$ |
| 1 ОДК | $\frac{{0.005}}{{0.002}}$ | $\frac{{0.150}}{{0.022}}$ | $\frac{{0.005}}{{0.001}}$ |
| 5 ОДК | $\frac{{0.007}}{{0.002}}$ | $\frac{{0.293}}{{0.012}}$ | $\frac{{0.007}}{{0.002}}$ |
| 10 ОДК | $\frac{{0.016}}{{0.002}}$ | $\frac{{0.032}}{{0.012}}$ | $\frac{{0.011}}{{0.002}}$ |
| Каштановая почва | |||
| Контроль | $\frac{{0.005}}{{0.001}}$ | $\frac{{0.033}}{{0.001}}$ | $\frac{{0.001}}{{0.001}}$ |
| 1 ОДК | $\frac{{0.008}}{{0.001}}$ | $\frac{{0.177}}{{0.012}}$ | $\frac{{0.002}}{{0.001}}$ |
| 5 ОДК | $\frac{{0.011}}{{0.002}}$ | $\frac{{0.247}}{{0.017}}$ | $\frac{{0.004}}{{0.001}}$ |
| 10 ОДК | $\frac{{0.032}}{{0.003}}$ | $\frac{{0.313}}{{0.021}}$ | $\frac{{0.007}}{{0.001}}$ |
Несмотря на то, что показатели химического состояния почв чутко реагируют на загрязнение, основным критерием для экологического нормирования является реакция биологических систем на загрязнение. Определение концентраций загрязняющих веществ, которые не нарушают основные экологические функции почв, является основой для разработки критериев качества почв [2, 6, 27, 29, 30 ] . Таким образом, для разработки критериев качества почв необходим системный подход, обеспечивающий уровень безопасного воздействия на живые организмы и качество сопредельных сред.
Оценка биологической активности незагрязненных почв по показателю базального дыхания показала, что максимальная эмиссия СО2 характерна для чернозема выщелоченного, она составляла 2.5 мкмоль/(г сут), для дерново-подзолистой и каштановой почвы – в 3.5–4 раза меньше. Для серой лесной почвы эмиссия СО2 – 2.1, мкмоль/(г сут) (рис. 1). Наименьшие значения эмиссии СО2 получены для каштановой почвы, что объясняется невысоким содержанием органического вещества и менее благоприятными физико-химическими свойствами.
Рис. 1.
Интенсивность эмиссии СО2 при различном содержании тяжелых металлов в дерново-подзолистой (А), серой лесной (Б), черноземе выщелоченном (В) и каштановой (Г) почвах.
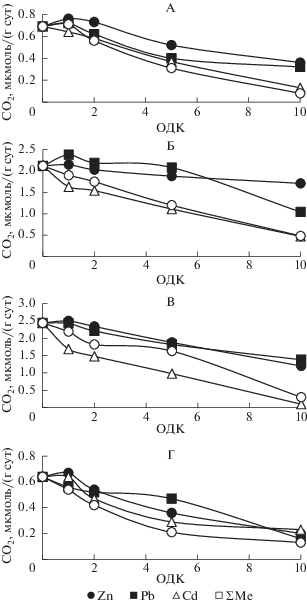
Внесение в почвы ТМ в дозе 1 ОДК вызвало небольшое увеличение интенсивности дыхания при загрязнении почв Zn, а при загрязнении Cd и смесью металлов наблюдали тенденцию к снижению активности дыхания. При увеличении уровней загрязнения отмечено постепенное снижение интенсивности дыхания почв, которое было выражено сильнее при загрязнении почв соединениями Cd и при полиэлементном загрязнении.
При внесении ТМ в дозе 5 ОДК произошло заметное снижение интенсивности дыхания для всех вариантов опыта. Интенсивность дыхания дерново-подзолистой почвы уменьшилась на 30–40% при загрязнении Zn и Pb, на 50–60% при загрязнении Cd и при полиэлементном загрязнении. Для серой лесной почвы, загрязненной соединениями Zn и Pb, интенсивность дыхания снизилась на 25%, а при таком же уровне загрязнения этой почвы Cd и смесью металлов интенсивность дыхания уменьшилась на 50%.
Эмиссия СО2 при загрязнении чернозема в дозе 5 ОДК снизилась на 25% в вариантах с Zn и Pb, а при загрязнении Cd и смесью металлов – на 50%. Дыхание каштановой почвы снизилось на 26–30% при загрязнении Zn и Pb, а минимальная интенсивность дыхания отмечена в вариантах с Cd и смесью металлов, на 55 и 60% соответственно. Следует отметить бóльшую токсичность соединений Cd и смеси металлов для всех почв. Таким образом, для всех исследованных почв при уровне загрязнения, равном 5 ОДК, отмечалось значительное угнетение микробиологической активности. При концентрации загрязняющих веществ, равной 10 ОДК, интенсивность почвенного дыхания была минимальной. Наибольшее снижение (до 80%) наблюдали при загрязнении почв соединениями кадмия и комплексном загрязнении. Наибольшей устойчивостью к загрязнению ТМ обладают чернозем выщелоченный и серая лесная почва.
Фитотестирование часто используется в природоохранной практике для оценки экологического состояния природных сред. Этот показатель характеризует границу, определяющую изменение продуктивности экосистемы, что является существенным для экологической оценки почв. По наблюдениям многих авторов уровень фитотоксичности почв отмечается при более высоких концентрациях ТМ, чем ПДК [15, 16]. Уровень фитотоксичности почв обычно определяют при снижении урожайности сельскохозяйственных растений на 20%.
Результаты вегетационных опытов показали, что концентрации ТМ, оказывающие достоверное негативное воздействие на растения, выявлены при разных уровнях загрязнения для дерново-подзолистой, серой лесной, чернозема выщелоченного и каштановой почв. Различия проявились как по количеству проросших семян, так и по высоте растений и энергии прорастания. Максимальная всхожесть семян горчицы белой была отмечена на черноземе, немного меньше на серой лесной почве, еще меньше на дерново-подзолистой и каштановой почвах. Этот ряд, видимо, отражает естественное плодородие изучаемых почв (рис. 2).
Рис. 2.
Всхожесть Sinapis alba на почвах: дерново-подзолистой (А), серой лесной (Б), черноземе выщелоченном (В) и каштановой (Г).
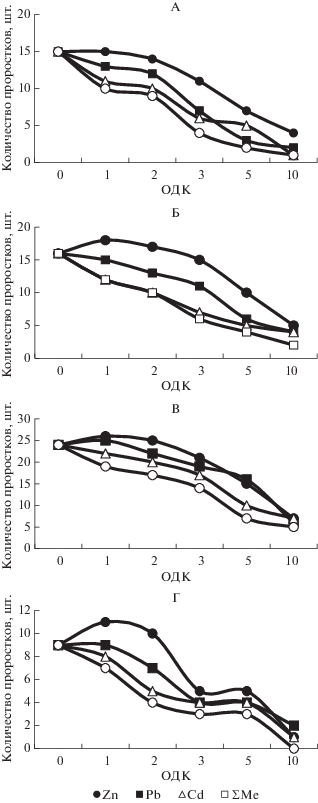
При загрязнении образцов дерново-подзолистой почвы Zn в дозах 1 и 2 ОДК культура росла хорошо, всхожесть была близка к контрольным вариантам, признаков угнетения не наблюдали на протяжении всего периода эксперимента. При уровне загрязнения 3 ОДК количество проростков тест-культуры было меньше, чем на контроле всего на 16%. При концентрации Zn, равной 5 ОДК, отмечали резкое снижение всхожести семян – более чем на 50% по сравнению с контролем. Культура обладала небольшой энергией прорастания, и к концу срока опыта наблюдали почти полное ингибирование роста горчицы. При максимальном уровне загрязнения (10 ОДК) количество проростков было на 74% меньше, чем на контроле. Проростки были ослаблены, характерно замедление роста растения в высоту, и к концу опыта наблюдали гибель растений.
При загрязнении почв Pb в дозах 1 и 2 ОДК признаков угнетения не наблюдали. Однако всхожесть и энергия прорастания были несколько ниже, чем в контрольных вариантах. При дозе 3 ОДК всхожесть была меньше на 40%, чем на контроле. При более высоких концентрациях Pb (5 и 10 ОДК) растения имели угнетенный вид и небольшую биомассу. Количество проростков было на 75% меньше, чем на контроле.
При загрязнении дерново-подзолистой почвы соединениями Cd и смесью металлов достоверное снижение всхожести отмечали уже при дозе 2 ОДК. Всхожесть и энергия прорастания были ниже контроля на 26%. При дозах 5 и 10 ОДК всхожесть горчицы составляла 25% от контроля, а к концу эксперимента происходило практически полное ингибирование тест-культуры, что говорит о высокой токсичности Cd и смеси металлов.
На серой лесной почве тест-культура отличалась высокой всхожестью и энергией прорастания. Наблюдали незначительное стимулирование роста растений при загрязнении почвы в дозах 1 и 2 ОДК Pb и Zn, признаков угнетения тест культуры не зафиксировано в течение всего опыта. При загрязнении почвы, равном 3 ОДК Pb и Zn, наблюдали снижение всхожести растений, а на 30‑й день количество жизнеспособных проростков начало сокращаться.
Наибольший токсический эффект проявлялся при загрязнении почв Cd и смесью металлов. При дозе, равной 2 ОДК, отмечено снижение всхожести на 32 и 41% соответственно по сравнению с контролем. При 5 ОДК наблюдали сильное подавление роста растений и уменьшение всхожести семян более чем в 2 раза при всех типах загрязнения.
На образцах чернозема выщелоченного наблюдали дружное прорастание семян. Всхожесть и энергия прорастания на этой почве были максимальными, а проростки более высокими по сравнению с проростками на других почвах при загрязнении от 1 до 3 ОДК. При дозах 1 ОДК Pb и Zn всхожесть семян была почти 100%, проростки испытывали незначительное стимулирующее действие малых концентраций. В нашем опыте небольшой положительный эффект малых доз был на черноземе и серой лесной почве. Вероятно, это может быть связано с тем, что Pb, связываясь компонентами почвы, вытесняет из органо-минеральных комплексов биофильные элементы, улучшая тем самым питание растений.
Благодаря высокой буферности чернозема токсическое действие ТМ проявлялось только при высоких уровнях их содержания. При загрязнении почв Zn и Pb в дозе 3 ОДК зафиксировано снижение всхожести растений горчицы на 15 и 20% соответственно. При дозе 5 ОДК уменьшение всхожести проростков по сравнению с контролем для Zn и Pb было 33–36% соответственно. Загрязнение чернозема соединениями Cd в дозе 3 ОДК вызвало снижение всхожести горчицы на 21%, а для смеси металлов – 36%. Загрязнение чернозема в дозе 5 ОДК для всех вариантов опыта привело к значительному подавлению роста и развития растений. Особенно отчетливо это проявлялось на почве, загрязненной соединениями Cd и смесью металлов, где количество проростков на 20-й день наблюдения было ниже контроля на 54 и 64% соответственно. При максимальной дозе, равной 10 ОДК, произошло еще большее подавление роста растений (до 70%) на образцах почвы со всеми видами загрязняющих веществ. Следует отметить, что в отличие от других почв даже при таком высоком уровне загрязнения на черноземе полного ингибирования прорастания семян не произошло благодаря высокой его буферности.
На каштановой почве всхожесть и энергия прорастания горчицы были ниже, чем на других почвах. При дозе загрязнения 1 ОДК Zn токсического эффекта не наблюдали, а при 1 ОДК Pb развитие проростков было заторможено, начиная с 20 дня. Уже при 2 ОДК тест-культура начала испытывать угнетение, всхожесть была меньше, чем на контроле, на 29% для Pb, 24% для Zn, 39% для Cd и 41% для комплексного загрязнения. При дозе, равной 3 ОДК, наблюдалось значительное подавление развития растений во всех вариантах опыта. Проростки были слабые, тест-культура начала засыхать на 25-й день наблюдения. Всхожесть семян была ниже, чем на контроле на 53% при загрязнении Pb, на 65% при загрязнении Zn и смесью ТМ и на 71% при загрязнении Cd. При дозах 5 и 10 ОДК на почвах, загрязненных Zn, Pb, Cd или смесью металлов, было отмечено полное ингибирование тест-культуры к концу эксперимента. Каштановая почва обладает меньшим природным плодородием и меньшей устойчивостью к загрязнению ТМ.
Таким образом, для исследованных почв были определены критические уровни загрязнения, оказывающие негативное воздействие на всхожесть и нормальное функционирование растений горчицы белой при разных видах загрязнения. Максимальной всхожестью и энергией прорастания характеризуется тест-культура на черноземе. Наименее устойчивой к загрязнению тяжелыми металлами является каштановая почва, но следует отметить, что уровни загрязнения дерново-подзолистой почвы были в 2 раза ниже, чем для остальных почв. Вероятно, для каштановой почвы нормативный уровень содержания ТМ должен быть ниже, чем для чернозема и серой лесной почвы. Черноземы наиболее устойчивы к загрязнению, вследствие высокой буферности, обусловленной большим содержанием органического вещества, тяжелосуглинистым гранулометрическим составом и нейтральной реакции среды. Полученные данные позволяют расположить почвы по убыванию устойчивости к ТМ в следующий ряд: чернозем выщелоченный, серая лесная, каштановая, дерново-подзолистая почва.
Длина проростков горчицы является чувствительным показателем загрязнения почв ТМ. Даже при дозе 1 ОДК наблюдается некоторое снижение длины проростков, а при дозах 3–5 ОДК отмечается резкое угнетение тест-культуры. Причем при загрязнении почв Cd отмечали пожелтение надземной части растений. Следует отметить, что Cd является наиболее токсичным элементом, который оказывает максимальное угнетающее действие на растения. Загрязнение почв Zn или Pb оказывает меньшее токсическое действие на тест-культуру, чем загрязнение Cd, или смесью ТМ. Возможно, невысокая фитотоксичность Pb связана с наличием действующей в растении системы инактивации элемента, проникающего в корневую систему. Основная часть Pb задерживается в корнях растений, как показано в работах [15, 16].
Важнейшей характеристикой качества растительной продукции является содержание ТМ в биомассе. Поступление ТМ в растения зависит от свойств почв, содержания подвижных соединений металлов и физиологических особенностей растений [15, 16, 19]. Между содержанием металлов в почвах и поглощением их корнями растений существует определенная зависимость (рис. 3). Содержание Zn и Pb в зеленой массе горчицы достигло ПДК при дозе этих элементов в почвах, равной 2 ОДК, несмотря на высокую чувствительность горчицы к загрязнению. Вероятно, это явление связано со строгими нормативами содержания этих элементов в почвах. При загрязнении почв кадмием содержание этого элемента в горчице достигло ПДК для растений при дозе 1 ОДК.
Рис. 3.
Содержание Pb, Zn и Cd в зеленой массе пр-оростков овса, выращенного на дерново-подзолистой (1), серой лесной (2), черноземе выщелоченном (3) и каштановой (4) почвах и ПДК для зерновых культур (5).

Показатели функционирования растений и почвенных микроорганизмов дают различные границы экотоксичности почв, загрязненных ТМ (табл. 6). Снижение всхожести Sinapis alba при загрязнении почв Pb или Zn отмечали при дозах, равных 3 ОДК, а при загрязнении почв Cd или смесью металлов при дозах 2 ОДК. Угнетение почвенного дыхания отмечено при большем уровне загрязнения почв.
Таблица 6.
Биологические показатели экотоксичности почв, загрязненных тяжелыми металлами
| Почва | Показатель экотоксичности почв | Микробиологический показатель | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| уменьшение длины ростков/корней Sinapis alba | уменьшение всхожести Sinapis alba | эмиссия CO2 | ||||||||||
| 20% от контроля | 25% от контроля | |||||||||||
| Pb | Zn | Cd | ∑Ме | Pb | Zn | Cd | ∑Ме | Pb | Zn | Cd | ∑Ме | |
| Дозы тяжелых металлов (кратность ОДК) | ||||||||||||
| Дерново-подзолистая | 2 | 2 | 1 | 1 | 3 | 3 | 2 | 2 | 4 | 3 | 2 | 2 |
| Серая лесная | 2 | 2 | 1 | 1 | 3 | 3 | 2 | 2 | 4 | 4 | 3 | 3 |
| Чернозем выщелоченный | 2 | 2 | 1 | 1 | 3 | 3 | 2 | 2 | 4 | 4 | 3 | 3 |
| Каштановая | 2 | 2 | 1 | 1 | 3 | 3 | 2 | 2 | 3 | 3 | 3 | 3 |
ЗАКЛЮЧЕНИЕ
При загрязнении почв отмечается резкое увеличение подвижности ТМ, которое является наиболее чувствительным диагностическим признаком загрязнения почв. Это подтверждается сравнением значений коэффициентов концентрации металлов для валового содержания и для подвижных соединений. Масштабы изменения подвижности элементов различны, что приводит к изменению соотношения между массами отдельных элементов как в твердой, так и в жидкой фазах почв. Следует отметить, что при полиэлементном загрязнении разница между содержанием подвижных соединений в загрязненных и незагрязненных почвах значительно возрастает.
С ростом дозы загрязняющего вещества для всех почв отмечается увеличение подвижности соединений элементов, входящих в его состав, а также доля от валового содержания и, следовательно, увеличивается опасность загрязнения почв и сопредельных сред. Следует отметить, что наибольшая подвижность Pb, Zn и Cd характерна при комплексном загрязнении почв ТМ. Этот факт следует учитывать, так как на практике чаще всего наблюдается полиэлементное загрязнение почв как в случае промышленного, так и транспортного загрязнения.
Для оценки загрязнения почв используют коэффициент концентрации – отношение среднего содержания металла в загрязненной почве к его фоновому содержанию или местному геохимическому фону [8, 11, 22]. Эти коэффициенты чрезвычайно контрастно отражают различия между загрязненными и незагрязненными почвами. При дозе, равной 1 ОДК, валовое содержание Zn в дерново-подзолистой почве увеличилось в 2.9 раза, а содержание подвижных и кислоторастворимых соединений в 13.7 и 15.5 раз соответственно. Еще более значительное увеличение подвижности металлов наблюдалось с ростом уровня загрязнения почв.
При полиэлементном загрязнении почв коэффициенты концентрации подвижных и кислоторастворимых соединений ТМ в 1.5–2 раза выше, чем при монометалльном.
Основным критерием для экологического нормирования является реакция биологических систем на загрязнение. Определение концентраций загрязняющих веществ, которые не нарушают основные экологические функции почв, является основой для разработки критериев качества почв.
Концентрации тяжелых металлов, способные оказывать достоверное негативное воздействие на растения и почвенную микробиоту, выявлены при разных уровнях загрязнения для дерново-подзолистой, серой лесной, чернозема выщелоченного и каштановой почв. По убыванию устойчивости к ТМ исследованные почвы можно расположить в ряд: чернозем выщелоченный, серая лесная, каштановая, дерново-подзолистая.
Результаты исследований показали, что токсичность соединений ТМ в значительной степени зависит от свойств почвы и чувствительности выращиваемых культур, что необходимо учитывать при разработке любых нормативных показателей.
Показатели функционирования растений и почвенных микроорганизмов дают различные границы экотоксичности почв, загрязненных ТМ. Ингибиpование дыхания исследованных почв наблюдали пpи бóльших дозах ТМ, чем снижение всхожести и длины проростков горчицы белой.
Список литературы
Агрохимические методы исследования почв / Под ред. Соколова А.В. М., 1975. 436 с.
Булгаков Н.Г. Индикация состояния природных экосистем и нормирование факторов окружающей среды. Обзор существующих подходов // Успехи современной биологии. 2002. Т. 122. № 2. С. 115–135.
Виноградов А.П. Геохимия редких и рассеянных элементов почвах. М.: Изд-во АН СССР, 1957.
Водяницкий Ю.Н., Плеханова И.О. Биогеохимия тяжелых металлов в загрязненных переувлажненных почвах (аналитический обзор) // Почвоведение. 2014. № 3. С. 273–282.
Водяницкий Ю. Н. Нормативы содержания тяжелых металлов и металлоидов в почвах // Почвоведение. 2012. № 3. С. 368–375.
Воробейчик Е.Л., Садыков О.Ф., Фарафонтов М.Г. Экологическое нормирование техногенных загрязнений. Екатеринбург: Наука, 1994. 280 с.
Воробьева Л.А. Теория и методы химического анализа почв. М.: Изд-во Моск. ун-та, 1995. 136 с.
Глазовская М.А. Методологические основы оценки эколого-геохимической устойчивости почв к техногенным воздействиям. М.: Изд-во Моск. ун-та, 1997. 102 с.
Гончарук Е.И., Сидоренко Г.И. Гигиеническое нормирование химических веществ в почве. М., 1986. 320 с.
Добровольский В.В. Ландшафтно-геохимические критерии оценки загрязнения почвенного покрова // Почвоведение. 1999. № 5. С. 639–645.
Иващенко К.В., Ананьева Н.Д., Васенев В.И., Кудеяров В.Н., Валентини Р. Биомасса и дыхательная активность почвенных микроорганизмов в антропогенно-измененных экосистемах (Московская область) // Почвоведение. 2014. № 9. С. 1077–1088.
Ильин В.Б. О нормировании тяжелых металлов в почве // Почвоведение. 1986. № 9. С. 90–98.
Ильин В.Б. Буферные свойства почвы и допустимый уровень ее загрязнения тяжелыми металлами // Агрохимия. 1997. № 11. С. 65–70.
Ильин В.Б., Сысо А.И. Микроэлементы и тяжелые металлы в почвах и растениях. Новосибирск: Изд-во СО РАН, 2001. 229 с.
Кабата-Пендиас А., Пендиас Х. Микроэлементы в почвах растениях. М.: Мир, 1989. 439 с.
Карпухин А.И., Бушуев Н.Н. Влияние применения удобрений на содержание тяжелых металлов в почвах длительных полевых опытов // Агрохимия. 2007. № 5. С. 76–84.
Манджиева С.С., Минкина Т.М., Мотузова Г.Н., Головатый С.Е., Мирошниченко Н.Н., Лукашенко Н.К., Фатеев А.И. Фракционно-групповой состав соединений цинка и свинца как показатель экологического состояния почв // Почвоведение. 2014. № 5. С. 632–640.
Плеханова И.О., Кутукова Ю.Д., Обухов А.И. Накопление тяжелых металлов растениями при загрязнении почв осадком сточных вод // Почвоведение. 1995. № 12. С. 1530–1536.
Плеханова И.О., Бамбушева В.А. Экстракционные методы изучения состояния тяжелых металлов в почвах и их сравнительная оценка // Почвоведение. 2010. № 9. С. 1081–1088.
Плеханова И.О. Влияние условий увлажнения на фракционный состав соединений тяжелых металлов в агродерново-подзолистых почвах, загрязненных осадком сточных вод // Почвоведение. 2012. № 7. С. 735–743.
Сает Ю.Е., Ревич Б.А., Янин Е.П. Геохимия окружающей среды. М.: Недра, 1990. 335 с.
Соколова Т.А. Специфика свойств почв в ризосфере: Анализ литературы // Почвоведение. 2015. № 9. С. 1097–1111.
Степанов А.Л., Лысак Л.В. Методы газовой хроматографии в почвенной микробиологии. М.: МАКС Пресс, 2002. 86 с.
Яковлев А.С., Евдокимова М.В. Экологическое нормирование качества почв и управление их качеством // Почвоведение. 2011. № 5. С. 582–596.
Adriano D.C. Trace elements in the terrestrial environment. N.Y.: Springer-Verlag, 1986. 533 p.
Coleman D.C. From peds to paradoxes: linkages between soil biota and their influences on ecological processes // Soil Biol. Biochem. 2008. V. 40. P. 271–289.
Meychik N.R., Yermakov I.P. Ion exchange properties of plant root cell walls // Plant and Soil. 2001. V. 234. P. 181–193.
Schlesinger W.H., Andrews J.A. Soil respiration and global carbon cycle // Biogeochemistry. 2000. V. 48. P. 7–20.
Wang M., Markert B., Shen W., Peng C., Ouyang Z. Microbiol biomass carbon and enzyme activities of urban soils in Beijing // Environ. Sci. Pollut. Res. 2011. V. 18. № 6. P. 958–967.
Дополнительные материалы отсутствуют.


