Почвоведение, 2019, № 12, стр. 1492-1501
Положительные аномалии содержания урана в торфяниках гумидной зоны (обзор)
Ю. Н. Водяницкий a, *, Н. А. Гребенкин b, Д. В. Манахов a, А. В. Сащенко b, В. М. Тюленева b
a МГУ им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
b Всероссийский научно-исследовательский институт минерального сырья им. Н.М. Федоровского
119017 Москва, Старомонетный пер., 31, Россия
* E-mail: yu.vodyan@mail.ru
Поступила в редакцию 09.01.2019
После доработки 20.03.2019
Принята к публикации 29.05.2019
Аннотация
В последние годы геологи обнаружили обогащенные ураном торфяники, которые являются примером эффективной работы природных органогенных геохимических барьеров в гумидной зоне. Отложение урана в торфах идет за счет биоредукции U(VI), который контролируется геохимическими факторами: составом органического вещества и почвенного раствора, редокс-потенциалом среды, способностью иона уранила к комплексообразованию с лигандами. По характеру обогащения ураном торфы можно разделить на две группы: торфяники, обогащенные ураном, привнесенным почвенно-грунтовыми водами, и торфяники, обогащенные ураном из подстилающих, обогащенных ураном, пород. В обзоре собрана и проанализирована информация о географии, генезисе и физико-химических условиях формирования положительных аномалий урана в торфяниках гумидной зоны.
ВВЕДЕНИЕ
Минеральная фаза торфов очень сильно зависит от химического и минералогического состава подстилающих пород. Обеднение или обогащение пород химическими элементами рассматривается как отрицательные (когда их содержание в золе торфа ниже кларка литосферы) или положительные (в противном случае) торфяные аномалии. Породы, обогащенные теми или иными химическими элементами в составе неустойчивых минералов, служат материалом для формирования положительных аномалий близлежащих толщ торфяников.
В практическом и теоретическом отношении особое значение имеют сильные положительные аномалии урана в торфяниках гумидной зоны. Они были обнаружены еще в 50-х гг. прошлого века. В начале 80-х гг. U-торфяник в северо-восточной части штата Вашингтон, США, начали эксплуатировать как источник урановой руды [35]. Геологи-поисковики часто выявляют торфяники с балансовыми содержаниями урана [12, 34, 43].
Открытия геологов могут быть очень полезными для почвоведов-геохимиков, как наглядные примеры эффективной работы природных геохимических барьеров в торфяниках гумидной зоны. Их детальное изучение позволит установить особенности функционирования геохимических барьеров в U-торфяниках. Они могут быть сорбционными, когда уран осаждается за счет сорбции органическими комплексами, восстановительными, когда уран осаждается в минеральных фазах U(IV), или смешанными с осаждением урана в различных формах.
Цель работы – собрать и проанализировать информацию о географии, генезисе и физико-химических условиях формирования сильных положительных аномалий урана в торфяниках гумидной зоны и их возрасте.
ГЕНЕЗИС УРАНСОДЕРЖАЩИХ ТОРФОВ
Геологи оценивают мощность положительных аномалий урана в торфяниках по запасам в них урана, выражая ее в тоннах U на месторождение.
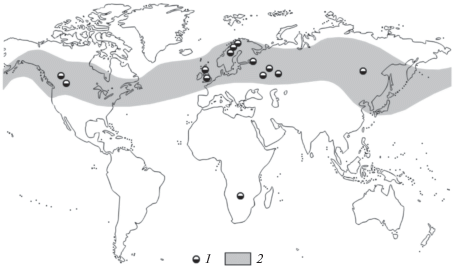
В Российской Федерации и других странах северного полушария поверхностные урановые месторождения располагаются исключительно в гумидной климатической зоне. Запасы урана в месторождениях гумидных районов США, Швеции и Великобритании колеблются от 100 кг в тонком слое обогащенных органическим веществом почв вблизи ураноносного родника до 500 т в минерализованных долинных осадках (в расчете на оконтуренное месторождение). На рис. 1 показано положение некоторых сильных положительных аномалий урана в торфах гумидной зоны Земли.
Рис. 1.
Схема размещения поверхностных месторождений мира по [12]. Условные обозначения: (1) торфяники и обогащенные органическими остатками озерно-аллювиальные отложения; (2) гумидная климатическая зона Земли.
Для геохимиков более привычна форма оценки положительных аномалий (урана или других элементов) в виде концентрации элемента в мг/кг и кларка концентрации (КК), то есть отношения содержания элемента в золе к его кларку в литосфере [13]. Кларк урана в литосфере – 2.3 мг/кг [4], в почвах мира – 3.0 мг/кг, среднее содержание урана в почвах Европы – 2.4 мг/кг [27]. Предполагается, что накопление урана идет и в настоящее время, причем этот процесс обратим, и при высыхании болота сухим летом возможно окисление урана и его мобилизация.
По характеру обогащения торфов ураном их можно разделить на две группы. К первой группе относятся торфяники, обогащенные ураном, привнесенным почвенно-грунтовыми водами. Ко второй – торфяники, обогащенные ураном из подстилающих пород. Они могут соседствовать в пределах одного крупного болота [12]. Торфяники первого типа часто образуются на осадочных породах, они характерны для равнинных территорий. Торфяники второго типа обычно образуются на магматических породах, например, на гранитоидах, обогащенных ураном, в горных областях.
Два типа обогащенных ураном торфяников заметно различаются по формам нахождения U. В ураноносных торфяниках, выполняющих роль восстановительного барьера на пути миграции почвенно-грунтовых вод, доминируют ионно-сорбционные формы U в ассоциации с органическим веществом и новообразованные восстановленные соединения урана. В торфяниках, образовавшихся непосредственно на ураноносных породах, помимо упомянутых форм, сохраняются частицы урансодержащих акцессорных минералов, унаследованные от материнской породы.
РОЛЬ РАСТЕНИЙ В НАКОПЛЕНИИ УРАНА В ТОРФАХ
Данные о содержании урана в растениях весьма противоречивы. По Перельману [13], в растениях КК урана равен 0.2. Есть сведения о более сильном поглощении урана растениями: от 0.5 до 4.4 мг U/кг золы [7], то есть КК ~ 1. Согласно сводке Хокса и Уэбба [15], среднее содержание урана в почвах ~1 мг/кг, а в золе растений – 0.6 мг/кг; КК равен 0.6.
Наши данные о содержании урана в торфе, состоящем в основном из мхов, свидетельствуют о нем как элементе среднего биологического накопления. На территории Хибино-Ловозерской провинции КК урана составляет 0.6–0.8 [2], что типично для элементов среднего биологического накопления [13]. Обычно увеличение валового содержания урана в почве ведет к росту его концентрации во мхах [2].
Характерно различие в биофильности урана и другого актинида – тория. Исследования содержания U и Th в горно-луговых и горно-лесных почвах северного Алтая провели Пузанов с соавт. [14]. Отношение Th : U в дерновых и нижележащих горизонтах заметно различается. В дерновых горизонтах оно составляет в среднем 3.1, а в нижних горизонтах – 4.1. Повышенное содержание урана в дерновом горизонте может быть связано с его большим, чем у тория, биологическим поглощением.
Тем не менее, биологический механизм накопления урана на поверхности торфа имеет второстепенное значение по сравнению с его накоплением в придонной части торфяных залежей.
БИОГЕОХИМИЯ УРАНА
Уран имеет переменную валентность, основные степени окисленности +4 и +6. Формы урана (степень окисления и тип лигандов в воде) влияют на физико-химические процессы и подвижность урана в зоне гипергенеза. Это определяет его чувствительность к редокс-условиям среды. В окислительной среде уран присутствует преимущественно в форме иона U(VI) – уранила $\left( {{\text{UO}}_{{\text{2}}}^{{{\text{2}} + }}} \right),$ который подвижен в широком диапазоне геохимических условий [1, 13, 16]. U(VI) редуцируется абиотически или микробиологически до иона U4+, который мало растворим и осаждается из раствора в виде уранинита (UO2) [36] или других, не уранитовых U(IV)-соединений [17]. Они определяют минералогию урана в торфах.
Процесс биоредукции U(VI) контролируется разнообразными геохимическими факторами. Среди них состав органического вещества и почвенного раствора, изменение заряда и окислительно-восстановительного потенциала, способность иона уранила к комплексообразованию с лигандами, а также активность металлоредуцирующих микроорганизмов.
Роль органического вещества
Роль органического вещества в закреплении урана в торфяных почвах очень велика. В особенности важна роль гуматов. Они представляют сложную смесь органических соединений, которые сильно влияют на физические, химические и биологические процессы в почвах [29]. Гуматы содержат обогащенные и обедненные электронами локусы, они ответственны за снабжение электронов и их прием, что делает их очень редокс-активными, способными участвовать в реакциях переноса электрона [24, 29]. Таким образом, гуминовые вещества облегчают перенос электрона от продуктов микробного метаболизма к металлам, в частности, к U(VI) с образованием мало растворимых оксидов (UO2).
Перечислим аспекты влияния органического вещества на накопление урана в торфяной толще.
1. Гумусовые кислоты способны образовывать комплексы с U(VI) [25], способствуя выщелачиванию урана из материнской породы.
2. Доступные микроорганизмам фракции органического вещества, такие как лактат, служат источником энергии, необходимой для восстановления U(VI) до U(IV) [29].
3. Гумусовые кислоты служат в качестве электронного челнока при бактериальной редукции U(VI) [24, 29]. Гуминовые вещества принимают электроны от микробных метаболитов и затем передают их металлам с переменной окисленностью [21, 29]. Бактерии Shawanella alga, Geobacter metallireducens и Geobacteraceae ускоряют перенос электронов урану(VI). Скорость редукции урана значительно повышается при наличии в системе гуминовых веществ.
Некоторые катионы подавляют биологическую редукцию U(VI). Исследовали роль гуматов в лабораторных кинетических опытах в присутствии ионов металлов Ca2+ и Ni2+, которые подавляют биологическую редукцию U(VI) [24]. В сильноанаэробных условиях гуминовые вещества повышают скорость редукции U(VI) до 10 раз и смягчают токсический эффект Ni2+ на микроорганизмы. Гуминовые кислоты более эффективны, чем фульвокислоты в процессах редукции U(VI). Такой эффект приписывают способности гуматов в содействии реакции переноса электрона и образованию комплексов с ионами Ni2+ и Ca2+. Полевые испытания показали существенно возросшую скорость редукции U(VI) после внесения в грунтовые воды гуминовых кислот. Образование комплексов с восстановленным U(IV) увеличивает скорость окисления урана [24].
Роль микроорганизмов-редукторов урана
Редукция урана – это биологический процесс, требующий органического вещества как источника энергии, а также участия биоты, образующей ферменты, действующие как катализаторы восстановительного процесса. Хорошо изучено действие микроорганизмов группы грамотрицательных бактерий Geobacter и Shewanella spp. и грамположительных бактерий Desulfitobacterium spp. В модельном опыте пять разных изолятов Desulfitobacterium spp. редуцировали 100 мкМ U(VI) до U(IV) менее чем за 10 сут, тогда как в абиотическом контроле с убитыми бактериями осадок U(IV) не образовался [22].
Кинетика микробной редукции U(VI) сильно зависит от типа лигандов уранила. Лабильные комплексы уранила (например, “свободный” гидратированный или гидроксид, или органические соединения уранила) представляют биологически доступную фракцию U(VI) [40]. Скорость биоредукции в присутствии растворенного неорганического углерода и Са2+ снижается за счет формирования стабильных Ca-уранил-карбонатных комплексов, которые более устойчивы к редукции и недоступны бактериям из-за слабого сродства к мембране клеток [18, 42].
Токсичность урана к бактериям Shewanella putrefaciens объясняют ингибированием биоредукции в условиях, когда биодоступность U(VI) достигает максимума. Жизнеспособность бактерий S. putrefaciens зависит больше от форм уранила, чем от общей концентрации растворенного урана как токсиканта.
Результаты анализов жизнеспособности бактерий свидетельствуют, что токсичность урана – главная причина прекращения биоредукции при высокой концентрации биодоступных уранил-карбонатных частиц. В определенных геохимических условиях уран становится токсичным для бактерий, что негативно сказывается на его редукции и образовании устойчивых осадков. Хотя некоторые виды бактерий в состоянии сохранять рост клеток, используя U(VI) в качестве терминального акцептора электронов в ходе анаэробного дыхания [30, 38], уран токсичен для многих микроорганизмов [28].
Уранил ${\text{UO}}_{{\text{2}}}^{{{\text{2}} + }}$ наиболее редуцируемая фракция урана в почвенных растворах, но чрезмерно высокая концентрация в растворе биодоступного уранила токсична для ряда бактерий-металлоредукторов [16]. Таким образом, даже в простой системе (в отсутствие других, кроме U(VI), терминальных акцепторов электронов) скорость биологической редукции зависит от геохимии среды, определяющей биологическую доступность и токсичность U(VI).
Так как токсичность металла зависит не от общей концентрации растворенного металла, а от его формы, то токсичность урана для водных организмов связывают с концентрацией в воде ионов UO2+ и UO2OH+ [32, 33].
Такие лиганды, как карбонаты [19, 32, 41], фосфаты [23], сульфаты [32] и растворенный органический углерод [39], уменьшают токсичность урана, уменьшая концентрацию ${\text{UO}}_{{\text{2}}}^{{{\text{2}} + }}$ и UO2OH+. Катионы Ca2+, Mg2+ и H+ снижают токсичность урана за счет конкуренции с комплексами уранила за органические лиганды [16].
ТОРФЯНИКИ, ОБОГАЩЕННЫЕ УРАНОМ, ПРИВНЕСЕННЫМ ПОЧВЕННО-ГРУНТОВЫМИ ВОДАМИ
Содержание урана в ураноносных торфах Швеции, достигающее 30 000 мг/кг (в золе), определяется концентрацией металла в грунтовых и поверхностных водах и количеством органического вещества в осадках [12]. В локальных торфяных аномалиях значение КК достигает 10 000 [35].
Накопление урана происходит не в любых болотах. Это отчетливо видно из сопоставления отношений Th : U в верховых и низинных торфах Томской области [8]. При низком содержании актинидов в верховых торфах (менее 0.4 мг/кг на сухое вещество) среднее отношение Th : U = 4.3, что близко к кларковому отношению. Но в низинных торфах (где актинидов более 0.4 мг/кг на сухое вещество) отношение Th : U резко снижается до 0.44 за счет обогащения ураном. Как правило, уран накапливается в низинных торфах благодаря поступлению из грунтового потока.
Примером U-торфов могут служить залежи торфа в американских штатах Вашингтон и Айдахо. Здесь большая часть низменной территории покрыта ледниковыми, ледниково-аллювиальными и ледниково-озерными осадками со слабым дренажем. U-торфяные почвы образуются в местах, где грунтовые воды, направляющиеся в речные долины, наталкиваются на геохимический барьер, где уран выпадает в осадок [12].
В болотах западной части Сьерры-Невады содержание урана в почвенно-грунтовых водах после прохождения вод через заболоченный луг снизилось в 10 раз [40]. Содержание в торфе урана зависит от размеров “сечения” U-водотока, содержания в нем урана и эффективности захвата урана торфом.
Уран накапливается в придонной части торфа и в подстилающем слое породы, всегда с признаками оглеения. Здесь при полном насыщении водой, благодаря дефициту кислорода, наличию доступного микроорганизмам органического вещества и активности бактерий-металлоредукторов, образуется восстановительный барьер. В результате U(VI) редуцируется до U(IV)-минералов, в которых уран надежно депонирован, но U(IV)-минералы сохраняются в торфе только до его высыхания.
Детальные исследования распределения тяжелых металлов в торфяной толще мощностью 7.5 м в междуречье Оби и Томи показали ведущую роль редокс-зональности в накоплении урана. Ураном обогащен (до 9–10 мг/кг) только придонный слой торфа на глубине 7.0–7.5 м и нижележащий слой оглеенного суглинка на глубине 7.5–8.0 м, тогда как в вышележащей толще торфа его количество было всего 0.07–0.56 мг/кг [6]. Накопление урана авторы справедливо связывают с восстановительными условиями в придонном слое торфа. Отметим, что в болотах провинции Британская Колумбия, Канада основные отложения урана отмечены не на поверхности, а глубже 1.5 м [20].
Редокс-условия в торфяных почвах отличаются сильной временной вариабельностью, что затрудняет выделение окислительных и восстановительных зон в профиле. Но все же прослеживается закономерность: в нижней части толщи условия более восстановительные (здесь и закрепляется уран), чем в верхней части торфа [9]. Восстановительный барьер для урана действует при Eh < 200 мВ при рН > 6, согласно рН ~ Eh диаграмме основных водных комплексов урана. На нем осаждаются U(IV)-минералы, которые выявлены в некоторых U-торфах гумидной зоны [1].
Таким образом, в восстановительной обстановке накопление урана обеспечивается активной ролью анаэробов, в частности, сульфат- и металл-восстанавливающих бактерий с участием органического вещества как источника энергии для редукционных процессов [3, 5].
ТОРФЯНИКИ, ОБОГАЩЕННЫЕ УРАНОМ ИЗ ПОДСТИЛАЮЩИХ U-ПОРОД
Основные литогенные источники урана в торфах гумидных районов – магматические породы, в первую очередь граниты и урансодержащие осадочные породы [12, 26, 37]. Большая часть урановых аномалий приходится на торф, образовавшийся непосредственно на породах, обогащенных ураном: $ \gg $5 мг/кг. Образованию сильных U аномалий в торфах способствуют высокая трещиноватость породы и неустойчивые формы нахождения в ней урана.
В качестве примера рассмотрим распределение содержаний урана в торфах Сиротинка и Орогочи в Витимо-Каренгском районе Забайкальского края. Эти U-торфы образовались прямо на поверхности урансодержащих пород. Основное оруденение формируется в активном почвенно-торфяном слое многолетней мерзлоты, который оттаивает в осенне-летний период. В верхней части разреза находится торф светло- и темно-коричневого цвета с примесью глины и песка.
Минералого-геохимические исследования включали рентгенографический фазовый количественный анализ с использованием дифрактометра X,PertPRO МРD (PANalytical). В целях характеристики микростроения тонкодисперсных минеральных систем, идентификации микрофаз, определения реального состава и строения минералов, а также выявления особенностей их локализации в породах, влияющей на степень извлечения урана, применяли просвечивающую и растровую электронную микроскопию. Использовали растровый электронный микроскоп Tesla ВS-301 (Словения), оснащенный рентгеновским дисперсионным спектрометром, фиксирующим химические элементы начиная с Na и способного определять концентрацию U > 0.8%. Применяли также микрорентгеноспектральный (микрозондовый) анализатор JХА-8100 фирмы JEOL (Япония), с энергодисперсионной приставкой Inca Energy 400 (Оxford Instruments-Великобритания).
Рудная часть представлена поверхностными практически нерадиоактивными рудами с содержаниями урана от первых сотых долей процента до 1–2%. Геохимическую специфику рудоносных почв характеризует ряд тяжелых элементов с концентрациями, превышающими кларки. Максимальное содержание тяжелых элементов, мас. %, в скобках относительно их кларков концентрации в глинистых породах: U ~ 0.3 (774), Mo ~ 0.004 (13.6), Pb ~ 0.004 (2), Th ~ 0.005 (4.3), Сe ~ 0.03 (4.6), Nd ~ ~ 0.006 (2.4); отношение Th : U низкое: 0.02.
Минеральный состав рудной части этих торфяных почв отражает состав материнских гранитоидов – источника U. Почвообразующие минералы здесь представлены в основном кварцем и К–Na полевыми шпатами, содержания которых в сумме достигает ~50% от общей массы почвообразующих минеральных фаз. Глинистые минералы представлены монтмориллонитом (>30%), иллитом (1–5%), хлоритом (1–3%). В U-торфах Сиротинка и Орогочи, наряду с вкраплениями сульфидов, присутствует гетит, что свидетельствует о неравновесной редокс-обстановке.
Определен химический состав нескольких U‑обогащенных включений (табл. 1). Спектр 002: растительные остатки в почвах, обогащенные U. Спектр 006: шаровидное образование, сложенное углистым веществом и слоистыми алюмосиликатами; почвенный рудный горизонт. Спектр 006-а: фрагмент шаровидного образования, сложенного углистым материалом. Спектр 009: контакт пористого углистого материала с тонкозернистым, тонкопластинчатым урансодержащим агрегатом слоистых алюмосиликатов, пропитанным органическим веществом. Спектр 012: остатки бактерий, насыщенные гидроксидами Fe. Спектр 017: органическое вещество, обогащенное U и ассоциированное со слоистыми алюмосиликатами, а также, возможно, с сульфидами. Спектр 020: гелеподобные, каплевидные хорошо растворимые образования, обогащенные U, локализованные на поверхности слоистых алюмосиликатов, обогащенных органическим веществом. Спектр 024: таблитчатая окатанная частица акцессорного монацита, обогащенного Ce, Nd, Th, U. Спектр 026: скорлуповидное образование, сложенное органическим веществом (возможно остатки флоры или фауны) и слоистыми алюмосиликатами, с высоким содержанием U и S.
Таблица 1.
Валовой химический состав урансодержащих включений в торфах Сиротинка и Орогочи, %
| Спектр | O | Al | Si | P | S | K | Ca | Ti | Mn | Fe | Zn | Sn | Ce | Nd | Pb | Th | U |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 002 | 44.05 | 9.84 | 22.39 | –* | 2.13 | 0.81 | 5.58 | 0.65 | – | 6.57 | – | – | – | – | – | – | 7.59 |
| 006 | 47.09 | 16.77 | 22.82 | – | 1.77 | 0.98 | 2.16 | 0.52 | – | 3.99 | – | – | – | – | – | – | 3.91 |
| 006-а | 44.68 | 13.71 | 21.50 | – | 1.38 | 1.05 | 4.30 | – | – | 8.04 | – | – | – | – | – | – | 5.36 |
| 009 | 40.44 | 3.95 | 14.28 | 2.02 | 2.37 | 1.00 | 8.15 | – | – | 25.05 | – | – | – | – | – | – | 2.74 |
| 012 | 35.18 | 4.01 | 7.72 | – | – | – | – | – | – | 53.10 | – | – | – | – | – | – | |
| 017 | 39.82 | 8.09 | 14.61 | 1.53 | 2.11 | 0.42 | 9.08 | 0.60 | 1.16 | 9.44 | 4.11 | – | – | – | – | – | 8.05 |
| 020 | 45.09 | 14.72 | 20.72 | – | 1.48 | 0.37 | 6.32 | – | – | 6.95 | – | – | – | – | – | – | 4.35 |
| 024 | 25.88 | – | 4.28 | 10.23 | – | – | 1.64 | – | – | 0.06 | – | – | 23.51 | 9.46 | 9.39 | 15.56 | |
| 026 | 42.60 | 5.68 | 21.24 | – | 4.21 | 1.55 | 4.48 | – | – | 9.04 | – | – | – | – | – | – | 9.84 |
Как видно из табл. 1, в торфяных почвах сохраняются разнообразные акцессорные минералы, содержащие уран и торий, что подчеркивает унаследованность от материнских гранитоидов. Акцессории представлены сфеном, цирконом, монацитом, рутилом, анатазом, фторапатитом, ильменитом и др. Частицы монацита обогащены Ce до 21.5% и Th до ~8%, содержание U в кристаллах циркона достигает 0.5%.
Как показал электронно-микроскопический анализ, основная часть урана сосредоточена в рентгеноаморфной фазе, связанной с полиэлементными стеклоподобными гелевыми частицами (рис. 2). Уран концентрируется и в растительных остатках, где у органического вещества обычно ячеистая древовидная структура, здесь содержание U достигает 2%. Уран также накапливается в шаровидных образованиях – почвенных конкрециях размером 200–500 мкм, в тонких агрегатах слоистых алюмосиликатов, ассоциированных с пленками органического вещества и иногда вкраплениями сульфидов. В оруднелой части торфа присутствуют также высокодисперсные собственные минералы урана: оксиды урана, нингиоит, реже коффинит, локализующиеся, главным образом, в органо-силикатном аморфном веществе и между чешуйками слоистых алюмосиликатов.
Рис. 2.
Микрофотографии урансодержащих включений в торфах Сиротинка и Орогочи: А – растительные остатки в почвах, обогащенные U (спектр 002); Б – шаровидное образование, сложенное углистым веществом и слоистыми алюмосиликатами; почвенный рудный горизонт (спектр 006); В – фрагмент шаровидного образования, сложенного углистым материалом (спектр 006-а); Г – контакт пористого углистого материала с тонкозернистым, тонкопластинчатым урансодержащим агрегатом слоистых алюмосиликатов (спектр 009), пропитанным органическим веществом; Д – скорлуповидное образование, сложенное углеродистым веществом (возможно, остатки флоры или фауны) и слоистыми алюмосиликатами, с высоким содержанием U и S (спектр 026).

ВОЗРАСТ U-ТОРФОВ
Возраст почв (и торфов, в частности) почвоведы чаще всего определяют радиоуглеродным методом по содержанию изотопов углерода [10]. Для обогащенных ураном торфов открывается возможность независимого определения возраста с помощью 230Th/234U-метода [11, 46].
Датировка по урану широко используется для реконструкции возраста четвертичных морских и земных отложений за последние 500 тыс. лет [27]. Это возможно и для торфов, которые аккумулируют уран при их формировании и затем сохраняются в закрытой системе.
Метод 230Th/234U датировки основан на последовательности радиоактивного распада 238U. Изотоп 238U распадается через различные дочерние радиоактивные продукты до стабильного 206Pb [46].
Геохимические процессы влияют на уран и торий по-разному из-за их химических различий. Уран легко растворяется и попадает в почвенно-грунтовые воды в отличие от тория, который в экзогенных природных условиях не растворим. Происходит геохимическое разделение урана и тория.
Нарушается цепочка распада 238U и геологические часы фиксируют нуль. Начиная с этого момента, 230Th c периодом полураспада 75 380 лет накапливается в результате распада 234U (период полураспада 245 500 лет) [23, 46].
Для применения метода 230Th/234U требуется, чтобы система оставалась закрытой по отношению к обоим элементам в течение всего времени существования. У этого метода, как и любого другого, имеются ограничения: они имеют различную природу. Во-первых, в момент захвата 234U может не находиться в равновесии со своим предшественником 238U. Во-вторых, в процессе формирования торфа в него возможно попадание 230Th, количество которого необходимо учитывать с помощью генетически не связанного с рядом 238U изотопа 232Th. Для учета загрязнения материала 230Th проводят анализ фракций, различающихся по химическим свойствам, и построение изохронной диаграммы в координатах 230Th/232Th–230Th/234U. В-третьих, торф за время своего существования может испытывать периоды осушения, что приводит к увеличению подвижности и выщелачиванию урана.
При использовании α-спектрометрического определения отношений 230Th/234U и 230Th/232Th можно датировать образцы возрастом от нескольких до 350 тыс. лет, а с помощью масс-спектрометрии с термоионизацией – от 10 до 550 тыс. лет [46].
Предполагается, что возраст урановых отложений отвечает началу формирования торфяной толщи. Таким образом, появляется возможность установить возраст U-торфов, что важно для уяснения их генезиса. Фогель и Кронфельд [45] впервые опубликовали результаты датирования по урану возраста серии U-торфов Европы. Ван дер Вейк с соавт. [44] исследовали несколько участков в северо-западной Европе, подтверждая хорошее совпадение радиоуглеродного возраста с возрастом по отношению 230Th/234U. Хейнис и ван дер Плихт [31] получили 230Th/234U-возраст для плейстоценовых торфяных отложений Северной Греции и Ирландии: 122 и 118 тыс. лет соответственно. Кроме того, они показали принципиальную возможность использования 230Th/234U-датировок для открытых систем. Максимов с соавт. [11] получили среднеплейстоценовый возраст (около 200 тыс. лет) торфяных отложений Западной Сибири. Ваас с соавт. [46] показали методом 230Th/234U среднеплейстоценовый возраст (201–227 тыс. лет) для торфяных прослоек из глиняного карьера на севере Германии.
Возраст болот позволяет реконструировать климатические изменения в среднем и верхнем плейстоцене.
ЗАКЛЮЧЕНИЕ
В последние годы геологи обнаружили экстремально обогащенные ураном торфяники, которые могут представлять интерес как источник урановой руды. В теоретическом отношении для почвоведов-геохимиков сильные положительные аномалии урана в торфяниках являются примерами эффективной работы природных органогенных геохимических барьеров в гумидной зоне.
Отложение урана в торфах идет за счет процесса биоредукции U(VI), который контролируется многими геохимическими факторами: составом органического вещества и почвенного раствора, редокс-потенциалом среды, способностью иона уранила к комплексообразованию с лигандами. Особенно значительно влияние органического вещества: гумусовые кислоты способны образовывать комплексы с U(VI), способствуя выщелачиванию урана из материнской породы, доступные микроорганизмам фракции органического вещества служат источником энергии, необходимой для восстановления U(VI) до U(IV), гумусовые кислоты также служат в качестве электронного челнока при бактериальной редукции U(VI). Биота за счет ферментов действует как катализатор восстановительного процесса U(VI).
По характеру обогащения торфов ураном их можно делить на две группы. К первой группе относятся торфяники, обогащенные ураном, привнесенным почвенно-грунтовыми водами. Ко второй – торфяники, обогащенные ураном из подстилающих пород. Торфяники первого типа характерны для равнинных территорий с доминированием осадочных пород. В U-торфяниках, выполняющих роль восстановительного барьера на пути миграции почвенно-грунтовых вод, доминируют U-органические комплексы, а также новообразованные, восстановленные соединения урана. Торфяники второго типа обычно образуются на магматических породах, например, на гранитоидах, обогащенных ураном, в горных областях. В торфах, помимо упомянутых форм, сохраняются частицы урансодержащих минералов, унаследованные от породы.
Открывается также возможность определения возраста этих торфяников на основе метода 230Th/234U отношений.
Список литературы
Водяницкий Ю.Н. Химические аспекты поведения урана в почвах (обзор литературы) // Почвоведение. 2011. № 8. С. 940–952.
Водяницкий Ю.Н., Косарева Н.В., Савичев А.Т. Содержание лантанидов (Y, La, Ce, Pr, Nd, Sm) и актинидов (Th, U) в почвах Хибинско-Ловозерской провинции // Бюл. Почв. ин-та им. В.В. Докучаева. 2010. Вып. 65. С. 75–86.
Гидрогенные месторождения урана / Под ред. А.И. Перельмана. М., 1980.
Гринвуд Н., Эрншо А. Химия элементов. Т. 2. М.: БИНОМ, 2008. 670 с.
Дойникова О.А. Дисперсные минералы урана восстановительной зоны гипрегенеза: минералогия и кристаллохимия. Автореф. дис. … докт. геол.-мин. наук. М., 2005. 24 с.
Ефремова Т.Т., Ефремов С.П., Куценогий К.П., Онучин А.А., Переседов В.Ф. Биогеохимия Fe, Mn, Cr, Ni, Co, Ti, V, Mo, Ta, W, U в низинном торфянике на междуречье Оби и Томи // Почвоведение. 2003. № 5. С. 557–567.
Иванов В.В. Экологическая геохимия элементов. Редкие f-элементы. М.: Экология, 1997. Кн. 6. 607 с.
Инишева Л.И., Шурова М.В., Ларина Г.В., Шагаева Л.Л., Голубина О.А., Езупенок Е.Э. Экологический мониторинг болот Западной Сибири и горного Алтая // Современные проблемы загрязнения почв. III межд. науч. конф. М., 2010. С. 354–358.
Козловский Ф.И. О формах анаэробных процессов в торфянике Центральной Барабы // Теория и методы изучения почвенного покрова. М.: ГЕОС. 2003. С. 299–314.
Макеев А.О. Почвы в геологической истории Земли // Эволюция почв и почвенного покрова М.: ГЕОС, 2015. С. 253–320.
Максимов Ф.Е., Лаухин С.А., Арсланов Х.А., Кузнецов В.Ю., Шилова Г.Н., Чернов С.Б., Жеребцов И.Е., Левченко С.Б. Первая уран-ториевая датировка среднеплейстоценового торфяника в Западной Сибири // Доклады РАН. 2010. Т. 433. № 1. С. 106–110.
Миронов Ю.Б., Лебедева Г.Б., Пуговкин А.А. Поверхностные урановые месторождения гумидной климатической зоны Земли // Региональная геология и металлогения. 2015. № 63. С. 68–76.
Перельман А.И., Касимов Н.С. Геохимия ландшафта. М.: Астрея-2000, 1999. 762 с.
Пузанов А.В., Ельчининова О.А., Рождественская, Т.Д. Радионуклиды в почвах Северного и Центрального Алтая // Геохимия биосферы. М., 2006. С. 299–301.
Хокс Ч.У., Уэбб Дж.С. Геохимические методы поиска минеральных месторождений. М.: Мир, 1964. 486 с.
Behrends T., Van Cappellen P. Competition between enzymatic and abiotic reduction of uranium(VI) under iron reducing conditions // Chem. Geol. 2005. V. 220. P. 315–327. https://doi.org/10.1016/j.chemgeo.2005.04.007
Belli K.M., DiChristina T.J., Van Cappellen P., Taillefert M. Effects of aqueous uranyl speciation on the kinetics of microbial uranium reduction // Geochim. Cosmochim. A-cta. 2015. V. 157. P. 109–124. https://doi.org/10.1016/j.gca.2015.02.006
Bernier-Latmani R., Veeramani H., Vecchia E.D., Junier P., Lezama-Pacheco J.S., Suvorova E.I., Sharp J.O., Wigginton N.S., Bargar J.R. Non-uraninite products of microbial U(VI) reduction // Environ. Sci. Technol. 2010. V. 44(24). P. 9456–9462. https://doi.org/10.1021/es101675a
Brooks S.C., Fredrickson J.K., Carroll S.L., Kennedy D.W., Zachara J.M., Plymale A.E., Kelly S.D., Kemner K.M., Fendorf S. Inhibition of bacterial U(VI) reduction by calcium // Environ. Sci. Technol. 2003. V. 37(9). P. 1850–1858. https://doi.org/10.1021/es0210042
Burgos W.D., McDonough J.T., Senko J.M., Zhang G.X., Dohnalkova A.C., Kelly S.D., Gorby Y. and Kemner K.M. Characterization of uraninite nanoparticles produced by Shewanella oneidensis MR-1 // Geochim. Cosmochim. Acta. 2008. V. 72(20). P. 4901–4915. https://doi.org/10.1016/j.gca.2008.07.016
Burgos W.D., Senko J.M., Dempsey B.A., Rodrn E.E., Stone J.J., Kemner K.M., Kelly S.D. Soil humic acid decreases biological uranium(VI) reduction by Shewanella putrefaciens CN32 // Environ. Engineer. Sc. 2007. V. 24(6). P. 755–761. https://doi.org/10.1089/ees.2006.0009
Carvajal D.A., Katsenovich Y.P., Lagos L.E. The effects of aqueous bicarbonate and calcium ions on uranium biosorption by Arthrobacter G975 strain // Chem. Geol. 2012. V. 330–331. P. 51–59. https://doi.org/10.1016/j.chemgeo.2012.08.018
Cheng H., Edwards R.L., Hoff J., Gallup C.D., Richa-rds D.A., Asmero Y. The half-lives of uranium-234 and thorium-230 // Chem. Geology. 2000. V. 169(1–2). P. 17–33. https://doi.org/10.1016/S0009-2541(99)00157-6
Fletcher K.E., Boyanov M.I., Thomas S.H., Wu Q., Kemner K.M., Loffler F.E. U(VI) reduction to mononuclear U(VI) by Desulfitobacterium species // Environ. Sci. Technol. 2010. V. 44(12). P. 4705–4709. https://doi.org/10.1021/es903636c
Fortin C., Dutel L., Garnier-Laplace J. Uranium complexation and uptake by a green alga in relation to chemical speciation: The importance of the free uranyl ion // Environ. Toxicol. Chem. 2004. V. 23(4). P. 974–981. https://doi.org/10.1897/03-90
Francis A.J., Dodge C.J. Bioreduction of uranium(VI) complexed with citric acid by clostridia affects its structure and solubility // Environ. Sci. Technol. 2008. V. 42(22). P. 8277–8282. https://doi.org/10.1021/es801045m
Frechen M., Sierralta V., Oezen D., Urban B. Uranium-series dating of peat from central and Northern Europe // Developments in Quaternary Sciences. 2007. V. 7. P. 93–117. https://doi.org/10.1016/S1571-0866(07)80033-9
Fredrickson J.K., Zachara J.M., Kennedy D.W., Liu C.X., Duff M.C., Hunter D.B., Dohnalkova A. Influence of Mn oxides on the reduction of uranium(VI) by the metal-reducing bacterium Shewanella putrefaciens // Geochim. Cosmochim. Acta. 2002. V. 66(18). P. 3247–3262.
Gu B., Chen J. Enhanced microbial reduction of Cr(VI) and U(VI) by different natural organic matter fractions // Geochim. Cosmochim. Acta. 2003. V. 67(19). P. 3575–3582. https://doi.org/10.1016/S0016-7037(03)00162-5
Gu B., Yan H., Zhou P., Watson D.B., Papk M., Istok J. Natural humics impact uranium bioreduction and oxidation // Environ. Sci. Technol. 2005. V. 39(14). P. 5268–5275. https://doi.org/10.1021/es050350r
Heijnis H., van der Plicht J. Uranium/thorium dating of Late Pleistocene peat deposits in NW Europe, uranium/thorium isotope systematics and open-system behaviour of peat layers // Chemical Geology 1992. V. 94(3). P. 161–171. https://doi.org/10.1016/S0009-2541(10)80001-4
Higgo J., Kinnibugh D., Smith B., Tipping E. Complexation of Co2+, Ni2+, UO2+ and Ca2+ by Humic Substances in Groundwaters // Radiochim. Acta. 1993. V. 61(2). P. 91–104. https://doi.org/10.1524/ract.1993.61.2.91
Idiz E.F., Carlisle D., Kaplan I.R. Interaction between organic matter and trace metals in a uranium rich bog, Kern County, California, USA // Appl. Geoch. 1986. V. 1(5). P. 573–590. https://doi.org/10.1016/0883-2927(86)90065-X
Kabata-Pendias A. Trace elements in soils and Plants. CRC Press. Taylor&Francis Group. L.–N-Y. 2011. 440 p.
Konopka A., Plymale A.E., Carvajal D.A., Lin X.J., McKinley J.P. Environmental controls on the activity of aquifer microbial communities in the 300 area of the Hanford Site // Microb. Ecol. 2013. V. 66(4). P. 889–896. https://doi.org/10.1007/s00248-013-0283-3
Li W.C., Victor D.M., Chakrabarti L. Effect of pH and uranium concentration on interaction of uranium(VI) and uranium(IV) with organic ligands in aqueous solutions // Anal. Chem. 1980. V. 52(3). P. 520–523. https://doi.org/10.1021/ac50053a033
Markich S.J., Brown P.L., Jeffree R.A. The use of geochemical speciation modelling to predict the impact of uranium to freshwater biota // Radiochim. Acta. 1996. V. 74(s1). P. 321–326. https://doi.org/10.1524/ract.1996.74.special-issue.321
Moulin V., Tits J., Quaounian G. Actinide speciation in the presence of humic substances in natural water conditions // Radiochim. Acta. 1992. V. 58–59(1). P. 179–190. https://doi.org/10.1524/ract.1992.5859.1.179
Osterberg R., Shirshova L. Oscillating, nonequilibrium redox properties of humic acids // Geochim. Cosmochim. Acta. 1997. V. 61(21). P. 4599–4604. https://doi.org/10.1016/S0016-7037(97)00266-4
Otton J.K. Surficial Uranium Deposits in the USA, 1984. Surficial uranium deposits, IAEA, Vienna, 1984, IAEA-TECDOC-322. 237 p.
Otton J.K. Surficial Uranium Deposits: Summary and Conclusions. Surficial uranium deposits, IAEA, Vienna, 1984, IAEA-TECDOC-322. 243 p.
Sanford R.A., Wu Q., Sung Y., Thomas S.H., Amos B.K., Prince E.K., Loffler F.E. Hexavalent uranium supports growth of Anaeromyxobacter dehalogenans and Geobacter spp. with lower than predicted biomass yields // Environ. Microbiol. 2007. V. 9(11). P. 2885–2893. https://doi.org/10.1111/j.1462-2920.2007.01405.x
Sani R.K., Peyton B.M., Dohnalkova A. Toxic effects of uranium on Desulfovibrio desulfuricans G20 // Environ. Toxicol. Chem. 2006. V. 25(5). P. 1231–1238. https://doi.org/10.1897/05-401R.1
van der Wijk A., El-Daoushy F., Arends A.R., Mook W.G., Dating peat with U/Th disequilibrium: some geochemical considerations // Chemical Geology. 1986. V. 59. P. 283–292. https://doi.org/10.1016/0168-9622(86)90077-1
Vogel J.C., Kronfeld J. A new method for dating peat // South African J. Sci. 1980. V. 76(12). P. 557–558.
Waas D., Kleinmann A., Lepper J. Uranium-series dating of fen peat horizons from pit Nachtigall in northern Germany // Quarter. Int. 2011. V. 241(1–2). P. 111–124. https://doi.org/10.1016/j.quaint.2010.09.010
Дополнительные материалы отсутствуют.


