Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2019, № 10, стр. 36-41
Исследование химических превращений WF6 на подложке W методом инфракрасной спектроскопии
В. В. Душик 1, *, Н. В. Рожанский 1, Р. Х. Залавутдинов 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Россия
* E-mail: v.dushik@gmail.com
Поступила в редакцию 15.01.2019
После доработки 23.03.2019
Принята к публикации 09.04.2019
Аннотация
Предложена новая методика ИК-спектроскопии для исследования химических превращений газообразного WF6 на поверхности W, нагретой до 860 К в атмосфере водорода и аргона. Наблюдалась слабая хемосорбция WF6 на подложке W. При температурах выше 670 К промежуточными продуктами химического взаимодействия WF6 и W были пента- и тетрафториды вольфрама. Возможно присутствие других низших фторидов вольфрама в форме прочно адсорбированных на поверхности W молекул олигомеров (димеров или тримеров). Адсорбированные слои, сформированные на подложке W в смеси гексафторида вольфрама с водородом и в среде чистого гексафторида вольфрама, идентичны по составу.
ВВЕДЕНИЕ
Химическое газофазное осаждение является перспективным методом для осаждения функциональных покрытий с высокой плотностью, чистотой и контролируемой структурой. Хорошо известные покрытия, содержащие нитриды и карбиды переходных металлов VA группы (главным образом, Ti и V), используют в высокотехнологичных методах механической обработки в качестве покрытий режущих инструментов [1]. Широкое распространение среди низкотемпературных методов получило химическое газофазное осаждение слоев вольфрама из смеси гексафторида вольфрама с водородом.
Как тонкие (толщиной до 1 мкм), так и толстые (свыше 1 мкм) функциональные вольфрамовые покрытия могут быть сформированы посредством низкотемпературного химического газофазного осаждения с использованием процесса восстановления гексафторида вольфрама водородом. Большинство публикаций, касающихся тонких функциональных слоев W, относится к избирательной металлизации кремниевых пластин в микроэлектронике [2]. Вольфрам может быть осажден на кремниевую поверхность интегральной схемы, но он не осаждается на диоксид кремния. Процесс осуществляется в высоком вакууме при низких температурах с целью обеспечения избирательности и малой скорости осаждения.
В настоящее время возникает потребность в осаждении толстых вольфрамовых покрытий. Вольфрам и его покрытия занимают особое место среди материалов дивертора в реакторе ИТЭР [3]. Низкая химическая активность вольфрама в контакте с жидкими теплоносителями, в частности с литием, гелием, натрием и свинцом, допускает его применение в теплообменниках для передачи и преобразования тепловой или ядерной энергии [4, 5].
Как наиболее тугоплавкий металл, вольфрам также используется в высокотемпературных узлах. Осаждая вольфрам на профилированные медные подложки с последующим их растворением, можно получить вольфрамовые изделия сложной геометрии, например, тигли, капилляры и так далее [6].
На основе технологии химического газофазного осаждения вольфрама получили развитие новые направления, такие как кристаллизация сплавов вольфрама с переходными металлами (Ta, V, Nb, Mo, Re), позволяющая улучшить их механические свойства [7], а также синтез твердых покрытий карбидов вольфрама на конструкционных материалах [8, 9].
Ключевыми особенностями осаждения толстых W слоев являются высокая скорость осаждения, низкая температура и отличные физико-механические свойства покрытий (высокая плотность и адгезия). Процесс осаждения осуществляется при общем давлении газовой смеси 0.1–10 кПа и температуре подложки 650–920 К. Представляет практический интерес исследование in situ механизма роста толстых вольфрамовых слоев. Данные о химическом состоянии растущей поверхности имеют фундаментальное значение для выяснения механизма химической газофазной кристаллизации. Брутто-реакция осаждения W может быть записана в виде:
Отсутствие информации о поверхностных стадиях кристаллизации W на подложке вольфрама при восстановлении гексафторида вольфрама водородом препятствует развитию фторидной технологии. Используются различные методы для исследования адсорбированных слоев, которые, однако, адаптированы для высокого вакуума, что не соответствует действительным условиям осаждения вольфрама [10].
В настоящей работе использована методика ИК-спектроскопии для исследования in situ адсорбированных слоев, сформированных как при экспозиции поликристаллического вольфрама в среде WF6, так и при реакции смеси (WF6 + H2) на W подложке.
МЕТОДИКА ЭКСПЕРИМЕНТА
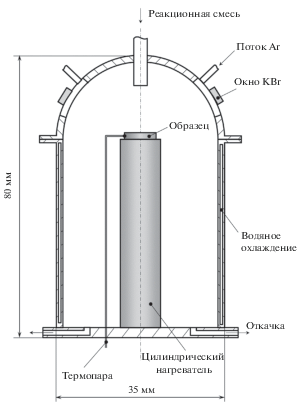
ИК-фурье-спектры с диффузным отражением in situ реакций W–WF6 и W–(WF6 + H2) регистрировали при 50-кратном сканировании с разрешением 2 см–1 в диапазоне 400–4000 см–1 на ИК-спектрометре Perkin Elmer (модель FT-IR 1700X) с помощью специальной ячейки. Схема экспериментальной ячейки показана на рис. 1. ИК-спектры были получены с использованием специальной установки, состоящей из экспериментальной вакуумной камеры, соединенной с установкой газофазного осаждения для контроля параметров процесса. Панель управления установки идентична панели, описанной в [11]. Вакуумная экспериментальная камера представляла собой водоохлаждаемый реактор из нержавеющей стали с внутренним цилиндрическим нагревателем, который позволяет достичь температуры 1300 К. Контроль температуры осуществляли посредством хромель-алюмелевой термопары, которая находилась в непосредственном контакте с образцом. Три окна из KBr (прозрачных для ИК-спектральной области) располагались на крышке камеры под углом 120° друг к другу. Они были защищены от взаимодействия с газообразным гексафторидом вольфрама потоком аргона. Конструкция камеры позволяет проводить юстировку образца в трех измерениях.
ИК-фурье-спектроскопия с диффузным отражением широко применяется для исследования адсорбированных слоев на шероховатой поверхности твердых тел. Простая юстировка оптики и незначительная модификация самого метода позволяют легко получать спектральные характеристики с высокой точностью. В экспериментах использовали вольфрамовые образцы (диаметром 10 мм и толщиной 1 мм), которые очищали в спиртовом растворе и травили в водном растворе HNO3 + HF с целью получения шероховатой поверхности. Затем образцы нагревали в потоке водорода при 1300 К для очистки поверхности от оксидов.
Перед экспериментом и после него записывали ИК-спектры подложки при дозированном напуске аргона в интервале температур 300–900 К. Исследование адсорбированных слоев проводили как при взаимодействии гексафторида вольфрама с подложкой W в потоке аргона, так и в ходе реакции WF6 + H2 + Ar при давлении ~0.1 кПа. Спектры получали и обрабатывали с использованием ИК-спектрометра. Исходные ИК-спектры также включали спектры пропускания газовой среды, которые затем отделяли. После четырех–семи измерений окна KBr заменяли свежими по причине их взаимодействия с газовой смесью, вызывающего изменение фона спектра.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Адсорбция WF6 на подложке W
Исследование адсорбции WF6 на поликристаллической поверхности W проводили следующим образом. После откачки камеры газофазного осаждения при комнатной температуре в течение нескольких часов до базового давления менее 7 × × 10–1 Па в камеру напускали пары WF6 с использованием газа-носителя (Ar). Вольфрамовую подложку не очищали гексафторидом вольфрама перед напуском WF6. На рис. 2а представлен экспериментальный ИК-спектр газообразного вольфрама, в котором наблюдаются только полосы поглощения, характерные для газообразного WF6. Молекула WF6 имеет форму октаэдра, и ее типичный вращательно-колебательный спектр содержит три полосы при 719, 712 и 707 см–1, как и в [12]. Ввиду того, что экспозиция длительная (при уровне 106 Па · с), предполагается, что был установлен адсорбционный баланс между газообразным WF6 и адсорбционным слоем на подложке. Через подложку пропускали газовый поток состава WF6 (30 см3/с, н.у.) + Ar (500 см3/с, н.у.) при комнатной температуре.
Рис. 2.
ИК-спектры газообразного (1) и адсорбированного на W (2) гексафторида вольфрама при комнатной температуре.
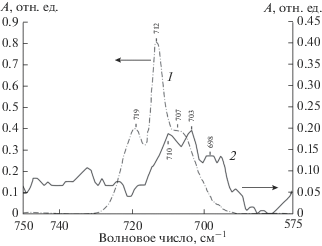
После перекрытия потока WF6 и откачки камеры характерный спектр газообразного WF6 (рис. 2а) исчезал и наблюдался аналогичный спектр, сдвинутый по отношению к предыдущему на 9 см–1 с полосами 710, 703 и 698 см–1. Сдвиги между полосами не изменились, следовательно, октаэдрическая форма молекулы WF6 сохранилась. Сдвиг может быть связан с хемосорбцией WF6 на W подложке и вызван изменением энергии связей W–F по причине ненулевого значения теплоты адсорбции WF6 на W подложке. Необходимо отметить, что интенсивность полос адсорбированного WF6 приблизительно в 10 раз меньше, чем в случае газообразного состояния. Других полос, связанных с расположением гексафторида вольфрама при комнатной температуре, не наблюдалось.
Спектр адсорбированного WF6 практически полностью исчезал после нагрева подложки до 350 К, и других полос в пределах чувствительности спектроскопа не появлялось. Этот факт подтверждает слабую хемосорбцию WF6 на поверхности W, что может быть объяснено отсутствием свободных валентных связей в молекуле гексафторида вольфрама. В соответствии с ИК-анализом WF6, адсорбированный на W подложке, не разлагается при комнатной температуре, и десорбция WF6 происходит в молекулярной форме. Вероятно, газообразный WF6 создает полимолекулярные слои на подложке W в температурном интервале 298–350 К при высоких экспозициях.
Это предположение согласуется с результатом [10], где адсорбцию и десорбцию WF6 на подложке W(100) исследовали методами термодесорбционной спектроскопии и рентгеновской фотоэлектронной спектроскопии. Было показано, что полимолекулярные слои WF6 присутствовали на чистой вольфрамовой поверхности при температуре ниже 150 К, а при температуре ~350 К были обнаружены два адсорбционных состояния, β1-WF6 и β2-WF6, что свидетельствовало о химических связях с поверхностью W. Адсорбция WF6 возрастала на поверхности, частично покрытой атомарным фтором (после нескольких циклов адсорции–десорбции WF6). Энергия сублимации гексафторида вольфрама из полимолекулярных слоев составила 36 ± 4 кДж/моль, что хорошо согласуется со значением 31 кДж/моль, полученным в [12]. Необходимо отметить, что данные результаты справедливы только для умеренных экспозиций (5.3 × 10–8–2.7 × 10–7 Па · с) в сверхвысоком вакууме, так что механизмы распада, десорбции и сублимации WF6 могут отличаться от механизмов, наблюдаемых при больших экспозициях.
Распад WF6 на поликристаллической вольфрамовой подложке, нагретой до 680–860 К, исследовали в потоке гексафторида вольфрама и аргона при соотношении расходов 1 : 10 и общем давлении 1 кПа в течение нескольких минут с последующим удалением WF6 из газовой смеси. Адсорбция WF6 на подложке W, нагретой до 680 К, приводила к появлению сложного спектра адсорбированного слоя (рис. 3а). Расшифровка спектра достаточно сложна, однако, основываясь на экспериментальных и литературных спектроскопических данных, представленных в табл. 1, можно сделать некоторые заключения. Адсорбированный слой состоял из двух низковалентных фторидов, появившихся в результате взаимодействия WF6 с подложкой W. Некоторые спектроскопические полосы, полученные экспериментально, совпадают с теоретическими значениями. Полосы могут соответствовать пентафториду вольфрама (685, 664 и 513 см–1) и тетрафториду вольфрама (721 и 488 см–1). Сдвиг волновых чисел можно объяснить отличием данных от твердых кристаллов фторидов и их адсорбционных слоев.
Рис. 3.
ИК-спектры адсорбционного слоя после обработки вольфрамовой подложки в смеси WF6 + Ar (1) и WF6 + H2 + Ar (2).
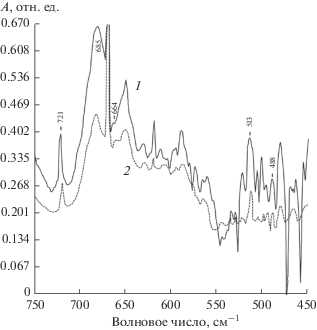
Таблица 1.
Экспериментальные и литературные данные о волновых числах (см–1) молекул фторидов в инфракрасном спектре
| Соединение | Мода | Экспериментальные данные | Литературные экспериментальные данные | Расчетные данные | ||
|---|---|---|---|---|---|---|
| WF6 | υ3 | 712 | 713 [13] | 713 [13] | ||
| 712 [14] | 711 [15] | |||||
| 703* | 712 [16] 711 [17] | |||||
| υ4 | 258 [18] | 259 [19] | ||||
| 258 [17] | 258 [15] | |||||
| 252 [13] | ||||||
| WF5 | υ3 | 685* | 700 [20] | 700 [21] | 680 [19] | 687 [15] |
| υ4 | 513* | 511 [20] | 300 [21] | 260 [19] | 511 [15] | |
| υ5 | 664* | 647 [20] | 650 [21] | 680 [19] | 664 [15] | |
| υ6 | 280 [21] | 260 [19] | 253 [15] | |||
| υ7 | 160 [21] | 110 [19] | 164 [15] | |||
| WF4 | υ3 | 721* | 724 [18] | 730 [21] | 585 [15] | 700 [19] |
| υ4 | 488* | 482 [18] | 180 [21] | 177 [15] | 180 [19] | |
| WF3 | υ1 | 582 [15] | 700 [21] | |||
| υ2 | 244 [15] | 300 [21] | ||||
| υ3 | 549 [15] | 650 [21] | ||||
| υ4 | 197 [15] | 250 [21] | ||||
| WF2 | υ1 | 517 [15] | 670 [21] | |||
| υ2 | 235 [15] | 160 [21] | ||||
| υ3 | 537 [15] | 735 [21] | ||||
| WF | υ1 | 530 [13] | ||||
К сожалению, литературные данные о существовании низших фторидов WF3, WF2 или WF в газообразном или конденсированном состоянии отсутствуют. Однако известно, что низковалентные фториды имеют тенденцию к формированию олигомеров. Димеры W2F10, W2F8 и тример W3F15 обнаружены в газообразной системе W–F; их термохимические константы представлены ранее [22–24]. Часть неидентифицированных полос в ИК-спектре (рис. 3) может быть связана как с адсорбированными низковалентными фторидами, так и с осцилляциями лигандов адсорбированных молекул, что требует дальнейшего исследования.
Интенсивность соответствующих полос незначительно изменяется с увеличением температуры подложки до 860 К. Это свидетельствует о том, что в отличие от гексафторида вольфрама низковалентные фториды прочно хемосорбированы на подложке вольфрама. Это легко объяснить тем фактом, что низковалентные фториды имеют ненасыщенные связи, и поэтому могут сильно хемосорбироваться на твердой поверхности.
Данные [10] о фотоэлектронных спектрах подтверждают, что WF6 диссоциирует на поверхности W(100) при 150 К с образованием адсорбированного WF5 по реакции:
С учетом вышеизложенного можно предложить следующий путь протекания реакции разложения WF6 на поверхности W при температурах ниже 860 К:
Реакция разложения WF6 на поликристаллическом W и W(100)
Вторая часть исследования посвящена качественному анализу состава адсорбированного слоя, возникшего в результате взаимодействия WF6 и H2 на поликристаллических вольфрамовых подложках. При реакции WF6 и H2 на подложке W, нагретой до 680–860 К, наблюдаются все полосы ИК-спектра, обнаруженные при разложении WF6 на вольфрамовой подложке. Спектр адсорбированного слоя, сформировавшегося при соотношении объемных расходов WF6 : H2 : Ar = 1 : 10 : 10, температуре подложки 680 К и общем давлении 0.1 кПа, представлен на рис. 3. Регистрация спектра проходила после удаления водорода и гексафторида вольфрама из газовой фазы. Очевидно, что все полосы, отмеченные на рис. 2, присутствовали и на рис. 3, но с меньшей интенсивностью. Это может быть связано с меньшей концентрацией WF4 и WF5 в адсорбционном слое по сравнению с разложением WF6 без участия водорода на поверхности W. Интенсивность полос падает с повышением температуры подложки, чего не наблюдалось в экспериментах по разложению WF6 без участия водорода.
Анализ спектров показывает, что осаждение вольфрама на растущей поверхности из смеси WF6 с H2 происходит с образованием адсорбированного слоя, состоящего из тонких промежуточных продуктов, таких как пентафторид и тетрафторид вольфрама, адсорбированных на поверхности с высокой энергией адсорбции. Полосы, соответствующие адсорбции водорода на W, не идентифицировали. Однако наблюдалась широкая полоса в интервале 1720–1897 см–1, которая может быть связана с адсорбцией водорода или его соединений с вольфрамом [26]. Эта полоса появляется сразу после напуска смеси WF6 + H2 в реакционную камеру, но при комнатной температуре. Возможно, реакция гексафторида вольфрама с вольфрамом на поверхности способствует адсорбции водорода. Взаимодействие одновременно адсорбированных WF6 и дейтерия на монокристаллической поверхности W(100) в ультравысоком вакууме исследовали методами термодесорбционной спектроскопии и рентгеновской фотоэлектронной спектроскопии [10]. Предполагалось, что адсорбированный дейтерий восстанавливает адсорбированный гексафторид или субфториды, которые сформировались из-за разложения WF6, но фторид водорода не был обнаружен. Потенциальная причина этого явления – тот факт, что энергия активации десорбции водорода меньше энергии активации реакции восстановления WF6 водородом.
С учетом вышесказанного можно предложить следующий путь реакции адсорбированного фтора с газообразным водородом: H2(г) + F(адс) → HF(г) + + H(адс). Согласно [7] скорость этой реакции зависит от парциального давления H2 в газовой фазе и не зависит от адсорбированного водорода.
ЗАКЛЮЧЕНИЕ
Разработана новая методика исследования превращений высокоактивных материалов, таких как галогениды металлов, на подложке вольфрама. Наблюдалась слабая хемосорбция гексафторида вольфрама на поликристаллической подложке W. Низшие фториды вольфрама, напротив, адсорбируются гораздо прочнее, чем гексафторид вольфрама. Адсорбция WF6 при высоких (выше 680 К) температурах на поверхности W приводит к формированию промежуточных продуктов, таких как пента- и тетрафториды вольфрама. Присутствие других низковалентных фторидов вольфрама возможно в виде адсорбированных олигомерных молекул. Состав хемосорбированного слоя, сформированного в процессе осаждения вольфрама из смеси (WF6 + H2), идентичен наблюдаемому при травлении вольфрамовой подложки газообразным гексафторидом вольфрама. Реакция гексафторида вольфрама с водородом на поверхности вольфрама также приводит к формированию пента- и тетрафторидов вольфрама. Предполагается, что путь реакции гексафторида вольфрама с водородом такой же, как при разложении WF6 на поверхности W без участия H2.
Список литературы
Pierson H.O. Hanbook of Chemical Vapor Deposotion (CVD). Principles, Technology and Application. Second Edition. Noyes publications, U.S.A., 1999. 506 p.
Creighton J.R., Parmeter J.R. // Crit. Rev. Solid State Mater. Sci. 1993. V. 18. P. 175.
Ezato K., Suzuki S., Seki Y. et al. // Fusion Eng. Design. 2018. V. 136. P. 683.
Rumbaut N., Casteels F., Brabers M. et al. Material Behavior and Physical Chemistry in Liquid Metal Systems. N.Y.: Plenum Press, 1982.
Merrigan M.A. Space Nuclear Power Systems. Orbit Book Comp., Malabar, FL. 1985.
Красовский А.И., Чужко Р.К., Трегулов В.Р., Балаховский О.А. Фторидный процесс получения вольфрама. Физико-химические основы. Свойства металла. М.: Наука, 1981. 261 с.
Лахоткин Ю.В., Красовский А.И. Вольфрам-рениевые покрытия. М.: Наука, 1989. 158 с.
Lakhotkin Yu.V., Kuzmin V.P. Tungsten Carbide Coatings and Method for Production the Same. Patent US 6.800.383 B1. 2004.
Lakhotkin Yu.V., Kuzmin V.P., Goncharov V.L. // Protection Metals Phys. Chem. Surf. 2009. V. 45. P. 833.
Chen W., Roberts J.T. // Surf. Sci. 1995. V. 324. P. 169.
Goncharov V.L., Lakhotkin Yu.V., Kuzmin V.P. et al. // Adv. Mater. Res. 2009. V. 59. P. 62.
Chase M.W.J., Davics C.A., Downey J.R.J., Frufip D.J., McDonald R.A., Syverud A.N. JANAF Thermochemical Tables. 3rd ed. New York: American Institute of Physics, 1986.
McDowell R.S., Asprey L.B. // J. Mol. Spectr. 1973. V. 48. P. 254.
Burke T.G., Smith D.F., Nielsen A.H. // J. Chem. Phys. 1952. V. 20. P. 447.
Основные свойства неорганических фторидов / Под ред. Галкина Н.П. М.: Атомиздат, 1976. 400 с.
Abramowitz S., Levin I.W. // Inorg. Chem. 1967. V. 6. P. 538.
Claassen H.H., Goodman G.L., Holloway J.H., Selig H. // J. Chem. Phys. 1970. V. 53. P. 341.
Буцкий В.Д., Первов В.С. // Журн. неорг. хим. 1977. Т. 22. С. 14.
Койба В.М., Мальцев А.А. Спектры и структура молекул. М.: Изд. дом МГУ, 1980.
Буцкий В.Д. Химические и структурные превращения низших фторидов молибдена и вольфрама: Автореферат дис. … канд. хим. наук: 02.00.01. М.: ИОНХ, 1979. 25 с.
Hildenbrand D.L. // J. Chem. Phys. 1975. V. 62. P. 3074.
Arara R., Pollard R. // J. Electrochem. Soc. 1991. V. 138. № 5. P. 1523.
Гусаров А.В., Первов В.С., Готкис И.С. и др. // ДАН СССР. 1974. Т. 216. № 6. С. 1296.
Lakhotkin Yu.V. // Thermodynamics. Interaction Studies – Solids, Liquids and Gases / Ed. Moreno-Pirajan J.C. Rijeka: InTech, 2011. P. 1751.
Lakhotkin Yu.V., Kukushkin R.V. // J. de Physique. 1991. V. 7. P. 43.
Jayasooriya U.A., Chesters M.A., Howard M.W. et al. // Surf. Sci. 1980. V. 93. P. 526.
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования