Радиотехника и электроника, 2021, T. 66, № 1, стр. 91-96
Устройство приема сигнала люминесценции для онкофлуориметрии ближнего инфракрасного спектрального диапазона
И. П. Шилов a, *, Г. Л. Даниелян b, С. В. Маречек a, Л. Ю. Кочмарев a
a Фрязинский филиал Института радиотехники и электроники им. В. А. Котельникова РАН
141190 Фрязино, Московской обл., пл. Введенского, 1, Российская Федерация
b Институт общей физики им. А.М. Прохорова РАН
119991 Москва, ул. Вавилова, 38, Российская Федерация
* E-mail: laserlab@ms.ire.rssi.ru
Поступила в редакцию 27.11.2019
После доработки 12.04.2020
Принята к публикации 16.05.2020
Аннотация
Разработано малогабаритное высокочувствительное устройство для приема малого оптического сигнала люминесценции в ближнем инфракрасном (ИК) спектральном диапазоне (900…1100 нм) для лазерной онкофлуориметрии. Устройство состоит из корпуса с оптическими линзами, интерференционными фильтрами и разработанного высокочувствительного в ближнем ИК-диапазоне блока фотодиодного модуля с предусилителем, схемой защиты и блоком питания. Показано, что применение интерференционных фильтров типа SL 930–1100 позволяет существенно повысить эффективность работы всей конструкции в целом. Использование блока фотодиодного модуля, у которого пик чувствительности находится в окрестности 960 нм, что максимально совпадает с пиком люминесценции иттербиевых комплексов порфиринов, обеспечивает чувствительность приема малого сигнала люминесценции на уровне нескольких фемтоватт.
ВВЕДЕНИЕ
С конца 90-х годов ХХ в. в онкологии активно используются возможности люминесцентной диагностики (ЛД) рака, по сути являющейся оптической биопсией [1–3]. Эта диагностика основана на возможности детектирования опухолетропных фотосенсибилизаторов (ФС) по их характерной люминесценции, возбуждаемой излучением определенной длины волны. Для проведения спектрально-флуоресцентных измерений в России к настоящему времени разработаны диагностические установки и флуориметры типа “Спектр-Кластер” и ЛЭСА-01 [4]. Однако имеющиеся в распоряжении врачей спектральные устройства созданы в основном для малоперспективного спектрального диапазона 600…700 нм, часто дающего ложно положительные результаты из-за присутствия в биотканях эндогенных порфиринов. Эта аппаратура работает с ФС типа Фотодитазин, Фотофрин, Аласенс, которые создают при проведении флуоресцентной диагностики опухолей токсичные концентрации синглетного кислорода, разрушающие как больные ткани, так и здоровые. Наиболее перспективным для биомедицинских диагностических исследований является ближний инфракрасный (БИК) спектральный диапазон из-за большей глубины проникновения фотонов через биоткань и минимальной флуоресценции здоровых тканей в этом диапазоне спектра [2]. Флуориметр с его волоконно-оптическим зондом, по сути, является биофотонным локатором, сканирующем поверхность биообъекта. В настоящее время проводятся интенсивные исследования целой парадигмы наноразмерных малотоксичных иттербиевых комплексов порфиринов (ИКП), которые являются весьма перспективными субстанциями для ЛД рака в БИК-области спектра (900…1100 нм). В этом диапазоне с присущим ему так называемым “окном прозрачности” практически отсутствует фоновая люминесценция биотканей, обусловленная наличием в них эндогенных порфиринов. Для данного спектрального диапазона необходима разработка портативного переносного флуориметра, основным элементом которого является устройство приема малого сигнала люминесценции.
Скоординированные исследования специалистов в области оптики, биомедицины, биофотоники и волоконно-оптических устройств позволили разработать малогабаритное, экономически эффективное по себестоимости, высокочувствительное устройство приема сигнала люминесценции (УПСЛ) в БИК-спектральном диапазоне.
1. КОНСТРУКЦИЯ УПСЛ
Конструкция УПСЛ онкофлуориметра для БИК-спектрального диапазона представлена на рис. 1. УПСЛ собран в специальном корпусе, защищенном от электромагнитных помех и от проникновения света. На рис. 2 представлена фотография малогабаритного варианта УПСЛ со снятой крышкой. Функционально онкофлуориметр в общем можно представить в виде четырех основных элементов (рис. 3): блока лазерного возбуждения люминесценции (длина волны 405 нм, мощность оптического излучения до 50 мВт), волоконно-оптического спектрального зонда рефлексного типа, УПСЛ и компьютера с программой обработки и анализа спектральных характеристик.
Рис. 1.
Схема УПСЛ онкофлуориметра БИК-спектрального диапазона: 1 – оптический коннектор волоконно-оптического зонда (выход сигнала люминесценции), 2, 4 – короткофокусные линзы из чистого кварца, 3 – интерференционные фильтры, 5 – стыковочный блок фотодиодного модуля с предусилителем и со схемой оцифровки сигнала (выход на ПК).
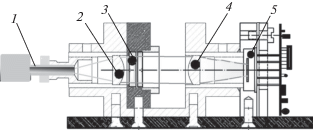
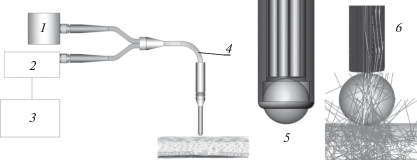
Рис. 3.
Блок-схема онкофлуориметра: 1 – блок лазерного возбуждения люминесценции, 2 – основной блок УПСЛ, 3 – ПК со входом оцифрованного сигнала по каналу USB, 4 – одна из разновидностей волоконно-оптического зонда рефлексного типа со сферической сапфировой линзой, прижатой к поверхности кожи, 5 – увеличенное изображение структуры наконечника зонда, 6 – оптимизация/моделирование картины распространения лучей света на специальной пятислойной модели рассеяния внутри слоев кожи.
Очевидно, что для достижения ряда задач по онкодиагностике в более глубоких мышечных слоях необходимо использование также волоконно-оптических зондов рефлексного типа с применением комбинированных типов оптических волокон, рассчитанных на контроль интенсивности люминесценции с более глубоких слоев биоткани [5]. Разработанный спектральный зонд имеет структуру волоконного жгута с большим количеством волокон, причем для ликвидации паразитного оптического сигнала между волокнами в жгуте типа “кросс-линк” использованы многомодовые кварцевые волокна с металлическим покрытием.
Оптический блок прибора состоит из линз, между которыми смонтированы две ячейки со сменными интерференционными фильтрами (ИФ), диаметром 10…20 мм, толщиной 2…3 мм. Конструкция устройства обеспечивает согласование с числовой апертурой световодов волоконно-оптического зонда (ВОЗ) вплоть до 0.30. Слева через SMA-905-разъем (см. рис. 1) подводятся детектирующие люминесценцию БИК-световоды (содержание в них гидроксил-ионов <1 ppm) многожильного ВОЗ. В правой части устройства размещен блок фотодиодного модуля (ФДМ) с предусилителем и схемой защиты. В блоке ФДМ используется микросхема S8746-01, позволяющая создать ИК-приемник оптимальной чувствительности при заданном быстродействии.
2. РЕЗУЛЬТАТЫ
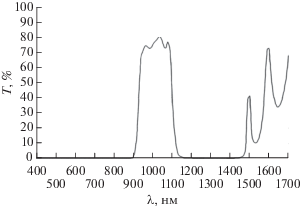
Жесткое размещение в корпусе устройства (см. рис. 1) двух ИФ позволяет существенно повысить надежность и эффективность работы всей конструкции УПСЛ. В качестве ИФ были использованы фильтры типа SL 930-1100. Их спектральные характеристики, выполненные на спектрофотометре “Shimadzu” UV-3600, представлены на рис. 4. Как видно из рис. 4, в оптическом диапазоне 900…1100 нм пропускание может быть вплоть до 80%. При этом степень блокировки возбуждающего излучения составляет не менее 10–4%. Короткофокусные линзы (f ~ 14 мм) позволяют надежно фокусировать малый сигнал люминесценции на активной площадке ФДМ.
Оптический сигнал люминесценции от объекта исследования (био-ткань) поступает посредством ВОЗ через ИФ на оптический вход блока ФДМ. Уровень оптического сигнала чрезвычайно мал. Фотодиод создает фототок на уровне 10–14…10–13 А. Это вызывает большие технические трудности для усиления таких малых уровней сигналов. Одну из основных проблем, которую удалось решить, это оптимизация приемно-усилительного тракта по уровню собственных шумов и создание источников питания блока ФДМ с низким уровнем помех. Шумовые явления бывают трех видов: дробовые шумы, или шумы Шоттки; тепловые шумы, называемые также шумами Джонсона, и фликкер-шумы, т.е. шумы вида 1/f. Эффективное (действующее) значение напряжения теплового шума ${{V}_{{\text{ш}}}}$ можно оценить по формуле Найквиста:
где K – постоянная Больцмана, равная 1.38 × × 10–23 Дж/К; Т – температура в градусах Кельвина; R – сопротивление источника сигнала в омах; ΔF – полоса пропускания в герцах.Эффективное (действующее) значение шумового тока ${{I}_{{\text{ш}}}}$, возникающего в полупроводниках, называется дробовыми шумами, и вызваны они дискретностью переноса зарядов, которое можно оценить по формуле
где q – заряд электрона, равный 1.6 × 10–19 Кл; I – среднее значение постоянного тока в полупроводнике.Анализируя эти выражения, можно видеть, что шум растет с увеличением температуры, тока, протекающего через полупроводник, и с увеличением полосы пропускания.
Кроме того, полупроводниковые усилители имеют низкочастотные шумы, называемые фликкер-шумами, или шумами вида 1/f. Такое название отражает тот факт, что фликкер-шумы обратно пропорциональны частоте, т.е. величина этого вида шума в области нулевой частоты может иметь очень большое значение. Поэтому информационная часть аналогового сигнала в разработанном устройстве преобразуется (переносится по спектру) в область частот, где фликкер-шум не столь велик. Обычно бывает достаточно перенести спектр сигнала из области частот вблизи нуля в область частот до несколько десятков герц. Для переноса спектра и служит операция модуляции сигнала в месте его генерации. В нашем случае это делается путем модуляции мощности лазера меандром, частота которого порядка 30 Гц. Значительное уменьшение уровня тепловой и дробовой составляющих шума можно достичь путем сужения полосы пропускания фотодиодного блока с предусилителем. Этот эффект обусловлен тем, что для получения информации можно использовать только первую гармонику сигнала. Сам сигнал коррелирован (коэффициент корреляции близок к 1) и имеет узкую полосу, а шумы имеют слабую корреляцию (коэффициент корреляции обратно пропорционален полосе частот, занимаемой шумом), поэтому при уменьшении полосы частот мощность первой гармоники сигнала не уменьшается, а шумовая составляющая уменьшается пропорционально корню из полосы частот. Сигнал с выхода фотодиодного блока с предусилителем поступает на синхронный детектор и интегратор, где осуществляется подавление флуктуаций сигнала и ликвидация помех, асинхронных с частотой модуляции.
Конструктивное оформление данного устройства обеспечивает требуемую защиту от электромагнитных помех разной природы происхождения и минимизацию уровня токов утечек путем использования в качестве изоляционного материала фторопласта.
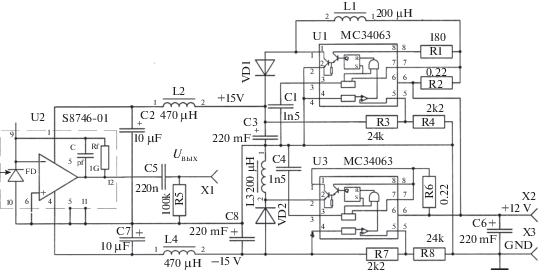
Схема разработанного блока ФДМ с предусилителем, схемой защиты и блоком питания представлена на рис. 5.
Излучение ИК-диапазона поступает через оптический вход микросхемы U2 (S8746-01) на рабочую поверхность фотодиода FD. В корпусе микросхемы интегрированы фотодиод, малошумящий операционный усилитель с очень малым значением входных токов и элементы отрицательной обратной связи операционного усилителя, состоящие из высокоомного резистора R1, номиналом 1 ГOм, и конденсатора C, номиналом 5 пФ, в цепи отрицательной обратной связи. Верхнюю границу полосы пропускания входных сигналов блока ФДМ с предусилителем можно найти по формуле
Для обеспечения максимально возможного значения флотационной чувствительности ФДМ были использованы упомянутые выше значения элементов цепи отрицательной обратной связи. При этом верхнее значение частоты полосы усиления ФДМ составило около 30 Гц. В блоке ФДМ было введено ограничение полосы пропускания цепью R5C5 для частот менее 10 Гц. Это сделано для ликвидации постоянной составляющей выходного сигнала, что обеспечивает работоспособность блока ФДМ в условиях изменчивости температуры и возможной паразитной засветки сторонними источниками света. Чувствительность блока ФДМ по фототоку можно определить по формуле
где Uвых – напряжение на выходе операционного усилителя; R1 – резистор цепи отрицательной обратной связи в операционном усилителе; Iф – ток фотодиода.Питание блока ФДМ осуществляется напряжением 12 В с использованием двух импульсных преобразователей на выходные напряжения, +15 и –15 В. Преобразователи выполнены на основе микросхемы MC34063, работающих на тактовой частоте 100 кГц. Поэтому в схему введены элементы дополнительной фильтрации питающих напряжений дросселями L2, L4 и танталовыми блокировочными конденсаторами с малым значением внутренних сопротивлений. Тактовая частота преобразователей значительно отличается от частоты модуляции, и поэтому с влиянием импульсных помех такой частоты бороться значительно проще, чем в случае применения источников питания с использованием трансформаторов, работающих на частоте 50 Гц.
Кроме перечисленных выше мероприятий по оптимизации методики приема и регистрации сигналов измерения, осуществлены мероприятия по минимизации шумов и помех, возникающих при непрофессиональной прокладке кабелей и жгутов внутри всего прибора. Для минимизации возможных неблагоприятных воздействий статического электричества и минимизации воздействия блуждающих токов, монтаж жгутов и соединений выполнен в полном соответствии с рекомендациями, изложенными в монографии [7].
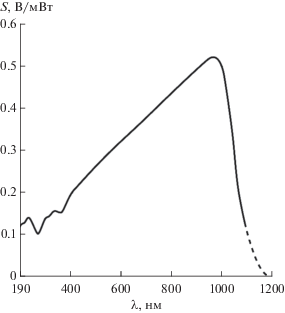
Оптические спектральные характеристики ФДМ с предусилителем представлены на рис. 6. Как видно из данного рисунка, пик чувствительности модуля находится в окрестности 960 нм, что максимально совпадает с пиком люминесценции ИКП [6].
Рис. 6.
Спектральные характеристики ФДМ с предусилителем: S – чувствительность ФДМ (В/Вт × 10–3) при нормальной типовой нагрузке 3 × 103 Ом и температуре 25°С.
Разработанная конструкция УПСЛ имеет следующие характеристики:
| Габариты, мм | 100 × 50 × 40 (без блока питания) |
| Тип интерференционных фильтров | SL 930-1100 |
| Тип микросхемы ФДМ с предусилителем | S8746-01 |
| Пороговая чувствительность устройства, фемтоВт | <10 |
| Длина волны максимальной чувствительности, нм | 960 |
| Рабочий спектральный диапазон, нм | 900…1100 |
| Входное напряжение блока питания ФДМ, B | +12 ± 10% |
| Выходные напряжения блока питания ФДМ, B | +15 ± 2% и –15 ± 2% |
| Максимальные значения выходных значений токов блока питания ФДМ, мА | 2.0 |
| Амплитуда пульсаций выходных напряжений блока питания ФДМ, мВ | 0.1 |
Разработанная конструкция УПСЛ была успешно апробирована в составе БИК-онкофлуориметра в клинике ГНЦ “Лазерная медицина” при проведении процесса люминесцентной диагностики (ЛД) кожных новообразований (кератомы, невусы, базальноклеточный рак кожи и др.), а также слизистых оболочек (вульвогениты, рак шейки матки и др.). Использовался иттербиевый комплекс 2,4-ди(α-метоксиэтил)дейтеропорфирина IX (Yb-ДМДП) в составе геля, который наносился на кожу и слизистые оболочки.
Люминесцентный контрастный индекс (отношение интенсивностей люминесценции больной ткани к соседней здоровой) составлял от 5 до 50 единиц (в зависимости от патологии). При этом минимальная доза Yb-ДМДП при проведении процесса ЛД составила менее 20 мкг/кг веса био-обьекта, что соответствует мировому уровню по чувствительности обнаружения фотосенсибилизатора в биотканях (5…20 мкг/кг).
Совместные исследования, проведенные в РОНЦ им. Н.Н. Блохина, также показали, что степень токсического действия Yb-ДМДП определяется величиной дозы в отношении массы тела. Исследования были проведены на мышах линий ВДF и BALB/C. Эксперименты выполняли в соответствии с международными правилами, изложенными в “Европейской конвенции по защите позвоночных животных, используемых для экспериментов или в иных научных целях” (СЕД 123). Показано, что доза ~100 мг/кг является не токсичной дозой. Таким образом, реально применяемые дозы субстанции Yb-ДМДП являются абсолютно не токсичными.
ЗАКЛЮЧЕНИЕ
Разработан макетный вариант малогабаритного высокочувствительного устройства для приема малого оптического сигнала БИК-люминесценции для лазерного онкофлуориметра, работающего в спектральном диапазоне 900…1100 нм.
Проведена успешная апробация устройства в составе БИК-онкофлуориметра в клинике ГНЦ “Лазерная медицина”.
Разработанное устройство может быть рекомендовано к использованию в клинической практике для оснащения им онкофлуориметров ближнего ИК-спектрального диапазона.
Список литературы
Тучин В.В. Лазеры и волоконная оптика в биомедицинских исследованиях. М.: Физматлит, 2010. С. 478.
Шилов И.П., Иванов А.В., Румянцева В.Д., Миронов А.Ф. Биофизические медицинские технологии / Под ред. А.И. Григорьева, Ю.А. Владимирова. М.: Макс Пресс, 2015. Т. 2. С. 110.
Чиссов В.И., Соколов В.В., Булгакова (Жаркова) Н.Н., Филоненко Е.В. // Рос. биотерапевтич. журн. 2003. Т. 2. № 4. С. 45.
Bulgakova N.N., Kazachkina N.I., Sokolov V.V., Smirnov V.V. // Laser Physics. 2006. V. 16. № 5. P. 889.
Danielyan G., Shilov I., Zamyatin A.A. et al. // Proc. SPIE. 2019. V. 11075. P. 1107515.
Stasheuski A.S., Knyukshto V.N., Ivanov A.V. et al. // J. Appl. Spectroscopy. 2015. V. 81. № 6. P. 938.
Отт Г. Методы подавления шумов и помех в электронных системах. М.: Мир, 1979. С. 317.
Дополнительные материалы отсутствуют.
Инструменты
Радиотехника и электроника