Радиотехника и электроника, 2021, T. 66, № 12, стр. 1233-1239
Особенности работы электронного тракта детектора телевизионного типа на медицинском ускорителе “Прометеуc”
В. В. Сиксин *
Физический институт им. П.Н. Лебедева РАН
119991 Москва, Ленинский просп., 53, Российская Федерация
* E-mail: antktech@yandex.ru
Поступила в редакцию 30.09.2020
После доработки 11.03.2021
Принята к публикации 19.03.2021
Аннотация
Изложен принцип совместной работы цифрового детектора получения изображений и ионизационной падовой камеры (ПК) устанавливаемой перед пациентом в процессе сеанса протонной терапии. Приведены структурные схемы для плат считывающей электроники (СЭ) ПК и общая структурная схема всей СЭ для многофукционалной ионизационной камеры (МИК). Представлены результаты испытания одного канала ПК, входящей в состав МИК, и результаты проверки прототипа МИК от источника гамма-квантов Co60, которые подтверждают квазилинейный вид вольт-амперной характеристики ПК.
ВВЕДЕНИЕ
В данной работе приведено описание разработки электронного тракта для оцифровки сверхмалых зарядов, которые возникают в многоканальной падовой камере (ПК), работающей совместно с детектором телевизионного типа (ДТеТ), применяемым в протонной терапии [1, 2]. Обозначение ДТеТ [1, 2] является формальной аббревиатурой и более правильно его называть – цифровой детектор получения изображений (ЦДПИ). Далее в работе будет использована именно эта аббревиатура.
Разработанная многоканальная ионизационная ПК предназначена для контроля интенсивности пучка на протонном ускорителе “Прометеус” в процессе проведения сеансов терапии. Камера наполняется газом или “теплой жидкостью”. “Теплая жидкость” – это активная среда ПК, в которой при прохождении пучка протонов за спот образуются свободные носители заряда, которые собираются считывающей электроникой ПК. “Теплые жидкости” при комнатной температуре относятся к неполярным диэлектрическим жидкостям и также, как благородные газы (аргон, ксенон), обладают преимуществами перед воздухом или другими газами. В отличие от благородных газов “теплые жидкости” работают в детекторах при комнатных температурах и не требуют применения дорогостоящих криогенных устройств. Так как плотность “теплой жидкости” в 300 раз выше плотности газа или воздуха, то точность измерения дозы (заряда, тока), проходящего через камеру, будет в десятки раз выше, чем у ионизационных камер (ИК), наполненных воздухом или газом. Обычные ИК, наполненные газами, имеют погрешность при измерении дозы около 30%. Погрешность дозиметра складывается из погрешности, вносимой самой камерой, и погрешности электрометра, измеряющего дозу (заряд, ток). Прототип ПК имеет малую погрешность и ввиду отсутствия внутреннего усиления имеет строго линейную зависимость величины измеряемого заряда от плотности дозы пучка, прошедшего через камеру за импульс. В качестве электрометра мы применяли сертифицированный медицинский дозиметр, паспортная точность которого около 15%.
Разработанные нами камеры представлены двумя видами: стриповая камера (СК), в которой анод разделен на полоски (стрипы), определяющие координату (x или y), и ПК. Наши СК и ПК, как и микрополосковые газовые счетчики, газовые электронные умножители, относятся к микроструктурным газовым и жидкостным детекторам (МСГД). Практически все современные детекторные установки крупных физических экспериментов – модернизируемые установки в CERN (ATLAS, CMS, LHCb и ALICE), новые эксперименты CBM на ускорительном комплексе FAIR (Германия) и установки MPD и SPD на коллайдере NICA (Россия) – будут включать в себя до нескольких тысяч каналов МСГД.
ЦДПИ предназначен для калибровки ускорителя перед сеансом протонной терапии. Он позволяет быстро, за несколько выводов (импульсов) ускорителя, точно определить, соответствует ли область энерговыделения пучка нужному месту в мишени, которую задает оператор ускорителя. Преимуществом применения пучков протонов перед электронными пучками является другая физическая природа энерговыделения электронного пучка. Электронный пучок, проходя через здоровые ткани до так называемой “области лечения пациента” (мишени), выделяет большую дозу энергии и поражает здоровые ткани, что приводит у пациента к побочным эффектам после прохождения курса лечения.
Особенность протонного пучка выделять практически всю свою энергию в самом конце своего пути в нужном месте в мишени носит название пика Брэгга. При этом не происходит переоблучения здоровых тканей пациента на пути к мишени.
При облучении области опухоли (мишени) у пациента на протонном терапевтическом ускорителе “Прометеус” обычно используют сканирующий пучок. Дело в том, что пучок должен быстро и равномерно облучить всю мишень пациента, чтобы не вызвать переоблучения остальных тканей и органов пациента. Это можно выполнить в сканирующем режиме, раздробив весь пучок на малые части, которые мы будем называть “долями”. Каждая доля будет облучать свою часть мишени (спот). Сначала долями облучают водный фантом (калибруют ускоритель). При переходе от калибровки с помощью ЦДПИ к установке МИК осуществляют координатную привязку: мишень у пациента должна быть расположена там же, где выделилась энергия в ЦДПИ. Затем ЦДПИ убирают и на его месте располагают нужным образом пациента.
1. ПРИНЦИП СОВМЕСТНОЙ РАБОТЫ ДЕТЕКТОРА ЦДПИ С КАМЕРОЙ ПК
Принцип работы ЦДПИ совместно с камерой ПК заключается в том, что при сканировании каждого спота в водном фантоме ЦДПИ определяет точно координату глубины пика Брэгга и его профиль по ширине, а ПК определяет дозу и число протонов, прошедших через спот за вывод.
На рис. 1 приведена схема совместной работы ЦДПИ и ПК. Детектор ЦДПИ, работающий в режиме сканирующего протонного пучка на ускорителе “Прометеус”, позволяет перед сеансом протонной терапии “откалибровать” ускоритель. Откалибровать – значить проверить, что траектории сканирующего пучка, проходящие через пады, не выходят за границу облучаемой мишени и энергия пучка выделяется внутри мишени. Если это выполняется, то ускоритель настроен правильно и может считаться откалиброванным.
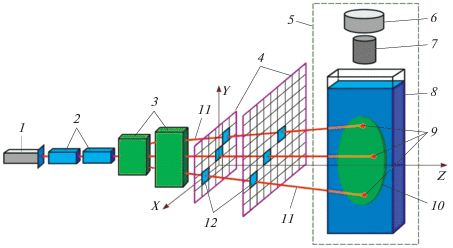
Рис. 1.
Схема совместной работы ЦДПИ с ПК: 1 – ускоритель; 2 – фокусирующие квадрупольные линзы; 3 – сканирующие магниты; 4 – две ПК, определяющие направление пучка протонов на облучаемую мишень; 5 – детектор ЦДПИ; 6 – цифровая камера ЦДПИ; 7 – объектив ЦДПИ; 8 – водный фантом ЦДПИ; 9 – точка остановки пучка в данном споте водного фантома, где выделилась энергия пика Брэгга; 10 – граница области мишени внутри водного фантома, которая облучается сканирующим пучком; 11 – траектория пучка, 12 – пады.
Для испытаний был разработан прототип ПК, представляющий собой ИК с площадью чувствительной области около 2.5 см2, разделенную на пады и предназначенную для проектирования СЭ рабочего варианта ПК и СК. Прототип ПК не только измеряет дозу каждого спота “карандашного” пучка, сканирующего мишень в фантоме детектора ЦДПИ, но и определяет число протонов, прошедших за данный спот в выводе, а также запускает ЦДПИ. Прототип располагается за сканирующими магнитами на расстоянии ~60 см от входа пучка в процедурную комнату, соосно перед ЦДПИ (либо перед пациентом). Сканирующие магниты направляют сходящийся пучок протонов на мишень в водном фантоме детектора ЦДПИ согласно заданной программе. Наполнение ПК “теплой жидкостью” осуществляется на установке, описанной в работе [3]. Кроме “теплой жидкости” тетраметилсилана ПК может наполняться изооктаном. В случае наполнения ПК изооктаном количество заряда, собранное с каждого пада при прочих равных условиях, будет в примерно в четыре раза меньше, чем при использования тетраметилсилана.
2. ВАРИАНТ ИСПОЛНЕНИЯ СЭ ПК НА “ТЕПЛОЙ ЖИДКОСТИ”
В работе использована СЭ прототипа ПК, состоящая из 64-х каналов. Каждый пад прототипа имеет размер 1.98 × 1.98 мм (пады идут с шагом 2 × 2 мм) и является частью анода ПК, на котором регистрируется заряд, подаваемый на СЭ. Диапазон заряда на входе в зарядово-чувствительные предусилители (ЗЧПУ) составляет от 1 до 400 пКл. Так как в самой ПК отсутствует внутреннее усиление, то она обладает линейной зависимостью величины собранного заряда от плотности пучка. При испытаниях одного канала прототипа все 64 пада ПК были объединены в один анодный электрод, что позволило при испытаниях СЭ применить всего один канал ЗЧПУ и УФ.
Ввиду того, что разрабатываемые ПК и СК, входящие в состав камеры многофункциональной ионизационной камеры (МИК), в зависимости от условий применения могут в дальнейшем иметь число каналов 256 и более, был использован подход, в котором вся СЭ выполняется в виде отдельных плат: П1 – плата многоканального электрометра, П2 – плата, запускающая на интегрирование П1, далее плата П3, где располагается программируемая матрица (FPGA), буфер памяти и интерфейсы для связи с компьютером. В варианте прототипа СЭ имеет П1, рассчитанную на 64 канала. Отметим, что известны (см., например, [4, 5]) аналогичные разработки СЭ в микроэлектронном исполнении в виде сложно функциональных специализированных интегральных микросхем, выполненных по современным КМОП-технологиям.
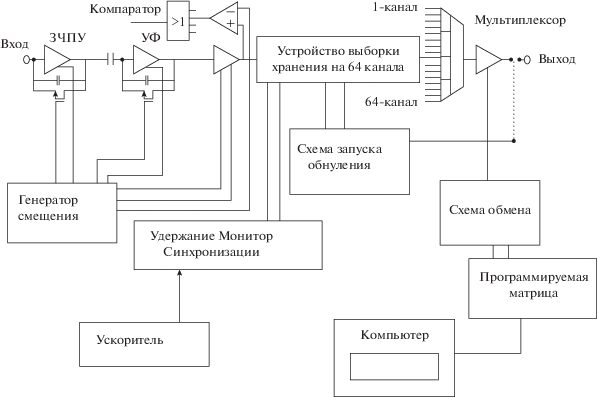
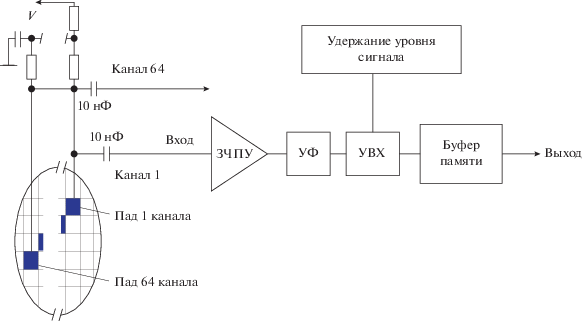
Анализ указанных структурных схем аналого-цифровых устройств [4, 5] привел к выбору схемы СЭ для ПК и СК, показанной на рис. 2. Структурная схема состоит из ЗЧПУ, УФ (медленного шейпера), устройства выборки хранения, компаратора и последующей цифровой обработки. УФ должен иметь фильтрующие каскады по частоте и должен получить отклик с хорошим отношением сигнал/шум. Весь канал должен иметь быстродействие ~1…2 мкс, так как нам необходимо за полный вывод (длительность импульса пучка протонов) ускорителя, составляющий около секунды, “опросить” все облученные за это время споты в мишени, количество которых может составлять около 100. На входе мы используем малошумящий ЗЧПУ с емкостью в цепи обратной связи, который имеет обратную связь по постоянному току для большого снижения коэффициента усиления в области низких частот. Устройство выборки хранения по тактовому сигналу позволяет считывать хранящуюся в ней информацию для оцифровки с помощью АЦП.
Рис. 2.
Структурная схема амплитудного канала СЭ ПК: УФ – усилитель-формирователь, УВХ – устройство выборки хранения.
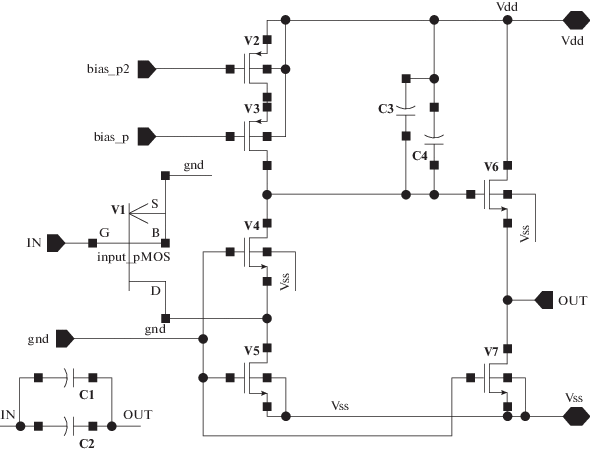
На рис. 3 приведена структурная схема ЗЧПУ из работы [6], который аналогичен используемому нами. Это схема каскода с параллельным питанием на транзисторах V1–V5, причем V1 – это полевой транзистор с малыми токами утечки, а V2, V3 и V5 поддерживают режимный ток и являются источниками динамических нагрузок. Роль каскодного элемента выполняет транзистор V4 для минимизации эффекта Миллера. Второй каскад является истоковым повторителем, построенном на транзисторах V6 и V7, и играет роль усилителя мощности. Чтобы добавить запас по фазе, т.е. подавить колебания в переходном процессе, в схему добавлены конденсаторы С3 и С4.
На рис. 4 приведена структурная схема аналогового канала, используемая в СЭ МИК для прототипа, рассчитанного на 64 канала.
Элементная база позволяет объединить разрозненные электронные блоки, обычно применяемые для выполнения аналогичной задачи, в одно устройство, которое размещается на внешней крышке ПК и на небольшом удалении от ускорителя. Пример использования разрозненных готовых элементов СЭ, которые применялись для решения задачи по регистрации синхротронного излучения, приведен в работе [7]. Предлагаемая СЭ функционально объединяет все перечисленные устройства, применяемые в работе [7], и располагается на корпусе камеры МИК.
3. ЭКСПЕРИМЕНТЫ ПО ТЕСТИРОВАНИЮ ПК
Предварительную проверку каналов прототипа ПК проводили при помощи импульсного рентгеновского источника (ИРИ) [8], который позволяет подводить экспозиционную дозу в чувствительную область ПК. Также было проведено тестирование чувствительной части прототипа ПК площадью 2.5 см2 от источника гамма-квантов Со60.
При проектировании ПК и оценке заряда, собираемого камерой, использовали формулу (2) из работы [8]. Важной характеристикой для “теплых” жидкостей является зависимость собранного с электродов заряда в активной среде ионизационной камеры от дозы ИРИ [8] за один импульс облучения камеры при достаточно большой напряженности поля между электродами. Из работ [9–11] следует, что эта зависимость описывается линейной функцией.
Все расчеты по количеству образования заряда за импульс облучения камеры ПК проводили по приведенной ниже формуле
где Gfi – выход пар свободных ионов; D – поглощенная доза (мР); $~\rho $ – плотность жидкости (г/см3); $v$ – объем измерительной ячейки (см3).Результаты оценки показывают, что ПК на тетраметилсилане и изооктане возможно калибровать и проверять с помощью ИРИ в области поглощенной дозы в диапазоне 0.1…1 cГр.
При проведении эксперимента для каждой экспериментально измеренной точки на рис. 5 подбиралось свое расстояние от ИРИ до ПК, при котором поглощенная доза в ПК составляла за импульс ИРИ от 0.1 до 1 cГр. Условно один импульс ИРИ (экспозиционное время) составлял 60 с.
Рис. 5.
Зависимости накопленного заряда Q от поглощенной дозы D, рассчитанные по формуле (1) (прямые линии) и полученные экспериментально (точки) для изооктана (нижняя кривая) и тетраметилсилана (верхняя кривая).
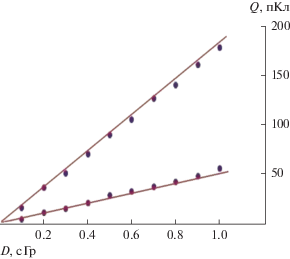
Для расчета по формуле использовали значения величин из табл. 1, где приведено сравнение параметров, наиболее часто применяемых “теплых жидкостей” с высокой степенью очистки [12]. Расчетные кривые и экспериментально измеренные величины заряда, собираемого с ПК при различном уровне поглощенной в камере дозы, приведены на рис. 5. Изменение уровня дозы в камере ПК создавали перемещением ИРИ относительно камеры. Заряд Q измеряли электрометром сертифицированного клинического дозиметра РРС-40.
Таблица 1.
Физические параметры “теплых жидкостей”, используемых в ионизационных камерах
| Жидкость | Тк, °С | ε | μ, см2/(В с) | Gfi | ρ, г/см3 |
|---|---|---|---|---|---|
| Изооктан | 99.24 | 1.936 | 5.3 | 0.33 | 0.69 |
| Тетраметилпентан | 140.3 | 2.05 | 29 | 0.42 | 0.72 |
| Тетраметилсилан | 26.65 | 1.84 | 105 | 0.74 | 0.65 |
| Тетраметилгерманий | 44.0 | 2.01 | 90 | 0.63 | 1.006 |
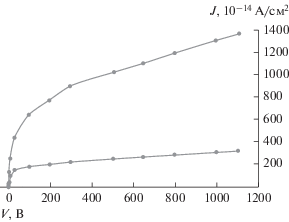
Были также проведены измерения чувствительной области ПК площадью 2.5 см2 от источника гамма-квантов Co60. Передвигая камеру ПК относительно источника гамма-квантов, выбрали две фиксированные мощности дозы фотонного излучения: 24 и 6 мГр/мин за 1 мин. С помощью того же дозиметра измеряли плотность j тока ионизации ПК в зависимости от величины высокого напряжения V, подаваемого на высоковольтный электрод камеры, т.е. фактически измеряли вольт-амперные характеристики структуры (см. рис. 6). Погрешность при измерении экспериментальных точек на рис. 5 и 6 равна погрешности дозиметра, которая по его паспортным данным составляет ±15%. Полученные результаты согласуются с данными работ по камерам на “теплых жидкостях” [11, 12].
ВЫВОДЫ
Проведены испытания прототипа ПК, позволяющие регистрировать мощность дозы излучения проходящего через нее пучка. Предложен вариант СЭ прототипа ПК. Применение ПК позволит улучшить безопасность протонной терапии за счет более точного измерения подводимой высокой дозы к мишени во время сеанса протонной терапии с точностью, рекомендуемой МАГАТЭ [13]. В случае отклонения пучка во время сеанса протонной терапии от области мишени система СЭ ПК будет мгновенно отключать ускоритель, чтобы пучок не повредил здоровые ткани пациента.
Список литературы
Сиксин В.В. // Краткие сообщения по физике ФИАН. 2018. Т. 45. № 12. С. 78. https://doi.org/10.3103/S1068335619010068
Сиксин В.В. // Краткие сообщения по физике ФИАН. 2019. Т. 46. № 2. С. 47. https://doi.org/10.3103/S1068335619020076
Сиксин В.В. // Изв. вузов. Материалы электронной техники. 2019. Т. 22. № 2. С. 118. https://doi.org/10.17073/1609-3577-2019-2-117-126
Baumeister D. Development and Characterization of a Radiation Hard Readout Chip for the LHCb-Experiment. PhD thesis. Heidelberg: Ruperto-Carola Univ., 2003. 196 p. https://inspirehep.net/files/ 29603525aa 5608600d33a0b3002ccb07.
Аткин Э.В., Волков Ю.А., Воронин А.Г. и др. // ПТЭ. 2010. № 4. С. 57.
Cилаев А.С. Аналого-цифровые микроканальные устройства амплитудной обработки сигналов микрополосковых детекторов. Дис. … канд. физ.-мат. наук. М.: НИЯУ “МИФИ”, 2010. 160 с.
Дорохов Д.В., Купер Э. A. // Автометрия. 2015. Т. 51. № 1. С. 92.
Сиксин В.В. // Краткие сообщения по физике ФИАН. 2018. Т. 45. № 7. С. 9. https://doi.org/10.3103/S1068335618070023
Hummel A., Allen A.O. // J. Chem. Phys. 1967. V. 46. № 5. P. 1604.
Schmidt W.F., Allen A.O. // J. Chem. Phys. 1970. V. 52. № 5. P. 2345.
Wickmann G., Nystrom H. // Physics in Medicine and Biology. 1992. V. 37. № 9. P. 1789. https://doi.org/10.1088/0031-9155/37/9/005
Hummel A., Schmidt W.F.// Radiation Research Rev. 1974. V. 5. № 3–4. P. 199.
Серия технических докладов № 398. Международные практические рекомендации по дозиметрии, основанные на эталонах единицы поглощенной дозы в воде. При поддержке IAEA, WHO, PAHO и ESTRO. МАГАТЭ Вена, 2004. https://www-pub.iaea.org/mtcd/publications/pdf/trs398r web.pdf.
Дополнительные материалы отсутствуют.
Инструменты
Радиотехника и электроника