Расплавы, 2020, № 3, стр. 246-257
Экспериментальное изучение процесса плавления минералов и горных пород
Р. Н. Соболев a, В. В. Мальцев a, Е. А. Волкова a, *
a Геологический факультет МГУ им. М.В. Ломоносова
Москва, Россия
* E-mail: el_volkova@rambler.ru
Поступила в редакцию 19.04.2019
После доработки 12.07.2019
Принята к публикации 23.08.2019
Аннотация
Осуществлен теоретический анализ процесса плавления отдельного минерального зерна и полиминеральной горной породы. Показано, что это длительный многостадийный процесс, который реализуется в интервале температур, и начинается в поверхностном слое зерен. Проведены экспериментальные исследования процесса плавления мономинеральных фракций (порошки и зерна) олигоклаза, щелочного полевого шпата и кварца, выделенных из гранитоидов и гнейсов, а также горных пород, из которых были выделены мономинеральные фракции. Показано, что при нагревании горной породы, образующие ее минералы плавятся при разных температурах. Плавление щелочного полевого шпата в образцах горной породы происходит в температурном диапазоне 1000–1160°С. В интервале 1160–1350°С наблюдается взаимодействие расплава щелочного полевого шпата с зернами плагиоклаза и образование макрогомогенного полевошпатового расплава. При T = 1350°С расплав начинает реагировать с зернами кварца. Соответственно, расплавы этих минералов при одной и той же температуре системы разупорядочены в разной степени. Полное плавление образца полиминеральной горной породы происходит при температуре значительно более высокой, чем температура плавления тонко диспергированной шихты того же образца. Рассмотрено два механизма образования расплава. Для отдельного зерна это фазовый переход I рода: поверхностное плавление → объемное плавление. При нагревании полиминеральной горной породы сначала происходит плавление самой низкотемпературной фазы. При повышении температуры расплав низкотемпературной фазы реагирует с поверхностным слоем более высокотемпературных фаз. В результате образуются расплавы промежуточного химического состава, а сам расплав приобретает зональное строение. При нагревании образца горной породы выделено три тренда последовательности образования расплава: тренд в объеме зерна минерала: внешняя → промежуточная → внутренняя части зерна; тренд последовательности перехода в расплав минералов: щелочной полевой шпат → плагиоклаз → кварц; тренд в объеме образца горной породы: внешняя → промежуточная → внутренняя части образца.
ВВЕДЕНИЕ
Установлению параметров образования кремнекислых алюмосиликатных расплавов посвящены многочисленные экспериментальные исследования. Как правило, такие работы выполняются с небольшим объемом тонкодиспергированного материала, а так же принимается, что в процессе проведения эксперимента кристаллический материал и расплав не претерпевают никаких изменений. По поводу таких работ В.А. Жариков отмечал: “При исследовании природных физико-химических процессов наиболее обычным как раз является такое положение, когда известны конечные результаты процесса, можно предполагать начальное состояние системы, но не имеется никаких данных о промежуточных состояниях, внутреннем механизме процесса и т.д.” [1]. Плавление – это процесс, проходящий в неравновесных условиях. Важной особенностью неравновесной системы является то, что она имеет нестационарное температурное поле, в котором каждому элементарному объему (нанообъему) соответствует своя собственная неравновесная температура, в явном виде зависящая от времени. Фазовый переход в нанообъемах происходит в пределах существующей исходной фазы, и обязательным его условием является чередование состояния локального термодинамического равновесия с его отсутствием [2, 3].
ТЕОРЕТИЧЕСКИЙ АНАЛИЗ
Образование расплава. При нагревании кристаллического тела увеличивается амплитуда и частота колебаний образующих его атомов. И, как следствие, происходит изменение их пространственного положения и ослабление связей между ними. Сначала исчезает ориентационный, а затем и позиционный порядок. Уменьшение степени порядка приводит к увеличению в кристаллах числа дефектов и вакансий, в результате чего уменьшается компенсация электростатических сил, деформируются электронные оболочки атомов, возникают длиннопериодические решетки. В первую очередь это происходит в поверхностном слое кристалла, толщина которого определяется радиусом действия поверхностных сил и радиусом межмолекулярных корреляций и составляет ~10–7 см. Поверхностный слой образуется под влиянием разности молекулярно-силовых полей, а электронные плотности между атомами в нем перераспределяются вдоль границы раздела и по нормали к ней. Это сопровождается возникновением поверхностной энергии и поверхностного электрического потенциала. Амплитуда тепловых колебаний атомов в поверхностном слое, в целом, обратно пропорциональна силам связей между атомами и массе атомов и прямо пропорциональна температуре. Таким образом, его толщина увеличивается с повышением температуры и достигает максимума при температуре фазового перехода [4, 5].
Перестройка поверхности кристалла (реконструкция), являющаяся результатом снятия различных напряжений в поверхностном слое, приводит к понижению свободной энергии. Периоды трансляций на поверхности значительно больше, чем в объеме. Свободная поверхность нестабильна из-за наличия большого количества ненасыщенных связей, и атомы смещаются из своих первоначальных положений, образуя новые связи друг с другом, что, в свою очередь, приводит к деформации их электронных оболочек. Смещение атомов сопровождается возникновением механических напряжений в кристаллической решетке и увеличением свободной поверхностной энергии. Поверхностные слои неоднородны в масштабе молекулярных размеров и анизотропны независимо от агрегатного состояния фаз. Присутствие в поверхностном слое некогерентных компонентов увеличивает деформацию решетки, следствием чего является уменьшение величины энергии, необходимой для отрыва атомов от решетки.
Для перемещения атома из одного положения в другое необходима энергия. Доля колебаний, приводящих к перескоку атома в данном направлении, определяется, главным образом, отношением добавочной энергии, необходимой для осуществления перескока, к средней кинетической энергии атомов в кристаллической решетке. При повышении температуры средняя кинетическая энергия атомов возрастает, а это приводит к увеличению частоты перескоков. При нагревании кристалла энергию сначала получают атомы поверхностного слоя. Образование расплава начинается тогда, когда среднеквадратичное смещение атомов становится больше доли внутриатомных расстояний [6]. Оторвавшиеся от поверхностного слоя кристаллической решетки атомы формируют на поверхности кристалла нанообъемы расплава. При повышении температуры они сливаются, и на поверхности кристалла образуется пленка. Температура, при которой это происходит, называется температурой поверхностного плавления (Тпов) [7–9].
Атомы, находящиеся внутри кристалла, имеют между собой более прочные связи. Соответственно для отрыва этих атомов требуется больше энергии. Поэтому образование расплава происходит при непрерывно повышающейся температуре. На определенном этапе процесса плавления достигается такое состояние, когда все находящиеся на поверхности атомы имеют с решеткой одинаково прочные связи, и для отрыва от решетки любого поверхностного атома требуется одинаковое количество энергии и, соответственно, одинаковая температура. Это температура объемного плавления (Тоб). Температура поверхностного плавления у кристаллов разных соединений составляет 50–87% от температуры объемного плавления [10–12].
Вещество из упорядоченного состояния (кристалл) можно перевести в неупорядоченное состояние (жидкость), не отвечающее минимуму свободной энергии, как изменением параметров состояния (давления, температуры), так и (теоретически) очень тонким измельчением. В обоих случаях необходимо затратить энергию. Чем больше степень диспергирования вещества (чем больше разорвано связей между атомами), тем меньше нужно затратить тепловой энергии для разрыва оставшихся связей и перевода вещества в состояние расплава. Поэтому температура плавления диспергированного вещества всегда ниже температуры плавления массивного образца того же вещества [13, 14].
Строение расплава. Степень упорядоченности расплава определяется температурой: чем выше температура, тем менее упорядочен расплав. Наиболее распространен кластерный тип расплава, который существует в широком диапазоне температур. Устойчивая конфигурация кластера определяется координатами составляющих его атомов, которые соответствуют минимумам поверхности потенциальной энергии в трехмерном пространстве. Свойства кластера отличаются от свойств образующих его атомов, а его верхняя размерная граница фиксируется по переходу от дискретного электронного энергетического спектра, свойственного отдельным атомам, к зонному электронному энергетическому спектру, характерному для кристаллического твердого тела [15–17].
В однокомпонентной системе химический состав расплава и кристаллической фазы аналогичны. Поэтому в процессе плавления химический состав в любой точке системы одинаков. Однако структурно эта система неоднородна: около кристаллической фазы расплав имеет квазикристаллическое строение, а с удалением от нее количество атомов, образующих кластер, уменьшается (рис. 1). Большинство горных пород состоит из нескольких минералов, имеющих различный химический состав. При нагревании горной породы, состоящей из нескольких кристаллических фаз с различной Tпов, расплав сначала образуется за счет поверхностного слоя кристаллического вещества, имеющего наиболее низкую температуру плавления. После образования расплава этот минерал больше не контактирует с другими минералами горной породы, т.к. отделен от них пленкой расплава. При повышении температуры расплав становится неравновесным со всеми минеральными фазами горной породы и реагирует с ними. Вследствие этого расплав приобретает зональное строение: непосредственно около зерна расплав соответствует химическому составу зерна. По мере удаления от поверхности зерна данного минерала, он обогащается химическими элементами других минералов (рис. 2), что приводит к образованию химической и структурной зональности расплава [11, 12].
Рис. 1.
Схема структурной неоднородности расплава: кристалл: 1 – поверхностный слой; расплав: 2 – расплав квазикристаллического типа, 3 – расплав оксидного типа, 4 – расплав ионного типа; ☼ – источник тепла; ][ – фазовая граница кристалл–расплав; ¦¦ – фазовый переход: расплав квазикристаллического типа → → поверхностный слой кристалла.

Рис. 2.
Схема структурной зональности расплава: А, В – фазы; к – кристалл; 1 – поверхностный слой кристалла; 2 – расплав квазикристаллического типа; е – расплав эвтектического состава. a – расплавы промежуточного состава (обогащение компонентом В); б – расплавы промежуточного состава (обогащение компонентом А).
При плавлении горной породы одновременно существуют несколько подсистем: “кристаллическая фаза–окружающий ее расплав”, которые различаются по химическому составу. Расплавы этих подсистем реагируют между собой. В трехкомпонентной системе (при условии, что температура поверхностного плавления всех кристаллических фаз одинакова) при плавлении кристаллических фаз (А, В и С) сначала происходит образование расплавов а, b и с. При взаимодействии этих расплавов образуются: а) расплавы, имеющие химическое и структурное зональное строение (рзс): а → b, b → с, с → а; б) котектические расплавы (а + b, b + с и с + а) и в) эвтектический расплав (а + b + с) (рис. 3). Вследствие медленного диффузионного обмена такое строение расплава сохраняется достаточно долгое время и после исчезновения кристаллических фаз.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для проверки изложенных выше соображений и решения поставленной задачи был исследован процесс плавления мономинеральных фракций (порошков и зерен) олигоклаза, щелочного полевого шпата (ЩПШ) и кварца, выделенных из гранитоидов и гнейсов, а также процесс плавления горных пород, из которых были выделены мономинеральные фракции. Эксперименты проводились в высокотемпературной камерной печи типа ПВК-1.6-5, снабженной хромит-лантановым нагревателем, и оснащенной микропроцессорным регулятором температуры, обеспечивающим работу по заданному графику. Точность поддержания температуры составляла ±1°С. Введение печи в режим происходило со скоростью 10°C/мин. Аналогичная скорость поддерживалась и при охлаждении.
Образование расплава при нагревании порошка. Зерна минералов дробились и тщательно растирались. Затем отсеивалась фракция размером <100 мкм. Шихта объемом 0.4–0.5 см3 помещалась в алундовые тигли и нагревалась в течение 6 ч. При температуре 900°С наблюдалось спекание мелких частиц щелочного полевого шпата. При 950°С происходит полное плавление этих частиц, а также начинается плавление олигоклаза и кварца. Чем меньше размер частиц, тем полнее плавление (рис. 4, 5). Следует отметить, что плавление мельчайших частичек всех минералов происходит при близких температурах. Это обусловлено тем, что с уменьшением размера порошинки процент атомов, находящихся на ее поверхности увеличивается, и при размере частички 3 мкм около 50% всех атомов находится на ее поверхности [18]. Связь между этими атомами очень слабая и поэтому для отрыва их от поверхности, необходимо минимальное количество энергии.
Рис. 4.
Олигоклаз (T = 950°C, τ = 6 ч). Первыми плавятся выступающие части обломков. Наиболее мелкие порошинки расплавились полностью. Черное – стекло. Николи скрещены.

Рис. 5.
Кварц (T = 950°C, τ = 6 ч). Первыми плавятся выступающие части обломков. Наиболее мелкие порошинки расплавились полностью. Черное – стекло. Николи скрещены.
Образование расплава при нагревании отдельного зерна. При нагревании зерна первыми отрываются атомы поверхностного слоя, имеющие наименьшее количество насыщенных связей. Сначала в расплав переходят атомы, находящиеся в вершинах кристаллической решетки. В процессе последовательного отрыва атомов форма зерна постепенно становится округлой. В результате все поверхностные атомы имеют одинаковое количество ненасыщенных связей и одинаковую энергию отрыва, а значит, отрыв от поверхности любого атома происходит при одинаковой температуре.
Для определения температуры поверхностного плавления исследовались отдельные зерна размером 2 ± 0.1 мм при длительности нагревания 6 ч. Установлено, что образование расплава за счет вещества поверхностного слоя у зерен ЩПШ, олигоклаза и кварца происходит при температуре 950, 1120 и 1350°С, соответственно (табл. 1).
Таблица 1.
Условия и результаты экспериментов
| Т, °С | τ, ч | Процесс и фазы |
|---|---|---|
| 900 | 6 | Спекание порошинок ЩПШ |
| 950 | 6 | Полное плавление порошинок ЩПШ; плавление мелких порошинок олигоклаза и кварца |
| 995 | 6 | Плавление периферической части зерен ЩПШ, расположенных на внешней части образца |
| 1055 | 6 | Зерна ЩПШ. расположенные на внешней части образца расплавились полностью. Во внутренней части образца сохранились реликты зерен ЩПШ. В гнейсах зерна ЩПШ расплавились на периферии |
| 1115 | 6 |
Зерна ЩПШ расплавились во всем объеме образца. В гнейсах зерна ЩПШ, расположенные на внешней части образца расплавились полностью |
| 200 | Плавление краевых частей зерен олигоклаза, находящихся на поверхности образца | |
| 1160 | 200 | Взаимодействие расплава ЩПШ с расплавом поверхностного слоя зерен плагиоклаза, находящихся внутри образца |
| 1350 | 6 | Плавление поверхностного слоя зерен кварца. Расплав полевошпатового состава взаимодействует с поверхностным слоем зерен кварца |
| 1400 | 6 | Расплав полевошпатового состава взаимодействует с зернами кристобалита |
| 1500 | 6 | Расплав полевошпатового состава взаимодействует с реститами кристобалита |
Образование расплава при нагревании образца полиминеральной горной породы. Для изучения процесса плавления горных пород были исследованы образцы среднезернистых гранитоидов и гнейсов (размер зерен 1.5–2.0 мм). Образцы объемом 0.5–1.0 см3 помещались в алундовые тигли и отжигались при температуре 1000, 1050, 1100, 1150, 1350, 1400 и 1500°С в открытой системе. Время выдержки (τ) составляло 6 и 200 ч. Результаты экспериментов приведены в табл. 1.
При нагревании образцов до 1000°С и длительности эксперимента 6 часов на поверхности зерен щелочного полевого шпата, контактирующих с воздухом, образовалась тонкая пленка расплава. При температуре 1050°С и τ = 6 ч наблюдается полное плавление зерен ЩПШ, находящихся на поверхности образца. При этой же температуре на поверхности зерен, расположенных во внутренней части, зафиксировано плавление поверхностного слоя. При T = 1100°С и выдержке 6 ч отмечается полное плавление зерен ЩПШ во всем объеме образца. При этой же температуре и длительности опыта 200 ч происходит плавление поверхностного слоя зерен плагиоклаза, контактирующих с воздухом. При последующем увеличении температуры до 1150°С и τ = 200 ч расплав ЩПШ взаимодействует с краевыми частями зерен плагиоклаза, расположенных во внутренней части образца. В результате образуется реакционная каемка промежуточного химического состава (рис. 6, табл. 2). При этих же температурно-временны́х параметрах расплав образуется и во внутренней части зерен плагиоклаза на поверхности плагиоклазовых доменов. При T = 1350°С и длительности опыта 6 ч во всем объеме образца наблюдается образование макрогомогенного полевошпатного расплава, который взаимодействует с поверхностью зерен кварца (рис. 7). При T = = 1400°С и τ = 6 ч кварц трансформируется в кристобалит, с зернами которого взаимодействует полевошпатовый расплав. При температуре 1500°С и той же длительности эксперимента в расплаве сохраняются реликты зерен кристобалита размером менее 10 мкм. Далее, при повышении температуры происходит плавление поверхностного слоя зерен кристобалита, реакция этого расплава с зональным расплавом и постепенное образование гомогенного расплава. Поэтому в объеме образца горной породы в разных его точках фиксируются разные стадии процесса плавления [11, 16, 19].
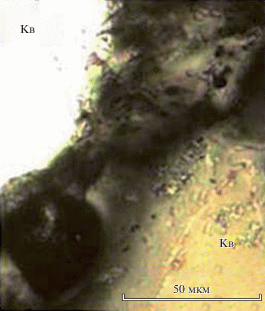
Рис. 6.
Гранодиорит (T = 1160°C, τ = 200 ч). Реакционная каемка образовалась в результате взаимодействия расплава щелочного полевого шпата с расплавом олигоклаза.
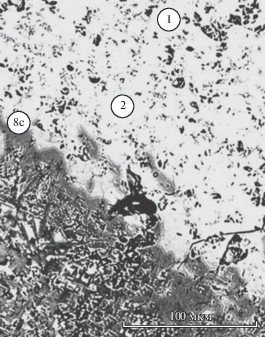
Таблица 2.
Таблица химического состава (к рис. 6)
| № анализа* | Na2O | MgO | Al2O3 | SiO2 | K2O | CaO | FeOΣ | ∑ |
|---|---|---|---|---|---|---|---|---|
| 1 | 5.25 | 0 | 21.31 | 65.20 | 8.60 | 0.49 | 0 | 100.85 |
| 2 | 5.03 | 0.34 | 20.87 | 65.98 | 7.37 | 0.54 | 0.44 | 100.57 |
| 8c | 7.72 | 0 | 19.91 | 62.78 | 4.44 | 2.76 | 1.75 | 99.36 |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Теоретические расчеты существенно отличаются от результатов экспериментальных исследований плавления тонкодиспергированного материала водонасыщенных систем [20, 21], т.к. породы сложены минералами, имеющими разную температуру плавления. В кварц – полевошпатовой горной породе образование расплава происходит в следующей последовательности: (1) плавление поверхностного слоя ЩПШ → → объемное плавление ЩПШ + плавление поверхностного слоя плагиоклаза; (2) образование полевошпатного расплава, как результат взаимодействия щпш и плагиоклаза; (3) взаимодействие полевошпатного расплава с расплавом поверхностного слоя кварца. Завершается процесс полным плавлением.
Фазовый переход кристалл–расплав у исследованных минералов происходит при разных температурах. Вследствие этого при одной и той же температуре в расплаве одновременно находятся упорядоченные в меньшей степени кластеры более легкоплавких минералов и кластеры более тугоплавких минералов, упорядоченные в большей степени. При нагревании полиминеральной породы непосредственно около каждого зерна минерала за счет поверхностного слоя образуется расплав, состав которого отвечает составу минерала. Минералы имеют разный химический состав, соответственно, и образующиеся за счет их вещества расплавы имеют разный химический состав. При повышении температуры эти расплавы взаимодействуют между собой посредством диффузии. В силикатных системах процесс проходит медленно, поэтому расплав длительное время имеет химическую и структурную неоднородность (зональное строение). Эта неоднородность сохраняется и при температуре несколько выше температуры полного плавления (+ΔТ) наиболее высокотемпературной кристаллической фазы. Расплав изолирует зерна минералов друг от друга и, вследствие этого, в единой системе (плавящаяся горная порода) одновременно существует несколько подсистем кристалл–расплав, число которых зависит от числа минералов, образующих горную породу.
При плавлении силикатов образующийся расплав имеет объем больше, чем объем исходной кристаллической фазы. Если окружающая среда не оказывает сопротивления увеличению объема, то для реализации фазового перехода I рода не требуется дополнительной энергии. В том случае, когда нагреваемое зерно минерала находится во внутренней части образца горной породы, увеличению его объема препятствуют окружающие минералы, которые при нагревании также изменяют свой объем. Таким образом, чтобы реализовался фазовый переход I рода необходимо преодолеть сопротивление со стороны окружающих минералов. Для этого требуется дополнительная энергия. Поэтому плавление зерен минералов, находящихся внутри образца происходит при более высокой температуре. Это описывается уравнением Клаузиуса–Клапейрона:
Около источника тепла температура расплава максимальна, значит, упорядоченность минимальна. Непосредственно около плавящейся кристаллической фазы температура расплава минимальна, а упорядоченность максимальна (квазикристаллический тип расплава). По мере удаления от поверхности кристалла и приближения к источнику тепла, температура расплава повышается и, соответственно, уменьшается его упорядоченность. Поэтому в системе расплав – кристалл, расплав всегда структурно гетерогенен.
Установлено, что температура плавления одних и тех же минералов из магматических (гранитоиды) и метаморфических (гнейсы) пород различается. При плавлении минералов гнейсов она на несколько десятков градусов выше. Обусловлено это разницей в концентрации примесей, вакансий, дислокаций и упорядоченности кристаллической решетки. Гнейсы больше “продвинулись” к состоянию термодинамического равновесия по сравнению с гранитоидами.
ЗАКЛЮЧЕНИЕ
1. Плавление минерала и горной породы это длительный многостадийный процесс, реализующийся в интервале температур.
2. Образование расплава начинается с плавления вещества поверхностного слоя, температура плавления которого значительно ниже температуры плавления внутренней части кристалла.
3. При нагревании образца горной породы существует три тренда последовательности образования расплава: тренд в объеме зерна минерала: внешняя → промежуточная → → внутренняя часть зерна; тренд последовательности перехода в расплав минералов: ЩПШ → плагиоклаз → кварц; тренд в объеме образца горной породы: внешняя → → промежуточная → внутренняя часть образца.
4. Существует два механизма образования расплава. Для отдельного зерна это фазовый переход I рода: поверхностное плавление → объемное плавление. При нагревании полиминеральной горной породы сначала происходит плавление самой низкотемпературной фазы. Одновременно с этим в других минералах происходит ослабление связей между атомами. При повышении температуры расплав низкотемпературной фазы реагирует с поверхностным слоем более высокотемпературных фаз. В результате образуются расплавы промежуточного химического состава, и расплав в целом приобретает зональное строение.
5. При нагревании горной породы, образующие ее минералы плавятся при разных температурах. Соответственно расплавы этих минералов при одной и той же температуре системы разупорядочены в разной степени (образованы кластерами разного типа).
6. Полное плавление образца полиминеральной горной породы происходит при температуре значительно более высокой, чем температура плавления тонкодиспергированной шихты того же образца.
7. Образование расплава, как и любой процесс, происходит в неравновесных условиях: при изменении температуры системы равновесие нарушается, и она стремится прийти в состояние нового равновесия.
Анализы выполнены в лаборатории локальных методов исследования вещества геологического факультета МГУ им. М.В. Ломоносова на микрозондовом комплексе на базе растрового электронного микроскопа “Jeol JSM-6480LV” с комбинированной системой рентгеноспектрального микроанализа, объединяющей энергодисперсионный “INCA-Energy 350” и волновой дифракционный спектрометр “INCA-Wave 500” (кристаллы LiF200, TAP, PET и LSM-80 N). В стеклах содержания F, Cl, Cr2O3, MnO, P2O5, TiО2 ниже предела чувствительности метода.
Список литературы
Жариков В.А. Основы физической геохимии. М: Изд-во МГУ. 2005.
Ubellodhde A. Melting and crystal structure. Oxford: Clarendon Press. 1965.
Соболев Р.Н., Мальцев В.В., Волкова Е.А. Температурный интервал при образовании расплава при нагревании кристаллического вещества // Бюлл. МОИП. Отд. Геол. 2018. 93. С. 9–15.
Фолмер М. Кинетика образования новой фазы. М.: Наука. 1986.
Wei X., Miranda P., Shen Y. // Phys. Rev. Lett. 2001. 86. P. 1554–1557. https://doi.org/10.1103/PhysRevLett.86.1554
Соболев Р.Н. Применение теории флуктуации к анализу магматических процессов // Бюлл. МОИП. Отд. Геол. 2015. 90. С. 52–59.
Dash J.G. Surface melting // Contemporary Physics. 1989. 30. P. 89–100. https://doi.org/10.1080/00107518908225509
Frenkel J.W.M., van der Veen J.F. // Phys. Rev. Lett. 1985. 54. P. 134–137. https://doi.org/10.1103/PhysRevLett.54.134
Pluis B., van der Gon A.W.D., Frenken J., Van der Veen J. // Phys. Rev. Lett. 1988. 59. P. 2678–2681. https://doi.org/10.1103/PhysRevLett.59.2678
Гусаров В.В., Суворов С.Ф. Температура плавления локально равновесных поверхностей фаз в поликристаллических системах на основе одной объемной фазы // Журнал прикладной химии. 1990. 63. С. 1689–1694.
Соболев Р.Н., Мальцев В.В. Процесс образования расплава при нагревании кварц-полевошпатовых пород // Доклады АН. 2011. 438. С. 671–674.
Sobolev R.N. Mechanism and conditionsof melts formation in the earth crust // Izvestia earth sciences section Russian academy of natural sciences. 2012. 34 IGC. P. 33–42.
Buffat P., Borel J.-P. // Phys. Rev. A. 1976. 13. P. 2287–2298. https://doi.org/10.1103/PhysRevA.13.2287
Shi F.G. // J. Mater. Res. 1994. 9. P. 1307–1314. https://doi.org/10.1557/JMR.1994.1307
Белов Н.В. Попытки кристаллохимического вмешательства в специфические вопросы минералогии и петрографии // Вестник МГУ. 1968. Сер. 4. Геология. 4. С. 78–90.
Гусев А.И. Наноматериалы, наноструктуры, нанотехнологии. М.: Наука. Физматлит. 2009.
Van Driessche A.E.S., Kellermeier M., Benning L.G., Gebauer D. Eds. New Perspectives on mineral nucleation and growth: from solution precursors to solid materials. Springer. 2017.
Roduner E. Nanoscopic Materials: Size-Dependent Phenomena and Growth Principles (Advanced textbook). The Royal Society of Chemistry, 2nd Ed. Cambridge, 2014.
Безбородов М.А. Самопроизвольная кристаллизация силикатных стекол. Минск: Наукаитехника.1981.
Muncill G.E., Lasaga A.C. Crystal-growth kinetics of plagioclase in igneous systems: isothermal H2O-saturated experiments and extension of a growth model to complex silicate melts // Amer. Mineral. 1988. 73. P. 982–992.
Рябчиков И.Д. Термодинамика флюидной фазы гранитоидных магм. М.: Наука. 1975.
Дополнительные материалы отсутствуют.