Расплавы, 2020, № 6, стр. 608-615
Термодинамическое моделирование карботермического процесса восстановления хрома из оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3
В. А. Салина a, *, В. И. Жучков a, А. В. Сычев a
a Институт металлургии Уральского отделения РАН
Екатеринбург, Россия
* E-mail: valentina_salina@mail.ru
Поступила в редакцию 14.07.2020
После доработки 19.07.2020
Принята к публикации 22.07.2020
Аннотация
В статье приведены результаты термодинамического моделирования карботермического процесса восстановления хрома из оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3 в интервале температур (T) 1673–1973 К с шагом 50 К при общем давлении в системе 0.1 МПа и количестве азота 2.24 м3. В качестве оксидной системы использовали составы хромовой руды, мас. %: 38 Cr2O3; 11.1 FeO; 0.17 CaO; 15 SiO2; 29.7 MgO; 6 Al2O3 и шлака феррохрома низкоуглеродистого (ФХНУ), мас. %: 13 Cr2O3; 4 FeO; 41.6 CaO; 21.2 SiO2; 12.8 MgO; 7.4 Al2O3, добавляемого к руде в количестве 0; 5; 10; 20%. В качестве восстановителя использовали углерод, расход которого увеличен на 10% от стехиометрии на восстановление Fe и Cr и на 8% от массы металла для образования карбидов железа, хрома и кремния. Термодинамическое моделирование осуществлено с использованием программного комплекса HSC Chemistry 6.12 (Outokumpu, Финляндия). В базу данных введены термодинамические данные соединения CrO(II), уточнены существующие в базе данных термохимические характеристики соединений: CaCr2O4, SiC, Cr3C2, Cr7C3, Cr23C6, Fe3C, Al4C3. Результаты термодинамического моделирования показали, что повышение температуры процесса c 1673 до 1973 К увеличивает степень восстановления хрома (ηCr) при различном содержании шлака в системе. Увеличение содержания шлака в системе с 0 до 20% уменьшает ηCr с 94.8 до 94% при температуре 1973 К. Наибольшее значение степени восстановления хрома характерно для состава системы с 0% шлака. Химический состав металла при температуре 1973 К и 0% шлака, мас. %: 65.6 Cr; 22.7 Fe; 0.26 Si; 11.5 C. Результаты термодинамического моделирования могут быть использованы при разработке технологии получения хромсодержащего сплава с вовлечением в металлургический передел шлака феррохрома низкоуглеродистого.
ВВЕДЕНИЕ
Переработка техногенных отходов металлургического производства является актуальной задачей во всем мире. Отходами металлургического производства, в том числе ферросплавного, являются шлаки, пыль и шламы газоочистных сооружений. Объемы образования отходов зависят от применяемых шихтовых материалов и технологии производства [1, 2].
В настоящее время в России в шлаковых отвалах накоплено более 300 млн т шлаков сталеплавильного, литейного и ферросплавного производств, которые подлежат переработке [3–6]. На ферросплавных предприятиях при объеме выплавки ~2 млн т всех видов ферросплавов образуется ~1 млн т шлаков и ~130 тыс т пылей и шламов [7].
Шлаки производства высокоуглеродистого феррохрома высокопрочные и применяются в виде щебня в дорожном строительстве, а шлаки низко- и среднеуглеродистого феррохрома при остывании рассыпаются в порошок фракции <0.1 мм из-за образования двухкальциевого силиката (2СаО · SiO2). После магнитной сепарации они складируются на отвалах либо используются в виде различных добавок [8].
В литературе приведены данные о прогнозировании фазового состава шлаков и их стабилизации [8, 9], термодинамическом моделировании процесса восстановления элементов [10], применении хромсодержащих шлаков в металлургическом переделе с последующим получением товарного продукта [11–15].
Термодинамическое моделирование равновесного охлаждения шлаков внепечной обработки стали с применением ПК FactSage, проведенное авторами работы [8], показало возможность прогнозирования фазового состава шлаков. Анализ полученных данных позволил определить необходимый для стабилизации расход борсодержащей добавки в зависимости от состава шлака. Стабилизация в этом случае связана с замещением силикатных ионных групп на боратные, в результате чего затрудняется диффузия атомов и ионов, участвующих в полиморфном превращении.
В работе [9] показано применение боратной добавки для стабилизации высокотемпературной полиморфной фазы хромсодержащих шлаков при производстве нержавеющей стали, путем формирования твердого раствора с 2CaO · SiO2. Результаты показали, что только определенная доля присаженного бората образует твердый раствор с 2CaO · SiO2, а основная часть обнаружена в фазе кальциевого боратосиликата.
В работе [10] изучен процесс карботермического восстановления элементов системы Fe–Cr–O и термодинамически определены возможные продукты процесса восстановления. Установлено, что при высоких температурах и низких соотношениях nC : nO (исходное молярное отношение С к O в образце) образуется больше раствора Fe–Cr–C и меньше остаточного содержания углерода. Карбиды металлов образуются на начальной стадии процесса восстановления, а раствор Fe–Cr–C образуется, когда степень восстановления достаточно высокая.
Авторами работы [11] разработана технология получения прочных комплексных хромовых окатышей с заданными физико-химическими характеристиками для выплавки в электродуговых печах хромовых ферросплавов. В качестве шихтовых материалов использовали мелкодисперсный хромовый концентрат Донского ГОКа (≥50% Cr2O3), шлаки рафинированного феррохрома, железистую (~10% Fe и 60% SiO2) и/или высокожелезистую (~25% Fe и 25% SiO2) диатомитовую руду Муголжарской группы месторождений и кокс АО “Сары-Арка” с последующим окатыванием и спеканием. Состав шихты с 3% кокса для получения неметаллизированных окатышей позволяет снизить температуру обжига окатышей с 1350 до 1200°С, причем без существенного изменения аппаратурно-технологического оформления процесса обжига. Химический состав полученных окатышей, мас. %: 44 Cr2O3; 6.08 Al2O3; 18.65 SiO2; 12.48 FeO; 1.57 CaO; 9.95 MgO; 7.27 остальное. Средняя прочность при температуре обжига окатышей, Н/окатыш: 1323 К – 2893; 1373 К – 3971,7; 1423 К – 4511,1; 1473 К – 5325. В работе [12] пыль газоочистки от производства хромовых ферросплавов (20–43% Cr2O3) применяли в качестве добавки при получении обожженных хромовых окатышей.
Авторами работы [13] разработана технология получения высокоуглеродистого феррохрома с использованием до 30–70% в навеске шихтовых материалов антрацита (Рd – 0.016%, Sd – 0.15%) в качестве частичной замены традиционного кокса. Шихтовые материалы: хромовая руда, металлоконцентрат, шлак ферросилиция, хромовые отходы, отсевы кварцита, хромовые брикеты. Коэффициент извлечения хрома составил 84.4% при использовании в качестве восстановителя кокса и антрацита (30–50% на колошу) и 84.7% при применении кокса и угля.
В работах [16, 17] изучено влияние основности шлака и количества восстановителя на степень восстановления хрома системы Cr2O3–FeO–Al2O3–SiO2–MgO–CaO–P2O5 с применением ПК HSC 6.12 Chemistry при температуре 1973 К. В качестве исходной системы использовали состав хромовой руды, содержащей 40% Cr2O3; восстановитель – ферросиликоникель. Определены оптимальная основность шлака (СаО)/(SiO2) и расход кремния-восстановителя, при которых степень восстановления хрома составила 95.1%.
Одним из способов утилизации шлаков и пылей производства ферро- и силикохрома является их добавка при выплавке. Процесс такого использования шлаков изучен недостаточно. В связи с этим нами проведено термодинамическое моделирование карботермического процесса восстановления хрома из состава смеси хромовой руды и шлака феррохрома низкоуглеродистого (ФХНУ).
ТЕРМОДИНАМИЧЕСКОЕ МОДЕЛИРОВАНИЕ
Целью настоящей работы является определение степени восстановления хрома (ηCr) от температуры (Т) и рационального расхода шлака ФХНУ методом термодинамического моделирования.
Термодинамическое моделирование процесса восстановления хрома из оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3 с применением в качестве восстановителя углерода проведено по следующим вариантам:
1) изучение влияния температуры процесса 1673–1973 К на степень восстановления хрома из смеси хромовой руды и шлака ФХНУ;
2) определение влияния количества шлака ФХНУ (0; 5; 10; 20%) на степень восстановления хрома при температуре 1973 К.
Химический состав материалов оксидных систем приведен в табл. 1. Состав материала 1 соответствует хромовой руде, состав 2 – шлаку ФХНУ.
Таблица 1.
Химический состав исходных материалов, мас. %
| № материала | Cr2O3 | FeO | СаО | SiO2 | MgO | Al2O3 |
|---|---|---|---|---|---|---|
| 1 | 38 | 11.1 | 0.17 | 15 | 29.7 | 6 |
| 2 | 13 | 4 | 41.6 | 21.2 | 12.8 | 7.4 |
В качестве восстановителя использовали углерод, расход которого увеличен на 10% от стехиометрически необходимого на полное восстановление железа и хрома и на 8% от массы металла для образования карбидов железа, хрома и кремния, что соответствует реальным условиям получения углеродистого феррохрома.
Для проведения термодинамического моделирования использовали программный комплекс (ПК) HSC Chemistry 6.12, разработанный Outokumpu, и основанный на минимизации энергии Гиббса и вариационных принципах термодинамики [18]. Равновесный состав многокомпонентной оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3 определен с применением подпрограммы “Equilibrium Compositions”. Исходные параметры для проведения термодинамического моделирования: интервал температур 1673–1973 К с шагом 50 К, общее давление 0.1 МПа, количество N2 2.24 м3. В базу данных ПК HSC Chemistry 6.12 введены термодинамические характеристики оксида хрома CrO(II), уточнены термохимические характеристики, существующие в базе соединений: CaCr2O4, Fe3C, Cr3C2, Cr7C3, Cr23C6, SiC, Al4C3 [19].
РЕЗУЛЬТАТЫ ТЕРМОДИНАМИЧЕСКОГО МОДЕЛИРОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Результаты термодинамического моделирования процесса восстановления хрома из многокомпонентной оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3 с применением в качестве восстановителя углерода представлены в виде следующих графических зависимостей:
1) изменение степени восстановления хрома от температуры (1673–1973 К) при содержании 0; 5; 10; 20% шлака ФХНУ (рис. 1);
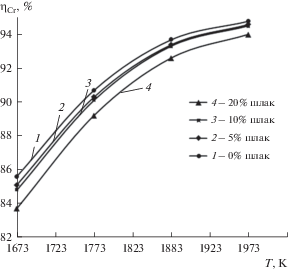
Рис. 1.
Изменение степени восстановления хрома (ηCr) от температуры (Т) при содержании 0; 5; 10; 20% шлака.
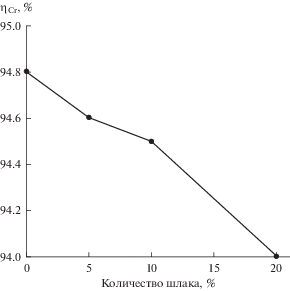
2) изменение степени восстановления хрома от количества шлака ФХНУ при температуре 1973 К (рис. 2).
На рис. 1 показано изменение степени восстановления хрома от температуры. Повышение температуры процесса с 1673 до 1973 К увеличивает степень восстановления хрома при различном содержании шлака ФХНУ в составе системы. Это связано с тем, что повышение температуры процесса увеличивает реакционную способность углерода, как элемента-восстановителя, что способствует образованию карбидов железа и хрома, которые затем выступают в качестве носителей углерода. Это приводит к дальнейшему восстановлению оксидов железа и хрома. Восстановление хрома в смеси Cr2O3–C–Fe наблюдается уже при 1373 К, тогда как без железа хром при указанной температуре не восстанавливается [20]. При повышении температуры процесса с 1673 до 1973 К степень восстановления хрома увеличилась на 9.2% для системы без шлака ФХНУ, на 9.5; 9.7 и 10.3% для систем с 5; 10 и 20% шлака соответственно. Наибольшее повышение степени восстановления хрома отмечено в интервале температур с 1673 до 1773 К, а наименьшее – с 1873 до 1973 К. Самая высокая степень восстановления хрома отмечена при температуре 1973 К для всех систем.
На рис. 2 показано изменение степени восстановления хрома от количества шлака в составе системы при температуре 1973 К. Повышение количества шлака с 0 до 20% уменьшает степень восстановления хрома с 94.8 до 94%. Это связано с уменьшением суммарного содержания Cr2O3 в системе при вводе шлака (с 38 до 33% Cr2O3 при 20% шлака). При содержании 5% шлака в системе степень восстановления хрома составила 94.6% при температуре 1973 К.
В табл. 2 приведен химический состав металла, образующегося при температуре 1973 К.
Таблица 2.
Химический состав металла, мас. %
| Элемент | Количество шлака, % | |||
|---|---|---|---|---|
| 0 | 5 | 10 | 20 | |
| Cr | 65.6 | 65.5 | 65.3 | 65.3 |
| Fe | 22.7 | 22.7 | 23.0 | 23.0 |
| Si | 0.26 | 0.22 | 0.20 | 0.16 |
| C | 11.5 | 11.5 | 11.6 | 11.5 |
При повышении количества шлака с 0 до 20% в составе шихты химический состав металла изменяется незначительно. Так, содержание хрома уменьшается с 65.6 до 65.3%, кремния – с 0.26 до 0.16%, а железа – увеличивается с 22.7 до 23.0%.
Термодинамический расчет показал возможность использования до 20% шлака ФХНУ при производстве высокоуглеродистого феррохрома без значительного снижения извлечения хрома в металл и изменения его химического состава.
ВЫВОДЫ
Результаты термодинамического моделирования карботермического процесса восстановления хрома из многокомпонентной оксидной системы Cr2O3–FeO–CaO–SiO2–MgO–Al2O3 при содержании 0; 5; 10 и 20% шлака низкоуглеродистого феррохрома в составе шихты показали, что повышение температуры процесса с 1673 до 1973 К незначительно увеличивает степень восстановления хрома при различном содержании шлака в составе шихты. Наибольшее значение степени восстановления хрома характерно для состава системы с 0% шлака. Увеличение количества шлака с 0 до 20% незначительно понижает степень восстановления хрома (с 94.8 до 94%) и изменяет состав образующегося металла. Результаты термодинамического моделирования могут быть использованы при разработке технологии получения хромсодержащего сплава с вовлечением в металлургический передел шлака ФХНУ.
Авторы выражают благодарность за помощь заведующему лаборатории “Бор” Химико-металлургического института им. Ж. Абишева, д.т.н., профессору А.А. Акбердину.
Работа выполнена при поддержки гранта РФФИ № 18-29-24 027.
Список литературы
Рысс М.А. Производство ферросплавов. М.: Металлургия. 1985.
Гасик М.И., Лякишев Н.П., Емлин Б.И. Теория и технология производства ферросплавов. М.: Металлургия. 1988.
Смирнов Л.А., Леонтьев Л.И., Сорокин Ю.В. Переработка и использование техногенных отходов металлургического производства // Тр. Междунар. конгресса “Фундаментальные основы технологий переработки и утилизации техногенных отходов”. Екатеринбург. 2012. С. 15–19.
Косырев К.Л., Паршин В.М., Фоменко А.П. Предпосылка и концепция создания энергометаллургических комплексов для переработки техногенных отходов // Тр. Междунар. конгресса “Фундаментальные основы технологий переработки и утилизации техногенных отходов”. Екатеринбург. 2012. С. 41–46.
Карпенко Н.И., Ярмаковский В.Н., Школьник Я.Ш. Состояние и перспективы использования продуктов переработки техногенных образований в строительной индустрии // Тр. Междунар. конгресса “Фундаментальные основы технологий переработки и утилизации техногенных отходов”. Екатеринбург. 2012. С. 49–56.
Государственный доклад “О состоянии и об охране окружающей среды Российской Федерации в 2015 г.”. Дата обращения 17.03.2020. http://www.mnr.gov.ru/docs/o_sostoyanii_i_ ob_okhrane_okruzhayushchey_sredy_rossiyskoy_federatsii/gosudarstvennyy_doklad_o_sostoyanii_i_ob_okhrane_okruzhayushchey_sredy_rossiyskoy_federatsii_v_2016_/.
Zhuchkov V.I., Zayakin O.V., Sychev A.V. Russian Metallurgy. 2020. 6. P. 662–666. https://doi.org/10.1134/S003602952006018X
Кушнерев И.В., Оржех М.Б., Либанов Б.Б., Коротеев С.А., Платонов А.А., Плюхин В.В. Стабилизация шлаков внепечной обработки стали от силикатного распада // Новые огнеупоры. 2018. № 4. С. 44.
Durinck D., Arnout S., Mertens G., Boydens E., Jones P.T., Elsen J., Blanpain B., Wollants P. // J. Amer. Ceramic Soc. 2008. 91. № 2. P. 548–554. https://doi.org/10.1111/j.1551-2916.2007.02147.x
Zhang Yang-ling, Liu Yang, Wei Wen-jie. // International J. Minerals, Metallurgy and Materials. 2013. 20. № 10. P. 931–940. https://doi.org/10.1007/s12613-013-0817-1
Bondarenko I.V., Tastanov E.A. // Metallurgist. 2019. 62. № 11–12. P. 1213–1218. https://doi.org/10.1007/s11015-019-00776-0
Beukes J.P., Dawson N.F., Van Zyl P.G. Theoretical and practical aspects of Cr (VI) in the South African ferrochrome industry // Proceedings of the Twelfth International Ferroalloys Congress. Sustainable Future. Helsinki. 2010. 1. P. 53–62.
Kaliakparov A.G., Baltabaev S.R., Strakhov V.M., Mukhtar A.A. // Metallurgist. 2017. 61. № 9–10. P. 765–769. https://doi.org/10.1007/s11015-018-0561-x
Жучков В.И., Сычев А.В., Заякин О.В., Леонтьев Л.И. Использование техногенных отходов ферросплавного производства // Тр. Междунар. конгресса “Фундаментальные исследования и прикладные разработки процессов переработки и утилизации техногенных образований "Техноген-2019". Екатеринбург. 2019. С. 96–99.
Демин Б.Л., Сорокин Ю.В., Смирнов Л.А., Щербаков Е.Н. Существующие способы переработки и направления использования ферросплавных шлаков // Сб. трудов научно-практической конференции “Перспективы развития металлургии и машиностроения с использованием завершенных фундаментальных исследований и НИОКР: “Ферросплавы”. Екатеринбург. 2018. С. 346–350.
Salina V.A., Zhuchkov V.I., Zayakin O.V. // Russian Metallurgy. 2019. № 2. P. 162–164. https://doi.org/10.1134/S003602951902023X
Салина В.А., Жучков В.И., Заякин О.В. Изучение силикотермического способа получения комплексных никельхромсодержащих ферросплавов методом термодинамического моделирования // Наука и техника Казахстана. 2017. № 3–4. С. 85–90.
Roine A. Outokumpu HSC Chemistry for Windows. Chemical reactions and Equilibrium software with extensive thermochemical database. Pori: Outokumpu research OY, 2002.
Глушко В.П. Термические константы веществ. М.: Академия наук СССР. 1979.
Ryabchikov I.V., Mizin V.G., Yarovoi K.I. // Steel in Translation. 2013. 43. № 6. P. 379–382. https://doi.org/10.3103/S096709121306017X
Дополнительные материалы отсутствуют.