Расплавы, 2021, № 5, стр. 450-459
Кинетика окисления расплавов на основе Ва–Ge кислородом воздуха
Н. С. Олимов a, И. Н. Ганиев b, *
a Таджикский государственный педагогический университет им. С. Айни
Душанбе, Таджикистан
b Институт химии им. В.И. Никитина Академии наук Республики Таджикистан
Душанбе, Таджикистан
* E-mail: ganievizatullo48@gmail.com
Поступила в редакцию 24.04.2021
После доработки 17.05.2021
Принята к публикации 05.06.2021
Аннотация
Методами термогравиметрии, ИК-спектроскопией и рентгенофазовым анализом (РФА) исследована кинетика окисления расплавов Ва–Ge кислородом воздуха. Показано, что добавки германия до 50 мас. % повышают устойчивость сплавов к окислению. Рост температуры способствует увеличению скорости окисления расплавов системы Ba–Ge. Процесс окисления исследуемых расплавов подчиняется параболическому закону. Истинная скорость окисления имеет порядок 10–4 кг/м2 · с. Кажущаяся энергия активации окисления в зависимости от состава сплавов составляет 39.08–262.0 кДж/моль. Продуктами окисления сплавов являются BaGe4O9 и GeO2. Установлен механизм влияния германия на кинетику окисления расплавов Ba–Ge. Доминирующую роль в формирования защитной оксидной пленки играет оксид BaGe4O9.
ВВЕДЕНИЕ
Решение многих задач современной техники связано с использованием материалов, обладающих высоким сопротивлением окислению. Высокой химической активностью отличаются расплавленные металлы. Так, расплавы алюминия, кремния, германия и щелочноземельных металлов (ЩЗМ) мгновенно вступают в реакцию с кислородом при ничтожно малых значениях его парциального давления. Эти элементы благодаря высокому химическому сродству к кислороду и сере, а также малой растворимости в железе, применяются при обработке стали и чугуна. Однако применение ЩЗМ в чистом виде связано с существенными трудностями. Это, прежде всего, невысокая плотность и температура кипения ЩЗМ, возникновение пироэффекта при обработке расплавленной стали, низкое усвоение и неравномерное распределение ЩЗМ. Поэтому, чистые ЩЗМ в металлургии черных металлов имеют весьма ограниченное применение [1–3].
Применение ЩЗМ в виде лигатур на основе кремния имеет существенные преимущества: сокращается время распределения элементов в объеме обрабатываемого металла, повышается использование и раскислительная способность элементов, упрощается аппаратурное оформление [4]. Согласно исследованиям [5] система Ва–Ge привлекает внимание исследователей, прежде всего наличием интерметаллидов с необычными типами упорядочения (в частности, клатратными соединениями). Эти соединения демонстрируют своеобразные термоэлектрические и сверхпроводящие характеристики.
Цель настоящего исследования заключается в экспериментальном определении кинетических и энергетических характеристик окисления расплавов на основе Ba–Ge кислородом из газовой фазы.
МАТЕРИАЛЫ И МЕТОДИКИ ИССЛЕДОВАНИЯ
Образцы сплавов для исследования массой 30 г получали в вакуумной печи СНВ-1.31.1/16 в атмосфере инертного газа в корундовых тиглях из бария марки БМ1 (ТУ 48-4-465-85) и монокристаллического германия марки Ге 000. Окисление сплавов в жидком состоянии проводили кислородом воздуха на установке, принцип работы которой описан в работах [6, 7]. Исследование продуктов окисления сплавов выполнено методами ИК-спектроскопии на двухлучевом ИК-спектрофотометре UR-20 в области 400–4000 см–1 и рентгенофазовым анализом (РФА) на установке ДРОН-1.5.
Для проведения исследований тигель с исследуемым металлом помещался в изотермической зоне печи. Температуру повышали со скоростью 2–3°С/мин. Перед разогревом печи катетометр настраивали на указатель пружины, записывали на шкале точки отчета и в течение нагрева контролировали изменение массы образца. При достижении заданного режима записывали новую точку отчета.
Изменение массы образца фиксировали по растяжению пружины с помощью катетометра КМ-8. В опытах использовались тигли из оксида алюминия диаметром 18–20 мм, высотой 25–26 мм. Тигли перед опытом прокаливали при температуре 1273–1473 К в окислительной среде в течение 1.5 ч до достижения постоянной массы. Массу образца из исследуемого сплава параллельно контролировали до и после опыта на аналитических весах.
В качестве регистрирующего прибора температуры использовали потенциометр ПП-63. По окончании опыта систему охлаждали, тигель с содержимым взвешивали и определяли реакционную поверхность. Погрешность эксперимента может быть рассчитана из исходной формулы константы скорости окисления
где m – масса металла; S – поверхность реагирования; t – время.Вычисленная относительная ошибка эксперимента складывается из суммы относительных ошибок
Температуру замеряли платина-платинородиевой термопарой, горячий спай которой находился на уровне поверхности образца. Точность измерения температуры принята равной ±2 К. Ошибка измерений температуры составила: $\frac{{\Delta T}}{T} = 2\left( {\frac{{100}}{{900}}} \right) = 0.22\% .$ Подробная методика исследования кинетики окисления сплавов описано в работах [8–15].
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Кинетика окисления сплавов системы барий–германий нами исследована во всем диапазоне концентрации компонентов с целью выбора состава лигатур со стабильным составом, отличающихся наименьшей окисляемостью при высоком содержании бария в сплаве [2, 3].
Система барий–германий характеризуется наличием следующих интерметаллических соединений составов Ba2Ge, Ba5Ge3, BaGe, β-Ba3Ge4, BaGe2, Ba3Ge4 [16] и BaGe4 [5]. Соединение BaGe плавится конгруэнтно. Эвтектика со стороны бария кристаллизуется при 96 мас. % бария и 818 К, а со стороны германия – при 80.5 мас. % германия и 1088 К [17]. Химический состав исследованных сплавов приведен в табл. 1.
Таблица 1.
Кинетические и энергетические параметры процесса окисления расплавов системы Ва–Ge
| Ва | Ge | Температура плавления сплава, К |
Температура окисления сплава, К | Истинная скорость окисления К · 104, кг /м2 · с |
Кажущаяся энергия активации, кДж/моль |
|---|---|---|---|---|---|
| мас. % | |||||
| 100.0 | 0.0 | 1002 | 1023 | 4.8 | 50.2 |
| 1073 | 5.8 | ||||
| 1273 | 16.6 | ||||
| 96.0 | 4.0 | 818 | 873 | 4.0 | 79.9 |
| 923 | 7.0 | ||||
| 75.0 | 25.0 | 1173 | 1223 | 10.0 | 120.6 |
| 1273 | 17.0 | ||||
| 1323 | 13.0 | ||||
| 66.7 | 33.3 | 1273 | 1223 | 16.0 | 127.7 |
| 1373 | 22.0 | ||||
| 1423 | 25.0 | ||||
| 50.0 | 50.0 | 1418 | 1473 | 3.3 | 262.0 |
| 1523 | 5.4 | ||||
| 1573 | 8.8 | ||||
| 33.3 | 66.7 | 1323 | 1373 | 11.0 | 115.2 |
| 1423 | 17.0 | ||||
| 1473 | 13.3 | ||||
| 19.5 | 80.5 | 1088 | 1133 | 8.0 | 104.3 |
| 1183 | 12.0 | ||||
| 1233 | 19.0 | ||||
| 8.5 | 91.5 | 1173 | 1273 | 10.0 | 72.0 |
| 1323 | 16.0 | ||||
| 0.0 | 100.0 | 1211 | 1223 | 4.4 | 39.8 |
| 1373 | 4.7 | ||||
Кинетику окисления жидкого сплава эвтектического состава, содержащего 4 мас. % Ge, исследовали при температурах 873 и 923 К. В течение 10 мин увеличение массы образца достигло 40 мг/см2, затем процесс окисления протекает по параболическому закону и характеризуется быстрым образованием защитной оксидной пленки. Максимальное значение величины Δm/S равняется 68 мг/см2 (рис. 1а), кажущаяся энергия активации достигает значения 79.97 кДж/моль. Оксидная пленка сплава в основном состоит из ВаО (табл. 2 и 3). Сплав, содержащий 25 мас. % Ge окисляли при температурах 1223, 1273 и 1323 К. Характер кривых показывает, что окисление расплава протекает по параболическому закону с диффузионными затруднениями, и процесс заканчивается на 60-й минуте. Максимальное значение величины Δm/S равняется 220 мг/см2 (рис. 1б). Кажущаяся энергия активации достигает значения 120.6 кДж/моль. Продукты окисления данного сплава состоят из двух фаз: ВаО и Ba2GeO4 (рис. 2).
Рис. 1.
Кинетические кривые окисления расплавов системы Ва–Ge, содержащих германий, мас. %: а – 4; б – 25; в – 33.3.

Таблица 2.
Частоты в ИК-спектрах продуктов окисления расплавов системы Ва–Gе
| Содержание германия в барии, мас. % | Частоты, см–1 | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 0.0 | 695 | 860 | 1060 | 1145 | 1750 | ||||
| 4.0 | 695 | 860 | 1060 | 1420 | 1490 | ||||
| 25.0 | 535 | 695 | 725 | 750 | 860 | 1060 | 1435 | ||
| 33.3 | 695 | 725 | 750 | 860 | 1060 | 1435 | |||
| 50.0 | 530 | 585 | 630 | 695 | 720 | 750 | 860 | 1120 | 1145 |
| 66.7 | 530 | 625 | 695 | 730 | 750 | 880 | 1120 | ||
| 91.5 | 695 | 730 | 750 | 880 | 965 | 1425 | |||
| 100.0 | 525 | 501 | 585 | 880 | 965 | 1045 | 1100 | 1325 | |
Таблица 3.
Фазовый состав продуктов окисления расплавов системы Ва–Gе
| Химический состав сплавов до окисления, мас. % | Фазовый состав продуктов окисления | |
|---|---|---|
| Ba | Ge | |
| 100.0 | 0.0 | BaO |
| 96.0 | 4.0 | BaO |
| 75.0 | 25.0 | BaO + Ba2GeO4 |
| 66.7 | 33.3 | Ba2GeO4 |
| 50.0 | 50.0 | BaGeO3 |
| 33.3 | 66.7 | BaGe4O9 + GeO2 |
| 19.5 | 80.5 | BaGe4O9 + GeO2 |
| 8.5 | 91.5 | BaGe4O9 + GeO2 |
| 0.0 | 100.0 | GeO2 |
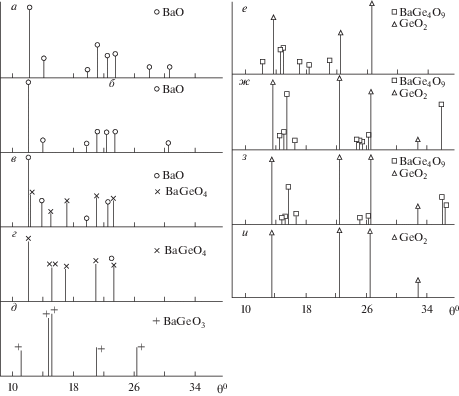
Рис. 2.
Штрих дифрактограммы продуктов окисления расплавов системы Ba–Ge, содержащих германий, мас. %.
На рис. 1в приведены кинетические кривые окисления жидкого сплава системы Ba–Ge, содержащего 33.3 мас. % Ge (Ва2Ge) при температурах 1323, 1373 и 1423 К. В течение первых 10 мин окисление протекает по линейному закону, затем приобретает параболический характер.
В штрих-дифрактограммах продуктов окисления рассматриваемого сплава преобладают интенсивности, относящиеся к оксиду германия GeO2 (рис. 2). Это подтверждается также ИКС-исследованиями (табл. 2).
Это свидетельствует, что первоначально окисление проходило с образованием рыхлой пленки, далее процесс протекал с диффузионными затруднениями. Максимальный привес данного сплава при 1423 К составил 265 мг/см2. Истинная скорость окисления изменяется от 16 ⋅ 10–4 кг/м2 · с при 1323 К до 25 ⋅ 10–4 кг/м2 · с при 1423 К. Энергия активации окисления исследуемого сплава составляет 70.4 кДж/моль. Методами ИК-спектроскопии и РФА установлено, что оксидная пленка сплава, содержащего 33.3 мас. % Ge, состоит лишь из Ba2GeO4 (табл. 2 и 3).
На рис. 3а приведены кинетические кривые окисления расплава, соответствующего химическому соединению ВаGe (50 мас. % Ge). Исследования проведены при температурах 1473, 1523 и 1573 К. Процесс характеризуется низкими скоростями окисления, кинетические кривые подчиняются параболическому закону, лимитирующим этапом которого являются диффузионные процессы в оксидной пленке.
Рис. 3.
Кинетические кривые окисления расплавов системы Ва–Ge, содержащих германий, мас. %: а – 50; б – 66.7; в – 80.5; г – 91.5.
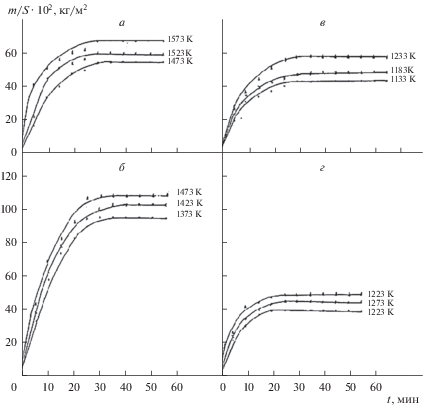
Для сплава данного состава при температуре 1573 К максимальная величина привеса Δm/S равна 34 мг/см2, минимальный привес 27 мг/см2 соответствует температуре 1473 К. Вычисленное значение энергии активации равняется 262 кДж/моль. Сложный оксид состава ВаGeО3 образуется лишь при окислении сплава, в котором соотношение Ва : Ge = 1 : 1. Это соотношение сохраняется также между компонентами в продуктах окисления (табл. 1 и 2). Данный оксид отличается высокими защитными свойствами, о чем свидетельствует высокое значение кажущейся энергии активации, равное 262 кДж/моль.
Окисление сплава, содержащего 66.7 мас. % Ge, что соответствует химическому соединению ВаGe2, с температурой плавления 1323 К изучали при температурах 1373, 1423 и 1473 К (рис. 3б). Характер кривых показывает, что окисление протекает по параболическому закону. Формирование оксидной пленки заканчивается к 30 минутам взаимодействия с кислородом воздуха. Рассчитанные значения истинной скорости окисления изменяется от 11 ⋅ 10–4 до 13.33 ⋅ 10–4 кг/м2 · с. Кажущаяся энергия активации процесса окисления составляет 115 кДж/моль. Продукты окисления данного сплава состоят из ВаGe4О9 и GeO2 (рис. 2).
Появление GeO2 в составе оксидной пленки несколько ухудшает его защитные свойства, о чем свидетельствует резкое падение величины кажущейся энергии активации от 262 кДж/моль для сплава с 50 мас. % до 115.2 кДж/моль для данного сплава, содержащего 66.7 мас. % Gе.
Кинетика окисления сплава эвтектического состава, содержащего 80.5 мас. % Gе, исследовали при температурах 1133, 1183 и 1233 К. Процесс характеризуется низкими скоростями окисления. Кинетические кривые окисления (рис. 3в) подчиняются параболическому закону. Истинная скорость окисления изменяется от 8 ⋅ 10–4 до 19 ⋅ 10–4 кг/м2 · с. Кажущаяся энергия активации равна 104.2 кДж/моль. При окислении данного сплава также образуется смесь оксидов BaGe4O9 и GeO2, которые обладают невысокими защитными свойствами (рис. 2).
Сплав, содержащий 91.5 мас. % Ge, окисляли при температурах 1223, 1273 и 1323 К. Кинетические кривые (рис. 3г), приближающиеся к параболической зависимости, характеризуют процесс, как взаимодействие металлического расплава с кислородом газовой фазы, который лимитируется диффузионными явлениями, т.е. массопереносом через оксидную пленку, а энергия активации равняется 127.7 кДж/моль.
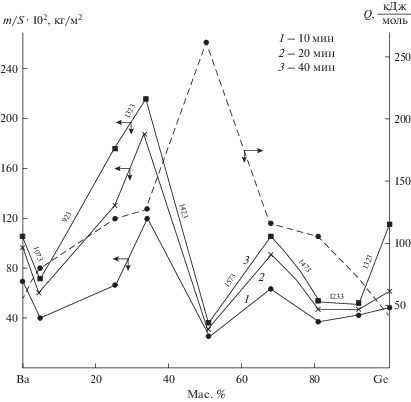
В обобщенном виде изохронны окисления расплавов системы Ва–Ge при 10, 20 и 40 мин приведены на рис. 4. Добавки германия несколько уменьшают скорость окисления жидкого бария, о чем свидетельствует рост энергии активации окисления сплава с 4 мас. % Gе. Добавки бария также уменьшают скорость окисления жидкого германия (табл. 1) за счет образования более сложных оксидов состава BaGe2O9 и BaGeO3, отличающихся высокими защитными свойствами.
ВЫВОДЫ
1. Методом термогравиметрии исследована кинетика окисления расплавов на основе Ва–Ge кислородом воздуха. Установлено, что добавки германия до 50 мас. % повышает устойчивость расплава к окислению. Скорость окисления сплавов с ростом температуры увеличивается независимо от химического состава. Истинная скорость окисления имеет порядок 10–4 кг/м2 · с1. Кажущаяся энергия активации окисления в зависимости от состава сплавов составляет 39.08–262 кДж/моль. Показано, что окисление сплавов починяется параболическому закону.
2. Методами РФА и ИКС показано, что продуктами окисления сплавов являются оксиды состава BaGe4O9 и GeO2. В процессе окисления сплавов доминирующая роль отводится оксиду BaGe4O9.
Список литературы
Липинских Б.М., Киселев В.И. Об окислении жидких металлов и сплавов кислородом из газовой фазы // Изв. АН СССР. Металлы. 1974. № 5. С. 51–54.
Вахобов А.В., Ганиев И.Н. Диаграммы состояния двойных систем с участием бария и стронция. Душанбе: Дониш. 1992.
Белоусова Н.В., Денисов В.М., Истомин С.А. и др. Взаимодействие жидких металлов и сплавов с кислородом. Екатеринбург: УрО РАН, 2004.
Денисов В.М., Истомин С.А., Подкопаев О.И. и др. Германий, его соединения и сплавы. Екатеринбург: УрО РАН. 2002.
Violetta K.P., Lydia M.P. Phase diagram of the Ge-rich of the Ba–Ge system and characterisation of single-phase BaGe4 // J. of Alloys and Compounds. 2014. 599. P. 228–233.
Олимов Н.С., Ганиев И.Н., Обидов З.Р., Ширинов М.Ч. Окисление сплавов системы Al–Ge, в жидком состояния // Расплавы. 2015. № 4. С. 1–8.
Ширинов М.Ч., Олимов Н.С., Ганиев И.Н., Джабборов Б.Б. Окисление сплавов системы барий–кремний, в жидком состоянии // Вестник педагогического университета им. С. Айни. 2012. 49. № 6. С. 37–39.
Зокиров Ф.Ш., Ганиев И.Н., Бердиев А.Э., Сангов М.М. Кинетика окисления сплава АК12М2, модифицированного барием, в твердом состоянии // Известия Санкт-Петербургский государственный технологический институт (технический институт). 2020. 81. № 55. С. 28–33.
Бокиев Л.А., Ганиев И.Н., Хакимов А.Х., Джайлоев Дж.Х., Якубов У.Ш. Кинетика окисления алюминиевого сплава АЖ5К10 с церием // Вестник технологического университета (г. Казань). 2020. 23. № 8. С. 35–38.
Ганиев И.Н., Джайлоев Дж.Х., Рашидов А.Р., Якубов У.Ш., Зувайдуллозода Ф.З. Кинетика окисления сплавов алюминия с никелем, в твердом состоянии // Вестник Санкт-Петербургского государственного университета технологии и дизайна. Серия 1. Естественные и технические науки. 2020. № 1. С. 104–108.
Давлатов О.Ш., Ганиев И.Н., Одиназода Х.О., Раджабалиев С.С. Кинетика окисления алюминиевого сплава АЖ2.4М5.3Мг1.1Ц4Кр3, легированного оловом, в твердом состоянии // Известия Санкт-Петербургского государственного технологического института (технического университета). 2021. 82. № 56. С. 17–22.
Джайлоев Дж.Х., Ганиев И.Н., Ганиева Н.И., Якубов У.Ш., Хакимов А.Х. Кинетика окисления алюминиевого сплава АЖ2.18, модифицированного стронцием // Вестник Сибирского государственного индустриального университета. 2019. 40. № 4. С. 34–39.
Назаров Ш.А., Ганиев И.Н., Irene Calliari., Бердиев А.Э., Ганиева Н.И. Кинетика окисления сплава Al + 6%Li, модифицированного лантаном, в твердом состоянии // Металлы. 2018. № 1. С. 34–40.
Назаров Ш.А., Ганиев И.Н., Эшов Б.Б., Ганиева Н.И. Кинетика окисления сплава Al + + 6%Li, модифицированного церием // Металлы. 2018. № 3 С. 33–38.
Ганиев И.Н., Ганиева Н.И., Эшова Д.Б. Особенности окисления алюминиевых расплавов с редкоземельными металлами // Металлы. 2018. № 3. С. 39–47.
Benhafid R., Belgacem Bouzida A., Djaballah Y., Candan A., İyigör A., Uğur G. Thermodynamic Modeling of the Al–Ba and Ba-Ge Systems Supported by First-Principles Calculations // J. Phase Equilib. Diffus. 2019. 40. P. 195–205.
Лякишев Н.П., Банных О.А., Рохлин Л.Л. и др. Диаграммы состояния двойных металлических систем: Д44 Справочник: В 3-х т.: Т. 1. М.: Машиностроение. 1996.
Дополнительные материалы отсутствуют.