Расплавы, 2023, № 2, стр. 144-155
Анодные процессы урановых сплавов, содержащих палладий и неодим в расплавах 3LiCl–2KCl–UCl3
Д. И. Никитин a, *, И. Б. Половов a, О. И. Ребрин a, А. В. Щетинский a, А. С. Дедюхин a
a Уральский федеральный университет
Екатеринбург, Россия
* E-mail: house.freshone@ya.ru
Поступила в редакцию 06.12.2022
После доработки 19.12.2022
Принята к публикации 16.01.2023
- EDN: MHPPRR
- DOI: 10.31857/S0235010623020081
Аннотация
На модуле переработки площадки опытно-демонстрационного энергетического комплекса Сибирского химического комбината поэтапно реализуется комбинированная технологическая схема переработки смешанного нитридного уран-плутониевого отработавшего топлива, состоящая из пирохимических операций, гидрометаллургического аффинажа урана, плутония и нептуния. Согласно данной схеме, целевые продукты пирохимической переработки, очищенные от основной массы продуктов деления с содержанием актиноидов не менее 99.9 мас. %, направляются на гидрометаллургический передел. Для пирохимической переработки необходимо разработать технологию элетрорафинирования металлизированного отработавшего ядерного топлива. Для проведения электролитического рафинирования необходимо определить процессы и режимы анодного растворения сплавов, моделирующих продукт этой головной операции “металлизации”. В настоящей работе представлены результаты исследования процессов анодного растворения модельных сплавов U–Pd и U–Pd–Nd с различными концентрациями палладия и неодима в расплавах на основе 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C с использованием различных методов. Урановые сплавы, содержащие палладий и неодим, были приготовлены прямым сплавлением металлического урана и порошков металлического палладия марки ПдАП-1, и металлического неодима (99.99%) в среде высокочистого аргона (99.998%). Электрохимические измерения проводили с использованием потенциостата/гальваностата Autolab 302N, оснащенного сильноточным модулем Booster 20A. Кривые анодной поляризации состоят только из одной волны окисления, которую отнесли к растворению металлического урана. Увеличение содержания палладия в сплаве с 1.5 до 10.0 мас. %, не влияет на форму поляризационных кривых. Увеличение содержания неодима в сплаве с 1.0 до 10.0 мас. % также не влияет на форму поляризационных кривых. Определены параметры электрорафинирования урановых сплавов, содержащих палладий и неодим. Предельная плотность тока выделения урана из урановых сплавов, содержащих палладий и неодим в электролите 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C, составила 0.4 А/см2. Показано, что в результате анодного растворения палладий в расплав не переходит, а неодим накапливается в электролите только при рафинировании сплава с содержанием 10.0 мас. % неодима, что существенно выше будущих реальных концентраций компонентов электрорафинируемого уранового сплава в технологической цепочке переработки отработавшего ядерного топлива.
ВВЕДЕНИЕ
Электролитическое рафинирование металлизированного отработавшего ядерного топлива (ОЯТ) в расплавленных солевых электролитах является одним из перспективных этапов пирохимической переработки ОЯТ. Целью рафинирующего электролиза является получение катодного осадка делящихся материалов (например, урана), в то время как электроположительные продукты деления (например, палладий) сохраняются в материале анода, а электроотрицательные продукты деления (например неодим) остаются в расплаве. Расплавленные соли на основе 3LiCl–2KCl имеют относительно низкую температуру плавления и могут использоваться в качестве рабочей среды для электроочистки ОЯТ.
Элементный состав ОЯТ зависит от множества факторов, а также изменяется во времени. В работе [1] показано, что при переходе от водных реакторов к реакторам на быстрых нейтронах наблюдается резкий рост выхода благородных металлов в ОЯТ. Среди продуктов деления одним из основных благородных металлов является палладий, образующийся с высоким выходом [2–4]. На текущий момент довольно широко исследованы фундаментальные термодинамические свойства интерметаллических соединений типа UxPdy [6–9]. Авторы подробно рассмотрели вопросы теплофизики и выполнили расчеты энергии Гиббса интерметаллидов UPd3, UPd4, U0.15Pd0.85. Также изучены различные параметры растворения интерметаллидов состава UPdx [10–11]. В литературе представлены диаграммы состояния систем U–Pd, U–Pd–Nd [12, 13], соответственно. В настоящее время в литературе отсутствуют данные о процессах анодного растворения сплавов U–Pd и U–Pd–РЗМ, исследованных в расплавах на основе 3LiCl–2KCl.
Задачей настоящей работы было изучение особенностей анодного растворения урановых сплавов, содержащих палладий и неодим в электролите 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В качестве рабочих солей-растворителей в экспериментах использовались хлорид калия (99.8%) и хлорид лития (99.0%). Отдельные хлориды щелочных металлов сушили в вакууме при 300°C в течение 3–5 ч. После этого соли расплавляли и продували смесью хлора и хлористого водорода в течение 5 ч. Дальнейшая обработка заключалась в продувке аргоном высокой чистоты (99.999%) для удаления растворенных хлорирующих агентов. Затем расплавленные соли заливали в алундовые тигли и охлаждали в эксикаторе. Полученные таким образом соли хранили в инертном сухом боксе, заполненном высокочистым аргоном (с контролем влаги и кислорода <10 ppm). Смеси хлоридов лития, калия и урана требуемого состава готовили в боксе с инертной атмосферой путем тщательного перемешивания очищенных индивидуальных солей непосредственно перед экспериментами.
Урановые сплавы, содержащие палладий и неодим, были синтезированы в печи резистивного нагрева прямым сплавлением металлического урана в виде брусков, порошка металлического палладия марки ПдАП-1, порошка металлического неодима (99.99%) в цилиндрическом тигле из оксида бериллия в среде высокочистого аргона (99.998%). Полученный слиток отделяли от тигля и перемещали в перчаточный бокс с инертной атмосферой, в котором слитки из уранового сплава приваривали аргонодуговой сваркой к токоподводу из молибдена марки МЧ. Рабочая поверхность электрода была экранирована трубкой из оксида бериллия, таким образом, торец электрода выполнял роль рабочей поверхности. Фотография уранового сплава с приваренным токоподводом и готовый электрод показаны на рис. 1.
Рабочие части электродов были прикреплены к молибденовым проволокам, а точка контакта располагалась над расплавом, чтобы предотвратить процессы переноса без тока. Рабочий электролит выдерживали в стеклоуглердном тигле. Стеклоуглеродный тигель также служил противоэлектродом. Все измерения выполнены с использованием хлорного электрода сравнения. Эксперименты проводили в специально сконструированной реторте с водяным охлаждением из нержавеющей стали, подробно описанной в [14–15], (рис. 2) при температуре 550°C в атмосфере высокочистого аргона.
Во время экспериментов по гальваностатическому растворению сплавов в качестве катода использовался отдельный катодный узел. Узел представлял из себя молибденовый электрод, погруженный в расплав хлорида свинца в чехле из кварца и отделенный от остального расплава диафрагмой из асбеста (рис. 3).
Такое конструктивное решение катодного узла было использовано для того, чтобы исключить выделение щелочного металла в катодной зоне, в начальный момент электролиза, и для аналитической оценки процесса накопления урана в расплаве. Контроль температуры в рабочей зоне осуществлялся с помощью кабельной термопары типа хромель–алюмель. Электрохимические измерения проводили с использованием потенциостата/гальваностата Autolab 302N, оснащенного сильноточным модулем Booster 20A.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Урановые сплавы, содержащие палладий
Для определения величины электродного потенциала растворения в данной работе гальваностатическим коммутаторным и хронопотенциометрическим методами изучены процессы анодной поляризации уран-палладиевых сплавов. Все эксперименты проводили в расплавах 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при температуре 550°C. Полученные хронопотенциограммы показаны на рис. 4.
Рис. 4.
Зависимости “потенциал–время”, зафиксированные в процессе анодного растворения сплава в расплаве 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C, плотностях тока 0.12–1.20 А/см2: а – U–Pd (1.5 мас. %), б – U–Pd (10.0 мас. %).
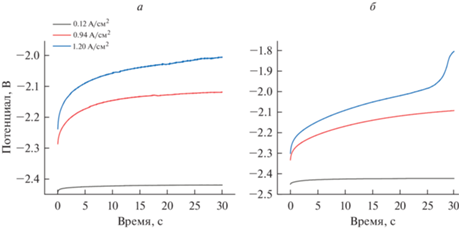
При плотностях тока менее 0.94 А/см2 присутствие палладия в материале электрода не отражается на характере кривых “потенциал–время” анодного растворения урановых сплавов. Каких-либо перегибов на кривых включения, связанных с наложением электродных процессов при низких плотностях тока (ниже 0.94 А/см2) обнаружить не удалось.
Вместе с тем в сплаве с содержанием палладия 10.0 мас. % при плотностях тока выше 1.0 А/см2 на хронопотенциограммах появляется перегиб, сопровождающийся ростом потенциала, что может быть обусловлено достижением потенциала растворения интерметаллида UPd3 [11, 12] или формированием в приэлектродном слое непроводящей солевой фазы. При растворении сплава с содержанием палладия 1.5 мас. % даже при максимальных для использованного прибора токах (1.20 А/см2) подобных перегибов не наблюдается.
Вывод об отсутствии влияния на характер растворения, увеличение концентрации палладия в материале электрода, подтверждается сравнением поляризационных кривых (рис. 5) для сплавов с 1.5 и 10.0 мас. % палладия.
Рис. 5.
Сравнение анодной поляризации сплавов U–Pd в расплаве 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C.

Увеличение плотности анодного тока до 0.4–0.5 А/см2 приводит к значительной поляризации, что может привести к ионизации примесных компонентов, растворению интерметаллидов палладия или инициированию перезарядки урана U(III) → U(IV).
Исходя из полученных данных, можно сделать вывод, что повышение плотности анодного тока выше 0.4 А/см2 нежелательно.
Была проведена серия экспериментов по гальваностатическому анодному растворению U–Pd сплава при плотностях тока 0.35 А/см2 (для 10.0 мас. % палладия в сплаве). В эксперименте использовали катодный узел, показанный на рис. 3. Электролиз проводили поэтапно с интервалом в 3 ч. После окончания каждого цикла электролиза отбирали пробу электролита для химического анализа на содержание урана и палладия. Пробоотбор проводили кварцевым капилляром. Изменение содержания урана в солевом расплаве в процессе анодного растворения сплавов уран–палладий представлено на рис. 5.
Из данных представленных на рис. 6 видно, что процесс анодного растворения переходит в режим насыщения, при этом концентрация урана в расплаве практически перестает изменяться. Данное насыщение может быть связано с превышением растворимости трихлорида урана в электролите при заданных условиях и выпадением в твердую фазу соединения K2UCl5 [16]. В результате проведенных экспериментов и полученных данных о процессе анодного растворения сплавов урана с палладием можно сделать вывод, что при плотностях тока до 0.35 А/см2 не происходит растворения палладия и перехода его из металлической фазы в солевую.
Урановые сплавы, содержащие палладий и неодим
Для определения величины сдвига электродного потенциала сплава U–Pd–Nd в данной работе гальваностатическим коммутаторным и хронопотенциометрическим методами изучены процессы анодной поляризации урановых сплавов, содержащих палладий и неодим. Все эксперименты проводились в расплавах 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при температуре 550°C. Полученные хронопотенциограммы показаны на рис. 7.
Рис. 7.
Зависимости “потенциал–время”, зафиксированные в процессе анодного растворения сплава в расплаве 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C, плотностях тока 0.12–1.20 А/см2: а – U–Pd (1.5 мас. %)–Nd (1.0 мас. %), б – U–Pd (1.5 мас. %)–Nd (10.0 мас. %).

При плотностях тока до 1.20 А/см2 присутствие заданных концентраций палладия и неодима в материале электрода не отражается на характере кривых “потенциал–время” анодного растворения урановых сплавов. Каких-либо перегибов на кривых включения, связанных с наложением электродных процессов при плотностях тока до 1.20 А/см2 обнаружить не удалось.
Вместе с тем в сплаве с высоким содержанием неодима (10.0 мас. %) при плотностях тока 1.20 А/см2 на хронопотенциограммах отмечена нестабильность, что может быть обусловлено разрушением поверхности анода или осыпанием интерметаллида UPd3.
Вывод об отсутствии влияния на характер растворения увеличения концентрации палладия и неодима в материале электрода подтверждается сравнением поляризационных кривых (рис. 8) для сплавов с 1.5 мас. % палладия и от 1.0 до 10.0 мас. % неодима.
Рис. 8.
Сравнение анодной поляризации сплавов U–Pd–Nd в расплаве 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C.

Как и в случае с изучением U–Pd сплавов была проведена серия экспериментов по гальваностатическому анодному растворению U–Pd–Nd сплава при плотности тока 0.35 А/см2 (для 10.0 мас. % неодима в сплаве). Электролиз проводили аналогичным, ранее описанным образом, с интервалом в 3 ч. После окончания каждого цикла электролиза отбирали пробу электролита для анализа расплава на содержание урана, палладия и неодима. Изменение содержания компонентов слава в солевом расплаве в процессе анодного растворения электрода представлено на рис. 9.
Рис. 9.
Содержание урана, палладия и неодима в электролите при анодном растворении сплава U–Pd (1.5 мас. %)–Nd (10.0 мас. %) в расплаве 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C.

Полученные данные о ходе растворения U–Pd–Nd сплава в электролите (рис. 7 и 8) показали, что палладий, входящий в анодный материал не переходит в электролит. Неодим накапливается в электролите в количестве существенно меньшем, чем уран. Накопление урана приходит в режим насыщения при концентрации в электролите около 25.0 мас. %, что определяется фазовой диаграммой состояний [16], которая накладывает ограничение по растворимости UCl3 в 3LiCl–2KCl, что приводит к образованию твердой фазы-соединения K2UCl5.
ЗАКЛЮЧЕНИЕ
Процессы анодного растворения урановых сплавов, содержащих палладий и неодим с различным содержанием компонентов были подробно изучены гальваностатическим коммутаторным и хронопотенциометрическим методами. В дополнение к стационарным и нестационарным электрокинетическим методам исследования использовался метод аналитического контроля содержания палладия в расплавах на основе 3LiCl–2KCl при электролизе с заданной плотностью анодного тока. Кривые анодной поляризации состоят только из одной волны окисления, которую можно отнести к растворению металлического урана. Увеличение содержания палладия в сплаве с 1.5 до 10.0 мас. %, не влияет на форму поляризационных кривых. Увеличение содержания неодима в сплаве с 1.0 до 10.0 мас. % также не влияет на форму поляризационных кривых. Также были изучены предельные токи выделения урана из урановых сплавов, содержащих палладий и неодим. В электролите 3LiCl–2KCl–UCl3 (10.1 мас. % UCl3) при 550°C, предельная анодная плотность тока составила 0.4 А/см2.
При плотности тока 0.35 А/см2, даже при длительном растворении сплава (10 А · ч) палладий в расплав не переходит, а ионы неодима накапливаются в электролите только при рафинировании сплава с его содержанием 10.0 мас. %
Реальная концентрация компонентов сплава в технологической цепочке переработки отработавшего ядерного топлива будет значительно ниже, чем 10 мас. %, соответственно, замедлится и нежелательный процесс перехода неодима в расплав. В процессе электрорафинирования не будет достигаться и предельное содержание ионов урана в расплаве в следствии его постоянного выделения на катоде.
Работа была выполнена при финансовой поддержке АО “Прорыв”.
Список литературы
Imoto S. Chemical state of fission products in irradiated UO2 // Nuclear Materials. 1986. 140. № 1. P. 19–27.
Bush R.P., Recovery of platinum group metals from high levelradioactive waste. Possibilities of separation and use re-evaluated // Platinum Metals Reviews. 1991. 35. № 4. P. 202–208.
Любимов Д.Ю., Дерябин И.А., Булатов Г.С., Гедговд К.Н., Термодинамическое моделирование фазового состава смешанного уранплутониевого мононитрида с примесью кислорода при облучении до выгорания 140 ГВт сут/т и температуре 900—1400 K // Атомная энергия. 2015. 118. № 1. С. 24–19.
Булатов Г.С., Гедговд К.Н., Любимов Д.Ю., Термодинамический анализ химического и фазового составов облученного быстрыми нейтронами уран-плутониевого нитрида в зависимости от температуры и выгорания // Материаловедение. 2009. 1. С. 2–7.
Kleykamp H. The chemical state of the fission products in oxide fuels // Nuclear Materials. 1985. 131. № 2–3. P. 221–246.
Middlemas S.C., Craig M.M., Adkins C.A., Lemma F.D., Tolman K.R., Benson M.T., Hin C.J. Effects of intermetallic compounds on the thermophysical properties of uranium–palladium alloys // Alloys and Compounds. 2021.
Prasad R., Dash S., Parida S.C., Singh Z., Venugopal V.J. Gibbs energy of formation of UPd3(s) // Nuclear Materials. 2000. 277. № 1. P. 45–48.
Kleykamp H. Highlights of experimental thermodynamics in the field of nuclear fuel development // Nuclear Materials. 2005. 344. № 1–3. P. 1–7.
Cordfunke E.H.P., Muis R.P., Wijbenga G., Burriel R., Zainel H., To M., Westrum. E.F.Jr., Thermodynamics of uranium intermetallic compounds. I. Heat capacity of UPd3 from 5 to 850 K // The Journal of Chemical Thermodynamics. 1988. 20. P. 815–823.
Кесикопулос В.А., Потапов А.М., Дедюхин А.Е., Зайков Ю.П. Изготовление интерметаллида UPd3 и исследование его термодинамических характеристик // Сборник трудов семинара “Электрохимия в распределенной и атомной энергетике”. Нальчик. Ажур. 2022. С. 224–226.
Strepetov K.E., Osipenko A.A., Volkovich V.A. Electrochemical behavior of uranium–palladium alloys in molten eutectic mixture of lithium, potassium and cesium chlorides // AIP Conference Proceedings 2022. 2466. № 1. P. 050033.
Okamoto H. Pd–U (Palladium–Uranium) // Journal of Phase Equilibria. 1992. 13. № 2. P. 222–223.
Parnell D.G., Brett N.H., Haines H.R., Potter P.E. Phase relationships in the ternary system U–Nd–Pd // J. Less Common Metals. 1986. 118. № 1. P. 141–152.
Zolotarev D.A., Nikitin D.I., Polovov I.B. Electrode processes in 3LiCl–2KCl–UCl3 melts: Investigation of temperature and uranium concentration influence // AIP Conference Proceedings 2019. 2174. P. 020276.
Никитин Д.И., Половов И.Б., Щетинский А.В., Дедюхин А.С., Волкович В.А., Ребрин О.И. Процессы анодного растворения сплавов U–Pd в расплавах 3LiCl–2KCl–UCl3 // Сборник трудов семинара “Электрохимия в распределенной и атомной энергетике”. Нальчик. Ажур. 2022. С. 294–297.
Hames A.L., Paulenova A., Willit J.L., Williamson M.A. Phase Equilibria Studies of the LiCl–KCl–UCl3 System // Journal Nuclear Technology. 2018. 203. № 3. P. 272–281.
Дополнительные материалы отсутствуют.






