Теплоэнергетика, 2022, № 3, стр. 31-40
Развитие модели радиолиза воды в модуле AERMOD
Д. С. Синицын a, *, Д. А. Назаров a, О. В. Тарасов a, Н. А. Мосунова a, А. А. Сорокин a, b, **
a Институт проблем безопасного развития атомной энергетики РАН
115191 Москва, Большая Тульская ул., д. 52, Россия
b Объединенный институт высоких температур РАН
125412 Москва, Ижорская ул., д. 13, стр. 2, Россия
* E-mail: sinitcyn.dmitriy@mail.ru
** E-mail: sorokin@ibrae.ac.ru
Поступила в редакцию 18.07.2021
После доработки 02.08.2021
Принята к публикации 25.08.2021
- EDN: IYTDPF
- DOI: 10.1134/S0040363622030092
Аннотация
При развитии аварийных ситуаций, связанных с разгерметизацией твэлов, на водо-водяных энергетических реакторах (ВВЭР) для правильного моделирования поведения продуктов деления необходимо учитывать их потенциальное взаимодействие с накопленными в теплоносителе продуктами радиолиза. Поскольку такое взаимодействие способно повлечь за собой образование значительного количества летучих соединений, которые могут представлять угрозу при выходе в окружающую среду, был создан соответствующий блок в интегральном коде, который позволяет моделировать данное явление. В работе представлено описание модели радиолиза воды в составе модуля AERMOD, разработанной для расчета радиационно-химических превращений в воде при воздействии ионизирующего излучения. Модель позволяет отслеживать изменение концентраций отдельных продуктов радиолиза при различных значениях начальной концентрации примесей в воде и мощности поглощенной дозы. Модель дополнена также механизмом межфазного переноса для определения выхода летучих продуктов радиолиза (например, водорода) в газовый объем. Представлен метод численного решения полученных систем уравнений, проведено сравнение модели с существующими отечественными аналогами. Приведены результаты валидации на экспериментальных данных модели радиолиза воды и выхода водорода в газовую полость.
В статье описаны алгоритмы и программная реализация модели радиолиза воды в расчетном модуле AERMOD, предназначенном для расчетного обоснования безопасности реакторов типа ВВЭР. Он включает в себя моделирование всех основных физико-химических процессов образования и динамики аэрозолей и радиационно-химических процессов продуктов деления в I контуре реактора при разгерметизации твэлов и выходе продуктов деления в поток теплоносителя. Модуль AERMOD может использоваться при расчете их поведения и радиолиза воды в бассейне выдержки. Модуль входит в состав теплогидравличекого кода HYDRA-IBRAE/H2O программно-технического комплекса “Виртуально-цифровая АЭС с ВВЭР”.
Следствием радиолиза воды при воздействии ионизирующего излучения является образование взрывоопасной смеси водорода и кислорода в газопаровых областях элементов I контура ВВЭР: в компенсаторе давления, коллекторах парогенератора и под крышкой реактора, особенно при его эксплуатации в переходных режимах – расхолаживания, горячего и холодного останова и разогрева. Кроме того, при наличии негерметичных твэлов в теплоносителе будут протекать различные химические реакции между продуктами радиолиза и продуктами деления. В результате продукты деления, такие как йод, цезий, теллур, могут переходить в летучие соединения [${{I}^{ - }} \to {{I}_{2}}(газ),$ аэрозоль CsI, SnTe, CsxTey]. Аналогичные процессы могут происходить и в бассейне выдержки. Поэтому для описания процесса образования продуктов радиолиза воды и их взаимодействия с продуктами деления представляется важной разработка специального программного модуля в составе интегрального кода оценки безопасности реактора с водяным теплоносителем.
МОДЕЛЬ, МЕТОД РЕШЕНИЯ И ПРОГРАММНАЯ РЕАЛИЗАЦИЯ В КОДЕ
В основу модели радиолиза воды в расчетном модуле AERMOD положена схема химических реакций в воде и ее растворах с примесями Н2, Н2О2 и O2, инициируемых воздействием ионизирующего излучения. Модель относится к гомогенному этапу процесса радиолиза, который наступает примерно спустя 0.1 мкс после начала облучения [1, 2]. К этому моменту времени области с первичными ионами и радикалами в воде (“шпоры”) приходят к относительному равновесию по составу ионов и радикалов и равномерно распределяются в объеме облучаемого раствора. Предполагается наличие однофазного замкнутого объема жидкости с одинаковой мощностью поглощенной дозы во всех точках.
Используемый набор реакций между продуктами радиолиза представлен в табл. 1 и соответствует данным из работы [3]. Схема реакций применима для воды с показателем кислотности pH в диапазоне от 1 до 10. Этот диапазон pH может быть расширен до 13 при добавлении реакций из табл. 2. Данные наборы сопровождаются константами, используемыми для вычисления скорости реакции в зависимости от температуры среды.
Таблица 1.
Реакции, используемые для моделирования радиолиза воды, их константы скорости и значения энергии активации ${{E}_{a}}$ (pH = 1–10)
| Реакция | υf, дм3/(моль ∙ с) | Ea, кДж ∙ моль |
|---|---|---|
| OH + H2 = H + H2O | 3.74 × 107 | 18.0 |
| OH + ${\text{HO}}_{2}^{ - }$ = OH– + HO2 | 7.50 × 107 | 12.6 |
| OH + H2O2 = HO2 + H2O | 3.80 × 107 | 14.0 |
| OH + ${\text{O}}_{2}^{ - }$ = O2 + OH– | 9.96 × 109 | 12.6 |
| OH + HO2 = O2 + H2O | 7.10 × 109 | 12.6 |
| OH + OH = H2O2 | 5.30 × 109 | 8.0 |
| OH + eaq* = OH– | 3.0 × 1010 | 12.6 |
| H + O2 = HO2 | 2.0 × 1010 | 12.6 |
| H + ${\text{O}}_{2}^{ - }$ = ${\text{HO}}_{2}^{ - }$ | 2.0 × 1010 | 12.6 |
| H + HO2 = H2O2 | 2.0 × 1010 | 12.6 |
| H + H2O2 = OH + H2O | 3.44 × 107 | 13.6 |
| H + OH = H2O | 7.0 × 109 | 12.6 |
| H + H = H2 | 7.9 × 109 | 12.6 |
| eaq + O2 = O2– | 1.94 × 1010 | 13.0 |
| eaq + ${\text{O}}_{2}^{ - }$ = OH– + ${\text{HO}}_{2}^{ - }$ | 1.3 × 1010 | 18.8 |
| eaq + HO2 = ${\text{HO}}_{2}^{ - }$ | 2.0 × 1010 | 12.6 |
| eaq + H = H2 + OH– | 2.5 × 1010 | 12.6 |
| eaq + H2O2 = OH + OH– | 1.14 × 1010 | 15.1 |
| eaq + H+ = H | 2.3 × 1010 | 12.2 |
| eaq + eaq = H2 + OH– + OH– | 5.6 × 109 | 20.5 |
| O2– + HO2 = O2 + ${\text{HO}}_{2}^{ - }$ | 9.5 × 107 | 8.8 |
| HO2 + HO2 = H2O2 + O2 | 8.1 × 105 | 24.7 |
| HO2 + H2O2 = H2O + O2 + OH | 3.7 | 20.0 |
| HO2 = H+ + ${\text{O}}_{2}^{ - }$ | 7.0 × 105** | 12.6 |
| H2O2 = H+ + ${\text{HO}}_{2}^{ - }$ | 3.56 × 10‒2*** | 12.6 |
| H2O = H+ + OH– | 2.5 × 10‒5**** | 12.6 |
| H + OH– = eaq + H2O | 1.80 × 107 | 26.0 |
| ${\text{O}}_{2}^{ - }$ + O2– = ${\text{HO}}_{2}^{ - }$ + O2 + OH– | 0.3 | 12.6 |
| ${\text{O}}_{2}^{ - }$ + H2O2 = O2 + OH– + OH | 16.0 | 20.0 |
Таблица 2.
Дополнительные реакции, используемые для моделирования радиолиза воды, и их константы скорости (pH = 1–10)
| Реакция | υf, дм3/(моль ∙ с) |
|---|---|
| OH– + OH = O– + H2O | 1.3 × 1010* |
| O– + OH– = ${\text{HO}}_{2}^{ - }$ | 2.0 × 1010 |
| O– + O– = ${\text{HO}}_{2}^{ - }$ + OH– | 1.0 × 109 |
| O– + eaq = OH– + OH– | 2.2 × 1010 |
| O– + ${\text{O}}_{2}^{ - }$ = O2 + OH– + OH– | 6.0 × 108 |
| O– + H2O2 = ${\text{O}}_{2}^{ - }$ + H2O | 5.0 × 108 |
| O– + ${\text{HO}}_{2}^{ - }$ = ${\text{O}}_{2}^{ - }$ + OH– | 4.0 × 108 |
| O– + H2 = H + OH– | 8.0 × 107 |
| O– + ${\text{O}}_{2}^{ - }$ = ${\text{O}}_{3}^{ - }$ | 3.6 × 109** |
| O– + ${\text{O}}_{3}^{ - }$ = ${\text{O}}_{2}^{ - }$ + ${\text{O}}_{2}^{ - }$ | 7.0 × 108 |
| ${\text{O}}_{3}^{ - }$ + H2O2 = O2 + ${\text{O}}_{2}^{ - }$ + H2O | 1.6 × 106 |
| ${\text{O}}_{3}^{ - }$ + HO2– = O2 + ${\text{O}}_{2}^{ - }$ + OH– | 8.9 × 105 |
| ${\text{O}}_{3}^{ - }$ + H2 = O2 + H + OH– | 2.5 × 105 |
| ${\text{O}}_{3}^{ - }$ + OH = O2 + ${\text{HO}}_{2}^{ - }$ | 8.5 × 109 |
| ${\text{O}}_{2}^{ - }$ + ${\text{HO}}_{2}^{ - }$ = O2 + OH– + O– | 0.13 |
| ${\text{HO}}_{2}^{ - }$ + eaq = OH– + O– | 3.5 × 109 |
Радиационно-химические процессы, протекающие в водном растворе при данных условиях, могут быть описаны с помощью моно- и бимолекулярных уравнений. Математическую модель для гомогенной смеси продуктов радиолиза в выделенном объеме водной среды можно представить системой обыкновенных дифференциальных уравнений следующего вида:
Данная система дифференциальных уравнений принадлежит классу “жестких” систем, для которых характерна возможность наличия одновременно для разных компонентов существенно различных временных масштабов изменения их концентрации. Это явление обусловлено большим различием в константах скоростей химических реакций и концентрациях компонентов. При использовании явных разностных схем для решения такой системы уравнений может потребоваться неприемлемо малый шаг по времени. Поэтому для решения был выбран неявный метод Розенброка 3-го порядка [4]. Этот метод является сравнительно быстрым, одношаговым, и для него в поставленной задаче существует возможность получить якобиан системы уравнений, что имеет решающее значение для эффективности и надежности данного расчетного метода.
При программной реализации модели радиационно-химических превращений в воде одним из основных условий была универсальность работы модуля. Под универсальностью понимается возможность для пользователя самостоятельно расширять список используемых в расчете реакций с указанием соответствующих констант скоростей, не затрагивая при этом непосредственно программную часть. При этом пользователь может выбрать набор реакций, который он хочет применить в своих расчетах, поскольку модуль сам сформирует систему уравнений и соответствующую матрицу Якоби для численного решения.
Отличительной особенностью моделируемого процесса является тот факт, что продукты радиолиза обладают разной степенью летучести. Такие продукты с конечной скоростью могут дегазироваться из раствора и переходить в газовую фазу над ним. Поэтому при разработке модуля радиолиза учитывалась необходимость одновременного расчета межфазного переноса продуктов радиолиза. При этом важно было учитывать, что межфазный перенос происходит одновременно с испарением воды со свободной поверхности. Данное явление играет определяющую роль, например, при радиолизе воды в бассейне выдержки отработанного ядерного топлива (ОЯТ). Кроме того, испарение воды оказывает существенное влияние на выход и накопление водорода в парогазовых зонах контура циркуляции.
Процессы радиолиза и массопереноса различаются характерным временем протекания, поэтому при программной реализации логично разделить их на два последовательных блока вычислений. На рис. 1 в соответствии с работой [5] приведена схема процесса массообмена растворимых в воде газов в условиях сопутствующего испарения воды с поверхности в приближении двухпленочной модели.
Рис. 1.
Дегазация неконденсирующегося газа в приближении двухпленочной модели. Концентрация вещества: Cg – в газообразном состоянии; $C_{g}^{{int}}$ – в газообразном состоянии на межфазной границе; Cl – в растворенном состоянии; $C_{l}^{{int}}$ – в растворенном состоянии на межфазной границе; толщина пограничного слоя: δg – со стороны газа; δl – со стороны жидкости
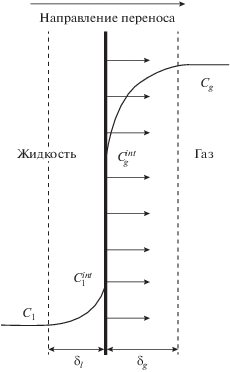
Согласно модели из [5], формулы для потоков массы растворимой примеси через поверхность раздела фаз, кг/с, могут быть записаны следующим образом:
После некоторых преобразований можно прийти к системе следующих дифференциальных уравнений для расчета концентраций примесей в жидкой и газовой фазах:
Очевидно, что в отсутствие испарения $(E = 0)$ система упрощается и переходит в классический вариант уравнений межфазного массообмена.
Коэффициенты массообмена получены в [5] при условии доминирования естественной конвекции вблизи поверхности воды. В этом случае коэффициент массопереноса для газовой примеси можно оценить из соотношения подобия с переносом молекул воды в паровой фазе:
Использование такой модели для описания массопереноса через границу раздела фаз позволяет моделировать процесс при различных значениях температуры фаз и давлений в системе. Решение данной системы уравнений реализовано в модуле с использованием модифицированного метода Эйлера.
Следует отметить, что наиболее известными в России аналогичными программными средствами для расчета радиолиза воды при воздействии ионизирующего излучения являются код МОРАВА-H2 [6] и йодный модуль в составе кода КУПОЛ-М [7].
Код МОРАВА-Н2 предназначен для описания процесса образования и распределения водорода и других газов, а также технологических добавок теплоносителя в оборудовании I контура реакторных установок с ВВЭР в проектных режимах эксплуатации, включая проектные аварии. Программное средство может применяться также для анализа химического состава теплоносителя при разработке и обосновании норм водно-химического режима I контура и при расследовании инцидентов, связанных с его нарушениями. В расчетах учитываются следующие явления: радиолиз жидкой фазы теплоносителя, радиолиз водяного пара, пароциркониевая реакция и межфазный перенос веществ. Решение системы дифференциальных уравнений реализовано с помощью неявного метода Гира. При решении уравнений массопереноса используется метод Рунге–Кутты 4-го порядка. Валидацию модели проводили как на данных лабораторных экспериментов, так и на результатах измерений на действующих энергоблоках с ВВЭР.
Стоит отметить, что используемый набор реакций и реагирующих компонентов в коде фиксирован, и возможность его расширения или изменения без участия разработчика не предусмотрена. Базовые модули программы реализованы на алгоритмических языках Pascal, Fortran и Assembler. Погрешность расчета концентраций компонентов в элементах оборудования по программе МОРАВА-Н2 в сравнении с экспериментальными данными может достигать 50%.
Цель разработки йодного модуля в составе кода КУПОЛ-М – прогнозирование радиационных последствий, вызванных выбросами радиоактивного йода в помещениях защитной оболочки ВВЭР. Соответственно в коде моделируется большой перечень физико-химических явлений, связанных с поведением йода в водной и паровоздушной атмосфере. В коде реализована модель радиолиза водного теплоносителя, необходимая для правильного описания химических взаимодействий растворенного йода. Также большой блок кода посвящен расчету показателя кислотности pH теплоносителя. В коде реализована модель межфазного массопереноса для водорода, летучих соединений йода и других примесей. Для решения системы дифференциальных уравнений, так же как и в коде МОРАВА-Н2, используется метод Гира. Изначально модуль был создан с применением пакета MATLAB, однако для его интеграции в код КУПОЛ-М он был переписан с использованием языка Fortran 77. При этом за основу метода решения системы дифференциальных уравнений из свободной математической библиотеки SLATEC был взят пакет DASSL. Погрешность при расчете изменения показателя кислотности воды в сравнении с экспериментальными данными составляет 5%, а при расчете концентрации соединений йода варьируется в диапазоне от 10 до 35%.
Таким образом, каждый из указанных кодов имеет определенные преимущества и недостатки. Код МОРАВА-Н2 широко используется на практике и обладает большой валидационной базой в части механизмов радиолиза воды. При этом он является автономным с фиксированной системой химических реакций, что ограничивает область его применения для отличных от рассматриваемых в коде условий. Йодный модуль кода КУПОЛ-М используется в задачах оценки радиационной безопасности в помещениях станции. Его отличительная особенность – детальная модель физико-химического поведения соединений с йодом, не затрагивающая других продуктов деления, поэтому применение данного кода ограничено расчетами для условий в помещениях защитной оболочки водо-водяного реактора.
Сравнение модели радиолиза в модуле AERMOD с моделями из этих кодов по набору и константам реакций радиолиза воды и полученным расчетным результатам будет представлено в отдельной публикации.
РЕЗУЛЬТАТЫ ВАЛИДАЦИИ
Валидацию приведенной в работе модели радиолиза воды выполняли с привлечением результатов нескольких экспериментов. В данной работе для примера представлена только часть из них.
В соответствии с рекомендациями РБ-166-20 оценка погрешностей результатов расчетов, полученных по программе для ЭВМ, основывается на методике, описанной в стандарте ASME V&V 20 – 2009 [8], а также на методиках, разработанных в ИБРАЭ РАН [9]. При валидации для каждого эксперимента проводилось 100 многовариантных расчетов (данное число удовлетворяет требованиям указанных методик), в которых основные параметры варьировались случайным образом в диапазоне, определяемом с учетом экспериментальных погрешностей. Распределение параметров по интервалу предполагалось гауссовым. Данное число расчетов обеспечивает покрытие двустороннего интервала с вероятностью выше 0.9. В результате проведения многовариантных расчетов были получены коэффициенты чувствительности многомерной линейной регрессии к каждому из варьируемых параметров и затем представлены в виде гистограмм. При последующем статистическом анализе вычислялись минимальные, средние и максимальные значения моделируемых параметров.
Основным результатом проведенного соответственно методике [8, 9] анализа погрешности расчетных результатов является определение интервала полученных погрешностей [ε ‒ utot, ε + utot], где ε – отклонение результата расчета по программе для ЭВМ от экспериментальных данных, использованных для ее валидации; utot – неопределенность валидации, зависящая от неопределенности исходных данных, неопределенности измерений и неопределенности численных методов, реализованных в программе для ЭВМ.
Главной целью проведения эксперимента [10] являлось исследование влияния растворенных в воде водорода и кислорода на процессы образования и разложения пероксида водорода при гамма-радиолизе раствора воды. Для этого в эксперименте с помощью источника гамма-квантов 60Co в специальной камере облучали герметичные стеклянные ампулы, содержавшие различные растворы вышеуказанных веществ. Проводился промежуточный анализ состава растворов на заданных промежутках времени. На рис. 2 показано изменение концентрации пероксида водорода ${{C}_{{{{H}_{2}}{{O}_{2}}}}}$ в растворе в зависимости от времени облучения $\tau $ при начальных концентрациях кислорода и водорода в растворе – 25.8 и 700 мкмоль/дм3 соответственно.
Рис. 2.
Изменение во времени $\tau $ концентрации пероксида водорода ${{C}_{{{{H}_{2}}{{O}_{2}}}}}$ в образце при начальном значении концентрации ${{C}_{{{{{\left( {{{O}_{2}}} \right)}}_{0}}}}}$ = 25.8 мкмоль/дм3, ${{C}_{{{{{\left( {{{H}_{2}}} \right)}}_{0}}}}}$ = 700 мкмоль/дм3. Пунктирные линии – минимальные и максимальные расчетные значения; сплошная линия – среднее расчетное значение; символы – данные эксперимента с погрешностью
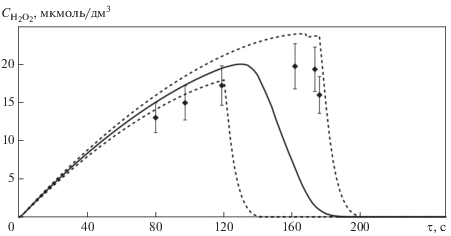
Как видно из представленных на рис. 2 данных, концентрация пероксида водорода увеличивается с ростом поглощенной энергии излучения до момента, пока кислород полностью не израсходуется. После этого начинается быстрое уменьшение содержания пероксида в растворе. Такое поведение обусловлено следующими реакциями:
Изначально находящийся в растворе водород реагирует с образующимися из-за радиолиза OH-радикалами по реакции (1) с образованием атомов H. Затем, из-за наличия в растворе кислорода вследствие реакции (2) и начальной его добавки, атомарный водород преимущественно реагирует по (3) с образованием пероксильного радикала, поскольку скорость реакции (3) на два порядка больше, чем реакции (4). Как только весь кислород прореагировал, водород начинает интенсивно разрушать накопившийся пероксид, запуская цепные реакции (4) и (1).
Максимальное отклонение результатов расчетов от экспериментальных данных для максимальной концентрации пероксида водорода не превысило 5%, а для момента достижения максимальной концентрации отклонение составило 25%. Значения неопределенности валидации для указанных величин не превышают 19% (табл. 3).
Таблица 3.
Оценка погрешностей результатов расчетов для экспериментов из работы [10] (результат моделирования эксперимента № 2 представлен на рис. 2)
| Номер эксперимента | Показатель | Отклонение ε, % | Неопределенность валидации utot, % | [ε – utot; ε + utot], % |
|---|---|---|---|---|
| 1 | Максимальная концентрация H2O2 | 0.7 | 18.8 | [–18.1; 19.5] |
| Время достижения максимума | –24.8 | 18.1 | [–42.9; –6.7] | |
| 2 | Максимальная концентрация H2O2 | 1.4 | 18.7 | [–17.3; 20.1] |
| Время достижения максимума | –19.6 | 14.6 | [–34.2; –5.0] | |
| 3 | Максимальная концентрация H2O2 | 4.0 | 18.2 | [–14.2; 22.2] |
| Время достижения максимума | –18.1 | 13.7 | [–31.8; –4.4] |
Цель следующего эксперимента [11] состояла в исследовании радиолиза водных растворов, содержащих примеси пероксида водорода, водорода и кислорода при воздействии гамма-излучения. Для этого с помощью 60Co облучали герметичные стеклянные ампулы с различными растворами указанных веществ. В процессе облучения проводился промежуточный анализ состава растворов на заданных промежутках времени. На рис. 3 для сравнения показаны расчетные и экспериментальные данные изменения концентрации веществ в системе в зависимости от времени облучения $\tau $ при следующих начальных значениях концентраций: ${{C}_{{{{{\left( {{{H}_{2}}{{O}_{2}}} \right)}}_{0}}}}}$ = 2.87 × × 10‒3 моль/дм3, ${{C}_{{{{{\left( {{{H}_{2}}} \right)}}_{0}}}}}$ = 0.78 × 10‒3 моль/дм3.
Рис. 3.
Сравнение результатов расчетов и экспериментальных данных [11]. Начальные значения концентраций: ${{C}_{{{{{\left( {{{H}_{2}}{{O}_{2}}} \right)}}_{0}}}}}$ = 2.87 ммоль, ${{C}_{{{{{\left( {{{H}_{2}}} \right)}}_{0}}}}}$ = 0.78 ммоль; мощность поглощенной зоны излучения 0.67 Дж/(кг ∙ c). Пунктирные линии – минимальные и максимальные расчетные значения; сплошные линии – средние расчетные значения; символы – данные эксперимента с погрешностью. Исследуемые вещества: 1 – H2O2; 2 – H2; 3 – O2
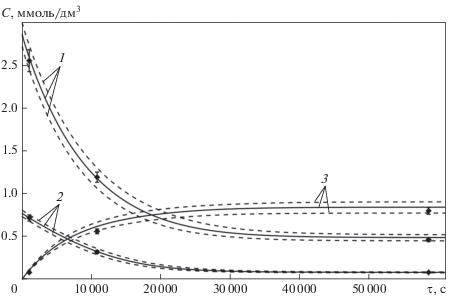
Полученные зависимости аналогичны кривым разложения пероксида водорода, поскольку данный процесс является основной реакцией. При этом в системе образуется кислород, концентрация которого вместе с концентрацией водорода H2 стабилизируется. При повышении начальной концентрации пероксида водорода в растворе концентрация кислорода также становится больше. Таким образом, наблюдается нелинейное изменение концентраций компонентов в растворе при воздействии излучения. Отмечается, что для моделирования кинетических процессов в такой системе требуются довольно сложные расчетные модели, учитывающие наработку и деструкцию различных водородных и кислородных радикалов.
Максимальные отклонения результатов расчетов от экспериментальных данных для концентраций H2O2, H2 и O2 составили 2, 1 и 15% соответственно. Неопределенность валидации находилась в пределах 30%. Конкретные значения по каждому из проведенных экспериментов указаны в табл. 4.
Таблица 4.
Оценка погрешностей результатов расчетов для некоторых экспериментов из работы [11] (результат моделирования эксперимента № 1 представлен на рис. 3)
| Номер эксперимента | Концентрация | Отклонение ε, % | Неопределенность валидации utot, % | [ε – utot; ε +utot], % |
|---|---|---|---|---|
| 1 | H2O2 | 1.9 | 7.2 | [–5.3; 9.1] |
| H2 | 1.0 | 6.3 | [–5.3; 7.3] | |
| O2 | 15.5 | 15.2 | [0.3; 30.7] | |
| 2 | H2O2 | 1.3 | 9.0 | [–7.7; 10.3] |
| H2 | 12.5 | 28.6 | [–16.1; 41.1] | |
| O2 | 14.1 | 20.8 | [–6.7; 34.9] |
Для проверки модели дегазации совместно с радиолизом использовались результаты исследования [12]. Мощность поглощенной дозы гамма-излучения в эксперименте составляла 2.5 Дж/(кг · с) во всей облучаемой камере. Облучение раствора проводилось в стеклянных ампулах объемом 20 мл. Площадь поверхности межфазного переноса газ – жидкость равнялась площади поперечного сечения ампулы и составляла 3.14 см2. Ампулы закрывались алюминиевыми обжимными колпачками с силиконовыми мембранами для обеспечения герметичного уплотнения и предотвращения потерь газообразных веществ.
В представленном эксперименте атмосфера ампулы заполнялась аргоном, а вода деаэрировалась с заданным уровнем кислотности pH 10.6. В процессе измерений фиксировались концентрация водорода в газовом объеме над раствором и концентрация пероксида в жидкости. Для моделирования использовался полный набор реакций из табл. 1 и 2. На рис. 4 представлены результаты сравнения измеренной и рассчитанной концентраций водорода в газовом объеме в зависимости от времени облучения $\tau $ при соотношении объемов газовой и жидкой фаз 1 : 1.
Рис. 4.
Сравнение результатов расчетов и экспериментальных данных по газообразному водороду. Обозначения см. рис. 2
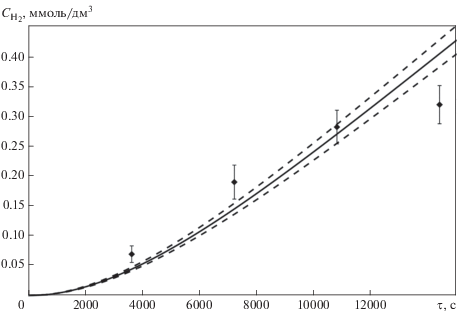
Отклонение расчетных значений концентрации газообразного водорода от измеренных при данных условиях составило – 10%, а неопределенность валидации равнялась 31%.
Следует отметить, что после дополнительных исследований сходимости результатов расчетов при изменении временной и пространственной сеток было установлено, что неопределенность, связанная с использованием различных пространственных разбиений моделируемой области (одна, две, четыре ячейки), и неопределенность, обусловленная выбором максимального шага по времени (0.010, 0.005, 0.001 с), являются незначительными.
Таким образом, проведенные для данного эксперимента расчеты показали, что расчетная модель радиолиза воды с примесями пероксида водорода, водорода и кислорода, включая дегазацию радиолитического водорода через границу раздела фаз, позволяет правильно моделировать изменение во времени концентрации компонентов в растворе и в газовой фазе над раствором при различных начальных концентрациях примесей, значениях мощности поглощенной дозы гамма-излучения и разных соотношениях объемов фаз. Интегральные результаты валидации модели для рассмотренных экспериментов по радиолизу воды приведены в табл. 5.
Таблица 5.
Основные результаты валидации модели радиолиза в модуле AERMOD
| Параметр | Диапазон погрешности моделирования, % |
|---|---|
| Концентрация компонентов [H2O2, H2 (в растворе и над поверхностью), O2] при радиолизе воды с примесями пероксида водорода, водорода и кислорода | [–53.5; 55.8] |
| Максимальная концентрация пероксида водорода в водном растворе с различной начальной концентрацией кислорода и постоянной начальной концентрацией водорода | [–18.1; 22.2] |
| Время достижения максимальной концентрации пероксида водорода в водном растворе с различной начальной концентрацией кислорода и постоянной начальной концентрацией водорода | [–42.9; –6.7] |
ВЫВОДЫ
1. Разработанная кинетическая модель радиолиза воды в составе программного модуля AERMOD дает возможность расчетным путем определять образование продуктов разложения воды и радиационно-химические превращения водных растворов при воздействии ионизирующего излучения в широком диапазоне концентраций, значений кислотности воды, поглощенной дозы и мощности излучения, температуры воды (до момента кипения) и давления порядка атмосферного.
2. Модель дополнена механизмом межфазного массопереноса, что позволяет учитывать образование летучих примесей продуктов радиолиза воды (водород, кислород) и их выход в газовый объем над водой.
Список литературы
Бяков В.М., Ничипоров Ф.Г. Радиолиз воды в ядерных реакторах. М.: Энергоатомиздат, 1990.
Бяков В.М., Степанов С.В., Магомедбеков Э.П. Начала радиационной химии. II: Радиолиз жидкой воды. М.: РХТУ им. Д. И. Менделеева, 2017.
Ershov B.G., Gordeev A.V. A model for radiolysis of water and aqueous solutions of H2, H2O2 and O2 // Radiat. Phys. Chem. 2008. V. 77. Is. 8. P. 928–935. https://doi.org/10.1016/j.radphyschem.2007.12.005
Benchmarking stiff ode solvers for atmospheric chemistry problems. II: Rosenbrock solvers / A. Sandu, J.G. Verwer, J.G. Blom, E.J. Spee, G.R. Carmichael, F.A. Potra // Atmos. Environ. 1997. V. 31. Is. 20. P. 3459–3472. https://doi.org/10.1016/S1352-2310(97)83212-8
Herranz L.E., Fontanet J., Cantrel L. Modelling liquid-gas iodine transfer under evaporative conditions during severe accidents // Nucl. Eng. Des. 2009. V. 239. Is. 4. P. 728–734. https://doi.org/10.1016/j.nucengdes.2009.01.006
Архипов О.П. Математическая модель термо- и радиационно-химических процессов в теплоносителе водо-водяных энергетических реакторов и ее реализация в программном средстве: дис. … канд. техн. наук. М.: ОКБ “Гидропресс”, 2002.
Лебедев Л.Э. Модель оценки радионуклидов йода в выбросах при тяжелых авариях на АЭС с ВВЭР и ее реализация в интегральном коде: дис. … канд. техн. наук. СПбГПУ, 2012.
Standard for verificaton and validation in computational fluid dynamics and heat transfer. ASME V&V 20, 2009.
Моисеенко Е.В., Мосунова Н.А. Методика оценки неопределенностей результатов расчета для задач обоснования безопасности объектов использования атомной энергетики // Вопросы радиационной безопасности. Т. 90. № 2. С. 24–34.
Barr N.F., Allen A.O. Hydrogen atoms in the radiolysis of water // J. Phys. Chem. 1959. V. 63. Is 6. P. 928–931. https://doi.org/10.1021/j150576a037
Hochanadel C.J. Effects of cobalt γ-radiation on water and aqueous solutions // J. Phys. Chem. 1952. V. 56. Is. 5. P. 587–594. https://doi.org/10.1021/j150497a008
Yakabuskie P.A., Joseph J.M., Wren J.C. The effect of interfacial mass transfer on steady-state water radiolysis // Rad. Phys. Chem. 2010. V. 79. Is. 7. P. 777–785. https://doi.org/10.1016/j.radphyschem.2010.02.001
Дополнительные материалы отсутствуют.
Инструменты
Теплоэнергетика


