Теплофизика высоких температур, 2020, T. 58, № 5, стр. 739-748
Кинетика процессов в потоке азотной плазмы с примесью углерода
О. В. Коршунов 1, Д. И. Кавыршин 1, *, В. Ф. Чиннов 1
1 ФГБУН Объединенный институт высоких температур РАН (ОИВТ РАН)
Москва, Россия
* E-mail: dimakav@rambler.ru
Поступила в редакцию 25.06.2019
После доработки 25.06.2019
Принята к публикации 24.12.2019
Аннотация
С целью изучения эффективности воздействия потока азотной плазмы на графитовые поверхности исследована эволюция кинетики плазмы, движущейся от выхода плазмотрона до объекта воздействия. Движение сопровождается уменьшением температуры от 10 до 7 кК с потерей ~60% вложенной энергии и нарастанием плотности углеродосодержащих примесей при частичном сохранении локального термодинамического равновесия. Основными реакциями являются термические процессы образования и гибели молекул, диссоциативная рекомбинация и перезарядка ионов азота, а при наличии углеродных примесей к ним добавляются реакция замещения С + N2 ↔ CN + N, электронно-столкновительные процессы ступенчатой ионизации и рекомбинации и целый ионно-молекулярный каскад перезарядок и замещений. Установлено, что малая примесь углерода (~0.1%) проявляет себя только в ионно-молекулярной кинетике, увеличивая концентрацию электронов, определяя ионный состав плазмы и тем самым нарушая равновесие между ее нейтральной и заряженной компонентами. Это приводит, в частности, к рекомбинационной неравновесности распределения атомов углерода по электронным состояниям. Другие углеродосодержащие примеси (CN и C2) малосущественны.
ВВЕДЕНИЕ
Использование азотных плазменных струй для испытаний новых теплозащитных и высокотемпературных композитных материалов [1‒4] приводит к необходимости исследований пространственно неоднородных плазменных сред с меняющимся из-за абляции этих материалов составом [1, 3, 5, 6]. Особенности разрушения мишени из изотропного и анизотропного графита при воздействии струи азотной плазмы атмосферного давления экспериментально изучались в работах [6‒8]. Наиболее важным для настоящего исследования результатом этих работ явились спектральные данные по пространственному распределению концентраций углеродосодержащих частиц: атомов углерода C и молекул циана CN (рис. 1).
Рис. 1.
Этап 2: пространственные изменения концентраций С и CN по интенсивностям излучения CI 247.9 нм (1) и CN 388.3 нм (2) на 40-й (а), 100-й (б) и 140-й (в) секундах.

Данная работа посвящена кинетическому исследованию плазмы азотной струи, взаимодействующей с поверхностью мишени из мелкозернистого плотного графита [7, 8] в атмосфере, с целью установления пространственных изменений состава плазмы и влияния углеродосодержащих примесей. Использовался графит марки МПГ-6, диаметр образца – 2 см, длина – 3 см, ток – 300 A, тепловой поток – 1.0 кВт/см2. Движение струи по пути длиной ~15 мм от выходного сопла плазмотрона (T0 = 10 000 К [7, 8]) до поверхности разрушаемого углеродного образца (Tw ≈ 3000 К [6, 7]) происходит со скоростью v ≈ (3–10) × 103 см/с и сопровождается изменением параметров плазмы. На первом этапе движения истекающую в затопленное пространство плазменную струю можно считать чисто азотной по составу, охлаждающейся в процессе теплопроводности. На втором этапе (последняя треть пути) в спектре наблюдаются аблирующий с графитовой поверхности атомарный углерод и продукт его взаимодействия с азотом – циан, излучающие в линии CI 247.8 нм и фиолетовых полосах CN, переход ${{B}^{2}}\Sigma _{u}^{ + }{\kern 1pt} --{\kern 1pt} {{X}^{2}}\Sigma _{g}^{ + }$ (рис. 1). В соответствии с этими этапами исследуются кинетика процессов в плазме без учета и с учетом углерода, а также особенности приповерхностной плазмы.
ЭТАП 1. АЗОТНАЯ ПЛАЗМА
Для мощного теплового воздействия на графитовую поверхность (на рисунках показана вертикальными линиями со штрихами) использовалась азотная плазма, которая, в соответствии с полученными экспериментальными данными [6–8], на выходе из плазмотрона находится в равновесном состоянии с температурой ~10 кК. Параметры такой плазмы рассчитывались, например, в [9, 10]. Внешних причин нарушения локального термодинамического равновесия (ЛТР) до начала этапа взаимодействия с продуктами разрушения поверхности, показанного на рис. 1, нет. К этому моменту плазменный поток охлаждается до температуры T = 8.5 кК [6–8]. Дальнейший спад Т до ~7 кК и ниже на следующем этапе взаимодействия с углеродосодержащими частицами показан на рис. 2.
Рис. 2.
Распределение температуры электронов Te на втором этапе следования плазменного потока: ∼40 с (1), ∼60 с (2), ∼115 с (3); вертикальные линии со штрихами – местоположение поверхности мишени, разрушаемой плазмой.

Таким образом, на первом этапе происходит только нежелательный спад температуры движущегося в атмосфере потока равновесной азотной плазмы с 10 до 8 кК. В такой плазме атомарные компоненты плазмы преобладают над молекулярными при Т > 6.5 кK. При Т = 10 кК концентрация атомов азота [N] превышает концентрацию его молекул [N2] в 90 раз, а концентрация ионов [N+] больше концентрации молекулярных ионов [${\text{N}}_{2}^{ + }$] в 180 раз. При Т = 7 кК концентрации атомных и молекулярных компонент близки между собой (при Т = 6530 К они равны) [10].
Основные процессы. Анализ основных процессов для тяжелых компонент плазмы начинается с реакций термической диссоциации и трехчастичной ассоциации [11]:
(2)
${\text{N}}_{2}^{ + } + {\text{М}} \leftrightarrow {{{\text{N}}}^{ + }} + {\text{N}} + {\text{M}}.$Здесь [М] – суммарная концентрация нейтральной компоненты плазмы: [M] = [N] + [N2].
Для констант реакции (1) используются данные [11]: k1 = (1.2–45) × 10–15 см3/с (прямая реакция), α1 = (8.6–7.2) × 10–34 см6/с (обратная реакция). Для аналогичных реакций с заряженными частицами в литературе есть только одно, по мнению авторов завышенное, значение α2 ~ ~ 10–29 см6/с [12, 13] для обратной реакции (2), более чем на четыре порядка превышающее α1. Поскольку константа равновесия реакции (1), равная k1/α1, всего в 1.16–1.97 раза выше константы равновесия реакции (2), то для прямой реакции (2) получается оценка k2 ~ 6 × 10–10 см3/с. Она тоже представляется завышенной (такую скорость имеет резонансная перезарядка [14]). Однако это оказывается неважным, так как есть другой, еще более быстрый процесс, приводящий к тому же результату – равновесной связи между плотностями N+ и ${\text{N}}_{2}^{ + }$ (см. ниже).
Все приведенные здесь и далее диапазоны соответствуют диапазону температур 7–10 кК, при котором равновесная степень ионизации плазмы составляет большую величину ne/[M] ~ 10–4–10–2 [10]. Это говорит о значительной роли процессов с участием электронов, прежде всего в кинетике ионизации и рекомбинации, сопровождающихся заселением возбужденных состояний атомов и молекул. При этом роль прямых (по отношению к основным состояниям атомов и молекул) процессов ионизации и рекомбинации будет несущественной, поскольку температура электронов сравнительно невелика: Те = 0.6–0.9 эВ, тогда как потенциалы ионизации атома и молекулы азота составляют 14.2 и 15.8 эВ соответственно. Ступенчатые процессы ионизации и рекомбинации с образованием промежуточных возбужденных состояний можно представить в виде
(3)
${\text{N}} + е \leftrightarrow {\text{N*}} + е \leftrightarrow {\text{N**}} + e \leftrightarrow {{{\text{N}}}^{ + }} + 2e,$(4)
${{{\text{N}}}_{2}} + е \leftrightarrow {\text{N}}_{2}^{*} + е \leftrightarrow {\text{N}}_{2}^{{{\text{**}}}} + e \leftrightarrow {\text{N}}_{2}^{ + } + 2e.$Эта схема является основой для анализа заряженной и возбужденной компонент плазмы в рамках модифицированного диффузионного приближения [15], в соответствии с которым при Т = 7–10 кК константа скорости ступенчатой ионизации (3) k3 = 1.2 × 10–15–6.1 × 10–13 см3/с, константа скорости тройной рекомбинации α3 = (54–8.7) × 10–27 см6/с.
Эти значения в слабоионизованной плазме могут быть несколько ниже. Согласно работам [15, 16], при низкой концентрации электронов нарушаются условия равновесия для распределений по электронным, колебательным и вращательным степеням свободы. Причиной этого является выход излучения, который в рассматриваемой плазме преобладает над электронно-столкновительным расселением уровней при ne < < 1014 см–3. Такие низкие концентрации электронов отвечают периферии плазменного потока, но и там в отношении основных параметров плазмы это скажется несущественно, так как сами процессы (3), (4), как будет показано ниже, не вносят заметного вклада в баланс основных компонент плазмы.
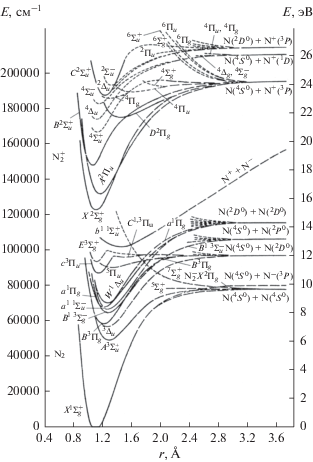
Возбужденные молекулы могут диссоциировать не только термически (реакция (1)), но и при так называемой предиссоциации [17] – спонтанных или столкновительных переходах на разлетные или слабосвязанные состояния:
Рис. 3 отображает многообразие таких состояний в структуре термов молекулы азота.
Реакция (5) идет с гораздо большей скоростью, чем ступенчатая ионизация или тройная рекомбинация, разрушая молекулы азота с частотой ~1011 с–1 [17], характерной для столкновительных переходов между близкими высоковозбужденными уровнями. В холодном газе, в отсутствие обратного процесса, реакция (5) препятствует ступенчатым процессам ионизации и тройной рекомбинации, что подтверждается экспериментальными исследованиями электроразрядной плазмы [19], в которых отмечена невозможность создания диффузного разряда в холодном азоте. При этом в работе [19] диффузный режим горения разряда был легко достигнут в аргоне, где ступенчатая ионизация идет по схеме (3) , не встречая препятствий. В молекулярном азоте диссоциативный канал (5) практически заменяет ступенчатую ионизацию (4). Такая картина свойственна, по-видимому, всем молекулярным газам.
В горячем газе реакция (5) идет также быстро, но уравновешивается обратным процессом двух- или трехчастичной ассоциации атомов, что, по-видимому, и имеет место в рассматриваемой равновесной плазме.
Еще бόльшую роль в азотной плазме играют процессы диссоциативной рекомбинации с обратной ей двухчастичной ассоциацией
и реакции замещения, идущие по схеме перезарядки:Диссоциативная рекомбинация имеет гораздо бόльшую скорость, чем процессы (3) и (4), а реакция (7) сопоставима с реакцией (2) и по скорости, и по результату (уравновешивает плотности атомарных и молекулярных ионов). При Т = 7–10 кК константа скорости реакции (6) составляет α6 = = (6–5) × 10–8 см3/с [12, 20], реакции (7) – α7 = = (1.7–2.4) × 10–11 см3/с [12, 21]. При этом большие скорости имеют и обратные реакции (6), (7): k6 = 2.4 × 10–17–1.9 × 10–15 см3/с, k7 = (1.9–4.7) × × 10–11 см3/с. Их энергетические барьеры в основном невелики: продукты диссоциативной рекомбинации (6) – возбужденные атомы азота – образуются в 2D- и 2Р-состояниях с выделением кинетической энергии 3.44, 2.25 и 1.06 эВ [21], причем основным является канал с наименьшей энергией. Примерно такой же величины (1.05 эВ – разница энергий диссоциации N2 и ${\text{N}}_{2}^{ + }$) энергетический эффект и у реакции (7). Реакции (6) и (7) в рассматриваемом состоянии ЛТР находятся в детальном равновесии со своими обратными реакциями.
Кроме рассмотренных видов тяжелых частиц, в азотной плазме образуются также ионы ${\text{N}}_{3}^{ + }$, ${\text{N}}_{4}^{ + }$, которые быстро разрушаются в реакциях диссоциативной рекомбинации и замещения [20, 12, 13 ], аналогичных (6), (7), но через которые может происходить перераспределение ионно-молекулярного состава. Однако их ролью можно пренебречь, поскольку еще быстрей они будут термически разрушаться в процессах, детально обратных процессам их образования, вследствие малой энергии связи. Так, энергия связи ${\text{N}}_{2}^{ + }$–N2 составляет величину, соизмеримую с температурой: 0.8 эВ [18].
Уравнения баланса частиц. Таким образом, состав равновесной азотной плазмы атмосферного давления прост: это атомы N, молекулы N2, ионы N+ и ${\text{N}}_{2}^{ + }$ и электроны. Общая плотность тяжелой компоненты при атмосферном давлении и Т = 7–10 кК [N] + [N2] = [M] = (10.5–7.34) × 1017 см–3, соответствующая ей величина ne = 1.5 × 1014–6.5 × × 1015 см–3. Равновесные плотности атомных и молекулярных частиц при Т = 7 кК близки между собой, а при Т = 10 кК плотность молекулярных частиц на два порядка меньше.
Пусть изменение температуры сопровождается квазистационарной перестройкой состава плазмы, при которой применимы стационарные уравнения баланса частиц. Прежде чем их записать, сравним скорости процессов гибели этих частиц для выявления несущественных процессов, а затем сделаем оценки применимости квазистационарного приближения, сравнивая полное время движения струи (τ0 ≈ 200–600 мкс) с временами основных процессов. Начнем с нейтральных частиц. Скорость разрушения молекул азота определяют процессы (1), (4) и (7) (обратный). Отношение их скоростей в рассматриваемом диапазоне температур
(8)
$\begin{gathered} {{{{k}_{1}}[{\text{M}}]} \mathord{\left/ {\vphantom {{{{k}_{1}}[{\text{M}}]} {{{k}_{4}}{{n}_{e}}}}} \right. \kern-0em} {{{k}_{4}}{{n}_{e}}}} \approx 6 \times {{10}^{3}}{\kern 1pt} - {\kern 1pt} 4, \\ {{{{k}_{7}}[{{{\text{N}}}^{ + }}]} \mathord{\left/ {\vphantom {{{{k}_{7}}[{{{\text{N}}}^{ + }}]} {{{k}_{4}}{{n}_{e}}}}} \right. \kern-0em} {{{k}_{4}}{{n}_{e}}}} \approx 9 \times {{10}^{3}}{\kern 1pt} - {\kern 1pt} 40 \\ \end{gathered} $(9)
$({{\alpha }_{1}}[{\text{N}}][{\text{M}}] + {{\alpha }_{7}}[{\text{N}}_{2}^{ + }])[{\text{N}}] = ({{k}_{1}}[{\text{M}}] + {{k}_{7}}[{{{\text{N}}}^{ + }}])[{{{\text{N}}}_{2}}].$Уравнение баланса молекул N2 (9) ответственно за отношение плотностей нейтральных атомов и молекул. Время установления квазистационарности этого уравнения и плотности N2 в диапазоне температур 7–10 кК составляет τ9 = (k1[M] + + k7[N+])–1 = 300–3 мкс. Критерий квазистационарности τ9 < τ0 в целом выполняется, лишь при Т = 7 кК в приповерхностной плазме эти времена соизмеримы.
Судьбу атомарных ионов определяют реакции (2), (3), (7). Скорости гибели ионов N+ находятся в соотношениях
(10)
${{{{k}_{7}}} \mathord{\left/ {\vphantom {{{{k}_{7}}} {{{\alpha }_{2}}[{\text{M}}]}}} \right. \kern-0em} {{{\alpha }_{2}}[{\text{M}}]}} = 2{\kern 1pt} --{\kern 1pt} 7,\,\,\,\,{{{{k}_{7}}[{\text{N}}]} \mathord{\left/ {\vphantom {{{{k}_{7}}[{\text{N}}]} {{{\alpha }_{3}}n_{e}^{2}}}} \right. \kern-0em} {{{\alpha }_{3}}n_{e}^{2}}} = {{10}^{4}}{\kern 1pt} --{\kern 1pt} 90,$(11)
$({{k}_{2}}[{\text{M}}] + {{\alpha }_{7}}[{\text{N])}}[{\text{N}}_{2}^{ + }] = ({{\alpha }_{2}}[{\text{N}}][{\text{M}}] + {{k}_{7}}[{{{\text{N}}}_{{\text{2}}}}])[{{{\text{N}}}^{ + }}].$Входящие в уравнение баланса ионов N+ (11) быстрые процессы одинакового действия (2) и (7) обеспечивают равновесное отношение плотностей атомарных и молекулярных ионов в широком диапазоне параметров плазмы. При этом процесс (2) является второстепенным, особенно при больших Т. Квазистационарность этого уравнения и плотности N+ в диапазоне температур 7–10 кК устанавливается за времена, на три–четыре порядка меньшие пролетного времени τ0: τ11 = = (α2[N][M] + k7[N2])–1 ≈ 0.07–0.17 мкс.
Суммарную плотность заряженной компоненты ne определяют реакции (3), (4), (6). Отношение скорости диссоциативной рекомбинации к суммарной скорости тройной рекомбинации (обратных процессов (3) и (4)) тоже весьма велико:
(12)
${{{{\alpha }_{6}}[{\text{N}}_{2}^{ + }]} \mathord{\left/ {\vphantom {{{{\alpha }_{6}}[{\text{N}}_{2}^{ + }]} {{{\alpha }_{3}}n_{e}^{2}}}} \right. \kern-0em} {{{\alpha }_{3}}n_{e}^{2}}} = 3 \times {{10}^{3}}{\kern 1pt} --{\kern 1pt} 5,$Уравнение баланса молекулярных ионов легко получить из уравнений (11), (13). Их концентрация определяется тремя быстрыми обратимыми процессами (6), (7) и (2), которые вкупе с реакцией (1) составляют четверку основных процессов рассматриваемой плазмы, регулирующих ее состав. Уравнения (9), (11) и (13) понадобятся в дальнейшем для анализа влияния углеродной примеси.
Энергетические потери азотной струи при истечении в атмосферу. Рассмотрим также изменение энергетического баланса плазмы. Оно связано с изменением T в исследованном выше диапазоне температур: от 10 кК на выходе из плазмотрона до 7 кК к концу второго этапа, когда молекулы влияют на кинетику и энергетику плазмы. Значительно уменьшаются также степень ионизации и плотность электронов. Охлаждение плазмы осуществляется процессами теплопроводности и излучения, которые расходуют энергию, вложенную в диссоциацию и ионизацию. В поступательные степени свободы частиц плазмы эта энергия выделяется, главным образом, при ассоциации атомов, а также при рекомбинации электронов, ассоциации ионов с атомами, предиссоциации и в других процессах. Даже на таком коротком расстоянии транспортировки плазменного потока к объекту его воздействия (1–2 см) большая часть вложенной в плазму энергии рассеивается в окружающую среду.
Простую оценку энергетических потерь можно сделать из следующих соображений. Пользуясь приведенными выше данными, нетрудно показать, что при создании плазмы основная энергия (90%) вложена в образование горячих атомов. Сопоставим их долю в составе плазмы в начале и в конце пути. Как ясно из предыдущего, атомарный при Т = 10 кК состав плазмы при Т = 7 кК становится наполовину молекулярным: [N] ≈ [N2], т.е доля свободных атомов [N]/([N] + 2[N2]) сократилась в три раза. Следовательно, 2/3 вложенной энергии вышли из потока в окружающую среду. Эта оценка всего на 6% превышает более точную оценку с учетом кинетической, колебательной и вращательной энергии молекул, энергии возбуждения атомов и молекул и энергии образования ионов, в соответствии с которой энергопотери составляют 60%. Отношение энтальпий равновесной азотной плазмы при 10 кК (55 080 кДж/кг) и 7 кК (25 590 кДж/кг) дает близкую величину 54% [22].
Таким образом, зная лишь падение температуры равновесной плазмы, можно рассчитать ее энергопотери в процессах теплообмена и излучения.
ЭТАП 2. АЗОТНО-УГЛЕРОДНАЯ ПЛАЗМА
По данным экспериментов [6–8], на втором этапе движения плазменного потока – в области его взаимодействия с продуктами разрушения графитовой поверхности (атомами и молекулами углерода) – температура падает до значений ~7 кК (при этом на самой поверхности она составляет около 3 кК). Как уже упоминалось, степень ионизации азота при этом снижается на два и более порядка и значение электронов в кинетике плазмы уменьшается; состав азотной плазмы становится молекулярным ([N2] ~ [N]). Вследствие этого, несмотря на равновесное в целом состояние плазмы, кинетика протекающих в ней процессов существенно усложняется, включая в себя более 50 ионно-молекулярных реакций. Рассмотрим эти реакции для углеродосодержащих нейтральных (С, С2, CN) и заряженных (C+, ${\text{C}}_{2}^{ + }$, CN+) частиц при температуре 7 кК в свете имеющихся экспериментальных данных [6, 7].
Нейтральные частицы. Максимальная концентрация атомарного углерода вблизи поверхности образца по данным эксперимента составляет ~1015 см–3 (см. рис. 1). Из сопоставления интенсивностей полос CN и ${\text{N}}_{2}^{ + }$ следует, что концентрация радикалов CN, по-видимому, не превышает 1014 см–3. То же следует из данных, приведенных на рис. 1. Нейтральные частицы вступают в реакции:
(14)
${\text{С}} + {{{\text{N}}}_{2}}(\nu > 1) \leftrightarrow {\text{CN}} + {\text{N}}\,\,\,\,\left( { \geqslant {\kern 1pt} - {\kern 1pt} 2.01{\text{ эВ}}} \right),$(15)
${{{\text{С}}}_{2}} + {{{\text{N}}}_{2}} \leftrightarrow 2{\text{CN}}\,\,\,\,\left( { - {\kern 1pt} 0.46{\text{ эВ}}} \right),$(16)
${{{\text{С}}}_{2}} + {\text{N}} \leftrightarrow {\text{CN}} + {\text{C}}\,\,\,\,\left( {1.55{\text{ эВ}}} \right),$(17)
${\text{С}} + {\text{N}} + {\text{M}} \leftrightarrow {\text{CN}} + {\text{M}}\,\,\,\,\left( {7.75{\text{ эВ}}} \right).$Константы реакций (14)–(17) при Т = 7 кК достаточно велики [11, 13, 23] для того, чтобы эти взаимодействия успевали происходить за время прохождения плазменного потока. Главным процессом, регулирующим соотношение между [C] и [CN], является реакция (14), поскольку в ней с обеих сторон участвуют основные компоненты плазмы N2 и N. Хотя порог реакции – 2.01 эВ (из-за большей, чем у молекулы CN, энергии диссоциации молекулы N2), однако концентрация последних достаточно велика (~1018 см–3), чтобы обеспечить высокий уровень заселения колебательных уровней с энергией 2 эВ (~1016 см–3), которые и вносят, по-видимому, основной вклад в прямую реакцию (14).
Рис. 1 иллюстрирует рассматриваемый второй этап движения потока, показывая наличие в плазме углеродосодержащих частиц С и CN, причем на достаточно большом удалении от мишени (5–10 мм). Причины появления атомов углерода на таком большом расстоянии от мишени еще недостаточно изучены. Это может быть его радиальная диффузия из окружающей среды, поскольку продольная диффузия из приповерхностной плазмы против потока не идет. Скорость потока диффузии С, по оценкам авторов, не превышает 103 см/с, тогда как скорость потока азотной плазмы – 103–104 см/с. При этом реакция (14) на несколько порядков быстрее всех возможных процессов переноса и других реакций с участием C и CN.
Оценим отношение концентраций молекул примеси C и CN. При Т = 7 кК константа равновесия реакции (14) K14 = 8.2 [11, 13, 23]. Тогда из условия равновесия получаем
(18)
${{\left[ {\text{С}} \right]} \mathord{\left/ {\vphantom {{\left[ {\text{С}} \right]} {{\text{[CN]}}}}} \right. \kern-0em} {{\text{[CN]}}}} = {{{{K}_{{14}}}[{\text{N]}}} \mathord{\left/ {\vphantom {{{{K}_{{14}}}[{\text{N]}}} {[{{{\text{N}}}_{2}}]}}} \right. \kern-0em} {[{{{\text{N}}}_{2}}]}} \approx 17$При [С] ≈ 1015 см–3 из (18) следует [CN] ≈ 6 × × 1013 см–3. Примерно такие концентрации на рис. 1 вблизи поверхности мишени. Однако вдали от мишени данные на рис. 1 не согласуются с уравнением (18). С ростом температуры отношение [С]/[CN] должно расти, поскольку равновесное отношение [N2]/[N] уменьшается сильнее, чем константа равновесия K14. При Т = 8.5 кК, что соответствует начальной координате на рис. 1, [С]/[CN] ≈ 80. Наблюдаемая на рис. 1 зависимость противоположна: отношение [С]/[CN] падает при удалении от мишени несмотря на повышение температуры с 7 до 8.5 кК, причем циана несколько больше, чем углерода, как при указанных малых Т ≈ 4 кК. На поздних стадиях эксперимента наблюдается участок примерного постоянства этого соотношения (см. рис. 1), но и он за 3 мм до мишени сменяется участком резкого роста. И только около мишени выполняется соотношение (18).
Такое несоответствие, вероятнее всего, говорит об излучении [С] и [CN] из разных областей плазменного потока, поскольку регистрация спектров была поперечной (хордовой). При такой регистрации измеряемая интенсивность в случае оптически тонкой плазмы представляет собой интегральную по линии наблюдения (чаще всего – диаметру) величину излучательной способности, которая определяется как видом распределения излучателей по линии наблюдения, так и пространственной протяженностью излучателей данного типа.
Вблизи мишени преобладает излучение из горячей центральной части потока, более однородное по диаметру благодаря перемешиванию при отражении от мишени и ее обтекании.
На удалении от мишени плазменный канал стабилен и структурирован. Благодаря прозрачности среды в центре потока наблюдается резкий спад излучения атомов С, которых становится все меньше. Молекул CN в соответствии с (18) там практически нет, а в “холодных” граничных областях потока они преобладают. Это подтверждает и отмеченный параллельный ход кривых [С] и [CN] вдали от мишени.
Главное, что во всех случаях идет реакция (14) и для расчета [С]/[CN] применимо соотношение (18), вопрос только в том, какая температура соответствует области наблюдения. Для спектра излучения атомов С это температурные зависимости на рис. 2, а для спектра излучения молекул CN, кроме приповерхностного участка, – низкие температуры периферии потока.
В отношении остальных реакций нейтральных частиц следует отметить, что реакции (15) и (16) – тоже достаточно быстрые процессы [11, 13, 23], которые регулируют концентрацию С2. В сравнении с экспериментальными значениями [CN] из условия равновесия в этих реакциях получаются почти на два порядка меньшие значения [С2]. Действительно, молекулы С2 в спектрах излучения практически не наблюдаются.
Ионно-молекулярная кинетика. Перейдем к ионно-молекулярному составу азотно-углеродной плазмы. Он регулируется следующими реакциями.
Реакции замещения и обмена:
(19)
${\text{N}}_{2}^{ + } + {\text{С}} \leftrightarrow {{{\text{N}}}^{ + }} + {\text{СN}}\,\,\,\,\left( {0.09{\text{ эВ}}} \right),$(20)
${\text{N}}_{2}^{ + } + {\text{СN}} \leftrightarrow {\text{C}}{{{\text{N}}}^{ + }} + {{{\text{N}}}_{2}}\,\,\,\,\left( { - 0.35{\text{ эВ}}} \right),$(21)
${\text{N}}_{2}^{ + } + {{{\text{С}}}_{2}} \leftrightarrow {\text{C}}{{{\text{N}}}^{ + }} + {\text{СN}}\,\,\,\,\left( { - 0.81{\text{ эВ}}} \right),$(22)
${{{\text{N}}}^{ + }} + {{{\text{С}}}_{2}} \leftrightarrow {\text{С}}{{{\text{N}}}^{ + }} + {\text{С}}\,\,\,\,\left( { - 0.9{\text{ эВ}}} \right),$(23)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{N}} \to {\text{N}}_{2}^{ + } + {\text{С}}\,\,\,\,\left( {2.36{\text{ эВ}}} \right),$(24)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{N}} \to {{{\text{N}}}^{ + }} + {\text{СN}}\,\,\,\,\left( {2.45{\text{ эВ}}} \right),$(25)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{N}} \to {{{\text{N}}}_{2}} + {{{\text{С}}}^{ + }}({{{\text{C}}}^{ + }}*)\,\,\,\,~\left( { \leqslant {\kern 1pt} 7.73{\text{ эВ}}} \right),$(26)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{CN}} \to {{{\text{N}}}_{2}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,~\left( { \leqslant {\kern 1pt} 4.66{\text{ эВ}}} \right),$(27)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{С}} \to {\text{N}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,~\left( { \leqslant {\kern 1pt} 2.55{\text{ эВ}}} \right),$(28)
${\text{С}}{{{\text{N}}}^{ + }} + {\text{С}} \to {\text{СN}} + {{{\text{С}}}^{ + }}({{{\text{C}}}^{ + }}*)\,\,\,\,\left( { \leqslant {\kern 1pt} 5.72{\text{ эВ}}} \right),$(29)
${\text{С}}{{{\text{N}}}^{ + }} + {{{\text{С}}}_{2}} \to {\text{СN}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,\left( { \leqslant {\kern 1pt} 4.1{\text{ эВ}}} \right),$(30)
${\text{С}}_{2}^{ + } + {\text{N}} \to {{{\text{C}}}^{ + }} + {\text{СN}}\,\,\,\,\left( {3.17{\text{ эВ}}} \right),$(31)
${\text{С}}_{2}^{ + } + {\text{C}} \to {{{\text{C}}}^{ + }} + {{{\text{С}}}_{2}}\,\,\,\,\left( {1.62{\text{ эВ}}} \right).$Реакции трехчастичной ассоциации и термической диссоциации:
(32)
${{{\text{С}}}^{ + }} + {\text{N}} + {\text{М}} \leftrightarrow {\text{C}}{{{\text{N}}}^{ + }} + {\text{M}}\,\,\,\,\left( {4.95{\text{ эВ}}} \right).$Реакции перезарядки:
(33)
${\text{N}}_{2}^{ + } + {\text{С}} \to {{{\text{N}}}_{2}} + {{{\text{С}}}^{ + }}({{{\text{C}}}^{ + }}*)\,\,\,\,~\left( { \leqslant {\kern 1pt} 4.32{\text{ эВ}}} \right),$(34)
${\text{N}}_{2}^{ + } + {{{\text{С}}}_{2}} \to {{{\text{N}}}_{2}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,\left( { \leqslant {\kern 1pt} 3.68{\text{ эВ}}} \right),$(35)
${\text{N}}_{2}^{ + } + {\text{СN}} \to {{{\text{N}}}_{2}} + {\text{С}}{{{\text{N}}}^{ + }}\,\,\,\,\left( {1.38{\text{ эВ}}} \right),$(36)
${{{\text{N}}}^{ + }} + {\text{С}} \to {\text{N}} + {{{\text{С}}}^{ + }}({{{\text{C}}}^{ + }}*)\,\,\,\,~\left( { \leqslant {\kern 1pt} 3.27{\text{ эВ}}} \right),$(37)
${{{\text{N}}}^{ + }} + {{{\text{С}}}_{2}} \to {\text{N}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,\left( { \leqslant {\kern 1pt} 2.63{\text{ эВ}}} \right),$(38)
${{{\text{N}}}^{ + }} + {\text{СN}} \leftrightarrow {\text{N}} + {\text{С}}{{{\text{N}}}^{ + }}\,\,\,\,\left( {0.33{\text{ эВ}}} \right),$(39)
${\text{C}}{{{\text{N}}}^{ + }} + {\text{С}} \to {\text{CN}} + {{{\text{С}}}^{ + }}({{{\text{C}}}^{ + }}*)\,\,\,\,\left( { \leqslant {\kern 1pt} 2.94{\text{ эВ}}} \right),$(40)
${\text{C}}{{{\text{N}}}^{ + }} + {{{\text{С}}}_{2}} \to {\text{CN}} + {\text{С}}_{2}^{ + }({\text{C}}_{2}^{{ + *}})\,\,\,\,\left( { \leqslant {\kern 1pt} 2.3{\text{ эВ}}} \right),$(41)
${\text{С}}_{2}^{ + } + {\text{C}} \leftrightarrow {{{\text{C}}}^{ + }} + {{{\text{С}}}_{2}}\,\,\,\,\left( {0.64{\text{ эВ}}} \right).$Реакции диссоциативной рекомбинации и ассоциативной ионизации:
(42)
$е + {\text{С}}_{2}^{ + } \leftrightarrow {\text{C}} + {\text{С}}({\text{C}}*)\,\,\,\,~\left( { \leqslant {\kern 1pt} 6.04{\text{ эВ}}} \right),$(43)
$е + {\text{С}}{{{\text{N}}}^{ + }} \leftrightarrow {\text{N}}({\text{N}}*) + {\text{С}}({\text{C}}*)\,\,\,\,~\left( { \leqslant {\kern 1pt} 6.29{\text{ эВ}}} \right).$Ступенчатые реакции ионизации и тройной рекомбинации:
(44)
$е + {\text{С}} \leftrightarrow 2е + {{{\text{С}}}^{ + }}\,\,\,\,\left( { - 11.26{\text{ эВ}}} \right),$(45)
$е + {\text{СN}} \leftrightarrow 2е + {\text{С}}{{{\text{N}}}^{ + }}\,\,\,\,\left( { - 14.2{\text{ эВ}}} \right),$(46)
$е + {{{\text{С}}}_{2}} \leftrightarrow 2е + {\text{С}}_{2}^{ + }\,\,\,\,\left( { - 11.9{\text{ эВ}}} \right).$Здесь в скобках приведен энергетический эффект реакции, выделяющийся в поступательные степени свободы продуктов; знак “минус” означает эндотермическую реакцию; знак неравенства – уменьшение энергетического эффекта, если продукт реакции образуется в возбужденном состоянии. В случаях, когда обратные реакции маловероятны, обратная стрелка отсутствует.
Кроме того, для молекул С2, CN имеют место такие же, как и для молекулы N2, процессы предиссоциации (5). В отличие от молекулы азота, где первое возбужденное состояние отстоит от основного на 6 эВ, у этих молекул электронные термы близко расположены друг к другу и к основному состоянию, а порог ионизации ниже. Поэтому их возбуждение и ионизация свободными электронами происходят при более низких ne и Te, чем молекулы азота. Все эти реакции вместе с рассмотренными в предыдущем разделе для чистого азота (1)–(7) в той или иной степени определяют кинетику разогретой азотно-углеродной плазмы, близкой к состоянию термодинамического равновесия.
По большинству этих реакций нет данных в литературе. Из ионно-молекулярных реакций (19)–(46) исследованы лишь последние пять реакций с участием электронов, больше всего диссоциативная рекомбинация, по которой есть экспериментальные данные [21, 12 ]. Вместе с тем кинетический анализ, основанный на характерных значениях констант скоростей для указанных реакций, позволяет сделать ряд важных выводов.
Ионно-молекулярный состав. Начнем с реакций перезарядки (33)–(41). Обычно они имеют большие константы скорости ~10–12–10–9 см3/с [21, 24], поэтому в наибольшей степени отвечают за ионный состав плазмы. Их совокупное действие приводит к преобладанию иона с наименьшей энергией ионизации, который уже не может ни на чем перезарядиться и становится основным ионом плазмы. В данном случае это ион C+, который вступает только в сравнительно медленную реакцию тройной рекомбинации (44) и еще более медленную реакцию трехчастичной рекомбинации (32), останавливая собой каскад перезарядок (33)–(41).
Из остальных реакций следует выделить реакции с участием основных компонент плазмы N2 и N, которые идут гораздо быстрее других, аналогичных им реакций с участием углеродосодержащих молекул, имеющих концентрацию на три порядка меньшую, чем атомы и молекулы азота. За одним исключением (реакция (20), обратная с участием N2), это реакции замещения атомом N одной из составляющих иона CN+ (23)–(25) и иона ${\text{C}}_{2}^{ + }$ (30). Реакции замещения имеют такие же большие константы скорости, как и реакции перезарядки [21]. В результате концентрация этих ионов должна стать еще ниже, чем в цепочке перезарядок. Выявляя таким образом главные процессы образования и разрушения имеющихся в плазме ионов, при [С] ≈ 1015 см–3 и Т ≈ 7 кК можно получить следующую иерархию ионных концентраций:
(47)
$[{{{\text{С}}}^{ + }}] \approx {{n}_{e}} \gg {\text{[}}{{{\text{N}}}^{ + }}{\text{]}} \approx [{\text{N}}_{2}^{ + }] \gg [{\text{С}}{{{\text{N}}}^{ + }}] \approx [{\text{С}}_{2}^{ + }]{\text{ }}.$Между [С+] и [${\text{N}}_{2}^{ + }$] отличие составляет около одного порядка величины, а между [N+] и [СN+] – около четырех, так что можно уверенно говорить об атомарном составе ионов рассматриваемой плазмы. Одной из главных причин чрезвычайно низкой концентрации молекулярных ионов наряду с указанными выше является диссоциативная рекомбинация, не уравновешенная для углеродосодержащих ионов обратным процессом ассоциативной ионизации атомов углерода в силу их низкой концентрации.
Концентрации электронов и ионов. Наличие в плазме сравнительно легкоионизируемых атомов C (энергия ионизации – 11.26 эВ), несмотря на преобладание атомов N (энергия ионизации – 14.53 эВ), приводит к росту потока ионизации плазмы: константа скорости ступенчатой ионизации k43 атомов C при T = 0.6 эВ в 2000 раз больше, чем k3 для атомов N. Это значит, что ne может заметно вырасти по сравнению с равновесными значениями в чисто азотной плазме. Рассмотрим возможный рост концентрации электронов.
Начнем с анализа применимости уравнений баланса [N2] (9), [N+] (11) и [N+] + [${\text{N}}_{2}^{ + }$] (13) при наличии данной углеродной примеси. В уравнении (9) должны появиться члены, отражающие вклад процессов (14)–(17), в уравнениях (11) и (13) – целый ряд процессов перезарядки и замещения. Нетрудно видеть, что все эти вклады столь же несущественны, сколь и вклады процессов, по которым сделаны оценки (8), (10), (12), так как характеризуются малым параметром – плотностью примеси [C], на три порядка меньшей, чем плотность азота, при том что константы скоростей сравниваемых процессов с участием C и N близки между собой.
Например, в правой части уравнения (11) должно появиться слагаемое
Теперь можно решить основную задачу: оценить плотность ионов C+. Уравнение баланса для них имеет вид
(48)
$[{\text{C}}]({{k}_{c}}[{{{\text{M}}}^{ + }}] + {{k}_{{43}}}{{n}_{e}}) = {{\alpha }_{{43}}}n_{e}^{2}[{{{\text{C}}}^{ + }}],$Это уравнение решается вместе с уравнениями квазинейтральности
и ионизационного равновесия ионов азота(50)
$[{{{\text{M}}}^{ + }}]{{n}_{e}} = {{K}_{3}}[{\text{N}}] + {{K}_{4}}[{{{\text{N}}}_{2}}]{\text{ }}.$Выражая из них плотности [M+] и [C+] и подставляя в (48), получаем
(51)
$\begin{gathered} {{n}_{e}} = \{ {{\left( {А + В} \right)} \mathord{\left/ {\vphantom {{\left( {А + В} \right)} 2}} \right. \kern-0em} 2} + [{{{{{\left( {А + В} \right)}}^{2}}} \mathord{\left/ {\vphantom {{{{{\left( {А + В} \right)}}^{2}}} 4}} \right. \kern-0em} 4} + \\ + \,\,A[{\text{C}}]{{{{k}_{c}}} \mathord{\left/ {\vphantom {{{{k}_{c}}} {{{\alpha }_{{43}}}}}} \right. \kern-0em} {{{\alpha }_{{43}}}}}{{]}^{{0.5}}}{{\} }^{{0.5}}}. \\ \end{gathered} $Здесь А = К3[N] + K4[N2], В = К43[С] = k43/α43[C]. Для расчета ne, кроме известных констант ионизационного равновесия К3, К4 и К43 [15], плотности [С] =1015 см–3 и плотностей N и N2, определяемых из условия равновесия реакции (1) при Т = 7 кК и [M] = 1.05 × 1018 см–3 (р = 1 атм), необходимы значения констант скоростей kc и α43. Для последней применимо модифицированное диффузионное приближение, которое дает α43 = 5.25 × × 10–26 см6/с [15]. Для kc возьмем диапазон возможных значений (2–50) × 10–12 см3/с, характерных для рассматриваемых ионно-молекулярных реакций [21, 24].
Тогда концентрация электронов принимает значения в диапазоне (2.8–4.4) × 1014 см–3, что в два–три раза больше равновесных значений в чистой азотной плазме. Концентрация ионов азота становится во столько же раз меньше: [M+] = = (8.5–5.4) × 1013 см–3, а ионы углерода, как и предполагалось, становятся основными ионами плазмы: [С+] = (1.9–3.8) × 1014 см–3. Их концентрация в пределах взятых значений kc растет несколько больше, чем ne, однако в целом при 25-кратном росте kc этот двукратный рост незначителен, зависимость от kc, как видно из (51), очень слаба (немного слабей, чем корень четвертой степени), что является благоприятным обстоятельством для оценок в отсутствие необходимых данных о многих реакциях.
Принимая среднее значение kс = 10–11 см3/с, вычислим наиболее вероятные плотности заряженных частиц при Т = 7 кК и [С] = 1015 см–3: ne = = 3.3 × 1014 см–3, [С+] = 2.6 × 1014 см–3, [N+] = 4.6 × × 1013 см–3, [${\text{N}}_{2}^{ + }$] = 2.6 × 1013 см–3. Ионов С+ почти 80%. В равновесной азотной плазме при тех же условиях $n_{e}^{^\circ }$ = [M+] = 1.5 × 1014 см–3, [N+] = 9.8 × × 1013 см–3, [${\text{N}}_{2}^{ + }$] = 5.5 × 1013 см–3. Сохранение равновесных условий для азотной компоненты означает ne[M+] = const, так что концентрация электронов растет из-за углеродной примеси во столько же раз, во сколько спадает концентрация ионов азота, – в 2.1 раза. Квазистационарность уравнения (48) и плотности С+ при Т = 7–10 кК и полученных ne = 3.3 × 1014 см–3 устанавливаются за времена, отвечающие критерию квазистационарности τ43 = (α43$n_{e}^{2}$)–1 ≈ 170 мкс < τ0 ≈ 200–600 мкс.
Следует отметить, что если для азота равновесные условия сохраняются, то для углеродной примеси и прежде всего ионов C+, а значит, и электронов они нарушаются. Это видно из уравнения (48), где первое слагаемое левой части, отвечающее неравновесным процессам, сопоставимо со вторым слагаемым, отвечающим за ионизационное равновесие с концентрацией электронов 2 × 1014 см–3. В результате получается бόльшая концентрация электронов ne = 3.3 × 1014 см–3. Отсюда следует, что ионно-молекулярные процессы перезарядки и замещения создают неравновесность рекомбинационного типа [15], редко встречающуюся в низкотемпературной плазме.
На рис. 4 приведены результаты расчета ионного состава азотно-углеродной плазмы по формулам (49)–(51) с использованием полученных экспериментальных распределений [C] (рис. 1) и T (рис. 2) на оси потока. Концентрации атомов и ионов углерода, как правило близкие между собой, около мишени превышают концентрацию ионов азота, причем эта область их преобладания уменьшается со временем. То же можно сказать и о концентрации электронов, на 40-й секунде заметно превышающей $n_{e}^{^\circ }$ после 11 мм пути, а на 140-й – только после 16 мм. Относительная величина этого превышения тоже уменьшается с ~2 до ~1.5 в максимуме. Такое ослабление влияния углерода связано с ростом Т и уменьшением [C] при длительном воздействии азотной струи на мишень, причины которых следует искать в утолщении области приповерхностной плазмы и ослаблении абляции поверхности мишени, что требует отдельного рассмотрения.
ЗАКЛЮЧЕНИЕ
Таким образом, малая примесь углерода (~0.1%), попадающая в термодинамически равновесную азотную плазму, движущуюся к графитовой мишени, проявляет себя только в ионно-молекулярной кинетике, двукратно увеличивая концентрацию электронов, определяя ионный состав плазмы и тем самым нарушая равновесие между ее нейтральной и заряженной компонентами. Это приводит, в частности, к рекомбинационной неравновесности распределения атомов углерода по электронным состояниям. Другие углеродосодержащие примеси (CN и C2) малосущественны.
На пути следования до мишени плазма теряет около 60% вложенной энергии, однако частично сохраняет ЛТР. При этом кинетика процессов определяется реакциями (1), (6), (7), а при наличии углеродосодержащих примесей к ним добавляются реакции (14), (44) и ионно-молекулярный каскад перезарядок и замещений.
Процессы, ответственные за распространение в плазменном потоке углеродных примесей на расстояния до ~1 см от мишени, до конца не ясны. Этот вопрос требует изучения приповерхностной плазмы, которое будет предпринято в следующей работе.
Исследование выполнено при государственной поддержке молодых российских ученых-кандидатов наук (грант Президента РФ № МК-2460.2019.8).
Список литературы
Helber B., Turchi A., Scoggins J.B., Hubin A., Magin T.E. Experimental Investigation of Ablation and Pyrolysis Processes of Carbon-phenolic Ablators in Atmospheric Entry Plasmas // Int. J. Heat Mass Transfer. 2016. V. 100. P. 810.
Toshiyuki Suzuki, Kazuhisa Fujita. Experimental Study of Graphite Ablation in Nitrogen Flow // J. Thermophys. Heat Transfer. 2008. V. 22. № 3. P. 382.
Lei Luo, Yiguang Wang, Liping Liu, Liuyang Duan, Guolin Wang, Yonghong Lu. Ablation Behavior of C/SiC Composites in Plasma Wind Tunnel // Carbon. 2016. V. 103. P. 73.
Михатулин Д.С., Полежаев Ю.В., Ревизников Д.Л. Теплообмен, термохимическое и термоэрозионное разрушение тепловой защиты. М.: Янус-К, 2011. 520 с.
Быкова Н.Г. Исследования спектров излучения продуктов разрушения аблирующих теплозащитных материалов в дозвуковом потоке низкотемпературной воздушной плазмы // Физико-химическая кинетика в газовой динамике. 2014. Т. 15. Вып. 1. http://chemphys.edu.ru/issues/2014-15-1/articles/76/
Chinnov V.F., Tyuftyaev A.S., Kavyrshin D.I., Ageev A.G., Sargsyan M.A., Gadzhiev M.Kh. Comprehensive Study of the Effect of Plasma Stream on Heat-Resistant Materials // High Temp. 2018. V. 56. № 1. P. 25.
Belevtsev A.A., Kavyrshin D.I., Sargsyan M.A., Chinnov V.F., Efimov A.V., Shcherbakov V.V. Spectral Diagnostics of Plasma in the Zone of its Destructive Interaction with Heat-resistant Materials // J. Phys. D: Appl. Phys. 2018. V. 51. 484002.
Chinnov V.F., Sargsyan M.A., Gadzhiev M.Kh., Khromov M.A., Kavyrshin D.I., Chistolinov A.V. Spatial-temporal Diagnostics of the System of a Plasma Stream Interacting with a Surface of Heat Resistant Material // J. Phys.: Conf. Ser. 2018. V. 946. 012174.
Суржиков С.Т. Вычислительные модели дозвуковой динамики низкотемпературной плазмы на основе уравнений Навье–Стокса // Энциклопедия низкотемпературной плазмы / Под ред. Фортова В.Е. М., 2009. Т. VII-1. Ч. 2. С. 183.
Meher K.C., Tiwari N., Ghorui S. Thermodynamic and Transport Properties of Nitrogen Plasma under Thermal Equilibrium and Non-equilibrium Conditions // Plasma Chem. Plasma Process. 2015. V. 35. № 4. P. 605.
NIST Chemical Kinetics Database Standard Reference Database 17. Version 7.0. Release 1.6.8. 2017. http://kinetics.nist.gov/kinetics
Kossyi I.A., Kostinsky A.Yu., Matveyev A.A., Silakov V.P. Kinetic Scheme of the Non-equilibrium Discharge in Nitrogen-Oxygen Mixtures // Plasma Sour. Sci. Tech. 1992. V. 1. P. 207.
Shavelkina M.B., Filimonova E.A., Amirov R.Kh., Isakaev E.Kh. Methane/nitrogen Plasma-assisted Synthesis of Graphene and Carbon Nanotubes // J. Phys. D: Appl. Phys. 2018. V. 51. № 29. 294005.
Смирнов Б.М. Асимптотические методы в теории атомных столновений. М.: Атомиздат, 1973. 296 с.
Биберман Л.М., Воробьев В.С., Якубов И.Т. Кинетика неравновесной низкотемпературной плазмы. М.: Наука, 1982. 376 с.
Методы исследования плазмы / Под ред. Лохте-Хольтгревена В. М.: Мир, 1971. 552 с.
Герцберг Г. Спектры и строение двухатомных молекул. Пер. с англ. М.: Изд-во иностр. лит., 1949. 404 с.
Радциг А.А., Смирнов Б.М. Справочник по атомной и молекулярной физике. М.: Атомиздат, 1980. 240 с.
Королев Ю.Д., Коршунов О.В., Хузеев А.П. и др. Исследование сильноточного диффузного разряда в аргоне // ТВТ. 1985. Т. 23. № 5. С. 853.
Florescu-Mitchell A.I., Mitchell J.B.A. Dissociative Recombination // Phys. Report. 2006. V. 430. P. 277.
Anicich V.G. Evaluated Bimolecular Ion-molecule Gas Phase Kinetics of Positive Ions for Use in Modeling Planetary Atmospheres, Cometary Comae, and Interstellar Clouds // J. Phys. Chem. Ref. Data. 1993. V. 22. № 6. P. 1469.
Низкотемпературная плазма. Т. 1. Теория столба электрической дуги. Новосибирск: Наука, 1990.
High Temperature Phenomena in Shock Waves / Ed. Brun R. France: Springer, 2012.
Атомные и молекулярные процессы / Под ред. Бейтса Д. Пер. с англ. М.: Мир, 1964. 777 с.
Дополнительные материалы отсутствуют.
Инструменты
Теплофизика высоких температур