Теоретические основы химической технологии, 2022, T. 56, № 3, стр. 369-373
Изучение кинетики растворения гидроксида никеля(II) в аммиачно-карбонатном водном растворе
С. В. Добрыднев a, *, О. А. Александрова a, Ю. Г. Резвов a
a Российский химико-технологический университет им. Д.И. Менделеева Новомосковский институт (филиал), Химико-технологический факультет Дружбы 8
301665 Тульская обл., Новомосковск, Россия
* E-mail: sdobrydnev@nirhtu.ru
Поступила в редакцию 09.09.2021
После доработки 16.12.2021
Принята к публикации 30.12.2021
- EDN: UZOTLE
- DOI: 10.31857/S0040357122020063
Аннотация
В работе представлены результаты изучения реакции взаимодействия гидроксида никеля(II) с аммиачно-карбонатным раствором с образованием аква-аммиачных комплексов никеля(II) в температурном интервале 20–40°С. Экспериментально установлено, что при растворении образуется в виде промежуточного продукта гидратированная форма гидроксида никеля [Ni(H2O)x](OH)2 с размером частиц менее 5–8 мкм. Были рассмотрены два механизма протекания процесса: последовательный и последовательно-параллельный. Результаты аналитической обработки кинетических данных позволили рассчитать константы скорости реакций на отдельных стадиях растворения при температурах 20, 30, 40°С, а также значения кажущихся энергий активации.
ВВЕДЕНИЕ
Изучение процессов растворения оксидов, гидроксидов и основных карбонатов металлов в аммиачно-аммонийных и аммиачно-карбонатных водных растворах является важной задачей для многих областей промышленности, включая коррозию металлов [1], пассивирование [2, 3], выщелачивание минералов [4–6], гидрометаллургию [7–9]. На кинетику растворения оксидов, гидроксидов и основных карбонатов металлов оказывают влияние, как физико-химические свойства твердой фазы, так и природа водных растворов электролитов [10]. Кислородсодержащие соединения никеля в гидрометаллургии подвергают химическому выщелачиванию кислотными растворами, состоящими в основном из разбавленной серной кислоты. По сравнению с металлургической переработкой никельсодержащего сырья, процесс выщелачивания в водно-аммиачных растворах, по мнению авторов [11], является более эффективным, а также способствует селективности растворения и уменьшению коррозионных воздействий на оборудование. Технология последующей переработки, полученных аква-аммиачных комплексов никеля, позволяет исключить выброс в атмосферу вредных газообразных продуктов, что делает аммиачно-карбонатную технологию перспективной не только с экономической, но и с экологической точки зрения [12].
Цель настоящей работы: изучение кинетики процесса растворения гидроксида никеля(II) в аммиачно-карбонатной смеси в зависимости от температуры.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Изучение растворения гидроксида никеля(II) (квалификация “Ч”, ГОСТ 48-3-63-90) проводили в бинарном водном растворе гидрокарбоната аммония (квалификация “ХЧ”, ГОСТ 3762-78) и водного раствора аммиака (квалификация “ЧДА”, ГОСТ 3760-7). Результаты рентгенофазового анализа показали, что гидроксид никеля (ГОСТ 48-3-63-90) представляет собой смесь β-модификации и α-модификации (номер карточки по базе данных JCPDS ICDD-1999 73-1520). Кинетика растворения гидроксида никеля(II) в аммиачно-карбонатном растворе в зависимости от температуры исследовалась двумя независимыми способами: гравиметрическим и спектрофотометрическим.
В стеклянный реактор, вносили навеску гидроксида никеля(II) массой 2 г (фракционный состав 50–63 мкм), а затем приливали 8 мл дистиллированной воды и включали перемешивание. Отдельно термостатировали 92 мл бинарного водного раствора гидрокарбоната аммония (1.32 М) и аммиака (1.05 М), который через 15 мин вливали в реактор и фиксировали время начала растворения. Через заданный интервал времени непрореагировавший осадок гидроксида никеля(II) отделяли фильтрованием на фильтре красная лента с размером пор 5–8 мкм (время отделения твердой и жидкой фаз не превышало 60 с). Фильтрат представлял собой гетерогенную смесь, включающую частицы твердой фазы менее 5–8 мкм и гомогенный раствор аммиачно-карбонатных комплексов никеля. Осадок, оставшийся на фильтре, сушили в течение 12 ч при температуре 50°С. Количество растворенного гидроксида никеля(II) оценивали по изменению массы:
где m0 – масса начальной навески гидроксида никеля(II); mос – масса осадка гидроксида никеля(II) после фильтрования.Фильтрат, полученный согласно вышеописанной методике, анализировался на спектрофотометре ПЭ-5400УФ для определения количественного содержания аква-аммиачных комплексов никеля(II). Зависимости значений оптической плотности при длинах волн 370 и 610 нм, соответствующих максимумам светопоглощения были построены от массы никеля в растворе в виде смешанных аква-аммиачных комплексных форм, в пересчете на гидроксид никеля (mp-p).
Эксперименты проводили для трех температур 20 ± 0.1°С, 30 ± 0.1°С, 40 ± 0.1°С и времени отбора проб: 10, 15, 20, 25, 30, 35, 40, 45, 50, 60 мин после начала опыта. Все эксперименты проводили в серии из трех параллельных опытов с последующей статистической обработкой полученных данных.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для установления состава промежуточных продуктов, образующихся на поверхности твердой фазы, навеску гидроксида никеля (ГОСТ 48-3-63-90) с размером частиц 50–63 мкм выдерживали в течение 48 часов в дистиллированной воде при температурах 20, 30, 40°С, фильтровали и сушили при 50°С в течение 12 ч. Рентгенофазовый анализ показал полное совпадение рентгенограмм осадков, после гидротермального растворения и исходного гидроксида никеля(II) (номер карточки по базе данных JCPDS ICDD-1999 73-1520) в дистиллированной воде. Однако, при растворении гидроксида никеля(II) в водно-аммиачной и аммиачно-карбонатной средах, согласно данных авторов работы [13], в результате интеркаляции молекул воды и аммиака в межслоевое пространство кристаллов гидроксида никеля(II) образуется гидратированная форма гидроксида никеля, которая может быть представлена формулой: [Ni(H2O)x](OH)2, (0.1 ≤ x ≤ 0.4).
Процесс растворения гидроксида никеля(II) в аммиачно-карбонатном водном растворе включает две стадии. На первой стадии протекает реакция гидратация гидроксида никеля(II) с образованием [Ni(H2O)x](ОН)2:
(2)
$\begin{gathered} {\text{Ni(OH}}{{)}_{2}} + x{{{\text{H}}}_{{\text{2}}}}{\text{O}} + {\text{N}}{{{\text{H}}}_{3}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}} = \\ = \,\,[{\text{Ni(}}{{{\text{H}}}_{{\text{2}}}}{\text{O}}{{)}_{x}}]{{{\text{(OH}})}_{2}} + {\text{N}}{{{\text{H}}}_{3}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}}. \\ \end{gathered} $На второй стадии протекает реакция растворения гидрата гидроксида никеля с образованием различных форм аква-аммиачных комплексов [14] (3):
(3)
$\begin{gathered} \text{[}{\text{Ni(}}{{{\text{H}}}_{{\text{2}}}}{\text{O}}{{)}_{x}}]{{{\text{(OH}})}_{2}} + (6 - x){\text{N}}{{{\text{H}}}_{3}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}} + \\ + \,\,{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{HC}}{{{\text{O}}}_{3}} = [{\text{Ni(N}}{{{\text{H}}}_{3}}{{)}_{x}}{{({{{\text{H}}}_{{\text{2}}}}{\text{O}})}_{{6 - x}}}]{\text{C}}{{{\text{O}}}_{3}} + \\ + \,\,(x + 2){{{\text{H}}}_{{\text{2}}}}{\text{O}}. \\ \end{gathered} $Также возможен и процесс растворения гидроксида никеля с образованием аква-аммиачных комплексов, согласно реакции (4):
(4)
$\begin{gathered} {\text{Ni(OH}}{{)}_{2}} + (6 - x){\text{N}}{{{\text{H}}}_{3}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}} + {\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{HC}}{{{\text{O}}}_{3}} = \\ = \,\,[{\text{Ni(N}}{{{\text{H}}}_{3}}{{)}_{x}}{{({{{\text{H}}}_{{\text{2}}}}{\text{O}})}_{{6 - x}}}]{\text{C}}{{{\text{O}}}_{3}} + 2{{{\text{H}}}_{{\text{2}}}}{\text{O}}. \\ \end{gathered} $Экспериментальные данные гравиметрического измерения уменьшения исходного количества гидроксида никеля (mос), в зависимости от времени и температуры опытов, представлены на рис. 1.
Рис. 1.
Изменение массы исходного Ni(OH)2, в зависимости от времени и температуры опытов: 1 – 20, 2 – 30, 3 – 40°С.
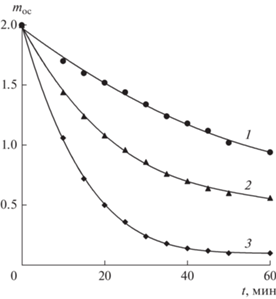
Масса Ni2+ (mp-p) в жидкой фазе в виде аква-аммиачных комплексов (результаты спектрофотометрических измерений) в зависимости от времени и температуры опытов, представлена на рис. 2.
Рис. 2.
Масса Ni2+ в виде аква-аммиачных комплексов (жидкая фаза), в зависимости от времени и температуры опытов: 1 – 20, 2 – 30, 3 – 40°С.
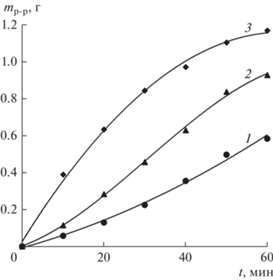
Реакционная смесь представляет собой суспензию, состоящую из прореагировавшего гидроксида никеля, гидратированной формы гидроксида никеля и аква-аммиачных комплексов. Следовательно, масса образовавшейся гидратированной формы гидроксида никеля (mгидр. ф) может быть рассчитана по уравнению (5):
(5)
${{m}_{{{\text{гидр}}{\text{.ф}}}}} = {{т}_{{\text{0}}}} - {{m}_{{{\text{ос}}}}} - {{m}_{{{\text{p}} - {\text{p}}}}}.$Результаты расчетов изменения массы (mгидр. ф) по уравнению (5), в зависимости от времени и температуры опытов, представлена на рис. 3.
Рис. 3.
Изменение массы гидратированной формы гидроксида никеля в зависимости от времени и температуры опытов: 1 – 20°С, 2 – 30°С, 3 – 40°С.
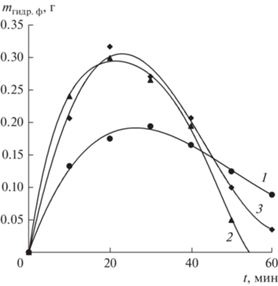
Как видно из данных, приведенных на рис. 1–3, упрощенно механизм процесса растворения гидроксида никеля в аммиачно-карбонатном растворе можно представить в виде двух параллельных необратимых реакций:
(6)
${{{\text{A}}}_{{{\text{тв}}}}}\xrightarrow{{{{k}_{1}}}}{{{\text{B}}}_{{{\text{гирд}}{\text{.ф}}}}}\xrightarrow{{{{k}_{2}}}}{{{\text{С}}}_{{{\text{р}} - {\text{р}}}}},$(7)
${{{\text{A}}}_{{{\text{тв}}}}}\xrightarrow{{{{k}_{3}}}}{{{\text{С}}}_{{{\text{р}} - {\text{р}}}}},$Для аналитического описания кинетики процессов химического растворения ускоренного типа в первом приближении можно использовать экспоненциальный закон [15]. Сделаем допущение, что скорости изменения массы реагентов Aтв и Вгидр. ф подчиняются уравнению необратимой реакции первого порядка, тогда в интегральной форме аналитические зависимости изменения Aтв (α), Вгидр. ф (β) и образования аммиачно-карбонатных комплексов никеля Cp-p (γ) могут быть выражены уравнениями (8)–(10):
(9)
${{\beta }}(t) = \frac{{{{k}_{1}}}}{{({{k}_{1}} + {{k}_{3}} - {{k}_{2}})}}(\exp ( - {{k}_{2}}t) - \exp ( - ({{k}_{1}} + {{k}_{3}})t)),$(10)
${{\gamma }}(t) = \left( {\exp ( - ({{k}_{1}} + {{k}_{3}})t) - \frac{{{{k}_{1}}}}{{{{k}_{2}} - {{k}_{1}} - {{k}_{3}}}}(\exp ( - {{k}_{1}} + {{k}_{3}})t) - \exp ( - {{k}_{2}}t)} \right),$Значения постоянных k1, k2, k3, рассчитанные на основе экспериментальных данных для трех изученных температурах также средняя квадратичная погрешность аппроксимации, представлены в табл. 1.
Таблица 1.
Значения постоянных, k1, k2, k3 и средняя квадратичная погрешность аппроксимации при температурах: 20°С, 30°С, 40°С
| Температура процесса растворения, °C | k1, мин–1 | k2, мин–1 | k3, мин–1 | Средняя квадратичная погрешность |
|---|---|---|---|---|
| 20 | 0.0134 | 0.0649 | 0 | 0.0183 |
| 30 | 0.0269 | 0.0770 | 0.000624 | 0.0267 |
| 40 | 0.0361 | 0.0486 | 0.0310 | 0.0156 |
Как видно из данных, представленных в таблице, средняя квадратичная погрешность с увеличением температуры опыта (от 30 до 40°С) уменьшается, что дает основания сделать предположение об изменении механизма протекания процесса растворения. При температуре 20°C константа k3 = 0, т.е. реакция (3) практически не идет. Однако, при температуре 40°C значение k3 равно 0.031 мин–1, что уже соизмеримо с константами k1 и k2.
Среднее значение кажущейся энергии активации, рассчитанное по уравнению Аррениуса в интегральной форме [16], для реакции (2), в интервале температур 20–30°C, составило ~51 308 Дж/моль, а реакции (3) ~12557 Дж/моль. В интервале температур 30–40°C значение кажущейся энергии активации для реакции (2), составило ~22 993 Дж/моль, а для реакции (3) ~–36 304 Дж/моль. При рассмотрении реакции (4), в интервале температур 20–30°C реакция практически не наблюдается, тогда, как в интервале 30–40°C значение кажущейся энергии активации достигает ~30 7963 Дж/моль. Это доказывает, что механизм протекания процесса растворения меняется и проходит без образования промежуточного продукта Вгидр. ф. Различия в кажущихся энергиях активации в интервалах температур 20–30 и 30–40°C также свидетельствуют об изменении механизма процесса растворения.
Как видно из сравнения значений кажущихся энергий активации 51 308 и 22 993 Дж/моль, в процессе растворения гидроксида никеля(II) в аммиачно-карбонатном растворе (2), увеличение температуры от 30 до 40°С, приводит к переходу кинетического режима к смешанному типу. На второй стадии процесса (3), с увеличением температуры наблюдается значительное повышение роли фактора диффузионного торможения реакции образования аква-аммиачных комплексов никеля.
ЗАКЛЮЧЕНИЕ
Исследование кинетики растворения гидроксида никеля(II) в аммиачно-карбонатном бинарном растворе (гидрокарбоната аммония 1.32 М, водный раствор аммиака 1.05 М) при температурах: 20, 30, 40°С позволило установить образование промежуточного продукта и установить механизм протекания процесса. Для температурного интервала 20–30°С предложен последовательный механизм протекания процесса растворения, а для температурного интервала 30–40°С: последовательно-параллельный. Рассчитаны константы скорости k1, k2, k3 на отдельных стадиях растворения при температурах: 20, 30, 40°С. Значения кажущихся энергий активации для температурного интервала 20–30°C на первой стадии процесса равно 51 208 Дж/моль, на второй стадии: 12 557 Дж/моль. В интервале температур 30–40°C значение кажущейся энергии активации на первой стадии составило 22993 Дж/моль, на второй стадии –36 304 Дж/моль. При температурах 20 и 30°С образование аква-аммиачных комплексов никеля(II) происходит из промежуточного продукта: [Ni(H2O)x](OH)2, а при температурах 30–40°С, наряду с образованием гидратированной формы гидроксида никеля(II), также протекает и прямая реакция комплексообразования.
ОБОЗНАЧЕНИЯ
| A, B, C | продукты |
| k | константа скорости |
| m | масса, г |
| t | время, мин |
| α, β, γ | относительные величины, показывающие изменения никеля в реакциях |
ИНДЕКСЫ
Список литературы
Орлова Е.А., Орлов А.В. Защита конструкционных материалов от коррозии в жидких металлах // Вопросы атомной науки и техники. Серия: ядерно-реакторные константы. 2016. № 4. С. 200. [Orlova E.A., Orlov A.V. Protection of structural materials from corrosion in liquid metals // Problems of atomic science and technology. Series: nuclear reactor constants. 2016. № 4. P. 200.]
Багаев Е.А., Журавлев К.С., Свешникова Л.Л., Щеглов Д.В. Изменение оптических свойств нанокластеров CdS, полученных методом Ленгмюра–Блоджетт, при пассивации в аммиаке // Физика и техника полупроводников. 2008. Т. 42. № 6. С. 718. [Ba-gaev E.A., Zhuravlev K.S., Sveshnikova L.L., Shcheglov D.V. Changes in the optical properties of CDs nanoclusters obtained by the Langmuir–Blodgett method during passivation in ammonia // Physics and Technology of semiconductors. 2008. V. 42. № 6. P. 718.]
Ларин В.И., Хоботова Э.Б., Даценко В.В., Добриян М.А. Химическое пассивирование меди в аммиачных хлоридсодержащих растворах // Журн. физической химии. 2008. Т. 82. № 9. С. 1676. [Larin V.I., Khobotova E.B., Datsenko V.V., Dobriyan M.A. Chemical passivation of copper in ammonia chloride-containing solutions // J. Physical Chemistry. 2008. V. 82. № 9. P. 1676.]
Варламова И.А., Чурляева Н.А., Калугина Н.А., Гиревая Х.Я. Аммонизация как перспективный метод экстрагирования меди и цинка из техногенного сырья // Современные проблемы науки и образования. 2015. № 1. [Varlamova I.A., Churlyaeva N.A., Kalugina N.A., Girevaya H.Ya. Ammonization as a promising method for extracting copper and zinc from technogenic raw materials // Modern problems of science and education. 2015. № 1.]
Перетрутов А.А., Чубенко М.Н. Растворимость оксидов меди и цинка в аммиачных растворах, насыщенных хлоридом аммония // Естеств. Тех. Науки, Неорг. Химия. 2008. № 2(34). С. 59.
Дударева Г.Н., Иринчинова Н.В. Сорбционное извлечение никеля в хлор-аммонийной технологии переработки окисленных руд // Известия вузов. Прикладная химия и биотехнология. 2016. Т. 6. № 2. С. 83. [Dudareva G.N., Irinchinova N.V. Sorption extraction of nickel in the chlorine-ammonium technology of processing oxidized ores // Izvestiya vuzov. Applied chemistry and biotechnology. 2016. V. 6. № 2. P. 83.]
Harvey R., Hannah R. Selective Precipitation of Mixed Nickel–Cobalt Hydroxide // Hydrometallurgy 2011. V. 105(3–4). P. 222. https://doi.org/10.1016/j.hydromet.2010.10.003
Mubarok M.Z., Lieberto J. Precipitation of nickel hydroxide from simulated and atmospheric-leach solution of nickel laterite ore // Procedia Earth and Planetary Science 2013. № 6. P. 457. https://doi.org/10.1016/j.proeps.2013.01.060}
Светлов А.В., Потапов С.С., Потапов Д.С., Кравченко Е.А., Ерохин Ю.В., Потокин А.С., Селиванова Е.А., Суворова О.В., Кумарова В.А., Нестеров Д.П., Макаров Д.В., Маслобоев В.А. Исследование возможности извлечения цветных металлов и производства строительных материалов из шлаков медно-никелевого производства // Вестник МГТУ. 2015. Т. 18. № 2. С. 335.
Alvaro Aracena, Javiera Pino and Oscar Jerez. Mechanism and Kinetics of Malachite Dissolution in an NH4OH System // Metals. 2020. № 10. P. 833. https://doi.org/10.3390/met10060833
Юрченко А.А., Бутенко А.Н., Лобойко А.Я. Кинетика процесса аммиачного выщелачивания соединений никеля из отработанных железо-никелевых аккумуляторов // Восточно-Европейский журн. передовых технологий. 2011. С. 7. [Yurchenko A.A., Butenko A.N., Loboiko A.Ya. Kinetics of the process of ammonia leaching of nickel compounds from spent iron-nickel batteries // East European J. Advanced Technologies. 2011. P. 7.]
Добрыднев С.В., Александрова О.А. Получение ультрадисперсных частиц оксида никеля для анодов твердооксидных топливных элементов. // Сб. докл. Первая международная конференция по интеллектоемким технологиям в энергетике (Физическая химия и электрохимия расплавленных и твердых электролитов) 18–22 сентября 2017 г. Екатеринбург. 2017. С. 61.
Hall D.S., Lockwood D.J., Bock C., MacDougall B.R. Nickel hydroxides and related materials: a review of their structures, synthesis and properties // Proceedings of The Royal Society A Mathematical Physical and Engineering Sciences. 2015. V. 471(2). P. 1.
Образование амминов металлов в водном растворе / Пер. с англ. канд. хим. наук Г.Ф. Губской и Г.С. Терешина. Под ред. акад. И. В. Тананаева. М.: Изд-во иностр. лит., 1961. С. 308.
Свиридова Т.В. Химия твердого тела: топохимическая кинетика. Учебное пособие. Минск: БГУ, 2011.
Вишняков А.В., Кизим Н.Ф. Физическая химия. Учебник для ВУЗ-ов. М.: Химия, 2012.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии



