Вестник РАН, 2022, T. 92, № 8, стр. 709-716
КОРОНАВИРУСНАЯ ИНФЕКЦИЯ COVID-19 И БЕРЕМЕННОСТЬ
М. А. Курцер *
Российский национальный исследовательский медицинский университет имени Н.И. Пирогова Минздрава России
Москва, Россия
* E-mail: m.kurtser@mcclinics.ru
Поступила в редакцию 31.01.2022
После доработки 31.01.2022
Принята к публикации 20.02.2022
- EDN: UOPZVF
- DOI: 10.31857/S0869587322080096
Аннотация
Новая коронавирусная инфекция SARS-CoV-2, вспышка которой возникла в Китае в декабре 2019 г., быстро распространилась по всему миру. 11 марта 2020 г. Всемирная организация здравоохранения (ВОЗ) присвоила данной инфекции статус пандемии. Особое место в структуре заболеваемости COVID-19 занимают беременные и родильницы. В Клиническом госпитале “Лапино” Группы компаний “Мать и дитя” более чем за полтора года накоплен значительный опыт ведения пациентов с COVID-19, в том числе беременных и родильниц. В статье представлены особенности течения новой коронавирусной инфекции у беременных и родильниц в различные периоды пандемии, опыт ведения беременности и родов у вышеуказанного контингента пациентов, методы лечения.
Коронавирусы являются важными патогенами для человека и животных. В конце 2019 г. новый коронавирус был выявлен как источник пневмонии в Ухане китайской провинции Хубэй. Вирусная инфекция быстро распространилась, что привело к эпидемии по всему Китаю, за которой последовала пандемия. В феврале 2020 г. Всемирная организация здравоохранения обозначила заболевание как COVID-19, то есть коронавирусная болезнь 2019 г. [1]. Вирус, вызывающий COVID-19, обозначается коронавирусом 2 тяжёлого острого респираторного синдрома (SARS-CoV-2), ранее он назывался 2019-nCoV. Это одноцепочечный РНК-содержащий вирус, относящийся к семейству Coronavidae, роду Betacoronovirus. Важным свойством этого вируса является его тропность (то есть способность поражать преимущественно конкретные органы и ткани) к клеткам-мишеням, имеющим рецепторы ангиотензинпревращающего фермента II типа (АПФ2), которые расположены на эндотелиальной и эпителиальной альвеолярной поверхности. Основной мишенью SARS-Cov-2 являются альвеолярные клетки II типа, что обусловливает развитие диффузного альвеолярного повреждения [2–4]. При новой коронавирусной инфекции может развиваться цитокиновый шторм – избыточный ответ иммунной системы, стремительное высвобождение цитокинов, развитие нарушений свёртываемости крови.
За 21 месяц (с марта 2020 по декабрь 2021 г.) в Клинический госпиталь “Лапино” госпитализировано более 5000 пациентов с новой коронавирусной инфекцией, из них 389 беременных и родильниц, проведено 145 родов, родился 151 живой ребёнок, в том числе 6 двоен. Диагностика COVID-19 в госпитале проводилась путём выявления РНК SARS-Cov-2 методом ПЦР, обнаружения Ig M и Ig G к SARS-Cov-2. Инструментальная диагностика включала в себя компьютерную томографию (КТ) органов грудной клетки и УЗИ лёгких и плевральных полостей. При лёгком течении заболевания отсутствовали характерные проявления (КТ – 0), при среднетяжёлом поражалось < 25% объёма лёгких (КТ-1) или 25–50% объёма лёгких (КТ-2), при тяжёлом распространённость поражения достигала 50–75% объёма лёгких (КТ-3) и при крайне тяжёлом – >75% (КТ-4). Лечение проводилось согласно Методическим рекомендациям Министерства здравоохранения РФ “Организация оказания медицинской помощи беременным, роженицам, родильницам и новорождённым при новой коронавирусной инфекции COVID-19” [5]. За весь период из 389 пациенток с лёгкой степенью течения заболевания было госпитализировано 94 (24%), со средней – 253 (65%), с тяжёлой – 34 (9%) и крайне тяжёлой – 8 (2%).
С начала пандемии по декабрь 2021 г. зафиксировано четыре волны новой коронавирусной инфекции (рис. 3). Первая волна, отмечавшаяся с марта по май 2020 г., была вызвана китайским штаммом COVID-19, во вторую волну (октябрь 2020 – март 2021 г.) к нему присоединился британский штамм, в третью (апрель–август 2021 г.) – индийский, четвёртая волна, продолжающаяся с сентября 2021 г., в основном вызвана индийским штаммом (рис. 1).
Во время первой волны COVID-19 в госпиталь “Лапино” было госпитализировано 84 беременных и родильниц, в основном (85.2%) с лёгкой и средней степенью тяжести заболевания. Возраст пациенток варьировался в пределах от 21 до 46 лет. Средний возраст в группе с тяжёлым течением был больше, чем в других группах, и составил 35.8 лет +/– 3.4 года. Срок беременности так же был больше, чем в среднем, – 32.2 недели +/– 3.8 недели. При ведении пациенток во время первой волны независимо от срока беременности использовались препараты осельтамивир и гриппферон. При средней и тяжёлой степени у большинства применялся ингибитор ВИЧ-1 и ВИЧ-2 протеазы – лопинавир + ритонавир (калетра). Большинство беременных и родильниц получали антибактериальную терапию. У родильниц применялся гидроксихлорохин (плаквенил). Ингибитор ИЛ-6 – тоцилизумаба (актемра) – использовался, когда предполагаемая польза превалировала над рисками. Показанием для введения блокаторов ИЛ-6 (вводился только родильницам) являлись данные КТ – КТ2-3 в сочетании с двумя и более признаками: снижение SpO2, СРБ>30 мг/л, лихорадка >38°С в течение трёх дней, число лейкоцитов <3.0 × 109/л, абсолютное число лимфоцитов <1.0–109 /л. Побочных явлений на фоне лечения актемрой не наблюдалось. К концу первой волны начали применять глюкокортикостероиды (дексаметазон – 8 мг два раза в сутки), которые значительно быстрее и эффективнее позволяли купировать цитокиновый шторм, улучшали сатурацию и лабораторные маркеры, что давало возможность пролонгировать беременность.
Из особенностей течения заболевания в первую волну следует отметить, что чаще тяжёлыми формами заболевания страдали беременные на сроках гестации до 32 недель, не отмечалось нарастания уровня ИЛ-6 более 100, не было быстрой прогрессии интерстициальных изменений, независимо от периода болезни и лихорадки изменения нарастали постепенно. В качестве лабораторных маркеров для оценки динамики использовались ОАК, СРБ, ИЛ-6, Д-димер. Тактика ведения беременности была выжидательная, при нарастании дыхательной недостаточности и/или ухудшении состояния плода проводилось экстренное родоразрешение, которое улучшало состояние пациенток.
Из 84 поступивших пациенток 79 были беременными: 50 из них (63%) выписаны с выздоровлением с пролонгирующейся беременностью, у 23 произошли своевременные или преждевременные роды, у четырёх беременность прервалась самопроизвольно, у одной диагностирована внематочная беременность. Одна пациентка, переведённая в госпиталь из другого медицинского учреждения в крайне тяжёлом состоянии, умерла на 13-е сутки после родоразрешения в результате двухсторонней полисегментарной тотальной пневмонии, сепсиса, полиорганной недостаточности. Все пять родильниц, поступившие в госпиталь, выписаны с выздоровлением.
Во вторую волну новой коронавирусной инфекции в госпиталь “Лапино” были госпитализированы 127 беременных и родильниц, из них 91.2% с лёгкой и средней степенью тяжести. Возраст варьировал от 19 до 49 лет. Средний возраст в группах с различной степенью тяжести не отличался. Беременные госпитализированы в сроке от 6 до 41 недели гестации. В среднем наибольший срок беременности был в группе со средней степенью тяжести – 29.6 недели +/– 10.3 недели. Во 2-ю волну пациентки с лёгкой степенью тяжести госпитализировались для родоразрешения. Изменились подходы к лечению: отказались от применения калетры и плаквенила, у родильниц применялся триазаверин, фавипиравир, активно использовались глюкокортикостероиды, антибактериальные препараты, которые позволяли пролонгировать беременность. При сроках беременности до 32 недель при неэффективности гормональной и антибактериальной терапии, при нарастании пневмонии и провоспалительных маркеров (цитокиновый шторм) с целью максимального пролонгирования беременности чаще стал вводиться тоцилизумаб, после введения которого отмечалась стабилизация процесса и удавалось избежать преждевременного родоразрешения. По жизненным показаниям применялись следующие ингибиторы ИЛ: сарилумаб (кевзара), левилимаб (илсира), олокизумаб (артлегия). В госпитале использовались цитокиновые колонки Jaffron 330 HA (цитокиновая сорбция), экстракорпоральная мембранная оксигенация (ЭКМО). Цитокиновые колонки применялись у девяти пациенток на 1–3 сутки после кесарева сечения при повышении уровня ИЛ-6 более 40 пг/мл. Проводилась гемосорбция через колонку Jafron HA 330 в течение 3–5 часов (или обработка 20–30 литров крови). Каждая пациентка получила от 1 до 3 процедур (по 1 процедуре в день). В результате мы наблюдали снижение интерлейкина-6, детоксикацию, повышение сатурации (во время процедуры).
К особенностям течения заболевания во вторую волну можно отнести постепенное развитие тотального поражения лёгочной ткани, несмотря на проводимую терапию. К лабораторным маркерам были добавлены фибриноген, ЛДГ, ферритин.
Из 127 госпитализированных пациенток 53 (42%) были выписаны с выздоровлением с пролонгированной беременностью, у 60 произошли роды, у восьми беременность прервалась самопроизвольно, у двух при поступлении диагностирована внематочная беременность. Все три родильницы, поступившие в госпиталь, выписаны с выздоровлением. Одна пациентка, переведённая в госпиталь из другого медицинского учреждения в крайне тяжёлом состоянии, умерла на 29-е сутки после родоразрешения в результате двухсторонней полисегментарной тотальной пневмонии, состояния после гемикраниэктомии, декомпенсированного сахарного диабета.
Третья волна COVID-19 в основном была вызвана штаммом Delta. По данным Центра по контролю и профилактике заболеваний США, этот штамм характеризует повышенная трансмиссивность, возможное снижение нейтрализации некоторыми видами лечения моноклональными антителами EUA, возможное снижение нейтрализации сыворотками после вакцинации. У варианта коронавируса Delta двойная мутация шиповидного белка, что позволяет вирусу быстрее проникать в клетки организма [6].
В третью волну среди госпитализированных в КГ “Лапино” было 109 беременных и родильниц. Их возраст варьировался от 22 до 45 лет. Средний возраст в группах с различной степенью тяжести не отличался и составил 33.2 лет +/– 6.9 года. Беременные госпитализированы на сроке от 4 до 41 недели гестации. Средний срок беременности составил – 31.6 недели +/– 7.9 недели.
Следует отметить, что по сравнению с предыдущими волнами в этот период наблюдалось увеличение числа госпитализаций пациенток в тяжёлом состоянии – 20 (18.3%), из них шесть находились на ИВЛ, три – на неинвазивной ИВЛ, 11-ти проводилась высокопоточная оксигенация. Продолжительность госпитализации в отделении реанимации и интенсивной терапии госпиталя составила 21.2 дня +/– 3.1 дня, всего в госпитале – 29.2 дня +/– 5.6 дня.
Третья волна имела свои особенности в течении заболевания и в терапии – быстро прогрессирующее течение с нарастанием дыхательной недостаточности и суточной прогрессией объёма поражения лёгких. В связи с этим до родоразрешения (или сразу после) чаще применялся тоцилизумаб. При отсутствии цитокинового шторма, неэффективности стандартной антибактериальной терапии и терапии ГКС однократное или двукратное введение тоцилизумаба приводило к положительной динамике и возможности пролонгации беременности. В связи с прогрессирующим нарастанием уровня ИЛ-6 применялся олокизумаб (артлегия). На сроках более 32 недель при разгаре болезни, быстром нарастании явлений дыхательной недостаточности, ИЛ-6 >100, плохо купирующейся лихорадке принималось решение о незамедлительном родоразрешении.
При цитокиновом шторме преимущественный метод родоразрешения – кесарево сечение. При тяжёлом течении заболевания даже своевременное родоразрешение (независимо от способа) могло не привести к ожидаемому улучшению состояния, а лишь давало возможность для применения биологической терапии, цитостатиков, мощных антимикробных и противовирусных средств, которые не применяются во время беременности. Следует отметить, что после своевременного родоразрешения явления дыхательной недостаточности часто усугублялись, поражение лёгких за несколько часов прогрессировало до КТ 3–4, что также было обусловлено нарастанием явлений отёчного синдрома. Диуретическая терапия позволяла уменьшить явления дыхательной недостаточности и уменьшить размер и плотность консолидации.
После родоразрешения, несмотря на купированную лабораторную картину цитокинового шторма биологической иммуноопосредованной терапией, продолжал нарастать объём поражения лёгочной ткани до 80–95% с формированием обширных зон консолидации, в том числе за счёт гемофагоцитарного лимфогистиоцитоза, при котором используются цитостатики для профилактики раннего фиброзирования. В этот период мы активно применяли цитокиновую сорбцию.
Из 109 госпитализированных пациенток были беременными 105, из них 46 (44%) выписаны с выздоровлением беременными, у 51 произошли своевременные и преждевременные роды, у семи беременность прервалась самопроизвольно, у одной диагностирована внематочная беременность. Умерли две пациентки, поступившие в госпиталь в крайне тяжёлом состоянии: одна родильница, смерть которой наступила на 57 сутки после родов, вторая – после искусственного прерывания беременности на сроке 20–21 неделя гестации (смерть на 22 сутки после прерывания беременности).
Во время четвёртой волны COVID-19 в госпиталь поступили 69 беременных и родильниц: 60 из них со средней степенью тяжести заболевания, девять – в тяжёлом состоянии. Средний возраст пациенток был таким же, как и в другие периоды эпидемии – 32.4 года +/– 3.4 года, средний срок гестации на момент госпитализации – 31.3 недели +/– 8.1 недели (от 6 до 39 недель).
В тяжёлом и крайне тяжёлом состоянии находились девять пациенток (13%), из них восемь дышали самостоятельно, одна находилась на ИВЛ, ЭКМО. Продолжительность госпитализации в отделении реанимации и интенсивной терапии составила 31.5 +/– 4.4 дня, в госпитале – 15. 4 +/– 5.9 дня.
Из особенностей течения заболевания в четвёртую волну необходимо отметить быстро прогрессирующее (иногда молниеносное) течение заболевания у беременных с нарастанием дыхательной недостаточности и суточной прогрессии объёма поражения лёгких по данным мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки. Наиболее информативным для диагностики окзались МСКТ ОГК, УЗИ лёгких (в первом и начале второго триместра). Глюкокортикостероиды применялись не ранее пятого дня болезни, активно использовались тоцилизумаб, левилимаб, сарилумаб, олокизумаб (артлегия).
Новым методом лечения в конце 2021 г. стало использование ковид-глобулина – иммуноглобулина человека против COVID-19, состоящего из белков плазмы человека, из которых не менее 95% IgG, обладающего активностью антител к SARS-CoV-2, и моноклональных антител. Моноклональные антитела бамланивимаб + этесевимаб, казиривимаб + имдевимаб и сотровимаб применяются для лечения COVID-инфекции у взрослых и детей весом более 40 кг. Препарат следует назначать как можно раньше после выявления вируса SARS-CoV-2 в течение 10 дней с момента появления симптомов коронавирусной инфекции [7–9]. В Клиническом госпитале “Лапино” бамланивимаб и этесевимаб вводились в стационаре шести беременным на сроке от 3 до 6 дня заболевания, при наличии клинических проявлений и результатах КТ 0–1. У пяти пациенток не было развития пневмонии, у одной наблюдался регресс клинической симптоматики. Ни одной из пациенток не потребовалось досрочного родоразрешения.
Как и в третью волну, на сроках более 32 недель гестации в разгар болезни, при быстром нарастании явлений дыхательной недостаточности, ИЛ-6 >100, плохо купирующейся лихорадке принималось решение о незамедлительном родоразрешении. Из 69 госпитализированных в четвёртую волну пациенток 39 (59.4%) выписаны с выздоровлением беременными, у 22 произошли своевременные или преждевременные роды, у трёх беременность прервалась самопроизвольно, у одной при поступлении диагностирована внематочная беременность.
По данным Центра по контролю и профилактике заболеваний США, уровень преждевременных родов среди беременных с COVID-19 составлял 11.6%, а частота кесарева сечения – 33.1% [10]. По нашим данным, доля преждевременных родов варьировалась от 13% в первую волну до 45% в четвёртую. Частота кесарева сечения в КГ “Лапино” была наименьшей во вторую волну – 28.3%, максимальной в первую волну – 73.3%.
При невозможности адекватной оксигенации на фоне ИВЛ и высоком риске летального исхода возможно использование вено-венозной (ВВ) экстракорпоральной мембранной оксигенации (ЭКМО) [11]. ВВ ЭКМО направлено на поддержание оксигенации, разгрузку малого круга кровообращения, что увеличивает необходимые временны́е лимиты для восстановления лёгочной ткани. Наиболее популярными доступами ВВ ЭКМО является канюляция дренажной канюлей правой бедренной вены, возвратной канюлей правой ярёмной вены. Оксигенированная кровь напрямую поступает в правые отделы сердца, снижая сопротивление лёгочного кровообращения и постнагрузку правого желудочка.
Показаниями к ВВ ЭКМО являются [12, 13]:
• PaO 2 / FiO 2 <80 mm более 6 часов;
• PaO 2 / FiO 2 <30 mm более 30 часов;
• pH <7.25 с PaCO2 >60 mm Hg более 6 часов.
Приведу пример успешного применения ВВ ЭКМО у беременной пациентки с тяжёлым ОРДС, вызванным инфекцией COVID-19.
Пациентка С., 37 лет с диагнозом: беременность 21–22 недели, новая короновирусная инфекция крайне тяжёлого течения, внебольничная двусторонняя полисегментарная пневмония, объём поражения лёгких более 90%. Поступила в отделение реанимации и интенсивной терапии Клинического госпиталя “Лапино”. Доставлена бригадой скорой медицинской помощи из другого лечебного учреждения на 16-й день болезни с положительным результатом ПЦР SARS-CoV-2. Находилась на стационарном лечении в течение 12 дней. На предыдущих этапах лечения проводились антибактериальная, антикоагулянтная и симптоматическая терапии. При поступлении состояние пациентки расценено как крайне тяжёлое. Во время транспортировки в госпиталь и в первые 12 часов госпитализации осуществлялась неинвазивная вентиляции лёгких через лицевую маску в режиме CPAP+PS с параметрами ПДКВ 9 mbar, Pподдержки 10 mbar, фракция кислорода во вдыхаемой смеси (FiO2) 90%. Была достигнута сатурация гемоглобина (SpO2) 95%, гемодинамика пациентки оставалась стабильной, остальные системы органов – без дисфункций. При поступлении по данным УЗИ и допплерометрии развитие плода соответствует сроку гестации.
Ввиду стремительного нарастания дыхательной недостаточности (тахипноэ до 40 дыханий в минуту, снижение сатурации до 80%) пациентка была переведена на инвазивную вентиляцию лёгких со следующими начальными параметрами вентиляции: Pупр. 28 mbar, с частотой 18/мин, ПДКВ 11 mbar, FiO2 100%, SpO2 96%. Были начаты продлённые седация пропофолом и дексмедетомидином, миорелаксация. По данным КТ органов грудной клетки объём поражения составлял более 90%. Продолжена антибактериальная терапия препаратами широкого спектра, антикоагулянтная и противовоспалительная терапия, симптоматическое лечение. На вторые сутки у пациентки развилась гемодинамическая нестабильность, что потребовало введения норадреналина в дозировке 0.05 мкг/кг/мин.
В течение первых трёх суток госпитализации имело место прогрессирование гипоксемии при следующих параметрах ИВЛ: Pупр. 29 mbar, дыхательный объём 280 мл, частота 18 дыханий в минуту, ПДКВ 11 mbar, FiO2 100%. Обращало на себя внимание значительное снижение динамической податливости лёгких и дыхательного объёма. Пронирование пациентки не приводило к улучшению оксигенации. Несмотря на проводимую респираторную поддержку и миорелаксацию, продолжалось прогрессирование критической гипоксемии. В экстренном порядке был собран мультидисциплинарный консилиум совместно со специалистами центра ЭКМО ГКБ № 52. Принято решение о начале процедуры вено-венозной ЭКМО. Установлены канюли 26 Fr в правую бедренную вену и 19 Fr в правую внутреннюю ярёмную вену. Стартовые параметры: поток крови 4.5 л/мин, скорость 7300 об/мин, поток свежего газа 7 л/мин, фракция кислорода 100%. Была достигнута SpO2 90%. ИВЛ в режиме BiPAP продолжалась с протективными параметрами: Pупр. 20 cmH2O, дыхательный объём 180 мл, частота 16/мин, ПДКВ 10 mbar, FiO2 70% (рис. 2).
Рис. 2.
КТ ОГК при поступлении пациентки. Субтотальное поражение лёгких, примерный объём выявленных изменений более 75%

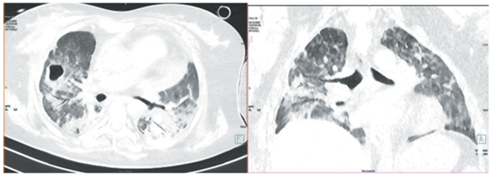
Рис. 3.
КТ ОГК на 29-й день стационарного лечения. На фоне субтотального вирусного поражения лёгких отмечается появление в правом лёгком воздушных полостей. Примерный объём поражения лёгких – более 90%
Учитывая крайне тяжёлое состояние пациентки, после начала ЭКМО принято решение о прерывании беременности оперативным путём. В условиях палаты отделения реанимации произведена нижнесрединная лапаротомия, малое кесарево сечение на сроке 20–21 неделя гестации. За ножку извлечён живой недоношенный плод массой 420 граммов длиной 24 см, оценкой по шкале Апгар 1–3 балла. Ребёнок погиб на 12 сутки жизни в отделении реанимации и интенсивной терапии новорождённых. После оперативного вмешательства пациентке выполнена чрескожно-дилятационная трахеостомия. ЭКМО продолжено со следующими параметрами: поток 4.3 л/мин, скорость 6500 об/мин.
Послеоперационный период протекал гладко. По данным контрольного УЗИ органов малого таза, свободной жидкости не выявлено, полость матки щелевидная. Через шесть часов после операции возобновлена инфузия гепарина до целевых значений АЧТВ 60–70 сек. Утром следующего дня отключена седация, восстановлено ясное сознание. На 11 сутки ЭКМО у пациентки проявились гипофибриногенемия и тромбоцитопения, на фоне чего развились геморрагический и анемический синдромы, что потребовало многочисленных трансфузий компонентов крови (табл. 1). Начиная с 14 суток лечения дальнейшее проведение ЭКМО осуществлялось без введения гепарина.
Таблица 1.
Объём трансфузии
| Компонент | Перелито суммарно, литров |
|---|---|
| Свежезамороженная плазма | 11.84 |
| Тромбоцитарная масса | 4 |
| Криопреципитат замороженный | 1.35 |
| Эритроцитная взвесь, обеднённая лейкоцитами | 9.3 |
| Суммарно | 26.49 |
На 17-е сутки стационарного лечения, несмотря на проводимую терапию, отмечено прогрессирование геморрагического синдрома, проявившегося в развитии носовых кровотечений, кровотечения из трахеостомического отверстия, послеоперационного шва. По данным УЗИ органов брюшной полости свободной жидкости не выявлено. Произведена ревизия операционной раны в пределах подкожно-жировой клетчатки, наложены гемостатические швы. На 15-е сутки развился спонтанный правосторонний пневмоторакс, было произведено дренирование плевральной полости. Лёгкое расправилось, дренаж удалён на 26-е сутки. В связи с нарастанием общего отёчного синдрома с целью контроля волемического статуса в течение семи суток проводилась заместительная почечная терапия в режиме гемодиафильтрации. На протяжении всего периода ИВЛ пациентке регулярно выполнялась санационная фибробронхоскопия, имела место картина геморрагического трахеобронхита. Улучшение эндоскопической картины произошло на 46-е сутки.
На протяжении госпитализации в ОРИТ пациентке проводился микробиологический мониторинг с оценкой антибактериальной резистентности выявляемых микроорганизмов. Коррекция антибактериальной терапии проводилась согласно результатам исследований. В первые 10 суток респираторная поддержка осуществлялась в режиме BiPAP. К 22-м суткам было отмечено максимальное ухудшение эластических свойств лёгочной ткани: дыхательный объём снизился до 20–40 мл, комплайнс до 10 мл/сmH2O. При переводе пациентки на вспомогательный режим вентиляции отмечалось увеличение дыхательного объёма и динамической податливости лёгких. С 20-х суток на фоне проводимой терапии отметилось улучшение эластических свойств лёгочной ткани, восстановление оксигенирующей функции лёгких, что позволило снизить объёмы ЭКМО поддержки. На 42-е сутки лечения в стационаре (58 день болезни) ЭКМО-терапия была прекращена, продолжена ИВЛ в режиме CPAP. Через 5 дней пациентка успешно отлучена от ИВЛ. На 51-й день пациентка переведена в отделение терапии для дальнейшего лечения и наблюдения. После проведения комплекса реабилитационных мероприятий выписана домой в удовлетворительном состоянии без кислородной поддержки.
Первое КТ-исследование после начала ЭКМО-терапии было выполнено на 29-е сутки стационарного лечения (рис. 3). Обращало на себя внимание появление многочисленных межплевральных скоплений воздуха. На последующих исследованиях отмечалось улучшение КТ-картины лёгких без значимого уменьшения объёма воздушных полостей (рис. 4). После выписки из стационара продолжено комплексное восстановительное лечение, дальнейшая активизация пациентки. При выполнении контрольного КТ органов грудной клетки через 30 дней отмечается стойкая положительная динамика, лабораторные анализы в пределах нормативных значений.
Рис. 4.
КТ ОГК на 59-й день стационарного лечения. Умеренная положительная динамика в виде разрешения ретикулярных изменений в правом лёгком, улучшения пневматизации верхушки правого лёгкого. Общий объём изменений >75%. Пневматоцеле правого лёгкого

Следует отметить, что у всех младенцев (151), рождённых от матерей с COVID-19, в Клиническом госпитале “Лапиноˮ не выявлен вирус SARS-CoV-2. Наши наблюдения совпадают с опубликованными результатами зарубежных исследователей. Так, в США по данным исходов более 20 000 родов 95% новорождённых от матерей, инфицированных SARS-CoV-2, родились в удовлетворительном состоянии. У некоторых новорождённых от инфицированных матерей развились лёгкие симптомы, не требующие респираторной поддержки, причём большинство этих случаев были связаны с передачей инфекции через дыхательные пути в послеродовой период [10].
Для своевременного лечения и профилактики осложнений при инфицировании SARS-CoV-2 важна оперативная диагностика Covid-19 и незамедлительное начало терапии: необходимо применение блокаторов рецепторов к ИЛ-6, направленных на снижение цитокинового шторма, эффективно применение моноклональных антител. С целью улучшения экскурсии лёгких, использования терапии, не применяемой во время беременности, необходимо раннее родоразрешение, применение цитостатических препаратов в послеродовом периоде.
Согласно Методическим рекомендациям МЗ РФ “Организация оказания медицинской помощи беременным, роженицам, родильницам и новорождённым при новой коронавирусной инфекции COVID-19ˮ специфическая профилактика показана беременным групп риска тяжёлого течения COVID-19 с 22-х недель гестации, что поможет снизить частоту материнской заболеваемости и смертности в условиях пандемии.
Список литературы
World Health Organization. Director-General’s remarks at the media briefing on 2019-nCoV on 11 February 2020. http://www.who.int/dg/speeches/detail/who-director-general-s-remarks-at-the-media-briefing-on-2019-ncov-on-11-february-2020 (accessed on February 12, 2020).
Azkur A.K. et al. Immune response to SARS-CoV-2 and mechanisms of immunopathological changes in COVID-19. Allergy, 2020.
Пресс-релиз FDA от 26 мая 2021 г. “Coronavirus (COVID-19) Update: FDA Authorizes Additional Monoclonal Antibody for Treatment of COVID-19”. https://www.fda.gov
Strope J.D., PharmD C.H.C. and Figg W.D. TMPRSS2: Potential Biomarker for COVID-19 Outcomes // The Journal of Clinical Pharmacology. 2020. № 60 (17).
Методические рекомендации МЗ РФ “Организация оказания медицинской помощи беременным, роженицам, родильницам и новорождённым при новой коронавирусной инфекции COVID-19” (версия 5 от 28.12.2021). https://static-0.minzdrav. gov.ru/system/attachments/attaches/000/059/052/ original/BMP_preg_5.pdf
https://www.cdc.gov/coronavirus/2019-ncov/variants/ variant-info.html#Consequence
Tay M.Z. et al. The trinity of COVID-19: immunity, inflammation and intervention // Nature reviews. Immunology. 2020. № 20. P. 1–12.
Planas D., Saunders N., Maes P. et al. Considerable escape of SARS-CoV-2 Omicron to antibody neutralization // Nature. 2021. https://www.nature.com/articles/d41586-021-03827-2
https://www.covid19treatmentguidelines.nih.gov/therapies/statement-on-therapies-for-high-risk-nonhospitalized-patients/
COVID-19: Pregnancy issues and antenatal care. https://www.uptodate.com/ Literature review current through: Nov 2021.
National Health Commission of the People’s Republic of China. Diagnosis and Treatment Protocol for COVID-19 (Trial Version 7). http://en.nhc.gov.cn/ 2020-03/29/c_78469.htm [Ref list].
Combes A., Hajage D., Capellier G. et al. Extracorporeal Membrane Oxygenation for Severe Acute Respiratory Distress Syndrome // N. Engl. J. Med. 2018. 378;21.
Xiaochun Ma, Menglin Liang, Min Ding, Weiming Liu, Huibo Ma, Xiaoming Zhou, Hongsheng Ren. Extracorporeal Membrane Oxygenation (ECMO) in Critically Ill Patients with Coronavirus Disease 2019 (COVID-19) Pneumonia and Acute Respiratory Distress Syndrome (ARDS) // Medical Science Monitor: International Medical Journal of Experimental and Clinical Research. August 2020. 26:e925364.
Дополнительные материалы отсутствуют.
Инструменты
Вестник РАН



