Высокомолекулярные соединения (серия А), 2019, T. 61, № 1, стр. 3-10
Влияние состава термо- и pH-чувствительных сополимеров N-(3-(диэтиламино) пропил)-N-метилакриламида и N,N-диэтилакриламида на их поведение в водных растворах
Н. В. Захарова a, *, А. П. Филиппов a, С. Н. Зелинский b, Е. Н. Даниловцева b, В. В. Анненков b
a Институт высокомолекулярных соединений Российской академии наук
199004 Санкт-Петербург, Большой пр., 31, Россия
b Лимнологический институт Сибирского отделения Российской академии наук
664033 Иркутск, ул. Улан-Баторская, 3, Россия
* E-mail: Na_Zar@inbox.ru
Поступила в редакцию 18.04.2018
После доработки 15.08.2018
Принята к публикации 29.08.2018
Аннотация
Методами светорассеяния и турбидиметрии изучены буферные растворы статистических сополимеров N-(3-(диэтиламино)пропил)-N-метилакриламида и N,N-диэтилакриламида, содержащих 7.5 и 5.0 мол. % звеньев N-(3-(диэтиламино)пропил)-N-метилакриламида, имеющих молекулярную массу 3.07 × 104 и 1.45 × 104 соответственно. Сополимеры синтезированы реакцией полиакрилоилхлорида с N,N-диэтил-N′-метил-1,3-пропандиамином и диэтиламином. Исследованы водные растворы в интервале концентраций 0.0003–0.04 г/см3 и pH 7.0–13.0. Определены интенсивности рассеянного света I и оптического пропускания I*. Установлены температуры фазового расслоения. Полученные результаты сопоставлены с данными для исследованного ранее сополимера того же строения, но содержащего 20 мол. % звеньев N-(3-(диэтиламино)пропил)-N-метилакриламида. Показано, что характеристики водных растворов сополимеров зависят от их состава. Увеличение доли N-(3-(диэтиламино)пропил)-N-метилакриламида приводит к образованию агрегатов в растворах сополимеров и повышению температур фазового расслоения.
ВВЕДЕНИЕ
Среди водорастворимых полимеров важное место занимают полимеры N-замещенных акрил- и метакриламидов, которые являются одними из самых распространенных реакционно способных функциональных полимеров. Для многих полимеров данного класса характерна термочувствительность, обусловленная наличием N-замещенной амидной группы в боковой цепи, что обеспечивает возможность регулировать гидрофильно-гидрофобный баланс. Для придания pH-чувствительности в макромолекулы вводят кислотные или основные сомономеры. Термо- и pH-чувствительные сополимеры на основе акрил- и метакриламидов играют существенную роль в развитии фармацевтики (контролируемое выделение лекарственных веществ), биотехнологии (очистка ферментов, биокатализаторы), электронике (датчики, сенсоры), экологии, гидрометаллургии и других областях жизнедеятельности [1–6]. В связи с этим получение новых водорастворимых стимул-чувствительных сополимеров с регулируемой температурой фазовых переходов и изучение их физико-химических свойств является актуальной задачей.
Исследование влияния структуры термо- и pH-чувствительных сополимеров акрил- и метакриламидов на их поведение в водных растворах активно проводятся на протяжении многих лет. Результаты изучения двойной чувствительности (температура и pH) различных сополимеров в значительной степени обобщены в обзоре [7]. В одной из пионерских работ [8] было показано, что наличие N-(2-гидроксипропил)метакриламидных звеньев в термочувствительных сополимерах – это определяющий фактор при формировании надмолекулярных структур вследствие взаимодействия амидной группировки с молекулами воды с образованием мостиковых связей между звеньями различных полимерных цепей. При исследовании структуры и свойств гидрофобно модифицированных полиакриламидов (ПАА) установлена высокая склонность таких сополимеров к внутри- и межмолекулярной агрегации, приводящая даже в разбавленных водных растворах к образованию надмолекулярных структур и зачастую вызывающая макрофазовое расслоение [9]. В значительной степени самоорганизация служит причиной недостаточно полной информации о молекулярных характеристиках таких сополимеров.
В работах [10, 11] синтезированы новые термочувствительные сополимеры винилового эфира этиленгликоля и N-изопропилакриламида (ИПАА). В водных растворах данного сополимера методом турбидиметрии зафиксировано фазовое расслоение, при этом с увеличением содержания звеньев ИПАА в сополимерах температура помутнения Tcp снижается вследствие усиления гидрофобных взаимодействий. Из фазовых диаграмм следует, что для данных систем характерна нижняя критическая температура расслоения, которую можно регулировать в достаточно широких пределах, варьируя состав сополимеров. Для статистических сополимеров ИПАА с N-[3-(диметиламино)пропил]метакриламидом (ДМАПМА) термически обратимые фазовые переходы наблюдались как в кислых, так и в щелочных областях рН среды при различных отношениях компонентов [12]. Зависимость температуры фазового расслоения от рН среды является более сильной для сополимеров, обогащенных сомономером ДМАПМА. Влияние строения компонентов сополимера на характеристики его водных растворов прослеживается также для линейных статистических сополимеров ИПАА с малеиновой и метакриловой кислотам [13, 14].
При исследовании водных растворов сополимеров N,N-диметиламиноэтилметакрилата с N,N-бутилакриламидом, додецилакрилатом, додецилметакрилатом, N-(3-диметиламинопропил метакриламидом) и акриловой кислотой показано, что введение гидрофобных сомономеров (метакриловых эфиров, N-алкилакриламидов и стиролов) приводит к снижению температур фазовых переходов [15]. S.H. Yuk с коллегами [16] исследовал pH- и термочувствительный сополимер N,N-диметиламиноэтилметакрилата с этилакриламидом и установил, что для него температура фазового перехода смещается на 4 градуса по сравнению с гомополимером.
Поли-N-(3-диэтиламино)пропил-N-метил-акриламид (ПДЭАПМАА) получен путем модификации полиакрилоилхлорида (взаимодействие с N,N-диэтил-N′-метил-1,3-пропандиамином) без деструкции его цепи [17]. Изучение водных 0.1 М NaCl растворов ПДЭАПМАА методами микрокалориметрии, потенциометрического титрования, турбидиметрии и светорассеяния показало, что он является термо- и pH-чувствительным, причем температура его фазового расслоения зависит от концентрации и pH. Аналогичным путем при взаимодействии полиакрилоилхлорида с N,N-диэтил-N'-метил-1,3-пропандиамином и диэтиламином синтезирован термо- и pH-чувствительный статистический сополимер (СП-20) ДЭAПМAА и N,N-диэтилакриламида (ДЭAА), содержащий 20 мол. % аминных звеньев [18]. СП-20 исследован методами светорассеяния и турбидиметрии в буферных растворах в широких интервалах pH (от 7 до 13) и концентраций (от 0.0003 до 0.07 г/см3 [18, 19]. Температура и ширина интервала фазового расслоения в растворах СП-20 увеличиваются с ростом кислотности среды и уменьшением концентрации.
Цель настоящей работы – установить влияние состава статистических сополимеров ДЭAПМAА с ДЭAА на характер процессов самоорганизации их макромолекул в водных растворах при вариации температуры, концентрации и кислотности. Для этого исследованы сополимеры ДЭAПМAА и ДЭAА
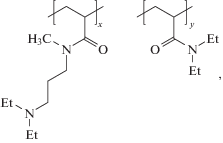
которые отличаются от описанного выше СП-20 меньшим содержанием x звеньев ДЭAПМAА: x = = 7.5 мол. % (сополимер СП-10) и x = 5.0 мол. % (СП-5). Важно отметить, что сополимеры СП-20 и СП-10 получены из одного и того же образца полимера-предшественника, т.е., отличаясь по составу, СП-20 и СП-10 идентичны по степени полимеризации N. Статистический сополимер СП-5 синтезирован из другого образца полиакрилоилхлорида, который имел меньшую степень полимеризации N.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез, структура и молекулярно-массовые характеристики сополимеров СП-10 и СП-5
Сополимер СП-10 получали взаимодействием полиакрилоилхлорида с N,N-диэтил-N′-метил-1,3-пропандиамином и диэтиламином как описано в работах [18–21] при мольном соотношении звеньев полиакрилоилхлорида, N,N-диэтил-N′-метил-1,3-пропандиамина, диэтиламина и триэтиламина 7.2:1:61.6:61.6, что соответствует 10 мол. % N,N-диэтил-N′-метил-1,3-пропандиамина в его смеси с диэтиламином. Синтез СП-5 проводили аналогичным образом при другом соотношении реагентов.
Состав СП-10 и СП-5 характеризовали по данным ЯМР 13С: сигналы метильных групп при 11–15 м.д. и сигнал метиленовой группы в триметиленовом фрагменте при атоме азота аминогруппы в области 48–49 м.д. Спектры ЯМР 13C регистрировали на приборе “DPX 400 Bruker” в CDCl3 при 100 MГц для ядер 13C. Спектр на ядрах 1H не позволяет определить состав сополимера. Содержание звеньев ДЭАПМАА составило 7.5 и 5.0 мол. % для СП-10 и СП-5 соответственно. Это согласуется с данными потенциометрического титрования, которое проводили в водной среде при концентрации сополимера 2.0 г/л в термостатированной ячейке на приборе “Мультитест ИПЛ-113”. В качестве титранта использовали 0.1 моль/л HCl. Перед началом титрования pH растворов доводили до 11 добавлением 0.1 моль/л NaOH.
Значения ММ и гидродинамического радиуса Rh-D макромолекул сополимеров СП-10 и СП-5 измеряли методами статического и динамического рассеяния света в разбавленных растворах в этаноле, а также в щелочных буферах при pH 10.01 и 13.01 при 21.0°С. Светорассеяние изучали на установке “Photocor Complex” (“Photocor Instruments Inc.”, Россия), источником света служил диодный лазер “Photocor-DL” (мощность 5–30 мВт, длина волны λ = 659.1 нм). Калибровку приборa проводили по бензолу (RV = 2.32 × 10–5 см–1). Корреляционную функцию интенсивности рассеянного света получали с помощью коррелятора “Photoсor-PC2” с числом каналов 288 и обрабатывали с помощью программного обеспечения DynalS. Асимметрия светорассеяния в указанных растворах отсутствовала, поэтому Мw сополимеров находили по методу Дебая. Инкременты показателя преломления измеряли на рефрактометре “Refractometer RA-620” (КЕМ, Япония): dn/dc = (0.150 ± 0.003) и (0.175 ± 0.005) см3/г для СП-10 в этаноле и в щелочных буферах соответственно, dn/dc = (0.148 ± 0.005) см3/г для СП-5 в этаноле.
Характеристическую вязкость [η] сополимеров измеряли в буферном растворе (pH 7.01) при 21.0°С в вискозиметре Оствальда с использованием термостата “Optima T100” (“Grant Instruments”, UK). Время истечения растворителя составляло 70.8 c. Значения [η], равные 10 см3/г для СП-10 и 7.2 см3/г для СП-5, определяли с помощью построения Хаггинса. Отметим, что для изученных сополимеров получены относительно высокие величины параметра Хаггинса k′ ∼ 0.9, что характерно для низкомолекулярных линейных полимеров [22, 23].
Изучение буферных растворов СП-5 и СП-10
Процессы самоорганизации в водных растворах СП-5 и СП-10 изучали методами статического и динамического рассеяния света и турбидиметрии на описанной выше установке “Photocor Complex”. Эксперименты проводили в интервале температур 15–68°C. Температуру изменяли дискретно с шагом от 0.3 до 5°C и поддерживали с точностью 0.1°С. Скорость нагревания/охлаждения раствора составляла 1.5 град/мин. Для поддержания устойчивого pH среды использовали готовые буферные растворы с pH 7.01, 10.01 и 13.01 (“Hanna Instruments”, США). Растворы СП-5 и СП-10 изучали в интервале концентраций c = 0.0003–0.01 г/см3. Растворы фильтровали через фильтры Chromafil Xtra PA c диаметром пор 0.45 мкм.
Процедура измерений подробно описана в работах [24, 25]. После установления температуры определяли только зависимости интенсивности рассеянного света I (при угле рассеяния 90°) и оптического пропускания I* от времени t. Когда изменения I составляли менее 1% за время накопления и обработки автокорреляционной функции или I не изменялось вовсе, получали распределение I по гидродинамическим радиусам Rh рассеивающих объектов (рис. 1). Вклад Si каждого типа присутствующих в растворах частиц в суммарную интенсивность светорассеяния оценивали по площади под кривой распределения интенсивности по размерам I(Rh). Эти измерения проводили в интервале углов светорассеяния от 35° до 135°.
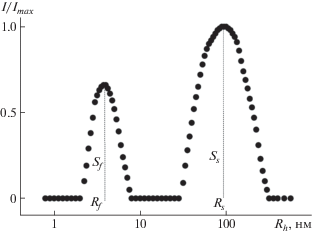
Рис. 1.
Зависимость относительной интенсивности рассеянного света I/Imax от гидродинамического радиуса Rh рассеивающих объектов для буферного раствора СП-10 при с = 0.010 г/см3, рН 13.01 и Т = 21°С. Imax – максимальная интенсивность рассеянного света при данных концентрации, pH и температуре.
Для всех исследованных растворов СП-5 и СП-10 время teq, необходимое для достижения постоянных во времени значений их характеристик, при низких температурах составляло 900–1200 с, а вблизи интервала фазового расслоения иногда превышало 3600 с. Все обсуждаемые ниже результаты получены в условиях “равновесного” состояния системы, т.е. когда характеристики растворов не изменяются во времени.
Отметим, что характеристики исследованных растворов при комнатной температуре (интенсивность светорассеяния, величина оптического пропускания, размеры рассеивающих объектов и их вклад в интегральную величину светорассеяния) не изменялись после многократного длительного (более 1 ч) прогревания растворов при высоких температурах (выше 65°С).
Интенсивность рассеянного света в ходе эксперимента изменялась на несколько порядков. Для сохранения линейности прибора по I фиксируемое светорассеяние ослаблялось диафрагмами и путем уменьшения мощности лазера так, чтобы измеряемая величина I не превышала 1.5 мГц.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
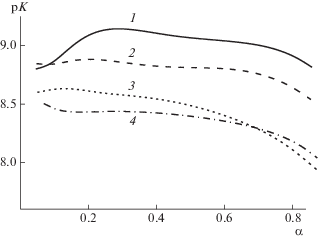
Данные потенциометрического титрования СП-10 (рис. 2) и СП-5 указывают на более слабую зависимость основности аминогрупп от степени их протонирования у этих сополимеров по сравнению с исследованным ранее сополимером СП-20, содержащим 20.4 мол. % звеньев ДЭАПМАА [18]. Данный факт объясним большей изоляцией друг от друга аминных звеньев при уменьшении их содержания в СП-10 и в СП-5, что приводит к уменьшению влияния электростатических эффектов на основность аминогрупп. При увеличении температуры кривые смещаются в область более низких pK, что, как и в случае изученного ранее СП-20, связано с компактизацией макромолекул за счет гидрофобных взаимодействий. При повышении степени ионизации сопряженной кислоты (уменьшении степени протонирования) происходит слабое понижение рK, соответствующее уменьшению основности. Можно предположить, что при этом усиливается компактизация макромолекул за счет уменьшения количества заряженных групп в цепи. При титровании при 10°С отмечается начальный рост рK, характерный для влияния электростатических взаимодействий на кислотно-основные свойства полимеров. По-видимому, при этой температуре в области низких α компактизация макромолекул минимальна, и полимер ведет себя подобно обычным полиэлектролитам.
Рис. 2.
Зависимость рK сопряженной кислоты от степени ионизации α для СП-10 при 10 (1), 20 (2), 30 (3) и 40°С (4).
По данным статического светорассеяния ММ сополимера СП-10 составила Мw = 28.8 × 103 и 32.6 × 103 при измерении в этаноле и в буферном растворе c pH 10.01 соответственно. Среднее значение Мw = 30700 ± 1500 отвечает степени полимеризации N = 200 ± 10. Кроме того, N сополимера можно оценить по значению N для исходного образца полиакрилоилхлорида, из которого получали СП-10 и СП-20. Для этого полиакрилоилхлорид переводили в полиакриловую кислоту путем гидролиза в водной среде [18]. Степень полимеризации полиакриловой кислоты определяли вискозиметрическим методом в диоксане, используя известное соотношение Марка–Куна–Хаувинка [26]. Полученное таким образом значение N = 220 хорошо согласуется с N, измеренной методом светорассеяния.
Для СП-10 методом динамического рассеяния света в этаноле и в буферных растворах зафиксировано унимодальное распределение рассеивающих объектов, гидродинамический радиус Rh-D которых равен (3.6 ± 0.2) нм. Такое значение Rh-D отвечает ММ образца СП-10, т.е. данные частицы являются изолированными молекулами сополимера.
Для образца СП-5 величина Мw = 14500 ± 700 и соответственно N = 103 ± 5. По данным динамического рассеяния света в этаноле гидродинамический радиус Rh-D = (3.6 ± 0.2) нм, что хорошо согласуется с молекулярной массой СП-5. Различие в N для СП-5 и СП-10 связано с тем, что они получены из разных образцов полиакрилоилхлорида.
Поведение СП-10 в буферных растворах при комнатной температуре зависит от концентрации c и pH. При pH < 13.01 при всех концентрациях получено унимодальное распределение частиц по размерам. В указанной области c и pH гидродинамический радиус Rh-f рассеивающих частиц не изменяется при вариации концентрации и кислотности. Среднее значение Rh-f = (3.6 ± 0.3) нм совпадает с величиной Rh-D, определенной в органическом растворителе. Соответственно в данной области c и pH растворы СП-10 при комнатной температуре являются молекулярно дисперсными. Такое поведение отлично от поведения сополимера СП-20 с большим содержанием звеньев ДЭAПМAА. Для последнего в буферных растворах существовало два типа частиц – макромолекулы с радиусом Rh-f и агрегаты, образующиеся вследствие взаимодействия гидрофобных фрагментов цепей разных макромолекул сополимера между собой [18]. Гидродинамические радиусы агрегатов Rh-s более чем на порядок превосходили размеры макромолекул. Для СП-10 подобное поведение наблюдается только при самых высоких значениях c ≥ 0.01 г/см3 и pH 13.01. Для таких растворов СП-10 при комнатной температуре Rh-f = 4 нм совпадает с размером макромолекул, а Rh-s = 100 нм. Агрегаты вносят больший вклад в суммарное светорассеяние: площадь Sf под пиком на кривой распределения I(Rh), соответствующим быстрой моде, в 2.5–5 раз меньше площади Ss под пиком медленной моды (рис. 1). Однако, учитывая тридцатикратную разницу в значениях Rh-f и Rh-s, можно заключить, что в растворе превалируют изолированные макромолекулы СП-10. Оценка доли агрегатов в рамках модели клубков показывает, что концентрация агрегатов составляет не более 0.5 мас. %.
Поведение СП-5 в буферных растворах качественно подобно тому, что наблюдалось для СП-10. При комнатной температуре при c < 0.01 г/см3 и pH < 13.01 растворы молекулярно дисперсны; гидродинамический радиус рассеивающих объектов Rh-f = (3.6 ± 0.4) нм совпадает с размерами макромолекул СП-5, определенными в этаноле. В случае более концентрированных растворов СП-5 и при больших значениях pH зафиксировано образование агрегатов с гидродинамическим радиусом Rh-s = (240 ± 20) нм. Несмотря на то, что агрегаты вносят ощутимый вклад в суммарное светорассеяние (Ss больше Sf в 2 раза), в растворе, также как и в случае СП-10, доминируют индивидуальные макромолекулы, концентрация которых составляет более 99 мас. %.
Отсутствие агрегации макромолекул СП-5 и СП-10 при низких температурах и ее появление при увеличении содержания аминных звеньев (СП-20) может быть связано с проявлением водородных связей с участием частично протонированных аминогрупп. Возможность подобной ассоциации, сочетающейся с гидрофобными взаимодействиями, отмечалась ранее [27].
При нагревании в области умеренных температур при всех концентрациях и pH характеристики растворов СП-5 и СП-10 (интенсивность рассеянного света I, оптическое пропускание I*, гидродинамические радиусы Rh рассеивающих объектов и их вклад Si в интегральную интенсивность светорассеяния) остаются постоянными. Сказанное иллюстрируют данные для СП-10, приведенные на рис. 3 и 4. Поведение растворов кардинально изменяется при температуре Т1, при которой начинаются резкий рост интенсивности I и спад оптического пропускания I*, продолжающиеся до температуры Т2 (рис. 3). Выше Т2 для большинства растворов наблюдается снижение I, которое можно объяснить вторичным рассеянием света, при этом величина I* не изменяется с температурой (при c > 0.0003 г/см3I* = 0, а при более низких концентрациях I* имеет минимальное значение). Температуры T1 и T2 можно рассматривать как температуры начала и завершения интервала фазового расслоения. Для всех растворов температуры T1 и T2, определенные по данным статического светорассеяния и турбидиметрии, различались не более чем на 1°C.
Рис. 3.
Температурные зависимости относительных величин интенсивности рассеянного света I/I0 (1–3) и оптического пропускания I*/I$_{0}^{*}$ (4–6) для буферных растворов СП-10 при с = 0.010 г/см3 и рН 7.01 (1, 2), 10.01 (3, 4), 13.01 (5, 6). I0 и I$_{0}^{*}$ – интенсивность светорассеяния и оптическое пропускание при 21°C соответственно.
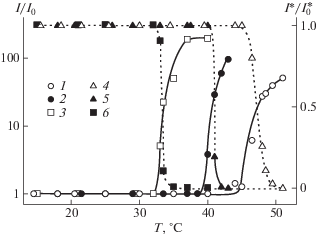
Рис. 4.
Температурная зависимость гидродинамических радиусов Rh-f (1–3) и Rh-s (4–6) для буферных растворов СП-10 при с = 0.010 г/см3 и рН 7.01 (1, 4), 10.01 (2, 5), 13.01 (3, 6).
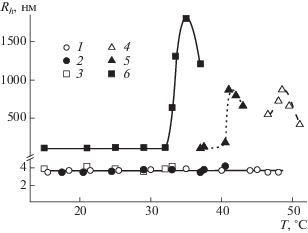
Вид температурных зависимостей I и I* в интервале от T1 до T2 объясняется ухудшением термодинамического качества растворителя, вызванным дегидратацией аминогрупп при повышении температуры. При c < 0.01 г/см3 и pH ≤ 13.01 последнее приводит к образованию агрегатов в растворах за счет объединения макромолекул, и уже вблизи T1 быстрая мода перестает фиксироваться методом динамического светорассеяния. Гидродинамический радиус агрегатов Rh-s увеличивается при нагревании, достигая максимального значения около T2 (рис. 4). В сильно щелочной среде при высоких концентрациях (c ≥ 0.01 г/см3 и pH 13.01) в интервале фазового расслоения происходит рост размеров агрегатов Rh-s и увеличение их вклада Ss в суммарное светорассеяние, а вклад макромолекул Sf резко падает до Sf = 0. Соответственно увеличение размеров агрегатов вызвано как их слиянием, так и присоединением к ним одиночных макромолекул СП-10. Выше T2 величина Rh-s уменьшается, что отражает компактизацию частиц (рис. 4). Поведение СП-5 при нагревании качественно подобно тому, что наблюдается для СП-10: до начала фазового перехода характеристики раствора не изменяются, а в интервале от T1 до T2 быстрая мода исчезает, а агрегаты появляются и увеличиваются в размерах.
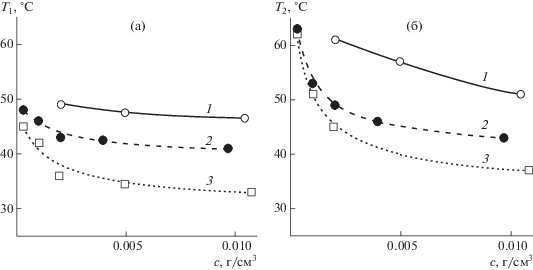
Температуры фазового расслоения T1 и T2 для СП-5 и СП-10 возрастают с уменьшением концентрации, что для СП-10 иллюстрируют данные рис. 5. Это представляется естественным, поскольку все исследованные концентрации лежат в области разбавленных растворов [η] c $ \gg $ 1. Как и можно было ожидать, Т1 и Т2 снижаются с ростом pH, что вызвано изменением степени протонирования аминогрупп при уменьшении кислотности среды. Отметим, что ширина интервала фазового расслоения ΔT = Т1 – Т2 увеличивается при разбавлении раствора и уменьшении pH.
Рис. 5.
Зависимости температур фазового расслоения T1 (а) и T2 (б) от концентрации сополимера для буферных растворов СП-10 при рН 7.01 (1), 10.01 (2) и 13.01 (3).
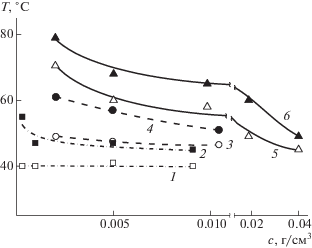
На рис. 6 сопоставляются температуры фазового расслоения для сополимеров СП-5, СП-10 и СП-20 при pH 7.01. Хорошо видно, что уменьшение содержания звеньев ДЭAПМAА приводит к снижению температур T1 и T2, тем большему, чем ниже pH среды. Например, для раствора сополимера СП-10 при с = 0.01 г/см3 и pH 7 значения T1 и T2 равны 46.5 и 51°C соответственно, в то время как для СП-20 при тех же концентрации и pH рассматриваемые температуры повышаются до T1 = = 58°C и T2 = 65°C. Для СП-5 температуры T1 = = 42°C и T2 = 45°C, т.е. еще ниже, чем СП-20 и СП-10. При этом ширина интервала фазового расслоения при заданной концентрации увеличивается при переходе от СП-5 к СП-20 (рис. 6). Такая же картина наблюдается и при других значениях концентрации и pH. Возможно, при начале фазового перехода (Т1) усиливается взаимодействие между боковыми полиаминными цепями, препятствующее электростатически и стерически дальнейшей агрегации, и чем больше в сополимере звеньев ДЭAПМAА, тем большая температура требуется для завершения фазового перехода. Разница между температурами расслоения сополимеров СП-10 и СП-20 уменьшается при увеличении pH, и при pH 13 значения Т2 практически совпадают, что связано с полным депротонированием звеньев ДЭAПМAА и прекращением влияния электростатических факторов на растворимость полимеров. Несколько неожиданным представляется снижение температур фазового расслоения при уменьшении доли ДЭAПМAА, в то время как при комнатной температуре растворы СП-5 молекулярные, а в растворах СП-20 существуют агрегаты. Отметим, что подобное поведение наблюдалось для ряда термо- и pH-чувствительных полимеров [28, 29], для которых, в частности, увеличение гидрофобности макромолекул сопровождалось не снижением, а ростом температур фазового расслоения. Данный факт можно объяснить именно особенностями самоорганизации, когда образование агрегатов или мицелл несколько “стабилизирует” систему. При этом надо учитывать, что формирование надмолекулярных структур при комнатной температуре обусловлено гидрофобностью макромолекул, связанной с соотношением гидрофобных и гидрофильных групп, а агрегатообразование вблизи фазового расслоения – взаимодействиями между утрачивающими при нагревании растворимость стимул-чувствительными фрагментами. В последнем случае на характер процессов может оказывать влияние морфология растворенных объектов.
Рис. 6.
Зависимость температур фазового расслоения T1 (1, 3, 5) и T2 (2, 4, 6) от концентрации сополимеров для буферных растворов СП-5 (1, 2), СП-10 (3, 4) и СП-20 (5, 6) при рН 7.01.
При сопоставлении данных для СП-5, с одной стороны, и для СП-10 и СП-20, с другой, необходимо учесть различие в степенях полимеризации N сравниваемых образцов. Изменение ММ термо- и pH-чувствительных полимеров может привести к изменению характеристик их растворов. Прежде всего это касается температур фазового расслоения, которые обычно снижаются при повышении ММ [30–32]. Среди изученных сополимеров наименьшую степень полимеризации имеет СП-5. Если бы она совпадала с N для СП-10 и СП-20, можно было бы ожидать снижения T1 и T2 для СП-5. Следовательно, различие в температурах фазового расслоения для СП-5 и СП-10, скорее всего, увеличилось бы.
ЗАКЛЮЧЕНИЕ
Анализ полученных результатов показывает, что изменение состава сополимеров N-(3-(диэтиламино)пропил)-N-метилакриламида и N,N-диэтилакриламида сопровождается изменением их поведения в водных растворах.
В буферных растворах сополимера СП-20 с большим содержанием звеньев ДЭAПМAА при комнатной температуре существовало два типа частиц – макромолекулы и агрегаты [12, 13]. Последние образуются в результате взаимодействия гидрофобных фрагментов разных макромолекул и водородных связей с участием аминных звеньев. Уменьшение доли звеньев ДЭAПМAА в статистическом сополимере привело к тому, что растворы СП-10 и СП-5 стали молекулярно дисперсными, за исключением случаев высокой концентрации (c ≥ 0.0107 г/см3) и низкой кислотности среды (pH ≥ 13). Снижение содержания ДЭAПМAА вызывает понижение температур фазового расслоения из-за уменьшения доли протонируемых звеньев, причем температуры T1 и T2 изменяются тем сильнее, чем ниже мольная доля звеньев ДЭAПМAА.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования Российской Федерации (проект АААА-Ф 16-116071450046-9 (Институт высокомолекудярных соединений Российской академии наук, определение молекулярно-массовых и гидродинамических характеристик и исследование термо- и pH-чувствительности) и проект 0345–2016–0001 (Лимнологический институт Сибирского отделения Российской академии наук, синтез полимера и изучение его кислотных свойств)).
Список литературы
Zardad A.Z., Choonara Y.E, du Toit L.C., Kumar P., Mabrouk M., Kondiah P.P.D., Pillay V. // Polymer. 2016. V. 8. № 10. C. 359.
Chen J.K., Chang C.J. // Materials. 2014. V. 7. № 2. P. 805.
Li J.X., Fan X.G., Yang L., Wang F., Zhang J., Wang Z.Y. // Int. J. Polym. Mater. Polym. Biomater. 2018. V. 67. № 6. P. 371.
Ciocoiu O.N., Staikos G., Vasile C. // Carbohydr. Polym. 2018. V. 184. P. 118.
Nagase K., Yamato M., Kanazawa H., Okano T. // Biomaterials. 2018. V. 153. P. 27.
Gong D.Y., Cao T., Han S.C., Zhu X.T., Iqbal A., Liu W.S., Qin W.W., Guo H.C. // Sens. Actuat. B – Chem. 2017. V. 252. P. 577.
Kocak G., Tuncer C., Bütün V. // Polym. Chem. 2017. V. 8. P. 144.
Anufrieva E.V., Krakovyak M.G., Anan’eva T.D., Lushchik V.B., Nekrasova T.N., Papukova K.P., Sheveleva T.V. // Polymer Science A. 2002. V. 44. № 9. P. 975.
Feng Y., Billon L., Grassl B., Khoukh A. // Polymer. 2002. V. 43. № 7. P. 2055.
Лебедева Т.Л., Мальчугова О.И., Валуев Л.И., Платэ Н.А. // Высокомолек. соед. A. 1992. Т. 34. № 9. С. 113.
Нуркеева З.С., Рахматуллаева Р.К., Кажиева А.К. // Наука и техника Казахстана. 2002. № 1. С. 118.
Tuncel A., Demirgoz D., Patir S., Piskin E. // J. Appl. Polym. Sci. 2002. V. 84. № 11. P. 2060.
Tarabukina E.B., Simonova M.A., Bucatari S., Harabagiu V., Fundueanu G., Filippov A.P. // Int. J. Polym. Anal. Charact. 2016. V. 21. № 1. P. 11.
Tarabukina E.B., Seednov E.C., Filippov A.P., Fundueanu G., Harabagiu V. // Macromol. Res. 2017. V. 25. № 7. P. 680.
Kamorin D.M., Shirsin K.V., Kazantsev O.A., Sivokhin A.P. // Polymer Science D. 2015. V. 8. № 2. P. 171.
Yuk S.H., Cho S.H., Lee S.H. // Macromolecules. 1997. V. 30. № 22. P. 6856.
Danilovtseva E.N., Aseyev V., Beloserova O.Yu., Zelinskiy S.N. Annenkov V.V. // J. Colloid Interface Scince. 2015. V. 446. P. 1.
Zakharova N.V., Simonova M.A., Khairullin A.R., Filippov A.P., Danilovtseva E.N., Zelinskii S.N., Annenkov V.V. // Polymer Science A. 2018. V. 60. № 2. P. 127.
Simonova M.A., Zakharova N.V., Khayrullin A.R., Filippov A.P., Annenkov V.V. // Int. J. Polym. Anal. Charact. 2018. V. 23. № 3. P. 236.
Annenkov V.V., Zelinskiy S.N., Danilovtseva E.N., Perry C.C. // ARKIVOC. 2009. P. 116.
Banfi D., Patiny L. // CHIMIA Int. J. Chem. 2008. V. 62. № 4. P. 280.
Будтов В.П. Физическая химия растворов полимеров. М.: Химия, 1992. С. 384.
Будтов В.П., Ицкович Л.А., Кабо В.Я., Масленников В.А., Минеев Л.В. // Высокомолек. соед. А. 1991. Т. 33. № 5. С. 950.
Amirova A.I., Dudkina M.M., Tenkovtsev A.V., Filippov A.P. // Colloid Polym. Sci. 2015. V. 293. № 1. P. 239.
Ivanova A.S., Zakharova N.V., Filippov A.P., Meleshko T.K., Yakimansky A.V. // Polymer Science A. 2017. V. 59. № 3. P. 281.
Newman S., Krigbaum W.R., Laugier C., Flory P.J. // J. Polym. Sci. 1954. V. 14. № 77. P. 451.
Pottier C., Morandi G., Dulong V., Souguir Z., Picton L., Cerf D. Le // J. Polym. Sci., Polym. Chem. 2015. V. 53. P. 2606.
Huber St., Hutter N., Jordan R. // Colloid Polym. Sci. 2008. V. 286. № 14–15. P. 1653.
Han X., Zhang X., Zhu H., Yin Q., Lie H., Hu Y. // Langmuir. 2013. V. 29. P. 1024.
Weber Ch., Hoogenboom R., Schubert U.S. // J. Progr. Polym. Sci. 2012. V. 37. № 5. P. 686.
Kumar A., Srivastava A., Galaev I.Yu., Mattiasson B. // J. Progr. Polym. Sci. 2007. V. 32. № 11. P. 1205.
Kumar A., Srivastava A., Galaev I.Yu., Mattiasson B. // J. Progr. Polym. Sci. 2007. V. 32. № 11. P. 1205.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


