Высокомолекулярные соединения (серия А), 2019, T. 61, № 6, стр. 532-541
ОБ УСЛОВИЯХ ФОРМИРОВАНИЯ ПОЛЫХ ЧАСТИЦ ИНТЕРПОЛИЭЛЕКТРОЛИТНЫМ КОМПЛЕКСОМ
А. А. Глаголева a, *, В. В. Василевская a, **
a Институт элементоорганических соединений им. А.Н. Несмеянова Российской академии наук
Москва, ул. Вавилова, 28, Россия
* E-mail: starostina@polly.phys.msu.ru
** E-mail: vvvas@polly.phys.msu.ru
Поступила в редакцию 29.04.2019
После доработки 04.06.2019
Принята к публикации 20.06.2019
Аннотация
Впервые методом компьютерного эксперимента были исследованы интерполиэлектролитные комплексы, образованные из линейных противоположно заряженных макромолекул с различным сродством к растворителю. Показано, что такие комплексы самоорганизуются в структуры, на поверхности которых преимущественно располагаются сольвофильные группы. Это могут быть плотные сферические частицы, полые везикулоподобные частицы, полые частицы с перфорированной оболочкой. Определены детали строения полученных морфологий.
ВВЕДЕНИЕ
Начатые в 1960–1970 гг. [1–3] исследования интерполиэлектролитных комплексов (ИПЭК) активно продолжаются до настоящего времени, позволяя находить все новые области их практического применения. ИПЭК используются как системы направленной доставки лекарственных средств, для генной трансфекции, при создании новых функциональных материалов, в роли эффективных флокулянтов и модификаторов поверхности [4–7].
Полиэлектролитные комплексы спонтанно формируются при смешении растворов противоположно заряженных полиионов. Движущей силой их создания являются сильные электростатические взаимодействия, а также значительный выигрыш в энтропии, обусловленный высвобождением сконденсированных низкомолекулярных контрионов.
Внутренняя структура и свойства комплекса зависят от длины и топологии входящих в него цепей, соотношения количества положительных и отрицательных зарядов, их распределения по цепи, pH и ионной силы среды [7–16].
Исследования, проведенные методом компьютерного эксперимента [17–20], показали, что формирование комплекса линейных макромолекул с одинаковыми степенями полимеризации и ионизации проходит в две стадии: сначала макроионы сближаются, цепи перепутываются, а затем размеры комплекса резко уменьшаются. Размеры комплекса определяются силой электростатических взаимодействий: чем сильнее электростатическое притяжение, тем меньше размер частицы. При достаточно сильных взаимодействиях возникает плотная сферическая частица, размеры R которой имеют характерную для глобулярных структур скейлинговую зависимость от степени полимеризации N: R ~ N1/3. В случае очень сильных электростатических взаимодействий ИПЭК не только принимает сферическую форму, но и переходит в стеклообразное состояние [19].
Сферическая форма характерна для ИПЭК, образованных гибкими макромолекулами. Макромолекулы в таких комплексах перепутаны, звенья, несущие противоположные заряды, распределены случайным образом. Это так называемая “scrambled-egg” структура [10, 21, 22]. Жесткие цепи образуют лестничную структуру [10, 22], в которой цепи выстраиваются параллельно друг другу, а противоположно заряженные звенья формируют ионные пары. Переход между структурами происходит как фазовый переход первого рода [22].
Сферические частицы ИПЭК, образованные гибкими макромолекулами, незаряженные звенья которых обладают разным сродством к растворителю, имеют сложную структуру [23–29]. Звенья в них перераспределяются таким образом, чтобы на поверхности преимущественно оказались гидрофильные группы одной из цепей, а гидрофобные звенья другой были смещены внутрь частицы. Перераспределение звеньев приводит к возникновению ИПЭК со структурой гидрофобное ядро–гидрофильная оболочка, что способствует расширению области их растворимости [23–30]. Таким образом, комплексы, сформированные из противоположно заряженных цепей с разным сродством к растворителю, обладают уникальным сочетанием свойств, важным для практического применения [4–7]: они электронейтральны, с одной стороны, а с другой (вследствие наличия защитной гидрофильной оболочки) – растворимы.
Цель настоящей работы – исследование деталей строения ИПЭК, состоящего из двух линейных цепей одинаковой длины и степени ионизации, но с различным сродством к растворителю.
МОДЕЛЬ
В соответствии со сформулированной выше задачей мы рассмотрели полиэлектролитный комплекс из двух противоположно заряженных макромолекул одинаковой степени полимеризации (N = 1024) и степени ионизации f (f = 0.5). Заряженные звенья каждой цепи несли единичный (положительный q = 1 или отрицательный q = –1) заряд и взаимодействовали друг с другом посредством сильных кулоновских взаимодействий. Комплекс был помещен в селективный растворитель. Качество растворителя оставалось хорошим для групп первой (для определенности отрицательно заряженной) цепочки, и изменялось от хорошего до плохого для групп другой (положительно заряженной) цепочки.
Временную эволюцию системы описывали посредством решения уравнений движения методом ланжевеновской динамики с использованием программного пакета LAMMPS [31]. Были учтены стерические и наводимые растворителем энергетические взаимодействия между несвязанными по цепи мономерными звеньями, кулоновские взаимодействия заряженных групп, а также наложены ограничения на длину связей.
Стерические ограничения (исключенный объем групп) вводили с помощью смещенного потенциала Леннард-Джонса, содержащего только отталкивательную часть:
(1)
${{E}_{{{\text{LJ}}}}}({{r}_{{ij}}}) = \left\{ {\begin{array}{*{20}{c}} {4{{\varepsilon }_{{{\text{LJ}}}}}\left[ {{{{\left( {\frac{\sigma }{{{{r}_{{ij}}}}}} \right)}}^{{12}}} - {{{\left( {\frac{\sigma }{{{{r}_{{ij}}}}}} \right)}}^{6}} + \frac{1}{4}} \right]} \\ {0,~~~~~~~~~~~~~~~~~~{{r}_{{ij}}} > {{r}_{c}}~} \end{array}} \right.,\quad {{r}_{{ij}}} \leqslant {{r}_{c}}$Здесь rij – расстояние между i-м и j-м звеньями, ${{r}_{c}} = \sqrt[{1/6}]{2}\sigma $ – радиус обрезки потенциала (радиус частиц). Параметр εLJ задает энергетическую шкалу, параметр σ – пространственные масштабы. Их численное значение положили равным ${{\varepsilon }_{{{\text{LJ}}}}}$ = = σ = 1, все результаты расчетов представлены в терминах этих величин.
Электростатические взаимодействия между заряженными звеньями были представлены кулоновским потенциалом:
(2)
${{E}_{{El}}}({{r}_{{ij}}}) = {{k}_{{\text{B}}}}T{{l}_{{\text{B}}}}\frac{{{{q}_{i}}{{q}_{j}}}}{{{{r}_{{ij}}}}},$Изменение качества растворителя для звеньев положительно заряженной цепи моделировали посредством введения взаимодействий притяжения между ними и описывали с помощью потенциала типа Юкавы:
(3)
${{E}_{{\text{Y}}}}\left( {{{r}_{{ij}}}} \right) = \left\{ {\begin{array}{*{20}{l}} {\frac{{\varepsilon \sigma }}{{{{r}_{{ij}}}}}{{{\left( {1 - {{{\left( {\frac{{{{r}_{{ij}}}}}{{{{r}_{{c{\text{Y}}}}}}}} \right)}}^{2}}} \right)}}^{2}},}&{{{r}_{{ij}}} \leqslant {{r}_{{c{\text{Y}}}}}} \\ {0,}&{{{r}_{{ij}}} > {{r}_{{c{\text{Y}}}}}} \end{array}} \right.~~$Здесь ${{r}_{{c{\text{Y}}}}} = 4\sigma $ – радиус обрезки потенциала, ε – энергетический параметр парных взаимодействий мономерных звеньев. При ε = 0 взаимодействие между звеньями сводится к стерическому (1), и растворитель является атермическим. Отрицательные значения ε отвечают притяжению между группами, соответственно чем больше |ε|, тем хуже качество растворителя. Отметим, что введение потенциалов взаимодействий между частицами как метод неявного учета растворителя является общепринятым в компьютерных экспериментах [33, 34].
Влияние противоионов не было учтено явным образом, поскольку полагали, что они высвобождаются в раствор при образовании комплекса [18–20] и находятся на значительном расстоянии от него.
Наконец, между соседними по цепи мономерными звеньями действовал потенциал ${{E}_{{bond}}}$, ограничивающий длину связи b:
где $K = 10000$ – постоянная, численное значение которой позволяет длине связи (b = 1) изменяться не более чем на 1%.Уравнения движения были дополнены слагаемым ланжевеновского нескоррелированного шума и силой трения, что позволило поддерживать постоянную температуру T методом термостатирования Ланжевена.
Полимерные цепи помещали в кубическую ячейку моделирования с длиной ребра L = 1200 и периодическими граничными условиями. При ε = 0 проводили уравновешивание в течение 107 шагов по времени. Затем значение параметра ε изменяли до ${\varepsilon } = - 3.0$ с шагом $\Delta {\varepsilon } = - 0.1$, проводя уравновешивание в течение 2 × 106 и вычисления в течение 2 × 106 шагов по времени на каждом этапе. Состояние комплекса характеризовали посредством расчета среднеквадратического радиуса инерции ${{R}_{g}} = \sqrt {\frac{1}{{2N}}\sum\nolimits_{i = 1}^{2N} {{{{({{{\mathbf{r}}}_{i}} - {{{\mathbf{r}}}_{0}})}}^{2}}} } $ (r0 – радиус-вектор центра масс), факторов формы, приведенной теплоемкости, пространственного распределения групп, а также доли звеньев, участвующих в образовании ионных пар. Форму комплекса оценивали, вычисляя отношение Rg к гидродинамическому радиусу ${{R}_{h}} = {{\left( {\frac{1}{{4{{N}^{2}}}}\sum\nolimits_{i \ne j} {\frac{1}{{{{r}_{{ij}}}}}} } \right)}^{{ - 1}}}$, а также соотношения k1 и k2 главных моментов тензора среднеквадратичного радиуса инерции ($R_{{g1}}^{2}$ ≤ ≤ $R_{{g2}}^{2} \leqslant R_{{g3}}^{2}$): ${{k}_{1}} = \frac{{R_{{g1}}^{2} + R_{{g2}}^{2}}}{{R_{{g2}}^{2} + R_{{g3}}^{2}}}$, ${{k}_{2}} = \frac{{R_{{g1}}^{2} + R_{{g3}}^{2}}}{{R_{{g2}}^{2} + R_{{g3}}^{2}}}$. Для полимерного клубка Rg/Rh ≈ 1.5–1.8, для сплошной сферы Rg/Rh ≈ 0.77, для тонкого сферического слоя Rg/Rh ≈ 1.0 [35, 36]. Значения k1 и k2 для идеальной сферы ${{k}_{1}} \to 1$, ${{k}_{2}} \to 1$, бесконечно длинного цилиндра ${{k}_{1}} \to 0$, ${{k}_{2}} \to 1$, бесконечно тонкого диска ${{k}_{1}} \to 0.5$, ${{k}_{2}} \to 0.5$ [34]. Приведенную теплоемкость CV рассчитывали как дисперсию потенциальной энергии системы, деленную на полное число звеньев. Пространственное распределение групп находили путем расчета их локальной концентрации ρ – числа групп данного типа в слое толщиной Δr = 1, находящемся на расстоянии r от центра масс комплекса, деленного на объем слоя. Считали, что противоположно заряженные звенья образуют ионную пару, если расстояние между ними не превосходит критического значения rbond = 1.5.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рис. 1 приведены мгновенные снимки комплексов при изменении качества растворителя ε.
Рис. 1.
Мгновенные снимки ИПЭК при ε = 0 (а), –0.8 (б), –1.2 (в), –1.6 (г), –2.0 (д), –2.3 (е) и –3.0 (ж). Заряженные и незаряженные звенья полианиона, для которого качество растворителя остается неизменно хорошим, показаны темно-синим и светло-синим цветом соответственно. Темно-красным и светло-красным цветом обозначены, соответственно, заряженные и незаряженные звенья цепи поликатиона, селективно взаимодействующей с растворителем. Мгновенные снимки комплексов изображены целиком (верхняя строка) и в сечении плоскостью, проходящей через центр масс комплекса (нижняя строка). Цветные рисунки можно посмотреть в электронной версии.

Видно, что при ε = 0 (рис. 1а) комплекс представляет собой довольно рыхлую частицу сферической формы, в которой противоположно заряженные цепи перепутаны в так называемую структуру “scrambled-egg” (“яичница-болтунья”) [10]. По мере роста |ε| размеры ИПЭК уменьшаются, плотность полимера внутри него увеличивается. При ${\varepsilon } = - 0.8$ (рис. 1б) ИПЭК представляет собой плотную сферическую частицу с круглым сечением и визуально гомогенно перепутанными звеньями.
Дальнейшее ухудшение качества растворителя (усиление притяжения между группами положительно заряженной, окрашенной в красные тона, цепи) приводит к переходу от структуры “scrambled-egg” с гомогенно и хаотично перемешанными звеньями к структурам, где звенья различных цепей сегрегированы. Это везикула, сферическая частица с тонкой бислойной практически сплошной оболочкой, стабильная в диапазоне $ - 1.6 \leqslant {\varepsilon }$ ≤ ≤ –1.3 (рис. 1г), полая частица с перфорированной оболочкой ($ - 2.3 \leqslant {\varepsilon } \leqslant - 1.7$, рис. 1д, 1е) и плотная структурированная частица ($ - 3.0 \leqslant {\varepsilon }$ ≤ ≤ –2.4, рис. 1ж).
Изменения размеров и структуры комплекса по мере ухудшения качества растворителя были охарактеризованы количественно. На рис. 2 приведена зависимость радиуса инерции Rg, нормированного на радиус инерции ${{R}_{g}}\left( 0 \right)$ комплекса в хорошем растворителе (ε = 0), от качества растворителя ε. Видно, что по мере ухудшения качества растворителя размеры комплекса монотонно уменьшаются. В очень плохом растворителе (${\varepsilon }$ = = –3.0) радиус инерции комплекса оказывается более чем в полтора раза меньше размеров комплекса в хорошем растворителе. Небольшой пик в окрестности ${\varepsilon \;}\sim - 2.2$ наблюдается при разрушении перфорированной полой частицы.
Рис. 2.
Зависимость радиуса инерции Rg (а), факторов формы k1 (темные точки), k2 (светлые) (б) и фактора формы Rg/Rh (в) комплекса от качества растворителя.
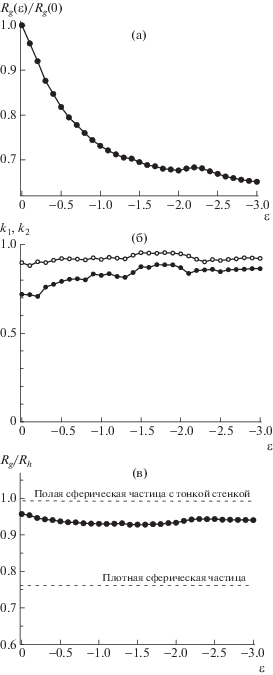
Расчетные величины, характеризующие форму ИПЭК, параметры формы (рис. 2б), отношение радиуса инерции к гидродинамическому радиусу (рис. 2в), оказались мало чувствительными к изменению структуры комплекса. Значения факторов формы k1 и k2 (рис. 2б) при всех ε характерны для структур, имеющих форму, близкую к сферической: ${{k}_{1}} > 0.7$, ${{k}_{2}} > 0.85$. Приведенные значения минимальны при ε = 0 и постепенно увеличиваются при ухудшении качества растворителя, достигая максимума (${{k}_{1}} = 0.88$, ${{k}_{2}} = 0.95$) в области $ - 1.9 \leqslant {\varepsilon } \leqslant - 1.5$, где комплекс имеет вид полой капсулы и его форма наиболее близка к идеальной сфере. При деформации капсулы значения k1 и k2 несколько снижаются (${{k}_{1}} = 0.86$, ${{k}_{2}}$ = = 0.92).
Отношение радиуса инерции к гидродинамическому радиусу ${{R}_{g}}{\text{/}}{{R}_{h}}$ представлено на рис. 2в. Для наглядности линиями показаны значения для плотной сферической частицы и полой частицы с предельно тонкой оболочкой. Видно, что в рассматриваемом случае ${{R}_{g}}{\text{/}}{{R}_{h}}$ флуктуирует в весьма узкой области: ${{R}_{g}}{\text{/}}{{R}_{h}}\sim ~~0.95$. Это значительно больше, чем соответствующее отношение ${{R}_{g}}{\text{/}}{{R}_{h}}$ ~ 0.77 для плотной частицы. Иными словами, по-видимому, комплекс довольно рыхлый даже в случаях его визуальной плотности. Кроме того, отношение ${{R}_{g}}{\text{/}}{{R}_{h}}$ меньше единицы в тех областях параметра ε, где комплекс имеет полую структуру. Такие отличия, на наш взгляд, обусловлены значительной по сравнению с размером полости толщиной оболочки.
На рис. 3 представлены локальные концентрации заряженных и электронейтральных звеньев как функции r расстояния от центра инерции. На рис. 3а видно, что в отсутствие специфических взаимодействий, наведенных растворителем (ε = 0), звенья всех типов распределены равномерно, их профили локальной концентрации совпадают. Локальная концентрация остается неизменной (ρ ≈ 0.075) во внутренней части комплекса, при r ≤ 9, и плавно снижается до нуля при 9 ≤ r ≤ 15. Такой профиль локальной концентрации характерен для полимерной глобулы [17].
Рис. 3.
Пространственное распределение незаряженных (1, 2) и заряженных (3, 4) групп поликатиона (1, 3) и полианиона (2, 4). ε = 0 (а), $ - 0.8$ (б), $ - 1.2$ (в), $ - 1.6$ (г), $ - 2.0$ (д) и $ - 3.0$ (е). Области с преобладанием заряженных звеньев заштрихованы. В электронной версии для более ясного представления кривые покрашены в те же цвета, что и соответствующие звенья на мгновенных снимках (рис. 1).
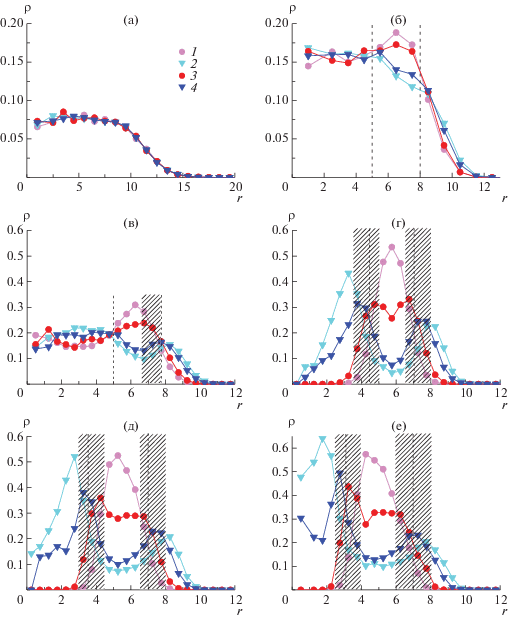
При ${\varepsilon } = - 0.8$ (рис. 3б) только в центральной части комплекса (r ≤ 5) локальные концентрации разных (заряженных и нейтральных, принадлежащих цепи полианиона и поликатиона) звеньев равны (ρ ≈ 0.15). В области 5 < r < 8 преобладают звенья поликатиона, а на периферии (8 ≤ r ≤ 11), напротив, выше концентрация звеньев полианиона. Границы областей, образованных преимущественно звеньями разных цепей, показаны на рис. 3 вертикальными линиями. Таким образом, комплекс имеет слоистую структуру. Это плотная центральная часть с перепутанными хаотично цепями, затем слой, в котором преобладают звенья поликатиона, плохо взаимодействующего с растворителем. Суммарная локальная концентрация звеньев в данном, примыкающем к центральной части, слое равна суммарной локальной концентрации звеньев во внутренней части. И наконец, опушка, в которой концентрация звеньев монотонно падает, и которая обогащена звеньями полианиона, имеющего сродство с растворителем.
Дальнейшее ухудшение качества растворителя (рис. 3в, ${\varepsilon } = - 1.2$) приводит не только к уменьшению размеров ИПЭК и росту суммарной локальной плотности звеньев в нем, но и к тому, что практически исчезает область, где звенья разных полиионов содержатся в равных количествах. Теперь в большей части центральной области комплекса (1.5 < r < 5), как и во внешней опушке, преобладают звенья полианиона. Также по сравнению с ${\varepsilon } = - 0.8$ в примыкающем к центральной части слое (5 < r < 8) выросло относительное содержание групп поликатиона, упало относительное содержание групп полианиона, т.е. заметно изменилась разница их локальных концентраций. Заметно выросла разность локальных концентраций групп макроионов также и во внешней опушке.
Профили локальных концентраций для полой частицы со сплошной оболочкой (ε = –1.6) представлены на рис. 3г. Видно, что в центральной части такой частицы полностью отсутствуют звенья поликатиона, а концентрация звеньев полианиона монотонно растет от весьма малых, практически нулевых, значений при r ~ 1 до ρ ~ 0.5 при r ~ 3–4. Отметим, что в указанной области концентрация неионогенных групп (кривая 2) всегда превышает концентрацию заряженных звеньев (кривая 4) этой же цепи. Затем следует область, в которой напротив, концентрация отрицательно заряженных групп выше концентрации групп нейтральных (кривые 4 и 2 меняют расположение относительно друг друга). Данная область сменяется областью с приблизительно одинаковым содержанием противоположно заряженных групп полиионов комплекса (кривые 3 и 4) и незначительным содержанием незаряженных (кривые 1 и 2) звеньев обеих цепей. Потом следует узкий слой, в котором наибольшее значение имеет концентрация положительно заряженных звеньев; затем широкий слой, где наибольшая концентрация у незаряженных групп поликатиона (кривая 1), несколько меньше концентрация положительно заряженных групп поликатиона и существенно более низкие концентрации звеньев заряженных и нейтральных звеньев полианиона и т.д. Таким образом, оболочка частицы имеет сложное слоистое строение. Ее каркас (сердцевину) составляют гидрофобные группы (кривая 1 имеет один ярко выраженный максимум) поликатиона. Заряженные группы поликатиона из сердцевины вытеснены в соседние слои, в которых они непосредственно контактируют с противоположно заряженными группами полианиона. На поверхности оболочки, внутренней и внешней поверхностях везикулы, размещены незаряженные, гидрофильные звенья полианиона. Схематическое изображение полой везикулоподобной структуры дано на рис. 4.
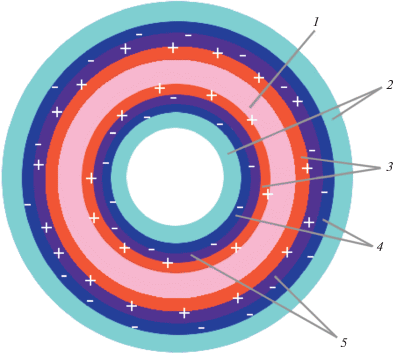
Рис. 4.
Схематическое представление полой везикулоподобной структуры ИПЭК ($ - 1.6 \leqslant \varepsilon \leqslant - 1.3$). Тип звеньев, имеющий наибольшую локальную концентрацию в данном слое: 1 – гидрофобные незаряженные группы поликатиона; 2 – гидрофильные незаряженные группы полианиона; 3 – положительно заряженные звенья гидрофобной цепи, 4 – отрицательно заряженные звенья гидрофильной цепи; 5 – область с приблизительно равными локальными концентрациями положительно и отрицательно заряженных групп.
Слоистое распределение звеньев характерно и для полых капсул с перфорированной оболочкой, а также плотных структурированных частиц (рис. 3д, 3е). В этих морфологиях также гидрофобные группы спрятаны, гидрофильные находятся на периферии, а между ними располагается скрепляющий слой из формирующих ионные пары противоположно заряженных мономерных звеньев обеих молекул.
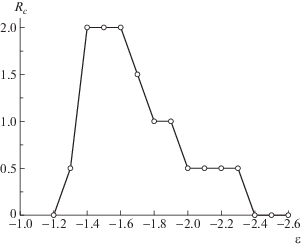
Зависимость размера полости внутри полых морфологий от качества растворителя показана на рис. 5. Наибольший радиус полости (Rc = 2) соответствует области везикулоподобных структур. При деформации оболочки капсулы и появлении отверстий в слое из гидрофобных групп (рис. 1д) размер полости постепенно уменьшается. Затем слой гидрофобных групп изменяется так, что отверстия в нем становятся больше, их количество уменьшается (рис. 1е), размер полости становится минимальным (Rc = 0.5). Наконец, при ${\varepsilon }$ = –2.4 полость исчезает.
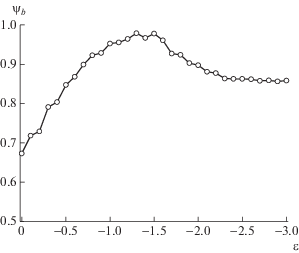
На рис. 6 представлена зависимость доли ψb заряженных звеньев, входящих в ионные пары с противоположно заряженными группами, от качества растворителя ${\varepsilon }$. Видно, что ψb является немонотонной функцией качества растворителя. Его минимальное значение, впрочем довольно высокое (ψb = 0.67), наблюдается при ε = 0, максимальное (ψb ~ 0.96–0.98) –при $ - 1.6 \leqslant {\varepsilon } \leqslant - 1.3$. В области $ - 1.3 < {\varepsilon } < 0$ параметр ψb монотонно растет, а при ${\varepsilon } < - 1.6$ падает и выходит на плато ψb ~0.86 при ${\varepsilon }\sim - 2.3$. Таким образом, максимальное число ионных пар формируется, что естественно, в области везикулоподобных структур. В процессе деформации оболочки везикулы часть заряженных групп переходит в объем, ранее занимаемый полостью, ψb убывает и выходит на постоянное значение при исчезновении полости внутри комплекса.
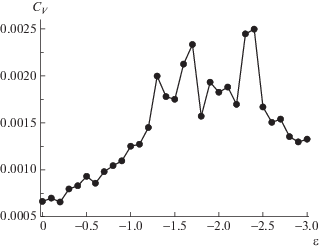
Зависимость приведенной теплоемкости CV от ε представлена на рис. 7. Значение CV с ухудшением качества растворителя плавно растет, затем флуктуирует в широкой области ε ($ - 2.4 \leqslant {\varepsilon }$ ≤ –1.3), в которой нет возможности выделить отдельные четкие максимумы, после чего уменьшается. Флуктуации при высоких значениях CV наблюдаются в диапазоне качества растворителя, где ИПЭК имеет полую структуру и соответствуют процессу перераспределения групп в комплексе. Значение CV начинает снижаться при формировании комплексом плотной структурированной частицы.
ЗАКЛЮЧЕНИЕ
Исследовано внутреннее строение полиэлектролитного комплекса из двух противоположно заряженных гибких полимерных цепей одинаковой длины, одинаковой степени ионизации f = 0.5 в растворителе, селективно взаимодействующем с группами одной из цепей (поликатионом) и неизменно хорошем для групп полианиона. Было показано, что в хорошем растворителе комплекс имеет сферическую форму и структуру “scrambled-egg”, где цепи гомогенно перепутаны. При ухудшении качества растворителя размеры комплекса уменьшаются, звенья перераспределяются, формируется структура с чередующимися слоями из звеньев поликатиона и полианиона, на границе которых преобладают заряженные группы. Другой особенностью комплекса является наличие внешней гидрофильной оболочки, описанной нами ранее в работах [34, 37]. Были выделены три характерных типа морфологий комплекса в плохом растворителе: относительно рыхлая частица с гидрофильной оболочкой, полая частица и плотная структурированная частица. Было показано, что полая “везикулоподобная” частица (толщина оболочки ~4σ сравнима с размером звена) наблюдается в весьма узкой области. Причиной формирования везикулы можно назвать эффективную амфифильность ИПЭК, в котором вследствие сильных электростатических взаимодействий оказываются связаны макромолекулы, отличающиеся сродством к растворителю. Это делает их похожими на амфифильные гомополимеры [38] или макромолекулы, амфифильные на уровне отдельного звена [34], которые также способны формировать полые частицы, в том числе с тонкой бислойной оболочкой [39–42], а также ряд других довольно сложных морфологических структур [37, 43]. Амфифильные гомополимеры обладают сравнимой с ПАВ способностью к самоорганизации, при этом формируемые ими структуры более стабильны и образуются при значительно более низких концентрациях. Такие свойства обусловливают их практическую применимость и вызывают огромный интерес к исследованию амфифильных гомополимеров, созданию новых амфифильных звеньев, поиску новых методов внедрения амфифильности в звено [42]. В этой связи ИПЭК из макромолекул с различным сродством к растворителю можно рассматривать как одну из возможностей реализаций такого рода задач и как новый перспективный тип самоорганизующихся амфифильных систем.
Работа выполнена при финансовой поддержке Российского научного фонда (проект 18-73-00335). В.В. Василевская выражает благодарность Министерству науки и высшего образования Российской Федерации.
Работа выполнена с использованием оборудования Центра коллективного пользования сверхвысокопроизводительными вычислительными ресурсами МГУ им. М.В. Ломоносова [44].
Список литературы
Michaels A.S., Miekka R.G. // J. Phys. Chem. 1961. V. 65. № 10. P. 1765.
Зезин А.Б., Рогачёва В.Б., Комаров В.С., Разводовский Е.Ф. // Высокомолек. соед. А. 1975. Т. 17. № 12. С. 2637.
Изумрудов В.А., Зезин А.Б. // Высокомолек. соед. А. 1976. Т. 18. № 11. С. 2488.
Kabanov A.V., Kabanov V.A. // Bioconjugate Chem. 1995. V. 6. № 1. P. 7.
Pergushov D.V., Zezin A.A., Zezin A.B., Müller A.H.E. // Adv. Polym. Sci. 2014. V. 255. P. 173.
Xie S.-X., Baoum A.A., Alhakamy N.A., Berkland C.J. // Int. J. Pharm. 2018. V. 547. № 1–2. P. 274.
Petzold G., Schwarz S. // Adv. Polym. Sci. 2014. V. 256. P. 25.
Izumrudov V.A., Zezin A.B., Kabanov V.A. // Russ. Chem. Rev. 1991. V. 60. № 7. P. 792.
Tsuchida E. // J. Macromol. Sci. A. 1994. V. 31. № 1. P. 1.
Thunemann A.F., Muller M., Dautzenberg H., Joanny J.F., Lowne H. // Adv. Polym. Sci. 2004. V. 166. P. 113.
Pergushov D.V., Izumrudov V.A., Zezin A.B., Kabanov V.A. // Polymer Science. 1995. V. 37. № 10. P. 1739.
Kabanov V.A., Sergeyev V.G., Pyshkina O.A., Zinchenko A.A., Zezin A.B., Joosten J.G.H., Brackman J., Yoshikawa K. // Macromolecules. 2000. V. 33. № 26. P. 9587.
Spruijt E., Leermakers F.A.M., Fokkink R., Schweins R., van Well A.A., Cohen Stuart M.A., van der Gucht J. // Macromolecules. 2013. V. 46. № 11. P. 4596.
Priftis D., Xia X., Margossian K.O., Perry S.L., Leon L., Qin J., de Pablo J.J., Tirrell M.V. // Macromolecules. 2014. V. 47. № 9. P. 3076.
Dähling C., Lotze G., Drechsler M., Mori H., Pergushov D.V., Plamper F.A. // Soft Matter. 2016. V. 12. P. 5127.
Nekrasova T.N., Pautov V.D., Anan’eva T.D., Meleshko T.K., Ivanov I.V., Yakimansky A.V. // Polymer Science C. 2018. V. 60. Suppl. 1. P. S172.
Srivastava D., Muthukumar M. // Macromolecules. 1994. V. 27. № 6. P. 1461.
Winkler R.G., Steinhauser M.O., Reineker P. // Phys. Rev. E. № 2. 2002. V. 66. 021802.
Winkler R.G. // New J. Phys. 2004. V. 6. № 1. P. 1.
Ou Z., Muthukumar M. // J. Chem. Phys. 2006. V. 124. № 15. 154902.
Kriz J., Dautzenberg H., Dybal J., Kurkova D. // Langmuir. 2002. V. 18. № 24. P. 9594.
Lazutin A.A., Semenov A.N., Vasilevskaya V.V. // Macromol. Theor. Simul. 2012. V. 21. № 5. P. 328.
Vasilevskaya V.V., Leclercq L., Boustta M., Vert M., Khokhlov A.R. // Macromolecules. 2007. V. 40. № 16. P. 5934.
Krotova M.K., Vasilevskaya V.V., Leclercq L., Boustta M., Vert M., Khokhlov A.R. // Macromolecules. 2009. V. 42. № 19. P. 7495.
Etrych T., Leclercq L., Boustta M., Vert M. // Eur. J. Pharm. Sci. 2005. V. 25. № 2–3. P. 281.
Boustta M., Leclercq L., Vert M., Vasilevskaya V. // Macromolecules. 2014. V. 47. № 11. P. 3574.
Machinskaya A.E., Leclercq L., Boustta M., Vert M., Vasilevskaya V.V. // J. Polym. Sci., Polym. Phys. 2016. V. 54. № 17. P. 1717.
Filippov S.K., Koňák C., Kopečková P., Starovoytova L., Špírková M., Štěpánek P. // Langmuir. 2010. V. 26. № 7. P. 4999.
Baulin V.A., Trizac E. // Soft Matter. 2012. V. 8. 6755.
Antonov Y.A., Moldenaers P., Cardinaels R. // Food Hydrocolloids. 2017. V. 62. P. 102.
Plimpton S. // J. Comp. Phys. 1995. V. 117. № 1. P. 1.
Pollock E.L., Glosli J. // Comput. Phys. Commun. 1996. V. 95. № 2–3. P. 93.
Allen M.P., Tildesley D.J. Computer Simulation of Liquids. Oxford: Clarendon Press, 1990.
Vasilevskaya V.V., Khalatur P.G., Khokhlov A.R. // Macromolecules. 2003. V. 35. № 26. P. 10103.
Burchard W. // Adv. Polym. Sci. 1983. V. 48. P. 1.
Egelhaaf S.U., Schurtenberger P. // J. Phys. Chem. 1994. V. 98. № 34. P. 8560.
Vasilevskaya V.V., Klochkov A.A., Lazutin A.A., Khalatur P.G., Khokhlov A.R. // Macromolecules. 2004. V. 37. № 14. P. 5444.
Kale T.S., Klaikherd A., Popere B., Thayumanavan S. // Langmuir. 2009. V. 25. № 17. P. 9660.
Glagoleva A.A., Vasilevskaya V.V., Khokhlov A.R. // Macromol. Theory Simul. 2015. V. 24. № 4. P. 393.
Glagoleva A.A., Vasilevskaya V.V. // Polymer Science A. 2016. V. 58. № 2. P. 292.
Larin D.E., Glagoleva A.A., Govorun E.N., Vasilevskaya V.V. // Polymer. 2018. V. 146. P. 230.
Vasilevskaya V.V., Govorun E.N. // Polym. Rev. 2019. V. 59. https://doi.org/10.1080/15583724.2019.1599013
Vasilevskaya V.V., Ermilov V.A. // Polymer Science A. 2011. V. 53. № 9. P. 846.
Sadovnichy V., Tikhonravov A., Voevodin Vl., Opanasenko V. // Contemporary High Performance Computing: From Petascale toward Exascale. Boca Raton: CRC Press, 2013. P. 283.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)