Высокомолекулярные соединения (серия А), 2019, T. 61, № 6, стр. 515-523
ВЯЗКОУПРУГИЕ РАСТВОРЫ ЧЕРВЕОБРАЗНЫХ МИЦЕЛЛ КАТИОННОГО ПОВЕРХНОСТНО-АКТИВНОГО ВЕЩЕСТВА И ЖЕСТКОЦЕПНОГО АНИОННОГО ПОЛИЭЛЕКТРОЛИТА
А. В. Шибаев a, Д. Ю. Митюк a, Д. А. Муравлев a, О. Е. Филиппова a, *
a Московский государственный университет имени М.В. Ломоносова. Физический факультет
119991 Москва, Ленинские горы, Россия
* E-mail: phil@polly.phys.msu.ru
Поступила в редакцию 04.05.2019
После доработки 25.06.2019
Принята к публикации 09.07.2019
Аннотация
Исследовано фазовое поведение и реологические свойства смесей червеобразных мицелл катионного поверхностно-активного вещества эруцил-бис-(гидроксиэтил)метиламмоний хлорида и противоположно заряженного жесткоцепного полиэлектролита ксантана. Показано, что в присутствии избытка низкомолекулярной соли, подавляющей комплексообразование между поверхностно-активным веществом и полимером, смешение позволяет добиться синергетического повышения модуля упругости системы, что может быть обусловлено образованием зацеплений между полимерными цепями и червеобразными мицеллами.
ВВЕДЕНИЕ
Комплексы полиэлектролитов с противоположно заряженными ПАВ широко исследуются последние пятьдесят лет [1–17]. Пионерские работы в этой области, опубликованные в 1972–1974 гг., принадлежат А.Б. Зезину и М.М. Фельдштейну [1, 2].
В первое время основные исследования были сконцентрированы на взаимодействии полимеров с разбавленными растворами ПАВ. Показано, что связывание ПАВ с противоположно заряженным полимером за счет электростатических взаимодействий приводит к высвобождению во внешний раствор большого числа противоионов как полиэлектролита, так и самого ПАВ, что дает преимущество в трансляционной энтропии системы. Локальное концентрирование ионов ПАВ в результате связывания с полимерной цепью способствует образованию мицелл, вызванному гидрофобными взаимодействиями между алкильными хвостами ПАВ. Критическая концентрация агрегации ПАВ вблизи полимера обычно значительно (на один-два порядка) ниже критической концентрации мицеллообразования того же ПАВ в водном растворе. Это обусловлено тем, что формирование мицелл ионогенного ПАВ в растворе вызывает частичную иммобилизацию противоионов вблизи сильно заряженной поверхности мицеллярных агрегатов, что невыгодно с точки зрения энтропии. В то же время, в присутствии противоположно заряженного полиэлектролита заряд мицелл нейтрализуется заряженными группами полимерной цепи, которые уже изначально иммобилизованы, поскольку встроены в макромолекулу и не обладают трансляционной энтропией. Следовательно, в этом случае энтропийные потери при мицеллообразовании существенно меньше, что и вызывает значительное падение ККМ. Это явление нашло практическое применение, в частности, в косметологии, где добавки полимеров используют для понижения содержания свободного ПАВ в системе, что позволяет уменьшить возможное раздражение кожи [17].
В последнее время интерес в исследовании систем полимер–ПАВ сместился в сторону более концентрированных растворов ПАВ, содержащих длинные червеобразные мицеллы (“мицеллярные цепи”) [18–27]. Длина таких мицелл может достигать несколько десятков микрон, и по многим свойствам (в частности, по способности образовывать вязкоупругие растворы) они напоминают полимеры [18, 21]. Вместе с тем, в отличие от полимеров, такие мицеллы являются лабильными структурами. Они постоянно разрываются и рекомбинируют, а также находятся в равновесии с одиночными молекулами ПАВ в растворе, которые способны обмениваться с молекулами ПАВ, встроенными в мицеллы [18]. В связи с этим, червеобразные мицеллы ПАВ часто называют “живущими” или “равновесными” полимерами [18, 27]. В полуразбавленных растворах такие ПАВ проявляют вязкоупругие свойства, что широко используется в ряде промышленных применений, например, в нефтедобыче [26, 28].
Основная цель введения противоположно заряженного полиэлектролита в растворы червеобразных мицелл ПАВ состоит, как правило, в модификации реологических свойств системы. В ряде работ [29–32] было проведено “армирование” червеобразных мицелл путем внедрения полимерных цепей в их ядра. Для этого использовали сополимеры, содержащие незаряженные гидрофобные звенья, стремящиеся разместиться в ядрах мицелл, и заряженные звенья, встраивающиеся между головками ПАВ, несущими противоположный заряд по отношению к полимеру. Обнаружено, что в некоторых случаях такие гибридные мицеллы могут обеспечить более высокую вязкость раствора, чем исходные компоненты [29, 33]. Однако часто внедрение полимера вызывает противоположный эффект: мицеллы становятся короче, что приводит к понижению реологических характеристик, таких как вязкость и модуль упругости [29].
В настоящей работе предложен новый подход к созданию систем, содержащих полиэлектролит и противоположно заряженные червеобразные мицеллы ПАВ. Он состоит в использовании сильно заряженного гидрофильного полимера, неспособного проникать в мицеллярные цепи. Ожидается, что в присутствии низкомолекулярной соли, подавляющей электростатическое притяжение между противоположно заряженными полимером и ПАВ, в растворе будет присутствовать сетка из зацепленных полимерных и мицеллярных цепей.
Растворы, полученные смешением лабильных мицеллярных цепей ПАВ со стабильными полимерными цепями, представляют особый интерес для исследования. Они являются аналогами смеси двух противоположно заряженных полимеров, но при этом один из компонентов такой смеси будет способен перестраиваться в зависимости от внешних условий. Для описания поведения таких систем чрезвычайно полезен опыт изучения интерполиэлектролитных комплексов в солевых растворах, накопленный, в частности, в научной школе А.Б. Зезина и В.А. Кабанова [34, 35].
Таким образом, цель настоящей работы состояла в исследовании влияния полиэлектролита на фазовое поведение и вязкоупругие свойства растворов противоположно заряженных червеобразных мицелл ПАВ. В качестве поверхностно-активного вещества использовано катионное ПАВ с мононенасыщенным гидрофобным хвостом, содержащим 22 атома углерода, – эруцил-бис-(гидроксиэтил)метиламмоний хлорид (ЭГАХ), а в качестве полимера – отрицательно заряженный полисахарид ксантан. Выбранный полимер является жесткоцепным полиэлектролитом (его персистентная длина составляет 120 нм [36]), благодаря чему его растворы обладают рядом ценных свойств, а именно, высокой вязкостью даже при низких значениях концентрации полимера и малой чувствительностью к добавкам низкомолекулярных солей [37].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В данной работе использовали ксантан Ziboxan F-200 молекулярной массы 1.0 × 103 фирмы “Shandong Deosen Corporation Ltd.” и хлорид калия фирмы “Acros” (степень чистоты >99.8%) без предварительной очистки. Средняя контурная длина полимерных цепей составляла 1170 нм [37]. Согласно данным спектроскопии ЯМР 1H [37, 38], содержание ацетатных и пируватных групп в ксантане (в молях в расчете на повторяющееся звено полимера) составляло 0.56 и 0.41 соответственно. Эксперименты проводили при значениях рН ~ 6, при которых практически все карбоксильные группы депротонированы [39].
Эруцил-бис-(гидроксиэтил)метиламмоний хлорид, содержащий 25 мас. % изопропанола, получили от фирмы “Akzo Nobel”. Очистку ЭГАХ от изопропанола проводили, разбавляя реактив деионизованной водой в соотношении 1 : 10 и затем лиофильно высушивая [40]. Отсутствие изопропанола после очистки было подтверждено методом спектроскопии ЯМР 1Н. Концентрация ПАВ намного превышала критическую концентрацию мицеллообразования ЭГАХ в 3 мас. % водном растворе KCl – 3.8 × 10–4 мас. % [40].
В работе применяли деионизованную дистилированную воду, полученную на установке “Milli-Q” фирмы “Millipore Waters” (США).
Для приготовления образцов смешивали водные растворы ксантана, ЭГАХ и хлорида калия. Затем все образцы перемешивали в течение суток при комнатной температуре и оставляли еще на двое суток для достижения равновесного состояния.
Для исследования фазового поведения готовили растворы, содержащие разные концентрации ксантана, ЭГАХ и хлорида калия. После чего эти растворы оставляли при комнатной температуре на одну неделю. Наличие фазового расслоения контролировали визуально. В расслоенных системах химический состав сосуществующих фаз определяли с помощью элементного анализа.
Реологические измерения
Реологические измерения осуществляли на реометре “Physica MCR 301” фирмы “Антон Паар” при двух режимах воздействия на образец – статическом и динамическом [41].
Измерения в статическом режиме проводили при постоянной скорости сдвига (в диапазоне от 0.005 до 15.0 1/с). В этих экспериментах определяли максимальную ньютоновскую вязкость η0 (вязкость при нулевой скорости сдвига).
Измерения в динамическом режиме выполняли в частотном диапазоне 0.001–10.0 Гц. В этих экспериментах к образцу прикладывали переменное гармоническое напряжение σ*(t) и регистрировали изменение его деформации во времени γ*(t). Эти две величины связаны соотношением σ* = G* · γ*, где G* = G ' + iG '' – комплексный динамический модуль упругости, G ' – модуль накоплений, который характеризует упругие свойства образца, а G '' – модуль потерь, показывающий его вязкие свойства.
Значения амплитуды напряжения подбирали так, чтобы обеспечить проведение всех экспериментов в линейной вязкоупругой области, где динамические модули накоплений G ' и потерь G " не зависят от амплитуды приложенного напряжения.
Для исследования образцов с высокой вязкостью (>0.1 Па с) и вязкоупругими свойствами использовали измерительную ячейку “конус–плоскость” с диаметром 50 мм и углом среза конуса 1°. Образцы с низкой вязкостью (<0.1 Па с) исследовали с помощью ячейки “коаксиальные цилиндры” с большой площадью рабочей поверхности (диаметр внешнего цилиндра 20.28 мм, диаметр внутреннего цилиндра 18 мм, высота 55 мм) [42, 43].
Малоугловое рассеяние нейтронов
Измерения методом малоуглового рассеяния нейтронов проводили на времяпролетном спектрометре ЮМО, установленном на четвертом канале высокопоточного импульсного реактора ИБР-2 в Объединенном институте ядерных исследований (г. Дубна), в диапазоне волновых векторов Q от 0.006 до 0.5 Å–1 с использованием двухдетекторной системы. Растворы для измерений готовили в D2O, в качестве фонового раствора использовали раствор хлорида калия в D2O. Аппроксимацию кривых рассеяния форм-фактором цилиндра выполняли с помощью программы SasView (http://www.sasview.org/). Более подробно проведение экспериментов и обработка полученных данных описаны в работах [44, 45].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Фазовое поведение
Исследования проводили в условиях, когда в исходном растворе ПАВ образуются длинные червеобразные мицеллы, что подтверждается данными малоуглового рассеяния нейтронов (рис. 1). Для таких мицелл кривая рассеяния хорошо аппроксимируется форм-фактором цилиндра с радиусом 24.3 Å, что близко к длине полностью вытянутого гидрофобного хвоста ЭГАХ. Для изучения фазового поведения концентрацию ПАВ и ксантана варьировали в достаточно широких пределах, включающих области разбавленных растворов, полуразбавленных растворов без зацеплений и полуразбавленных растворов с зацеплениями.
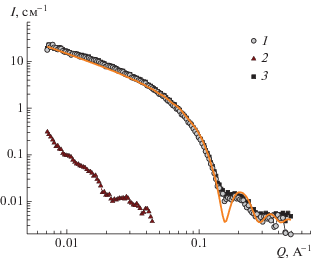
Рис. 1.
Кривые малоуглового рассеяния нейтронов для растворов ПАВ ЭГАХ (1), полимера ксантана (2) или смеси ксантан–ЭГАХ (3); сплошная линия – форм-фактор цилиндра с радиусом 24.3 Å. Растворитель – 4.75 мас. % раствор KCl в D2O. Здесь и на рис. 2в–6 концентрация ПАВ ЭГАХ 1.0 мас. % и полимера ксантана 0.1 мас. %; Т = 20°С.
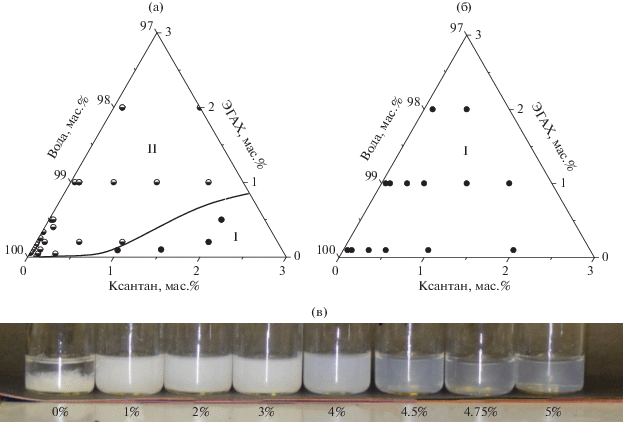
Полученные фазовые диаграммы в отсутствие и в присутствии низкомолекулярной соли представлены на рис. 2а и 2б. Видно, что при добавлении 4.75 мас. % KCl заметно расширяется область фазовой диаграммы, соответствующая однофазным системам. Фотографии растворов при разной концентрации KCl приведены на рис. 2в. Так, в отсутствие низкомолекулярной соли в системе наблюдали образование осадка, содержащего (согласно данным элементного анализа) эквимольный комплекс полимер–ПАВ. Это свидетельствует об ассоциативном фазовом расслоении, при котором оба компонента смеси сосредотачиваются преимущественно в одной фазе расслоенной системы [8]. В присутствии 1–4 мас. % KCl растворы были мутными, но осадок не выпадал, по меньшей мере, в течение нескольких месяцев. При концентрации KCl выше 4 мас. % растворы становились практически прозрачными (рис. 2в). Это связано с разрушением комплексов полимер–ПАВ под действием низкомолекулярной соли, вызывающей как экранирование электростатического притяжения между противоположно заряженными компонентами, так и понижение выигрыша в энтропии противоионов при их высвобождении во внешний раствор в результате комплексообразования полимера с ПАВ. Аналогичное поведение ранее наблюдали для комплексов полиэлектролитов со сферическими мицеллами ПАВ [7, 13], а также для комплексов противоположно заряженных полиэлектролитов [8, 46, 47]. Исследуемая в данной работе система имеет больше аналогии со смесью двух полимеров, так как агрегационные числа червеобразных мицелл велики (порядка сотен тысяч [48]), и количество выделяемых мицеллярной цепью противоионов во внешний раствор ближе к количеству противоионов полимерной цепи, а не сферической мицеллы (число агрегации порядка 50–100 [49]), в связи с чем роль энтропии противоионов при образовании комплексов полимер–ПАВ существенно выше в случае червеобразных мицелл ПАВ по сравнению со сферическими мицеллами.
Рис. 2.
Фазовые диаграммы водных растворов смесей ксантан–ЭГАХ при концентрации соли KCl 0 (а) и 4.75 мас. % (б), где I – однофазная и II – двухфазная система; в – фотография, демонстрирующая фазовое поведение водных растворов смесей полимер–ПАВ при различных значениях концентрации соли KCl.
Таким образом, изучение фазового поведения показало, что увеличение концентрации соли позволяет получить гомогенные смеси червеобразных мицелл катионного ПАВ и отрицательно заряженного полимера за счет предотвращения комплексообразования между ними.
Реологические свойства
Для исследования реологических свойств использовали гомогенные растворы ПАВ–полимер, полученные при высоких значениях концентрации низкомолекулярной соли KCl (4–6 мас. %).
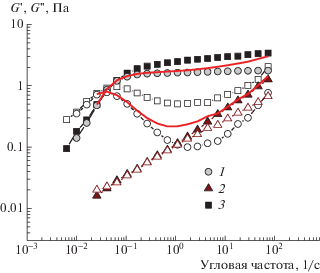
На рис. 3 представлены кривые течения и частотные зависимости модуля накоплений G ' и модуля потерь G " для смеси полимер–ПАВ и для ее отдельных компонентов (полимера и ПАВ) при концентрации KCl 4.75 мас. %. Видно, что у всех растворов на кривых течения (рис. 3а) наблюдается плато при низких значениях скорости сдвига и дальнейшее понижение вязкости с ростом скорости сдвига, связанное с выстраиванием червеобразных мицелл и(или) полимерных цепей вдоль направления течения. Кроме того, все растворы проявляют вязкоупругие свойства (рис. 3б). Так, при низких частотах механического воздействия значения упругой составляющей комплексного модуля упругости меньше значений вязкой составляющей G ' < G " (преобладают вязкие свойства), при высоких частотах, наоборот, G ' > G " (преобладают упругие свойства).
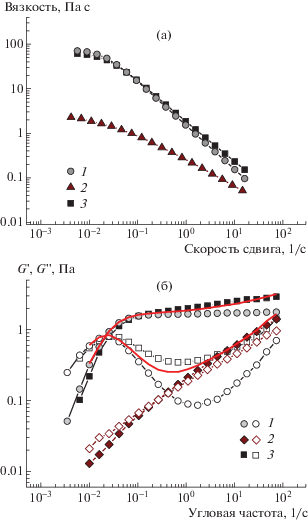
Рис. 3.
Кривые течения (а) и частотные зависимости модуля накоплений G ' (темные точки) и модуля потерь G '' (светлые точки) (б) для растворов ПАВ ЭГАХ (1), полимера ксантана (2) или смеси ксантан–ЭГАХ (3); сплошные линии – математические суммы частотных зависимостей G ' и G '' для раствора полимера и раствора ПАВ. Растворитель – 4.75 мас. % водный раствор KCl.
Рассмотрим сначала исходный раствор ПАВ. На рис. 3а видно, что он обладает высокой вязкостью при нулевой скорости сдвига, на 4.5 порядка превышающей вязкость воды. Кроме того, он имеет плато на частотной зависимости G '(ω) (рис. 3б), что указывает на наличие в растворе сетки переплетенных червеобразных мицелл ПАВ [50], так как при достаточно высоких частотах воздействия на образец топологические зацепления между мицеллами не успевают релаксировать и фактически ведут себя как “сшивки”, из-за чего сетка переплетенных мицелл приобретает свойство упругости. В этих условиях перемещение мицелл происходит, главным образом, путем рептации. Реологическое поведение раствора ЭГАХ хорошо описывается простой моделью Максвелла с одним временем релаксации, о чем свидетельствует близкая к идеальной полуокружности форма зависимости G " от G ' (кривой Коула–Коула) (рис. 4). Простое максвелловское поведение в растворах червеобразных мицелл обычно наблюдается в режиме “быстроразрывающихся” мицелл [19], когда за время рептации мицеллы много раз разрываются и восстанавливаются, что приводит к усреднению релаксационных процессов, позволяющему их описать с помощью единственного характерного времени релаксации.
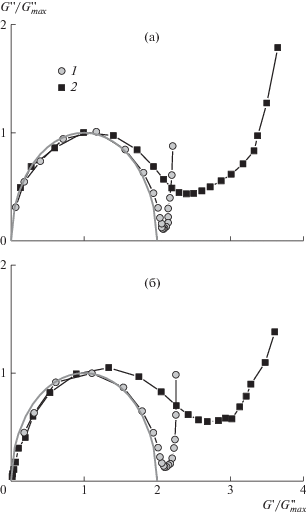
Рис. 4.
Нормированные зависимости модуля потерь G " от модуля накоплений G ' (кривые Коула–Коула) для растворов ПАВ ЭГАХ (1) или смеси ксантан–ЭГАХ (2); сплошные линии полуокружности описывают идеальное Максвелловское поведение вязкоупругого раствора с одним временем релаксации. Растворитель – 4.75 (а) и 6 мас. % (б) водный раствор KCl.
Что касается раствора полимера, то он характеризуется существенно меньшими значениями вязкости (рис. 3а), G ' и G ", а также полным отсутствием плато на частотной зависимости G '(ω) (рис. 3б). Это хорошо согласуется с тем фактом, что концентрация ксантана соответствует области полуразбавленного раствора без зацеплений (С* раствора ксантана в 4.75 мас. % KCl равна 0.045 мас. % [37], а концентрация перехода из полуразбавленного раствора без зацеплений в полуразбавленный раствор с зацеплениями – 0.17 мас. % [37]). Величина частоты ω0, при которой G ' = G ", позволяет определить терминальное время релаксации τ0 как τ0 = 1/ω0. Данные рис. 3б свидетельствуют, что время релаксации раствора полимера τ0 на порядок меньше, чем у раствора ПАВ. Это связано с тем, что при концентрации 0.1 мас. % полимер находится в полуразбавленном незацепленном режиме и сам по себе не образует сетку, в то время как мицеллы ПАВ находятся в полуразбавленном режиме с зацеплениями, и ввиду их большой длины обладают чрезвычайно высоким временем рептации.
Сравнение экспериментальных кривых на рис. 3б позволяет заключить, что добавление полимера к раствору ПАВ в присутствии 4.75 мас. % KCl приводит к значительному повышению G " и менее выраженному увеличению G '. Отметим, что повышение G " существенно более значительное, чем дает математическая сумма частотных зависимостей G ''(ω) для растворов ксантана и ЭГАХ, взятых по отдельности. Это указывает на более высокую диссипацию энергии в смешанной системе полимер–ПАВ, чем можно было бы ожидать при сохранении исходной структуры ее компонентов. Одной из причин такого поведения может быть уменьшение средней длины червеобразных мицелл $\bar {L}$ при их смешении с полимером. Действительно, в присутствии полимера соотношение ${{G}_{0}}{\text{/}}G_{{min}}^{{''}}$ понижается c 20.9 до 5.5, что может указывать на уменьшение $\bar {L}$ (при условии, что персистентная длина lp червеобразных мицелл не меняется), поскольку [18]
В то же время при добавлении полимера минимум $G_{{min}}^{{''}}$ на зависимости G ''(ω) смещается в сторону низких частот, что позволяет предположить [27], что время жизни мицелл увеличивается. Этот результат также можно объяснить уменьшением длины мицеллярных цепей. Действительно, чем короче цепи, тем меньше вероятность их обрыва, поскольку количество позиций, в которых обрыв возможен, уменьшается. Тот факт, что червеобразные мицеллы ПАВ при добавлении полимера становятся несколько короче, может быть связан с лабильной структурой мицелл, которые таким путем повышают выигрыш в энтропии при смешении с полимером.
Отметим, что укорочение червеобразных мицелл, предполагаемое на основе реологических данных, является незначительным и не отражается на кривой малоуглового нейтронного рассеяния, которая для системы полимер–ПАВ полностью идентична кривой рассеяния от исходных червеобразных мицелл ПАВ (рис. 1). Это указывает на то, что длина мицелл остается достаточно большой.
На рис. 3б видно, что терминальное время релаксации, определяемое как 1/ω0, в присутствии полимера почти не меняется; однако сравнение зависимостей Коула–Коула (рис. 4) свидетельствует о появлении отклонения от идеальной полуокружности, описывающей реологическое поведение в рамках модели Максвелла с одним временем релаксации. Отклонение наблюдается в области больших частот механического воздействия, что указывает на то, что полимер вызывает появление дополнительных релаксационных мод с относительно невысокими временами релаксации. Эти релаксационные моды могут быть связаны как с релаксацией полимерных цепей, так и с уменьшением средней длины червеобразных мицелл. Отклонение от модели Максвелла в результате уменьшения средней длины мицеллярных цепей было продемонстрировано ранее на примере многих систем [27].
Несмотря на то, что мицеллы становятся несколько короче, модуль накоплений на плато G0 не только не уменьшается, но даже становится несколько выше, что может быть связано как с тем, что длина мицелл остается намного бόльшей, чем расстояние между соседними зацеплениями, так и с возникновением новых зацеплений, образуемых между полимерными цепями и мицеллами. В этих условиях при добавлении полимера вязкость сохраняется неизменной (рис. 3а), так как появление дополнительных релаксационных мод с низкими временами релаксации компенсируется ростом модуля накоплений на плато за счет зацеплений: $\eta = {{G}_{0}}\tau $ [41].
Таким образом, ксантан не разрушает ни самих червеобразных мицелл ПАВ, ни образованную ими сетку. Этот результат не является тривиальным в связи с тем, что добавление полимера часто приводило к разрушению червеобразных мицелл ПАВ [51–55], превращая их либо в сферические [51–53], либо в короткие цилиндрические мицеллы [55]. Сохранение длинных мицелл ПАВ в присутствии полимера может свидетельствовать о подавлении добавленной солью взаимодействия полимер–ПАВ, приводящего к выпадению в осадок комплекса полимер–ПАВ.
При более высокой концентрации соли (6 мас. %) кривые G '(ω) и G ''(ω) для системы полимер–ПАВ сильно отличаются от математической суммы частотных зависимостей G '(ω) и G ''(ω) для растворов ксантана и ЭГАХ, взятых по отдельности. Особенно важным представляется тот факт, что кривая G '(ω) заметно выше, чем суммарная кривая для отдельных компонентов, что указывает на синергетическое повышение модуля накоплений (рис. 5). Наблюдаемый синергетический эффект можно объяснить образованием зацеплений между полимерными и мицеллярными цепями.
Рис. 5.
Частотные зависимости модуля накоплений G ' (темные точки) и модуля потерь G' ' (светлые точки) для растворов ПАВ ЭГАХ (1), полимера ксантана (2) или смеси ксантан–ЭГАХ (3); сплошные линии – математические суммы частотных зависимостей G ' и G '' для раствора полимера и раствора ПАВ. Растворитель – 6 мас. % водный раствор KCl.
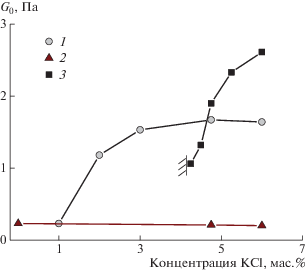
На рис. 6 представлена зависимость модуля накоплений на плато G0 для системы полимер–ПАВ от концентрации соли. Видно, что с ростом содержания соли G0 возрастает и становится выше, чем G0 исходного раствора червеобразных мицелл ПАВ. Поскольку в этих условиях в системе полимер–ПАВ не изменяются значения концентрации ни полимера, ни ПАВ, то такой рост G0 можно объяснить постепенным подавлением комплексообразования между полимером и ПАВ, приводящего к выпадению осадка, и возрастанием количества зацеплений между не участвующими в комплексообразовании червеобразными мицеллами ПАВ и полимерными цепями. Значит, в условиях, когда комплексообразование полимер–ПАВ полностью подавлено, эффект от зацеплений начинает проявляться наиболее ярко.
Рис. 6.
Зависимость модуля накоплений на плато G0 от концентрации соли KCl для растворов ПАВ ЭГАХ (1) или смеси ксантан–ЭГАХ (3); в случае раствора полимера ксантана (2) представлены значения модуля накоплений на частоте 1 с–1 в связи с отсутствием плато.
Отметим, что в 6 мас. % растворе KCl по сравнению с 4.75 мас. % раствором сильнее отклонения от максвелловского поведения в области высоких частот в присутствии полимера (рис. 4). Можно полагать, что когда комплексообразование полимер–ПАВ подавлено, то, помимо основной релаксационной моды цилиндрических мицелл, при высоких частотах дополнительный вклад вносят собственные релаксационные моды полимерных цепей, а также релаксация зацеплений между полимерными и мицеллярными цепями.
Таким образом, диссоциация комплекса ПАВ с противоположно заряженным жесткоцепным полиэлектролитом вследствие добавления соли приводит к формированию сетки зацеплений, образованной как цилиндрическими мицеллами ПАВ, так и переплетающимися с ними полимерными цепями.
ЗАКЛЮЧЕНИЕ
Смешение полиэлектролита и червеобразных мицелл противоположно заряженного ПАВ в присутствии низкомолекулярной соли позволяет получить прозрачный однородный раствор с высокими реологическими свойствами, превышающими таковые для суммы вкладов отдельных компонентов раствора. Данный синергетический эффект может быть обусловлен формированием зацеплений между макромолекулами и червеобразными мицеллами ПАВ, повышающим число эластически активных цепей в системе.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований в рамках научного проекта (код проекта 19-03-00879_а).
Авторы выражают благодарность А.И. Куклину за помощь при проведении исследований методом малоуглового рассеяния нейтронов.
Список литературы
Фельдштейн М.М., Зезин А.Б., Грагерова И.И. // Биохимия. 1972. Т. 37. № 2. С. 305.
Фельдштейн М.М., Зезин А.Б. // Молек. биология. 1974. Т. 8. № 1. С. 142.
Nagarajan R. // Chem. Phys. Lett. 1980. V. 76. № 2. P. 282.
Goddard E.D. // Colloids Surf. 1986. V. 19. № 2. P. 301.
Ибрагимова З.Х., Касаикин В.А., Зезин А.Б., Кабанов В.А. // Высокомолек. соед. А. 1986. Т. 28. № 8. С. 1640.
Василевская В.В., Крамаренко Е.Ю., Хохлов А.Р. // Высокомолек. соед. А. 1991. Т. 33. № 5. С. 1062.
Thalberg K., Lindman B., Karlström G. // J. Phys. Chem. 1991. V. 95. № 8. P. 3370.
Piculell L., Lindman B. // Adv. Coll. Int. Sci. 1992. V. 41. P. 149.
Khokhlov A.R., Kramarenko E.Yu., Makhaeva E.E., Starodubtzev S.G. // Macromolecules. 1992. V. 25. № 18. P. 4779.
Philippova O.E., Starodoubtzev S.G. // J. Polym. Sci., Polym. Phys. 1993. V. 31. № 11. P. 1471.
Antonietti M., Conrad J., Thunemann A. // Macromolecules. 1994. V. 27. № 21. P. 6007.
Magny B., Iliopoulos I., Zana R., Audebert R. // Langmuir. 1994. V. 10. № 9. P. 3180.
Хандурина Ю.В., Рогачева В.Б., Зезин А.Б., Кабанов В.А. // Высокомолек. соед. 1994. Т. 36. № 2. С. 241.
Zezin A.B., Izumrudov V.A., Kabanov V.A. // Macromol. Symp. 1996. V. 106. P. 397.
Philippova O.E., Chtcheglova L.A., Karybiants N.S., Khokhlov A.R. // Polym. Gels Networks. 1998. V. 6. № 5. P. 409.
Zakharova J.A., Otdelnova M.V., Ivleva E.M., Kasaikin V.A., Zezin A.B., Kabanov V.A. // Polymer. 2007. V. 48. № 1. P. 220.
Mohsenipour A.A., Pal R. // Handbook of Surface and Colloid Chemistry / Ed. by K.S. Birdi. London; New York: CRC Press Roca Baton, 2016. P. 639. Ch. 13.
Granek R., Cates M.E. // J. Chem. Phys. 1992. V. 96. № 6. P. 4758.
Cates M.E., Candau S.J. // J. Phys.: Condens. Matter 1990. V. 2. № 33. P. 6869.
Русанов А.И. Мицеллообразование в растворах поверхностно-активных веществ. СПб.: Химия, 1992.
Magid L.J. // J. Phys. Chem. B. 1998. V. 102. № 21. P. 4064.
Dreiss C.A. // Soft Matter. 2007. V. 3. № 8. P. 956.
Molchanov V.S., Philippova O.E. // J. Colloid Int. Sci. 2013. V. 394. № 1. P. 353.
Shibaev A.V., Kuklin A.I., Philippova O.E. // Colloid Polym. Sci. 2019. V. 297. № 3. P. 351.
Kwiatkowski A.L., Molchanov V.S., Orekhov A.S., Vasiliev A.L., Philippova O.E. // J. Phys. Chem. B. 2016. V. 120. № 49. P. 12547.
Dreiss C.A., Feng Y. // Wormlike Micelles: Advances in Systems, Characterisation and Applications. London: The Royal Society of Chemistry, 2017.
Kwiatkowski A.L., Molchanov V.S., Philippova O.E. // Polymer Science A. 2019. V. 61. № 2. P. 215.
Филиппова О.Е., Хохлов А.Р. // Нефтехимия. 2010. Т. 50. № 4. С. 279.
Nakamura K., Shikata T. // Macromolecules. 2003. V. 36. № 26. P. 9698.
Nakamura K., Shikata T., Takahashi N., Kanaya T. // J. Am. Chem. Soc. 2005. V. 127. № 13. P. 4570.
Kuntz D.M., Walker L.M. // J. Phys. Chem. B. 2007. V. 111. № 23. P. 6417.
Oikonomou E., Bokias G., Kallitsis J.K., Iliopoulos I. // Langmuir. 2011. V. 27. № 8. P. 5054.
Zhang L., Ni X., Cao Y., Ma X., Cao G. // RSC Adv. 2015. V. 5. № 124. P. 102759.
Зезин А.Б., Кабанов В.А. // Успехи химии. 1982. Т. 51. № 9. С. 1447.
Гуляева Ж.Г., Алдошина И.В., Зансохова М.Ф., Рогачева В.Б., Зезин А.Б., Кабанов В.А. // Высокомолек. соед. А. 1990. Т. 32. № 4. С. 776.
Sato T., Norisuye T., Fujita, H. // Macromolecules 1984. V. 17. № 12. P. 2696.
Philippova O.E., Shibaev A.V., Muravlev D.A., Mityuk D.Yu. // Macromolecules 2016. V. 49. № 16. P. 6031.
Чалых А.Е., Матвеев В.В., Муравлев Д.А., Митюк Д.Ю., Филиппова О.Е. // Росс. нанотехнологии 2017. Т. 12. № 1–2. С. 4.
Young S.-L., Martino M., Kienzle-Sterzerl C., Torres J.A. // J. Sci. Food Agric. 1994. V. 64. № 1. P. 121.
Shashkina Yu.A., Philippova O.E., Smirnov V.A., Blagodatskikh I.V., Churochkina N.A., Khokhlov A.R. // Polymer Science A. 2005. V. 47. № 11. P. 1210.
Малкин А.Я. // Основы реологии. СПб.: Профессия, 2018.
Shibaev A.V., Abrashitova K.A., Kuklin A.I., Orekhov A.S., Vasiliev A.L., Iliopoulos I., Philippova O.E. // Macromolecules. 2017. V. 50. № 1. P. 339.
Kwiatkowski A.L., Molchanov V.S., Sharma H., Kuklin A.I., Dormidontova E.E., Philippova O.E. // Soft Matter. 2018. V. 14. № 23. P. 4792.
Andreeva A.S., Philippova O.E., Khokhlov A.R., Islamov A.K., Kuklin A.I. // Langmuir. 2005. V. 21. № 4. P. 1216.
Shibaev A.V., Makarov A.V., Kuklin A.I., Iliopoulos I., Philippova O.E. // Macromolecules. 2018. V. 51. № 1. P. 213.
Philippova O.E., Akitaya T., Mullagaliev I.R., Khokhlov A.R., Yoshikawa K. // Macromolecules. 2005. V. 38. № 22. P. 9359.
Ayoubi M.A., Zinchenko A.A., Philippova O.E., Khokhlov A.R., Yoshikawa K. // J. Phys. Chem. B. 2007. V. 111. № 29. P. 8373.
Nagarajan R. // Langmuir. 2002. V. 18. № 1. P. 31.
Korchagina E.V., Philippova O.E. // Langmuir. 2012. V. 28. № 20. P. 7880.
Shibaev A.V., Tamm M.V., Molchanov V.S., Rogachev A.V., Kuklin A.I., Dormidontova E.E., Philippova O.E. // Langmuir. 2014. V. 30. № 13. P. 3705.
Brackman J.C., Engberts J.B.F.N. // Langmuir. 1991. V. 7. № 10. P. 2097.
Li X., Lin Z., Cai J., Scriven L.E., Davis H.T. // J. Phys. Chem. 1995. V. 99. № 27. P. 10865.
Massiera G., Ramos L., Ligoure C. // Langmuir. 2002. V. 18. № 15. P. 5687.
Francisco K.R., Da Silva M.A., Sabadini E., Karlsson G., Dreiss C.A. // J. Colloid Int. Sci. 2010. V. 345. № 2. P. 351.
Kwiatkowski A.L., Sharma H., Molchanov V.S., Orekhov A.S., Vasiliev A.L., Dormidontova E.E., Philippova O.E. // Macromolecules. 2017. V. 50. № 18. P. 7299.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


