Высокомолекулярные соединения (серия А), 2020, T. 62, № 1, стр. 57-64
Структура полиэлектролитных комплексов на примере гидрогелей хитозана с лямбда-каррагинаном
Ю. А. Щипунов *
Институт химии Дальневосточного отделения Российской академии наук
690022 Владивосток, пр. 100-летия Владивостока, 159, Россия
* E-mail: YAS@ich.dvo.ru
Поступила в редакцию 13.06.2019
После доработки 21.08.2019
Принята к публикации 03.09.2019
Аннотация
Рассмотрены взгляды А.Б. Зезина и В.А. Кабанова на структуру полиэлектролитных комплексов линейных полимеров, для подтверждения которых проведено изучение гидрогелей хитозана с лямбда-каррагинаном, сформированных методом регулируемого желирования. Визуализация комплексов осуществлена с помощью просвечивающей электронной микроскопии. Для контрастирования использован тетраоксид осмия.
ВВЕДЕНИЕ
Явление спонтанного фазового расслоения в растворах противоположно заряженных полиэлектролитов было известно с начала ХХ века. H.G. Bungenberg de Jong и H.R. Kruyt назвали его комплексной коацервацией в хорошо известной работе, опубликованной в 1930 г. [1]. Отмечено сходство с явлением флокуляции, поскольку в обоих случаях наблюдается выпадение осадка или фазовое расслоение с образованием нерастворимой пленки веществ на границе двух растворов. Комплексная коацервация – достаточно распространенное явление, получившее широкое практическое применение в пищевой, фармацевтической, агрохимической и текстильной промышленности [2–6]. Смеси противоположно заряженных полимеров – это частный случай. Из 12 примеров, приведенных H.G. Bungenberg de Jong и H.R. Kruyt, только один относится к их числу.
Комплекс, формирующийся в результате взаимодействия катионных и анионных синтетических полимеров – поли(винилбензилтриметиламмония) и поли(стиролсульфоната), был выделен одним из первых и изучен F.S. Michaels и R.G. Miekka в середине ХХ столетия [7]. Он был назван вначале поликатион-полианионным комплесом и полисолью, но затем его стали называть полиэлектролитным комплексом (ПЭК).
Работа F.S. Michaels и R.G. Miekka вызвала широкий интерес исследовательских групп, занимающихся синтетическими полимерами. Следует заметить, что биохимики, изучающие ДНК и РНК, к этому времени заметно продвинулись в понимании их ПЭК с белками. ДНК в клеточном ядре находится не в свободном состоянии, а в виде комплексов. В связи с этим предполагалась, что они играют важную роль в функционировании живой клетки. F. Mierscher в 1897 г. описал формирование и состав осажденного ПЭК при смешении растворов отрицательно заряженной ДНК и положительно заряженного протамина, которые предварительно были выделены и очищены из природного комплекса, находящегося в лососевых молоках [8]. Основной результат был подтвержден в более поздних работах, в которых наряду с протамином [9] большее внимание уделялось комплексообразованию с гистонами, с которыми ДНК также связана в клеточном ядре [10]. P. Spitnik с соавторами расширили исследования ПЭК, взяв вместо природных белков синтетические поликатионы – полипептид полилизин и полимер поливиниламин [11]. Они смогли выделить комплексы с ДНК, охарактеризовав главным образом их растворимость в солевых растворах. Комплексообразование полилизина было также показано в случае РНК, что было использовано для ее выделения [12]. F. Kremers и E. Fre-derico отметили увеличение упорядоченности РНК в комплексе [13]. Синтетические полинуклеотиды вместо ДНК были взяты в работе [14]. G. Felsenfeld и S. Huang в ней исследовали ПЭК с полилизином. Установлено, что полипептид способен вытеснять катионы двухвалентных металлов из комплекса с ДНК, формируя более прочные ассоциаты. В это же время был опубликован обстоятельный обзор A. Katchalsky, в котором он рассмотрел различные стороны взаимодействия противоположно заряженных полиэлектролитов, уделив большое внимание термодинамике процессов и биологическим аспектам [15].
Возрастающая активность в изучении ПЭК и увеличивающееся число публикаций не могли не обратить на себя внимание. В России исследования были начаты В.А. Каргиным в последние годы его жизни. Он одним из первых понял не только биологическую, но и практическую значимость ПЭК для формирования новых материалов. В исследования были вовлечены В.А. Кабанов, А.Б. Зезин и В.А. Изумрудов, которые создали российскую школу по ПЭК, являющуюся ведущей и признанной в мире. Результаты их систематического изучения всех аспектов комплексообразования в растворах противоположно заряженных полиэлектролитов заложили фундамент современных представлений о ПЭК.
К отличительной особенности российской школы можно отнести внимание, которое всегда уделялось структуре ПЭК. В.А. Каргин с соавторами в 1959 г., а затем в 1970 г. впервые привлекли просвечивающую электронную микроскопию для их изучения [16, 17]. Отмечена зависимость образуемых ПЭК от характера взаимодействий противоположно заряженных полиэлектролитов [16]. Вместо ожидаемой сетчатой структуры авторы обнаружили глобулярные частицы, формируемые солянокислым полилизином с полиакриловой кислотой в водно-спиртовых растворах и поли-4-винилэтилпиридиний бромида с полиакриловой кислотой в смеси воды с диметилформамидом (20%) [17]. Образование разветвленных структур установлено с увеличением содержания органического растворителя до 80%. В такой смеси электростатические взаимодействия между противоположно заряженными полиэлектролитами ослаблены, а их комплекс удается растворить.
В.А. Кабанов с А.Б. Зезиным в своих публикациях неоднократно касались проблемы структурной организации ПЭК. Различные стороны вопроса наиболее подробно рассмотрены в обзорной статье, опубликованной в журнале “Успехи химии” [18]. Они представили возможные варианты, учитывающие соотношение молекулярной массы и концентраций противоположно заряженных полиэлектролитов, их химическое строение и стехиометричность состава. Экспериментальное подтверждение практически не приведено за исключением результатов из выше цитированной статьи [17].
Указанный обзор В.А. Кабанова и А.Б. Зезина вышел в 1982 г. К тому времени подробно были изучены ПЭК линейных полиэлектролитов. В связи с этим они рассмотрели структуру только их комплексов. В более поздних исследованиях ПЭК стали формировать из нелинейных полимеров, блок-сополимеров, дендримеров, звездчатых полимеров, а также с поверхностно-активными веществами, которые имеют иную молекулярную структуру. В.А. Кабанов с А.Б. Зезиным в многочисленных публикациях также предложили модели их комплексов. Результаты обобщены в ряде обзоров, подготовленных в последние годы жизни [19–23]. При построении новых моделей они всегда основывались на статье 1982 г., адаптируя структуры ПЭК, предложенные для полиэлектролитов линейного строения, к полиэлектролитам с иным молекулярным строением.
Необходимо отметить, что получение и исследование ПЭК сталкивается с большими экспериментальными трудностями. Они обусловлены образованием нерастворимых комплексов при смешении растворов противоположно заряженных полиэлектролитов, если один из них не находится в большом избытке по отношению к другому [18, 24]. В.А. Каргин в соавторстве с В.А. Кабановым и А.Б. Зезиным впервые высказали предположение о том, что комплексообразование носит кооперативную природу [25], а затем А.А. Зезин с соавторами привели дополнительные доказательства, проанализировав c термодинамических позиций взаимодействие слабых полиэлектролитов [26]. Образование комплекса при кооперативных взаимодействиях проходит с высокой скоростью, что приводит к получению гетерогенного осадка, структура которого не отражает реальную структурную организацию ПЭК.
Цель настоящей работы – формирование и исследование однородных по составу комплексов линейных полиэлектролитов. Такие ПЭК образуются в том случае, когда ассоциация протекает не за счет кооперативных взаимодействий, а в режиме самоорганизации по методу регулируемого желирования, предложенному в работе для получения гидрогелей хитозана [27]. В настоящем сообщении его комплексы изготовлены с каррагинаном, структура которых визуализирована с помощью просвечивающей электронной микроскопии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
D-глюконо-δ-лактон, хитозан (~3 × 105) со степенью деацетилирования ~85% и 4%-ный водный раствор тетраоксида осмия приобретены в компаниях “Merck”, “Aldrich” и “Sigma-Aldrich” соответственно. Лямбда-каррагинан (1024 × 103) квалификации х.ч. был подарен компанией “Hercules Copenhagen A/S” (Denmark). Растворы готовили на деионизованной воде.
ПЭК хитозана с λ-каррагинаном формировали по методу, предложенному в работе [27], более подробное описание которого дано в работах [28, 29]. Навеску λ-каррагинана небольшими порциями засыпали в воду, которую перемешивали на магнитной мешалке, оставляя на 1 сутки до полного растворения. Хитозан в виде тонкого порошка вводили в полученный раствор, встряхивали, перемешивали с помощью магнитной мешалки, добиваясь его равномерного распределения в объеме. рН раствора равен приблизительно 6.0. В этих условиях хитозан находился в незаряженном состоянии. Для перевода в заряженное состояние добавляли навеску D-глюконо-δ-лактона. Ее вводили при перемешивании на магнитной мешалке, которое продолжалось до загустевания раствора. С ростом вязкости седиментация частиц хитозана постепенно замедлялась. Когда осаждение практически останавливалось, перемешивание прекращали, оставляя смесь для перехода в гелеобразное состояние, что составляло несколько часов. Полученные гидрогели выдерживали на протяжении нескольких дней для полного завершения процесса желирования. Частицы хитозана в них отсутствовали. Гидрогели имели ограниченную оптическую прозрачность из-за высокой опалесценции.
Структура ПЭК изучена с помощью просвечивающей электронной микроскопии (микроскоп “JEM-2010”, “JEOL”, Япония) высокого разрешения с ускоряющим напряжением 200 кВ. Для увеличения контраста изображений образцы обрабатывали тетраоксидом осмия. Концентрацию и длительность обработки подобрали экспериментально. Контрастирование основано на наноразмерных частицах размером порядка 1 нм, осаждающихся на группах –OH, –O– и –NH2, с которыми OsO4 вступает в реакцию [30]. Морфологическая картина выявлялась из их расположения. Хорошо разрешимые изображения получены после обработки тонких срезов гидрогелей. Небольшие кусочки затем диспергировали в спирте с помощью ультразвукового диспергатора. Каплю разбавленного раствора дисперсии наносили на медную сетку с аморфной полимерной пленкой и высушивали в термостате при 40°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
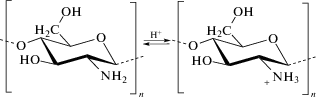
Структурные формулы хитозана и λ-каррагинана приведены ниже.
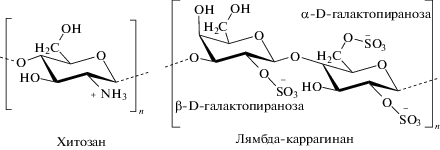
По молекулярной массе λ-каррагинан и хитозан различаются более, чем в 3 раза. По терминологии, предложенной В.А. Кабановым и А.Б. Зезиным [18], первый, имеющий большую молекулярную массу, можно назвать лиофилизирующим полиэлектролитом, а второй – блокирующим. Первый полисахарид состоит преимущественно из остатков 2-амино-2-дезокси-β-D-глюкопиранозы, связанных (1 → 4) связями [31], второй – из остатков дисахарида β-D-галактопиранозы и α-D-галактопиранозы, связанных соответственно (1 → 3) и (1 → 4) связями [32]. λ-каррагинан относится к группе сульфатированных полисахаридов. При этом сульфогруппа в β-D-галактопиранозе находится во втором положении, а в α-D-галактопиранозе – во втором и в четвертом. В соответствии с функциональными группами хитозан относится к числу слабых катионных полиэлектролитов, а λ-каррагинан – сильных анионных. Сильный–слабый полиэлектролит означает, что заряд первых зависит от рН раствора, а вторых – не зависит, оставаясь практически постоянным во всем диапазоне [33].
Смешение хитозана с λ-каррагинаном, как показано ранее [34, 35], приводит к формированию гидрогелей. В цитированных публикациях были изучены преимущественно механические (реологические) свойства. Показано также, что гелеобразование вызвано формированием трехмерной сетки из ассоциированных макромолекул. Исследование детальной структуры ПЭК, образующихся при смешении линейных полиэлектролитов, является предметом настоящей работы. Их характерные структурные особенности представлены на приведенном ниже рисунке, построенном в соответствии с моделями В.А. Кабанова и А.Б. Зезина [18].
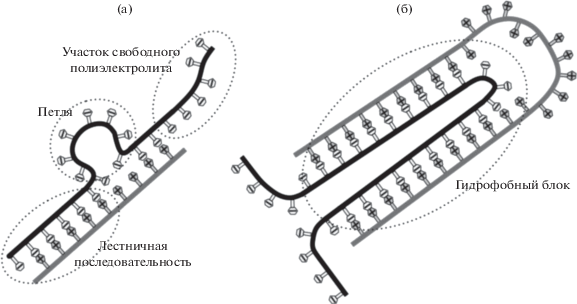
Линейные полиэлектролиты (а), как считали В.А. Кабанов и А.Б. Зезин, ассоциируют в результате электростатических взаимодействий с образованием двухтяжных участков, в которых обе цепи, расположенные в основном параллельно друг другу, связаны солевыми связями. Эти участки, являющиеся доминирующим структурным элементом ПЭК, были названы “лестничными последовательностями”. Дефекты, т.е., участки, на которых полиэлектролиты не образуют солевые связи, получили название “петель”. В случае избытка одного из компонентов по отношению к другому также имеются сегменты цепей, которые не вовлечены в комплекс, названные “участками свободного полиэлектролита”. Лестничные последовательности (б), по мнению В.А. Кабанова и А.Б. Зезина, могут ассоциировать друг с другом в силу гидрофобного характера, складываясь по месту петлеобразных дефектов. В таком случае можно ожидать образования “каплевидного кластера”. Такой кластер может быть составлен рядом лестничных последовательностей, достигая значительных размеров. (При рассмотрении структурных элементов ПЭК сохранена терминология статьи [18].)
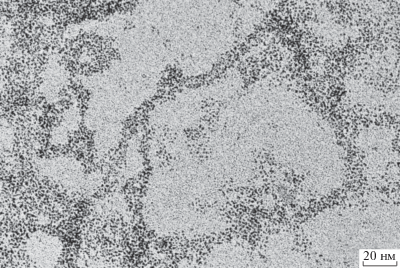
Изображение трехмерной сетчатой структуры комплекса хитозана с λ-каррагинаном можно видеть на рис. 1. Она характерна для однородного по составу материала, который удается сформировать только по методу регулируемого желирования, предложенному в работе [27]. С его помощью традиционное смешение растворов полиэлектролитов, при котором В.А. Каргин с соавторами получили частицы, обнаруженные с помощью электронной микроскопии [16, 17], заменяется на регулируемое заряжение хитозана in situ, предварительно введенного в незаряженной форме в раствор противоположно заряженного каррагинана. При этом вместо быстрых кооперативных взаимодействий проходит медленная самоорганизация. Заряжение осуществляется за счет подкисления раствора, при котором слабый катионный полисахарид, содержащий аминогруппы, переводится из незаряженного в заряженное состояние в соответствии с уравнением реакции
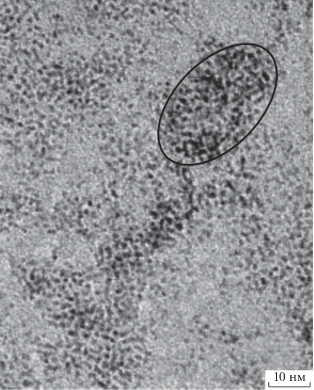
Рис. 1.
Электронно-микроскопическая фотография сетчатой структуры, образованной хитозаном с λ-каррагинаном. Овалом выделен возможный петлеобразный дефект. Пояснения в тексте.
Важное значение имеет то, каким образом происходит смещение рН. Добавление кислоты в реакционную смесь приводит к быстрому подкислению, которое сопровождается образованием гетерогенного осадка, как и при обычном смешении растворов. В предложенном методе используется лактон. Он медленно гидролизуется in situ до глюконовой кислоты [36]:
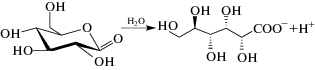
Появление кислоты в реакционной смеси обуславливает подкисление и соответственно заряжение хитозана. В то же время λ-каррагинан, который является сильным полиэлектролитом, содержащим сульфатные группы, не испытывает каких-либо изменений, оставаясь в заряженном состоянии. Как показано в ходе систематических исследований, метод применим для формирования гомогенных гидрогелей хитозана с разными анионными полисахаридами [27, 35, 37], наночастицами [28, 29, 38, 39], углеродными нанотрубками и даже с микрочастицами латексов, заряженными отрицательно [29]. В режиме самоорганизации получаются однородные по составу и структуре композиты, а в случае плоских наночастиц глины сапонит обнаружено образование нового кристаллического полиморфа [40].
Необходимо отметить, что А.Б. Зезин с В.А. Кабановым интересовались хитозаном и исследовали его комплексообразование с полиакриловой кислотой, используя традиционный подход [41]. Они наблюдали осаждение ПЭК. Установлена зависимость процесса от рН. Стехиометрический комплекс удалось получить при нейтральных значениях рН раствора, при которых хитозан заряжен частично. В этом случае его электростатические взаимодействия с полиакриловой кислотой в значительной степени ослаблены.
Детальный анализ изображений сетчатой структуры ПЭК хитозана с λ-каррагинаном выявил структурные особенности, которые были предсказаны А.Б. Зезиным с В.А. Кабановым в обзоре [18]. Они схематично показаны выше. На снимке исследуемого образца прежде всего следует отметить достаточно протяженные фибриллярные образования (рис. 1). Они являются основными структурными элементами сетки. Линейные полиэлектролиты, по мнению А.Б. Зезина и В.А. Кабанова, должны ассоциировать в структуры “лестничного строения”, которые были приведены в виде параллельно располагающихся цепей, скрепленных солевыми связями.
Анализ ряда экспериментальных данных привел их к выводу о наличии дефектов в структуре ПЭК, число которых может быть весьма значительным. Структура дефектов была представлена в виде петель. Они выявляются при рассмотрении рис. 1. Одна из петель выделена линией в виде овала. Петлеобразный дефект можно видеть также на фотографии, приведенной на рис. 2. Участки цепи одного из полиэлектролитов в области петли на обоих снимках не ассоциированы с противоположно заряженным компонентом. Так как функциональные группы не вовлечены в образование солевых связей, они оказывают значительное влияние на свойства комплексов, в частности, на абсорбцию полярных растворителей и набухание [18].
А.Б. Зезин и В.А. Кабанов предусмотрели образование не только линейных, но также и компактных структур, в которых участки ассоциированных полиэлектролитов могут складываться в виде “каплевидного кластера”. Кластеризация, по их мнению, возможна в области дефектов, в случае которых имеются изгибы цепей. Небольшой кластер наряду с дефектом, видимо, сформировался на участке, выделенном овалом на рис. 1. Поскольку при кластеризации площадь контакта гидрофобных ПЭК с полярной средой уменьшается, которая для них становится плохим растворителем, процесс с термодинамической точки зрения представляется вполне допустимым [18].
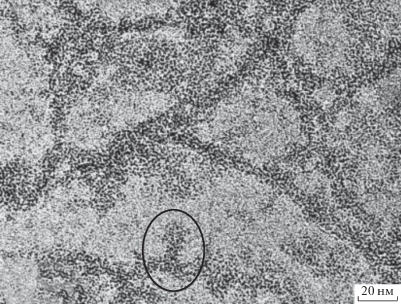
Выше показан вариант простейшего кластера, образованного ассоциацией двух участков цепей обоих полиэлектролитов. А.Б. Зезин и В.А. Кабанов считали возможным формирование объемных кластеров за счет многократного складывания лестничных структур, названное “внутримолекулярной сегрегацией”. Их выявление используемым методом представляется достаточно сложной задачей, так как в области кластеров создается повышенная концентрация наночастиц тетраоксида осмия. На снимке, приведенном на рис. 1, имеются участки, которые можно было бы отнести к таким кластерам, но они выглядят скорее как хаотичное скопление наночастиц из-за их большого числа, что не позволяет различить отдельные цепи. Анализ снимков выявил более однозначное изображение структуры, выделенное овальной линией на рис. 3, которая, возможно, является таким кластером. При рассмотрении можно различить свернутые цепи, уложенные в небольшой агрегат. Полученное изображение позволяет сделать вывод, что “каплевидные кластеры” в структуре ПЭК, предсказанные А.Б. Зезиным и В.А. Кабановым, вполне могут образовываться.
Рис. 3.
Изображение кластера, обведенного овальной линией. В верхней и нижней части кластера видны исходящие цепи полиэлектролитов. Более подробное обсуждение дано в тексте.
Дополнительный снимок трехмерной сетчатой структуры, сделанный при небольшом увеличении, приведен на рис. 4. При его анализе выявляются различные структурные элементы, отмеченные выше. В частности, хорошо видны протяженные линейные лестничные образования, составленные из ассоциированных макромолекул. Можно выявить несколько петлеобразных дефектов. Различимы также объемные кластеры, которые, возможно, сформировались в результате многократного складывания цепей. Рассмотрение деталей позволяет заметить структурные особенности, указывающие на возможную ассоциацию нескольких макромолекул. Такой вариант представляется вполне допустимым, если принять во внимание, что в двух мономерных остатках λ-каррагинана находится три заряженные группы, а в хитозане – в лучшем случае две.
ЗАКЛЮЧЕНИЕ
Проведенное небольшое исследование структуры ПЭК, сформированных по методу, в котором исключаются быстрые кооперативные взаимодействия между катионным хитозаном и анионным λ-каррагинаном за счет проведения медленного процесса самоорганизации, подтвердило в основном взгляды А.Б. Зезина и В.А. Кабанова на структурную организацию комплексов противоположно заряженных полиэлектролитов линейного строения. Показано формирование разветвленной трехмерной сетчатой структуры из ассоциированных макромолекул в виде нанофибрилл, имеющих, видимо, “лестничное строение”. Установлено также наличие петлеобразных дефектов и каплевидных кластеров из сложенных цепей. Лестничные структуры, дефекты и кластеры являются главными структурными элементами ПЭК линейных полиэлектролитов, с которыми связано образование гидрогелей и основные свойства. Выявление их на примере комплексов хитозана и λ-каррагинана подтвердило в полной мере предвидение А.Б. Зезина и В.А. Кабанова.
Работа выполнена при финансовой поддержке Министерства образования и науки Российской Федерации.
Список литературы
Bungenberg de Jong H.G., Kruyt H.R. // Kolloid. Z. 1930. V. 50. № 1. P. 39.
Yao K.D., Peng T., Yin Y.J., Xu M.X., Goosen M.F.A. // J. Macromol. Sci. C. 1995. V. 35. № 1. P. 155.
Peniche H., Peniche C. // Polym. Int. 2011. V. 60. № 6. P. 883.
Yang J.S., Han S.Y., Zheng H.C., Dong H.B., Liu J.B. // Carbohydr. Polym. 2015. V. 123. № 1. P. 53.
Carvalho I.T., Estevinho B.N., Santos L. // Int. J. Cosmet. Sci. 2016. V. 38. № 2. P. 109.
Liu L.K., Alva G., Huang X., Fang G.Y. // Renew. Sustain. Energy Rev. 2016. V. 66. № 2. P. 399.
Michaels A.S., Miekka R.G. // J. Phys. Chem. 1961. V. 65. № 10. P. 1763.
Mierscher F. Die Histochemischen Und Physiologischen Arbeiten. Leipzig: Vogel, 1897.
Alexander P. // Biochim. Biophys. Acta. 1953. V. 10. № 2. P. 595.
Crampton C.F., Lipshitz R., Chargaff E. // J. Biol. Chem. 1954. V. 206. № 3. P. 499.
Spitnik P., Lipshitz R., Chargaff E. // J. Biol. Chem. 1955. V. 215. № 4. P. 765.
Sober H.A., Schlossman S.F., Yaron A., Latt S.A., Rushizky G.W. // Biochem. 1966. V. 5. № 5. P. 3608.
Kremers F., Frederico E. // Eur. J. Biohem. 1969. V. 9. № 2. P. 275.
Felsenfeld G., Huang S. // Biochim. Biophys. Acta. 1959. V. 34. № 1. P. 234.
Katchalsky A. // Biophys. J. 1964. V. 4. № 1. P. 9.
Бакеев Н.Ф., Пшежецкий В.С., Каргин В.А. // Высокомолек. соед. 1959. Т. 1. № 12. С. 1812.
Рогачева В.Б., Мирлина С.Я., Каргин В.А. // Высокомолек. соед. Б. 1970. Т. 12. № 5. С. 340.
Zezin A.B., Kabanov V.A. // Russ. Chem. Rev. 1982. V. 51. № 9. P. 1447.
Kabanov V.A., Zezin A.B., Rogacheva V.B., Panova T.V., Bykova E.V., Joosten J.G.H., Brackman J. // Faraday Disc. 2005. V. 128. № 1. P. 341.
Pergushov D.V., Borisov O.V., Zezin A.B., Muller A.H.E. // Adv. Polym. Sci. 2011. V. 241. P. 131.
Pergushov D.V., Babin I.A., Zezin A.B., Muller A.H.E. // Polym. Int. 2013. V. 62. № 1. P. 13.
Pergushov D.V., Zezin A.A., Zezin A.B., Muller A.H.E. // Adv. Polym. Sci. 2014. V. 255. P. 173.
Zezin A.B., Mikheikin S.V., Rogacheva V.B., Zansokhova M.F., Sybachin A.V., Yaroslavov A.A. // Adv. Colloid Interf. Sci. 2015. V. 226. № 1. P. 17.
Shchipunov Y.A., Postnova I.V. // Composite Interf. 2009. V. 16. № 2. P. 251.
Зезин А.Б., Луценко В.В., Рогачева В.Б., Алексина О.А., Калюжная Р.И., Кабанов В.А., Каргин В.А. // Высокомолек. соед. A. 1972. Т. 14. № 4. С. 772.
Луценко В.В., Зезин А.Б., Калюжная Р.И. // Высокомолек. соед. A. 1974. Т. 16. №. 11. С. 2411.
Shchipunov Y.A., Ivanova N.A., Sarin S.A. // Mendeleev Commun. 2009. V. 19. № 3. P. 149.
Shchipunov Y.A., Silant’ev V.E., Postnova I.V. // Colloid J. 2012. V. 74. № 5. P. 627.
Postnova I., Sarin S., Silant’ev V., Ha C.S., Shchipunov Y. // Pure Appl. Chem. 2015. V. 87. № 8. P. 793.
Sawyer L.C., Grubb D.T., Meyers G.F. Polymer Microscopy. New York: Springer, 2008.
Roberts G.A.F. Chitin Chemistry. Basingstoke, Hampshir: MacMillan Ed., 1992.
Therkelsen G.H. Industrial Gums: Polysaccharides and their Derivatives / Ed. by R.L. Whistler, J.N. BeMiller. San Diego: Acad / Press, 1993. P. 145.
Dautzenberg H., Jaeger W., Kotz J., Philipp B., Seidel C. Polyelectrolytes: Formation, Characterization and Applications. Munich: Hanser, 1994.
Shumilina E.V., Shchipunov Y.A. // Colloid J. 2002. V. 64. № 3. P. 372.
Postnova I., Silant’ev V., Sarin S., Shchipunov Y. // Chem. Rec. 2018. V. 18. № 7–8. P. 1247.
Dziezak J.D. Encyclopedia of Food Science and Nutrition / Ed. by B. Caballero. New York: Acad. Press, 2004. P. 12.
Shchipunov Y., Sarin S., Kim I., Ha C.S. // Green Chem. 2010. V. 12. № 7. P. 1187.
Shchipunov Y.A., Ivanova N., Silant’ev V. // Green Chem. 2009. V. 11. № 11. P. 1758.
Shchipunov Y.A., Sarin S.A., Silant’ev V.E., Postnova I.V. // Colloid J. 2012. V. 74. № 5. P. 636.
Sarin S., Kolesnikova S., Postnova I., Ha C.S., Shchipunov Y. // RSC Adv. 2016. V. 6. № 40. P. 33501.
Скорикова Е.Е., Вихорева Г.А., Калюжная Р.И., Зезин А.Б., Гальбрайх Л.С., Кабанов В.А. // Высокомолек.соед. A. 1988. Т. 30. № 1. С. 44.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)