Высокомолекулярные соединения (серия А), 2020, T. 62, № 3, стр. 181-188
ВЛИЯНИЕ НАНОФИБРИЛЛ ХИТИНА НА СОРБЦИОННЫЕ СВОЙСТВА КОМПОЗИЦИОННЫХ ПЛЕНОК НА ОСНОВЕ ХИТОЗАНА
Е. Н. Дресвянина a, b, *, С. Ф. Гребенников a, И. П. Добровольская b, Т. П. Масленникова c, Е. М. Иванькова b, В. Е. Юдин b
a Санкт-Петербургский государственный университет промышленных технологий и дизайна
191186 Санкт-Петербург, ул. Большая Морская, 18, Россия
b Институт высокомолекулярных соединений Российской академии наук
199004 Санкт-Петербург, Большой пр., 31, Россия
c Институт химии силикатов им. И.В. Гребенщикова Российской академии наук
199034 Санкт-Петербург, наб. Макарова, 2, Россия
* E-mail: elenadresvyanina@gmail.com
Поступила в редакцию 28.04.2019
После доработки 29.07.2019
Принята к публикации 18.09.2019
Аннотация
Исследовано влияние нанофибрилл хитина на сорбционные свойства композиционных пленок. Величина сорбции снижается с увеличением содержания нанофибрилл хитина. Высказано предположение, что введение нанофибрилл хитина в хитозановую матрицу способствует более плотной упаковке макромолекул, формированию более упорядоченной кристаллической структуры композита и образованию мезофазы жидкокристаллического типа. Это предположение было подтверждено результатами рентгеноструктурного анализа.
ВВЕДЕНИЕ
В настоящее время хитозан, производный природного полисахарида хитина, находит широкое применение в медицине, фармакологии, косметологии и биотехнологиях [1–4]. Уникальный комплекс свойств, таких, как биосовместимость, биоразлагаемость, отсутствие цитотоксичности, бактерицидность, хорошие гемостатические характеристики, определяет перспективность разработки на его основе раневых покрытий, материалов для травматологии и ортопедии, гемостатических и шовных материалов, матриц для клеточных технологий, тканевой инженерии и трансплантологии [5–10]. Растворимость в разбавленных растворах кислот и хорошие пленко- и волокнообразующие свойства облегчают переработку этого полимера в пленки, волокна, трехмерные пористые материалы.
Разработка таких материалов должна предусматривать их дальнейшее использование в условиях повышенной влажности и в жидких средах. Обладая высокой гидрофильностью [11, 12], обусловленной наличием гидроксильных, карбонильных, амино- и ацетамидных групп, материалы из хитозана характеризуются высокой набухаемостью во влажном состоянии, изменением механических и релаксационных свойств при эксплуатации во влажной среде, что может негативно отразиться на результатах экспериментов при использовании хитозановых матриц в качестве подложек для пролиферации на них клеточных культур. Этот недостаток отчасти компенсируется температурной [13–16] или химической обработкой, использованием сшивающих агентов (глутарового альдегида, моно- и диглицидилового эфира, олигоэтиленоксида, додецилсульфата натрия и других) [17–20], которые приводят к межмолекулярным химическим сшивкам. Последний способ несет большую экологическую нагрузку, требует специального оборудования и защитных средств для персонала, а также повышает токсичность разрабатываемых материалов.
Другой способ регулирования свойств материалов из хитозана – создание композиционных материалов с наночастицами различной природы и морфологии [5]. При этом необходимыми требованиями к наполнителю являются его совместимость с полимерной матрицей, биосовместимость и способность к биорезорбции.
В качестве такого наполнителя в работе [21] использованы нанофибриллы хитина, поскольку хитин, близкий по химической структуре хитозану, обладает необходимой биосовместимостью, способностью к биорезорбции и может применяться в качестве матричного материала в тканевой инженерии [22]. Установлено [21], что нанофибриллы хитина в сухом состоянии формируют ленты с поперечным размером около 30 мкм и толщиной 0.1 мкм. Ленты состоят из нанофибрилл шириной 25 нм и длиной 400–500 нм, имеющих кристаллическую надмолекулярную структуру. В работах [23, 24] показана хорошая совместимость нанофибрилл хитина с макромолекулами хитозановой матрицы, что объясняется близкой химической структурой полимеров, их способностью создавать прочные водородные связи. Образование прочных водородных связей между макромолекулами хитозана и хитина и дополнительное формирование кластерной структуры нанофибрилл хитина (“жесткой структурной сетки”) приводит к снижению молекулярной подвижности, повышению модуля Юнга и разрывных напряжений композиционных образцов [23, 24]. Увеличение модуля авторы [23] объясняют также высокой кристалличностью самих нанофибрилл хитина. В то же время высказано предположение, что введение нанофибрилл хитина в низкокристаллическую хитозановую матрицу в количестве до 30 мас. % не приводит к заметному повышению степени кристалличности композиционных пленок.
Отмечено также [23], что величина набухания композиционного материала в воде снижается с увеличением содержания нанофибрилл хитина.
Однако результатов комплексных и систематических исследований по изучению взаимодействия композиционных материалов на основе хитозана, модифицированных нанофибриллами хитина, с водой и ее парами в литературе не представлено.
Таким образом, вопрос модификации материалов на основе хитозана с целью регулирования их надмолекулярной структуры, становится особенно актуальным. Настоящая работа направлена на изучение влияния нанофибрилл хитина на сорбционные свойства композиционных пленок на основе хитозана.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для приготовления пленок использовали креветочный хитозан производства “Biolog Heppe Gmbp” (Германия) с молекулярной массой (1.64 × 105)–(2 × 105), степенью деацетилирования 92.4% и нанофибриллы хитина производства “Mavi Sud s.r.l” (Италия). Содержание нанофибрилл хитина в водной дисперсии составляло 20 мг/мл.
Хитозан перемешивали в воде в течение 30 мин для его набухания. После этого в смесь вводили раствор уксусной кислоты при постоянном перемешивании, доведя концентрацию кислоты в растворителе до 2%. Концентрация полимера в растворе 4.0 мас. %. Она является оптимальной для формования волокон коагуляционным способом [24–27]. Раствор хитозана перемешивали 90 мин, после чего фильтровали, а затем обезвоздушивали в вакуумной камере не менее 24 ч при давлении 10 кПа.
Для получения композиционных пленок нанофибриллы хитина диспергировали в воде в течение 15 мин на ультразвуковом диспергаторе УЗВ-1.3 (Россия) при частоте 40 кГц. В полученную водную дисперсию добавляли хитозан таким образом, чтобы соотношение полимеров хитозан : : хитин было равно 99.5 : 0.5, 99 : 1, 95 : 5, 90 : 10, 70 : 30 и 1 : 99 (табл. 1). Далее растворы готовили по описанной выше схеме.
Таблица 1.
Константы уравнения (1)
| Образец | Содержание компонентов | Термический коэффициент α × 103, K–1 | Расчетные величины для исследуемых образцов | Расчетные величины для аморфных областей | |||
|---|---|---|---|---|---|---|---|
| хитозан | хитин | a0, г/г | E, Дж/моль | $a_{0}^{{\text{a}}}$, г/г | Eа, Дж/моль | ||
| 1 | 100 | 0 | –2.8 | 0.95 | 276 | 1.15 | 261 |
| 2 | 99.5 | 0.5 | –2.8 | 0.90 | 273 | 1.15 | 261 |
| 3 | 99 | 1 | –2.8 | 0.90 | 264 | 1.14 | 261 |
| 4 | 95 | 5 | –2.9 | 0.89 | 257 | 1.14 | 260 |
| 5 | 90 | 10 | –2.9 | 0.86 | 267 | 1.12 | 261 |
| 6 | 70 | 30 | –2.9 | 0.74 | 263 | 1.08 | 260 |
| 7 | 1 | 99 | –3.2 | 0.46 | 248 | 0.93 | 261 |
Исходные пленки получали формованием раствора через щелевую фильеру на стеклянную подложку с последующей сушкой при комнатной температуре в течение 24 ч. Толщина пленок 40 ± ± 10 мкм. Приготовленные методом сухого формования пленки из хитозана и композиционные пленки, модифицированные нанофибриллами хитина, выдерживали в спиртово-щелочной смеси 10%-ного водного раствора NaOH и C2H5OH в соотношении 1 : 1 в течение 10 мин, затем промывали дистиллированной водой и сушили на воздухе.
Сорбцию водяного пара измеряли изопиестическим методом [28], относительную влажность воздуха в эксикаторах создавали насыщенными растворами солей [29]. Эксикаторы термостатировали при 25°С. Перед измерением образцы высушивали при 80°С до постоянной массы [30], контроль за влагосодержанием осуществляли весовым способом. При каждом относительном давлении водяного пара образцы выдерживали до установления сорбционного равновесия (в течение 3–7 недель).
Рентгеноструктурный анализ проводили на дифрактометре ДРОН-3М (Научно-производственное объединение “Буревестник”) в режиме на отражение (геометрия Брегга–Бретано) с использованием CuKα-излучения (λ = 1.54183 Å, никелевый β-фильтр). Съемку проводили в кварцевых кюветах без усредняющего вращения. Регистрацию вели в пошаговом режиме в интервале углов 2θ = 10°–75° м с шагом 0.02° при экспозиции в точке 1 с. Обработку полученных данных и идентификацию пиков выполняли с использованием пакета программы DFWin и базы данных ICDD PDF-2.
Структуру пленок исследовали методом сканирующей электронной микроскрпии. Измерения проводили на электронном микроскопе “Carl Zeiss Supra 55 VP” фирмы “Carl Zeiss” (Германия). Перед исследованием на установке “Eiko-IB3” (“Ioncoater”) на материал напыляли слой золота толщиной ∼25 нм.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рис. 1 показаны изотермы сорбции хитозановых пленок и композиционных пленок, модифицированных нанофибриллами хитина.
Рис. 1.
Изотермы сорбции водяного пара пленками на основе хитозана и нанофибрилл хитина. Точки – эксперимент, кривые – расчет по формуле (1). Здесь и на рис. 2, 3 и 5 номера кривых соответствуют номерам образцов в табл. 1.
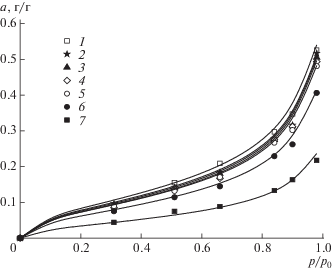
Все изотермы имеют вид, типичный для полимерных сорбентов, набухающих в парах сорбата. В области р/р0 > 0.4–0.6 наблюдается перегиб изотермы для всех исследуемых пленок, что свидетельствует о переходе аморфных областей полимеров в высокоэластическое состояние. Наибольшей сорбционной способностью по отношению к воде обладает хитозан, для композиционных пленок величина сорбции уменьшается с увеличением доли хитина в пленке.
Результаты исследования структуры пленок и волокон из хитозана, а также композитов, содержащих наночастицы различного химического строения, формы и размеров, приведены в монографии [5]. На рис. 2 представлена микрофотография скола в жидком азоте пленки из хитозана, а также композита, содержащего 5 мас. % нанофибрилл хитина. Видно, что поперечное сечение материалов их хитозана характеризуется равномерной, гомогенной структурой. Введение анизометричных нанофибрилл хитина способствует формированию слоистой структуры. Из анализа данных, полученных методами сканирующей электронной микроскопии, можно сделать вывод о двухфазной структуре хитозана, состоящей из менее упорядоченных, аморфных, и более упорядоченных, кристаллических, областей. Это позволяет применить уравнение (1), разработанное М.М. Дубининым в рамках модели объемного заполнения микропор, для оценки сорбционных свойств пленок на основе хитозана.
Рис. 2.
Микрофотографии скола в жидком азоте пленки из хитозана (а) и композита, содержащего 5 мас. % нанофибрилл хитина (б).

Можно предположить, что наночастицы хитина, которые характеризуются более упорядоченной по сравнению с хитозаном структурой и высокой кристалличностью [21, 31], обладают наименьшей сорбционной способностью.
Ранее сорбционные свойства пленок и порошков хитозана и хитина авторы [12] анализировали в рамках модели двойной сорбции, где локализованная сорбция (для исследуемых образцов в области р/р0 < 0.4) описывалась с помощью изотерм Ленгмюра, а нелокализованная (свободная вода) – с помощью изотерм Флори–Хаггинса (для исследуемых образцов при р/р0 > 0.6). Кластерообразование молекул воды в хитозановой/хитиновой матрицах рассматривали в рамках концепции Цимма–Ландберга [12].
В данной работе равновесную сорбцию водяного пара исследуемыми пленками анализировали с помощью термического уравнения сорбции [32]
(1)
$a = {{a}_{0}}\exp \left( { - {{{\left( {\frac{{ - \Delta {{\mu }_{1}}}}{E}} \right)}}^{n}} + \alpha \left( {T - {{T}_{0}}} \right)} \right)$Здесь а – величина сорбции при парциальном давлении пара р и температуре Т; а0 – предельная величина сорбции при давлении насыщенного пара р0 и температуре Т0; R = 8.314 Дж/моль К; Т0 = 298 K; Е – характеристическая энергия сорбции, Дж/моль; Δμ1 = RTln(p/p0) – изменение химического потенциала водяного пара при сорбции; р/р0 – равновесное давление и давление насыщенного водяного пара; n – ранг распределения Вейбулла, n = 0.3–0.33 для плотно упакованных и растворимых в сорбате полимеров; α – термический коэффициент сорбции, К–1.
Коэффициенты уравнения а0 и Е вычисляли из линейной формы уравнения (1) lna – lna0 – – ${{\left( {\frac{{ - \Delta {{\mu }_{1}}}}{E}} \right)}^{n}}$ и Т = Т0 = 298 K с использованием компьютерной программы Origin Pro v.8.5.
Термический коэффициент сорбции α = ${{\left( {\frac{{\partial {\text{ln}}a}}{{\partial T}}} \right)}_{{\Delta {{\mu }_{1}}}}}$ [33] характеризует основной вклад температуры в величину сорбции, его знак и величина определяются энергией взаимодействия молекул воды и элементарного звена полимера. Термический коэффициент может быть вычислен по уравнению [34]
(2)
$\alpha = ({\text{1}}{\text{.1}} \times {\text{1}}{{{\text{0}}}^{{ - {\text{3}}}}}) - ({\text{1}}{\text{.12}} \times {\text{1}}{{{\text{0}}}^{{ - {\text{5}}}}}) \times {\Delta }Е{\text{*(}}{\kern 1pt} \pm {\kern 1pt} {\text{9}}{\text{.4\% ),}}$Константы уравнения (1) приведены в табл. 1.
С увеличением содержания хитина предельная величина сорбции a0 снижается не аддитивно количеству хитина. Известно, что величина сорбции зависит от степени кристалличности полимера, поскольку кристаллиты обычно не доступны для молекул сорбата и могут вносить вклад в величину сорбции только за счет взаимодействия поверхностных сорбционных центров [36]. Следовательно, взаимодействие аморфно-кристаллических материалов с водой осуществляется в основном аморфными областями надмолекулярной структуры волокон, поэтому величина сорбции a связана со степенью кристалличности полимера xc [36]:
(aa – величина сорбции в аморфных областях полимера).D.W. van Krevelen [37] путем анализа изотермы сорбции воды рядом полимеров с известной степенью кристалличности предложил аддитивный метод вычисления величины сорбции в аморфных областях полимера:
(4)
${{a}^{{\text{a}}}} = ({{М}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}\sum {{{a}_{i}}} ){\text{/}}{{М}_{{{\text{зв}}}}},$Тогда степень кристалличности может быть определена как
В соответствии с этой схемой рассчитаны изотермы сорбции аморфными областями исследуемых образцов (рис. 3) и средние значения расчетных величин xc, которые представлены в табл. 2.
Рис. 3.
Изотермы сорбции водяного пара аморфными областями пленок на основе хитозана. Точки – эксперимент, кривые – расчет по формуле (1).
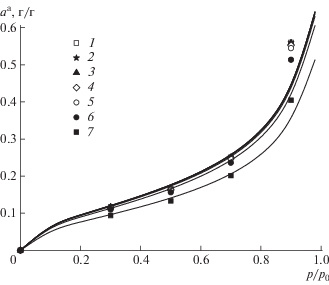
Таблица 2.
Расчетные величины коэффициентов формул (5) и (8)
| Образец | Содержание компонентов | Интегральная теплота сорбции, Дж/г | Степень кристалличности xc | |||
|---|---|---|---|---|---|---|
| хитозан | хитин | qi | $q_{i}^{{\text{a}}}$ | по формуле (5) | по формуле (8) | |
| 1 | 100 | 0 | 164 | 186 | 0.14 | 0.12 |
| 2 | 99.5 | 0.5 | 153 | 186 | 0.19 | 0.18 |
| 3 | 99 | 1 | 147 | 186 | 0.21 | 0.21 |
| 4 | 95 | 5 | 142 | 185 | 0.23 | 0.23 |
| 5 | 90 | 10 | 143 | 183 | 0.23 | 0.22 |
| 6 | 70 | 30 | 122 | 179 | 0.32 | 0.31 |
| 7 | 1 | 99 | 75 | 160 | 0.56 | 0.53 |
В работе [38] предложено вычислять степень кристалличности xc через интегральные теплоты сорбции, так как они отражают общий эффект взаимодействия активных групп макромолекул с молекулами воды. Величины интегральных теплот сорбции вычисляли по формуле (6) [36], которая следует из термического уравнения сорбции
(6)
${{q}_{i}} = \frac{{E{{a}_{0}}}}{{n{{М}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}}}(1 - \alpha T){\mathbf{Г}}(1{\text{/}}n)$Здесь qi – интегральная теплота сорбции; a0 – предельная величина сорбции, г/г; E – характеристическая энергия сорбции, Дж/моль; Г(1/n) – гамма-функция, при n = 0.33 она равна двум.
Тогда степень кристалличности
Результаты вычислений приведены в табл. 2 и на рис. 4.
Рис. 4.
Степень кристалличности хс исследуемых пленок, рассчитанная по формулам (5) (темные точки) и (7) (светлые).
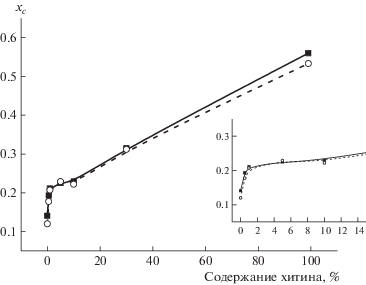
Величины степени кристалличности для пленки из хитозана, рассчитанные по формулам (5) и (7), близки: 0.12–0.14. При введении в хитозан нанофибрилл хитина степень кристалличности увеличивается. Рассматриваемые зависимости имеют в обоих случаях нелинейный характер. Введение нанофибрилл в очень небольшом количестве (0.5–1.0 мас. %) приводит к значительному увеличению хс. При содержании наполнителя более 10 мас. % наблюдается практически линейная зависимость (рис. 4).
В работе [24] показано, что композиционные волокна, содержащие 0.3–0.5 мас. % нанофибрилл хитина обладают повышенными прочностными и упругими характеристиками по сравнению с волокнами из чистого хитозана. Это объясняется хорошей адгезией макромолекул хитозана к поверхности наночастиц хитина. Расчет, проведенный методом молекулярной динамики, показал, что наиболее энергетически выгодным является расположение макромолекулы хитозана вдоль анизометричной наночастицы хитина. Такое расположение макромолекул хитозана должно способствовать кристаллизационным процессам.
Это подтверждают результаты исследования структуры исходных и композиционных пленок методом рентгеновской дифракции. На рис. 5 представлены рентгеновские дифрактограммы хитозана и композитов, содержащих различное количество нанофибрилл хитина. Видно, что для пленки из хитозана в основной форме характерно наличие двух широких дифракционных максимумов на углах 2θ = 10° и 20° (рис. 5, кривая 1), что согласуется с данными работы [13]. Однако введение небольшого количества нанофибрилл хитина (0.5 мас. %) приводит к появлению дифракционного максимума хитозана на угле 2θ = 15° (рис. 5, кривая 2). Аналогичная картина характерна и для пленочного композита, содержащего 1 мас. % хитина (рис. 5, кривая 3). При содержании нанофибрилл хитина более 5 мас. % интенсивность этого рефлекса хитозана уменьшается, но начинают проявляться рефлексы хитина [020] и [110], интенсивность которых увеличивается с повышением концентрации наполнителя.
Рис. 5.
Рентгеновские дифрактограммы пленок из хитозана и композиционных пленок с различным содержанием нанофибрилл хитина.
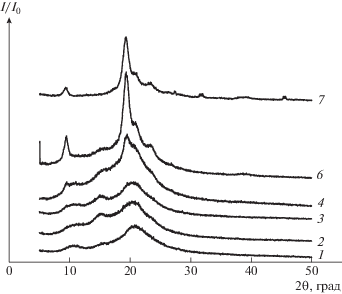
В угловом диапазоне 2θ = 14°–16° интенсивные рефлексы хитина не наблюдаются. Следовательно, появление рефлекса на угле 2θ =15° и рост его интенсивности при введении малого количества нанофибрилл хитина связано исключительно с упорядочением структуры хитозана и образованием более плотной упаковки макромолекул. Это объясняет заметное увеличение степени кристалличности композиционных пленок, содержащих 0.5 и 1.0 мас. % хитозана, определенной сорбционным и термодинамическим методами (рис. 4).
Ввиду особенностей строения макромолекулы хитозана, применение традиционных методов определения степени кристалличности, таких как ДСК и рентгеновская дифракция крайне затруднено. Температура терморазложения хитозана ниже температуры его плавления и близка к температуре стеклования [30], а значит, применение калориметрических методов, в частности ДСК, невозможно. Сополимерный состав макромолекулы хитозана препятствует кристаллизационным процессам; состав зависит от степени деацетилирования и может составлять 70–95% мономерных звеньев хитозана, остальное – звенья хитина. Кроме того, возможность наличия различных конформаций гликозидых звеньев в макромолекуле также затрудняет образование областей с трехмерным порядком. Два указанных основных фактора приводят к размытию рентгеновских дифракционных максимумов, что существенно осложняет определение их интегральной интенсивности вследствие некорректного отделения диффузной составляющей, определяющей аморфную фазу полимера. Поэтому сорбционный метод является практически единственным, позволяющим оценить степень кристалличности хитозана и композиционных материалов на его основе.
Увеличение кристалличности, формирование упорядоченной структуры пленок и образование более плотной упаковки полимерных цепочек, обусловливающие снижение величины сорбции при увеличении содержания хитина (даже при небольшом содержании хитина) может быть связано с формированием мезофазы макромолекул хитозана. Надмолекулярная структура композиционного материала представляет собой сложную гетерогенную систему. Образование надмолекулярной структуры начинается на стадии приготовления раствора для формования пленок (волокон). Диспергированный не растворимый в воде хитин состоит из нанофибрилл, которые приближенно можно представить в виде плоских частичек размером 25 × 25 × 500 нм [21]. Тогда одна нанофибрилла будет иметь геометрическую поверхность 5.1 × 104 нм2, объем 3.12 × 105 нм3, массу (при плотности 1.35 г/см3 [35]) 4.21 × 10–16 г, соответственно геометрическая удельная поверхность составит 120 м2/г. Это достаточно высокая величина, которая характеризует хитин как эффективный адсорбент хитозана из водного раствора. Далее дисперсию хитина смешивают с раствором хитозана и поскольку хитин и хитозан имеют достаточно высокое термодинамическое сродство, хитозан будет адсорбироваться на поверхности нанофибрилл хитина [36]. При следующей операции (сушке) концентрация хитозана в растворе растет, что повышает величину адсорбции, и нельзя исключить в адсорбционном слое на поверхности хитина самоорганизацию макромолекул хитозана в мезофазу жидкокристаллического типа [39], не доступную для воды при дальнейшей абсорбции водяного пара композиционным материалом [40]. Совокупность этих явлений, вероятно, приводит к тому, что изотермы абсорбции воды (рис. 1) в широком интервале концентраций хитина в композиционном материале (0.5–30%) достаточно близко группируются между изотермами абсорбции воды хитином и хитозаном.
Образование мезофазы или увеличение кристалличности композиционных материалов подтверждают практически постоянную интегральную теплоту сорбции для образцов 2–5, т.е. часть цепей хитозана входит в организованные структуры (кристаллиты иди жидкие кристаллы), не доступные молекулам воды.
ЗАКЛЮЧЕНИЕ
Введение нанофибрилл хитина снижает сорбционную способность хитозановых пленок, что может быть обусловлено увеличением упорядоченности в композиционных пленках, образованием более плотной упаковки макромолекул хитозана в адсорбционном слое на поверхности нанофибрилл хитина с формированием мезофазы жидкокристаллического типа из макромолекул хитозана.
Степень кристалличности пленок из хитозана составляет 0.12–0.14, введение нанофибрилл в количестве 0.5–1.0 мас. % вызывает значительное увеличение хс. Степень кристалличности хитина составляет 0.5–0.55.
Методом рентгеноструктурного анализа было показано, что при введении хитина в количестве 0.5–1.0 мас. % наблюдается дифракционный максимум на угле 2θ = 15°, с повышением содержания хитина более 5 мас. % интенсивность этого рефлекса хитозана уменьшается, но начинают проявляться рефлексы хитина [020] и [110], интенсивность которых увеличиваются с ростом концентрации наполнителя. Это может быть связано с самоорганизацией макромолекул хитозана и образованием более плотной упаковки макромолекул.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (код проекта 18-29-17011 мк).
Список литературы
Вихорева Г.А., Гальбрайх Л.С. Хитин и хитозан. Получение, свойства и применение / Под. ред. К.Г. Скрябина М.: Наука, 2002.
Kumar M.N.V.R., Muzzarelli R.A.A., Muzzarelli C., Sashiwa H., Domb A.J. // Chem. Rev. 2004. V. 104. P. 6017.
Sashiwa Hitoshi, Aiba Sei-ichi // Progr. Polym. Sci. 2004. V. 29. P. 887.
Kumar M.N.V.R. // React. Funct. Polymers. 2000. V. 46. P. 1.
Dobrovolskaya I.P., Yudin V.E., Popryadukhin P.V., Ivan’kova E.M. Polymer Scaffolds for Tissue Engineering. Saint-Petersburg.: Mediapapir, 2018.
Di Martinoa Al., Sittingerc M., Risbud M.V. // Biomaterials. 2005. V. 26. P. 5983.
Venkatesan J., Vinodhini P.A., Sudha P.N., Kim S.K. // Adv. Food Nutr. Res. 2014. V. 73. P. 59.
Levengood S.L., Zhang M. // J. Mater. Chem. B. 2014 . V. 2. № 21. P. 3161.
Shabunin A.S., Yudin V.E., Dobrovolskaya I.P., Zinovyev E.V., Zubov V., Ivan’kova E.M., Morganti P. // Cosmetics. 2019. V. 6. № 1. P. 16.
Pogorielov M.V., Sikora V.Z. // Eur. J. Medicine B. 2015. V. 1. № 2. P. 24.
Смотрина Т.В. // Бутлеровоские сообщения. 2012. Т. 29. № 2. С. 98.
Chalykh A.E., Petrova T.F., Khasbiullin R.R., Ozerin A.N. // Polymer Science A. 2014. V. 56. № 5. P. 614.
Ageev E.P., Vikhoreva G.A., Zotkin M.A., Matushkina N.N., Gerasimov V.I., Zezin S.B., Obolonkova E.S. // Polymer Science A. 2004. T. 46. № 12. C. 1245.
Zotkin M.A., Vikhoreva G.A., Derbenev M.A., Smotrina T.V. // Fibre Chem. 2004. T. 36. № 1. C. 16.
Агеев Е.П., Матушкина Н.Н., Вихорева Г.А. // Коллоид. журн. 2007. Т. 69. № 3. С. 300.
Mudarisova R.Kh., Monakov Yu.B., Kulish E.I., Kuzina L.G., Kolesov S.V. // Russ. J. Appl. Chem. 2009. V. 82. № 8. P. 1479.
Смотрина Т.В., Кильдеева Н.Р. // Бутлеровские сообщения. 2013. Т. 33. № 3. С. 138.
Kulish E.I., Kuzina L.G., Chudin A.G., Mudarisova R.Kh., Kolesov S.V., Monakov Yu.B. // Russ. J. Appl. Chem. 2007. V. 80. № 5. P. 810.
Chernyshova E.B., Berezin A.S., Tuzhikov O.I. // Russ. J. Appl. Chem. 2017. V. 90. № 7. P. 1165.
Vikhoreva G.A., Shablyukova E.A., Kil’deeva N.R. // Fibre Chemistry. 2001. V. 33. № 1. P. 59.
Dobrovol’skaya I.P., Kasatkin I.A., Yudin V.E., Ivan’kova E.M., Elokhovskii V.Y. // Polymer Science A. 2015. V. 57. № 1. P. 52.
Михайлов Г.М., Лебедева М.Ф., Пинаев Г.П., Юдинцева Н.М., Блинова М.И., Панарин Е.Ф. // Клеточная трансплантология и тканевая инженерия. 2006. Т. 4. № 6. С. 56.
Sriupayo J., Supaphol P., Blackwell J., Rujiravanit R. // Carbohydr. Polymers. 2005. V. 62. № 2. P. 130.
Yudin V.E., Dobrovolskaya I.P., Neelov I.M., Dresvyanina E.N., Popryadukhin P.V., Ivan’kova E.M., Elokhovskii V.Yu., Kasatkin I.A., Okrugin B.M., Pierfrancesco Morganti // Carbohydr. Polymers. 2014. V. 108. P. 176.
Dresvyanina E., Yudenko A., Maevskaya E., Yudin V., Yevlampieva N., Gubarev A., Slyusarenko M., Heppe K. // Vlakna Textil. 2018. V. 25. № 2. P. 27.
Dresvyanina E.N., Dobrovol’skaya I.P., Popryadukhin P.V., Yudin V.E., Ivan’kova E.M., Elokhovskii V.Y., Khomenko A.Y. // Fibre Chemistry. 2013. V. 44. № 5. P. 280.
Tamura H., Tsuruta Y., Itoyama K., Worakitkanchanakul W., Rujiravanit R., Tokura S. // Carbohydr. Polym. 2004. V. 56. № 2. P. 205.
Внучкин А.В., Гребенников С.Ф., Новоселов Н.П. Сорбционные процессы. СПб.: Санкт-Петербургский гос. ун-т промышленных технологий и дизайна, 2011.
Справочник химика / Под ред. С.А. Зониса, Г.А. Симонова. М.; Л.: Гос. науч.-техн. изд-во хим. лит-ры, 1962. Т. 1.
Dresvyanina E.N., Dobrovol’skaya I.P., Smirnova V.E., Popova E.N., Vlasova E.N., Yudin V.E. // Polymer Science A. 2018. V. 60. № 2. P. 179.
Chao Wang, Alan R. Esker // Carbohydr. Polymers. 2014. V. 102. P. 151.
Гребенников С.Ф., Кынин А.Т. // Журн. прикл. химии. 1982. Т. 55. № 10. С. 2299.
Grebennikov S.F., Chulkova Yu.S. // Russ. J. Phys. Chem. A. 2009. V. 83. № 4. P. 660.
Grebennikov S.F., Kynin A.T., Zaitseva E.I., Chulkova Yu.S. // Russ. J. Appl. Chem. 2007. V. 80. № 12. P. 2113.
Иощенко Ю.П., Каблов В.Ф., Заиков Г.Е., Абзальдинов Х.С. // Вестн. Казанского технол. ун-та. 2012. Т. 15. № 7. С. 106.
Гребенников С.Ф., Эльтеков Ю.А. Сорбция в полимерных системах. СПб.: Санкт-Петербургский гос. ун-т промышленных технологий и дизайна, 2014.
Van Krevelen D.W. Properties of Polymers. Amsterdam: Elsevier, 1997.
Папков С.П., Файнберг Э.З. Взаимодействие целлюлозы и целлюлозных материалов с водой. М.: Химия, 1976.
Жидкокристаллические полимеры / Под ред. Н.А. Платэ. М.: Химия, 1988.
Zhizhenkov V.V., Grebennikov S.F., Busygin K.N., Kvachadze N.G., Smotrina T.V., Smotrin V.A. // Polymer Science A. 2017. V. 59. № 2. P. 198.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


