Высокомолекулярные соединения (серия А), 2022, T. 64, № 3, стр. 200-213
Самосборка гелеобразных частиц и везикул в растворах полимеров с амфифильным повторяющимся звеном
А. И. Буглаков a, b, *, В. А. Иванов b, c, В. В. Василевская a
a Институт элементоорганических соединений им. А.Н. Несмеянова Российской академии наук
119334 Москва, ул. Вавилова, 28, Россия
b Московский государственный университет им. М.В. Ломоносова. Физический факультет
119991 Москва, Ленинские горы, 1, Россия
c Institute of Physics, University of Halle
06099 Halle, Germany
* E-mail: buglakov@polly.phys.msu.ru
Поступила в редакцию 26.10.2021
После доработки 03.01.2022
Принята к публикации 24.01.2022
- EDN: JIACDK
- DOI: 10.31857/S2308112022030063
Аннотация
Методом мезоскопического компьютерного моделирования исследованы особенности самосборки амфифильных гомополимеров с сольвофобной основной цепью и сольвофильными подвесками в разбавленных растворах. Обнаружено, что в таких системах возможно образование сферических, цилиндрических, дискообразных и многослойных везикул, причем переходы между ними происходят при изменении качества растворителя по отношению к сольвофильной подвеске. Амфифильные гомополимеры способны образовывать также червеобразные разветвленные агрегаты с гелеобразной структурой. Проведено сравнение с ранее полученными результатами (Macromolecules. 53 (2020) 4783-4795) для растворов амфифильных гомополимеров с сольвофильным остовом и сольвофобной подвеской и обнаружены принципиальные различия в самосборке двух типов макромолекул.
ВВЕДЕНИЕ
Самоорганизация молекул в сложные супрамолекулярные структуры является важным процессом в цикле функционирования “живых” систем [1–5]. Особую роль в процессах самосборки играет амфифильность, т.е. наличие у молекул одновременно химических групп, которые имеют сродство к растворителю, и групп, которые не смешиваются с ним [6]. Амфифильность многих биомолекул, таких как липиды [7], полипептиды [8, 9], глипокопротеины [10] и поликислоты [11], позволяет им проявлять при определенных условиях высокую поверхностную активность, что определяет их способность к микроструктурированию при агрегации. Амфифильность мономерного звена проявляется у некоторых биомакромолекул. Например, амфифильность мономерных звеньев у природных полипептидов ответственна за избирательную адсорбцию ферментов на различных поверхностях в “живых” системах [12], а амфифильность нуклеотидов, проявляющаяся в некоторых случаях, используется в распространенном методе ренатурации двойной спирали ДНК [13].
Интенсивное развитие химии высокомолекулярных соединений привело к возможности создания макромолекул различной архитектуры, которые способны имитировать самоорганизацию биомакромолекул [14–16]. Среди них особое место занимают гомополимеры с амфифильным повторяющимся звеном [16–18]. Обладая поверхностной активностью на уровне мономерного звена, данные макромолекулы могут самоорганизовываться в сложные структуры, такие как мицеллы, фибриллы и физические гели, везикулы [16, 18]. От широко исследуемых блок-сополимеров амфифильные гомополимеры отличают пониженная концентрация мицеллообразования, возможность самосборки мономолекулярных структур и тонкослойных (до нескольких нанометров) везикул, а также простота полимеризации и возможности последующей модификации [16, 18]. На данный момент существует множество примеров синтетических амфифильных мономеров, из которых были синтезированы соответствующие гомополимеры [18–22]. Их можно разделить на две группы, отличающиеся в архитектурном смысле: либо разным сродством к растворителю обладают две “подвески”, например, в случае пришивки этих групп к стиролу в разных положениях, либо амфифильность проявляется на уровне остов–подвеска. Для второго архитектурного типа амфифильных гомополимеров была теоретически [23] и экспериментально [20] обнаружена асимметричность самосборки при выборе различных в селективности по отношению к остову или к группам подвески растворителей.
Амфифильность повторяющегося звена проявляется при определенных условиях у некоторых интенсивно исследуемых водорастворимых полимеров. Так, поли-N-изопропилакриламид (ПНИПА) в присутствии соли NaSCN приобретает высокую поверхностную активность и способен претерпевать при изменении температуры морфологические переходы из сферической мицеллы в червеобразную мицеллу и далее в везикулу [24]. Кроме того, поливиниловый спирт в смеси с симвастатином действует как амфифильный гомополимер [25].
При теоретическом рассмотрении амифифильных гомополимеров, в случае, если амфифильность проявляется на уровне остов–подвеска, удобно использовать модель мономеров-“гантелей”, впервые предложенную для описания растворимости полимерных глобул в работе [26]. В рамках этой модели каждый мономер представляется в виде двух соединенных связью частиц, одна из которых сольвофильная, другая – сольвофобная. Применение данной концепции позволило методами аналитической и компьютерной статистической физики воспроизвести и предсказать множество экспериментально наблюдаемых морфологий гомополимеров [14, 23, 27–30].
Моделирование самосборки свободных амфифильных гомополимеров в разбавленном растворе было проведено для случая одной цепи методом молекулярной динамики в условиях неявного учета растворителя [27]. Недавно наша группа исследовала процессы самосборки амфифильных макромолекул с сольвофильным остовом и сольвофобными подвесками в разбавленном растворе методом диссипативной динамики частиц [28], который позволяет учитывать молекулы растворителя в явном виде. Кроме того, была теоретически описана возможная разница в конформационном поведении макромолекул с различной селективностью по отношению к отдельным группам гомополимера с гантелеобразной архитектурой мономерного звена [23]. На этом фоне остается открытым вопрос о поведении многих цепей гомополимера с сольвофобным остовом и сольвофильными подвесками в селективном растворителе в режиме разбавленного раствора.
В настоящей работе методом диссипативной динамики частиц [31] исследуются процессы самосборки амфифильных гомополимеров в режиме разбавленного раствора в селективном растворителе, который является хорошим растворителем для групп подвески и плохим растворителем для групп основной цепи. Особенности морфологии самоорганизующихся агрегатов изучены в зависимости от степени сродства растворителя с отдельными группами макромолекул и представлены в виде диаграммы состояний. Особое внимание уделено структуре гелеобразных агрегатов и везикул различной геометрии.
МОДЕЛЬ И МЕТОД
В данной работе амфифильный гомополимер описан в рамках простой модели связанных “гантелей”, в которой каждый мономер представляет собой две сферические частицы (A и B) радиуса rc, соединенные друг с другом фантомной связью. Цепь макромолекулы собирается из отдельных “гантелей” посредством последовательного соединения N частиц A друг с другом линейным образом. В таком случае частицы A составляют линейный остов макромолекулы, а частицы B являются подвесками, и каждая цепь обозначается A–graft–B. Равновесная длина связей A–A и A–B для простоты выбрана одинаковой и равной l. Растворитель моделируется в явном виде за счет введения сферических частиц S с радиусом, равным радиусу частиц A и B. Используемая модель проиллюстрирована на рис. 1.
Рис. 1.
Модель цепи, используемая в расчетах, и мгновенный снимок ячейки моделирования в начальный момент времени. Цветные рисунки можно посмотреть в электронной версии.
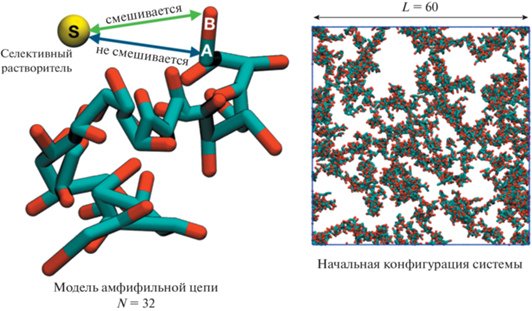
Такая модель позволяет легко ввести амфифильность мономерного звена при назначении различного сродства с растворителем для частиц А и В. Частица называется сольвофильной, если она эффективно притягивается к растворителю, и сольвофобной, если эффективно отталкивается от него. В свою очередь растворитель называется селективным, если он притягивается к одним группам макромолекулы и отталкивается от других. В настоящей работе мы рассматриваем макромолекулы с сольвофобным остовом и сольвофильными подвесками. Для этого мы принимаем, что частицы A эффективно отталкиваются от частиц растворителя S, а частицы B, наоборот, эффективно к ним притягиваются.
Разбавленный раствор цепей амфифильного гомополимера в селективном растворителе моделировался помещением молекул A–graft–B с объемной долей c, равной числу частиц, входящих в состав полимера, деленному на число всех частиц в системе N, и частиц растворителя S с объемной долей (1 – с) в кубическую ячейку с ребром L (длина в модели измеряется в эффективных радиусах частиц rc). На ячейку моделирования по всем осям были наложены периодические граничные условия. Режим разбавленного раствора соблюдался за счет выполнения неравенства c < c*, в котором c* – объемная доля перекрывания полимерных клубков. В ячейке была установлена среднечисленная плотность ρ, определяющая среднее число частиц в единичном объеме. Таким образом, суммарное число частиц в системе было постоянным и составляло N = L3ρ.
Численное моделирование описанной системы было проведено методом диссипативной динамики частиц (ДДЧ) [31]. Как было неоднократно показано [32–37], этот метод является удобным инструментом моделирования полимерных систем на мезомасштабе, на котором обычно и происходят процессы самосборки коллоидных систем. В методе ДДЧ динамика системы задается уравнениями движения Ньютона, а силы устанавливаются “мягкими” отталкивающими потенциалами. Выбор мягких потенциалов взаимодействия позволяет использовать большой шаг интегрирования уравнений движения, что и обусловливает “мезоскопичность” ДДЧ на временном масштабе.
Моделирование проводилось в каноническом ансамбле (постоянные температура T, число частиц N и объём ячейки V). Между частицами действует парная сила, записываемая в виде ${\mathbf{F}}_{{ij}}^{{}}$ = ${\mathbf{F}}_{{ij}}^{C}$ + + ${\mathbf{F}}_{{ij}}^{B}$ + ${\mathbf{F}}_{{ij}}^{D}~$+ ${\mathbf{F}}_{{ij}}^{R}$ (${\mathbf{F}}_{{ij}}^{C}$ – консервативная сила, ${\mathbf{F}}_{{ij}}^{B}$ – упругая сила, а ${\mathbf{F}}_{{ij}}^{D}~$ и ${\mathbf{F}}_{{ij}}^{R}$ – диссипативная и случайная силы соответственно). Консервативная сила рассчитывается как ${\mathbf{F}}_{{ij}}^{C}$ = $\left\{ \begin{gathered} {{a}_{{\alpha \beta }}}\left( {1 - {\text{\;}}\frac{{{{r}_{{ij}}}}}{R}} \right)\frac{{{{{\mathbf{r}}}_{{ij}}}}}{{{{r}_{{ij}}}}}\quad ~{{r}_{{ij}}} \leqslant {{r}_{c}} \hfill \\ 0\quad {{r}_{{ij}}} > {{r}_{c}} \hfill \\ \end{gathered} \right.$, где rij – пространственный вектор, соединяющий частицы i и j, ${{r}_{{ij}}} = \left| {{{{\mathbf{r}}}_{{ij}}}} \right|$, параметры ${{a}_{{\alpha \beta }}}$ задают амплитуду ${\mathbf{F}}_{{ij}}^{C}$ и определяют сродство между частицами различного типа (α, β = B, P, S, G), а ${{r}_{c}}~$– радиус обрезки взаимодействия, который также представляет собой эффективный радиус частиц и выбирается в качестве единицы длины (${{r}_{c}}$ = 1). Важно отметить, что эффективный размер “мягкой” частицы задается еще и амплитудой взаимодействия – чем больше ${{a}_{{\alpha \beta }}}$, тем меньше область пересечения двух частиц. Далее, сила, действующая между любыми двумя связанными частицами, определяется как ${\mathbf{F}}_{{ij}}^{B} = - K\left( {{{r}_{{ij}}} - l} \right)\frac{{{{{\mathbf{r}}}_{{ij}}}}}{{{{r}_{{ij}}}}}$, где K = 4.0 – жесткость связи, а l = 1.0 – ее равновесная длина. ${\mathbf{F}}_{{ij}}^{D}$ и ${\mathbf{F}}_{{ij}}^{R}$ в свою очередь задают термостат системы в ДДЧ. Их точный вид можно найти в работе [31]. Все используемые в моделировании параметры даны в конвенциональных безразмерных величинах.
Все проведенные компьютерные эксперименты были выполнены при следующих макропараметрах: размер ячейки моделирования L = 60, объем системы V = L3= 216 000; ρ = 3 (численная плотность системы была выбрана, согласно рекомендациям в работе [31]); степень полимеризации макромолекул N = 32; объемная доля полимера с = 0.02. Таким образом, суммарное число частиц в ячейке составляло N = V · ρ = 648 000, из них на частицы полимера приходилось Npol = = N · c = 12 960, т.е. в процессах самосборки участвовало 203 макромолекулы; температура T = 1.
Как было сказано выше, в ДДЧ сродство между частицами задается параметрами отталкивания aαβ. В рамках классической схемы ДДЧ взаимодействие между частицами одного типа задается как aαα = aββ = 25. Эффективное притяжение или отталкивание частиц разного типа определяется через aαβ (α ≠ β) так, что если aαβ ≤ aαα, частицы обладают сродством друг с другом, а если aαβ > aαα, частицы эффективно отталкиваются. Исходя из этого, мы установили aAB = 50, что соответствует сильной несмешиваемости частиц A и B. С целью построения морфологической диаграммы состояния амфифильного гомополимера A–graft–B в разбавленном растворе и определения влияния селективности растворителя на самосборку макромолекул параметры aAS и aBS варьировались в следующих пределах: 40 ≤ aAS ≤ 150 и 10 ≤ aBS ≤ 30; в этой области параметров остов макромолекул является сольвофобным, а частицы подвески – сольвофильными.
Каждую систему с заданными параметрами моделировали в течение 107 шагов алгоритма для трех независимых пробегов. Статистику исследуемых параметров собирали последние 106 шагов моделирования и по всему ансамблю независимых компьютерных экспериментов.
Визуальный анализ уравновешенных систем был проведен с помощью пакета VMD [38]. Численно системы были охарактеризованы на основании расчетов агрегационных чисел Nagg и числа агрегатов Magg, выполненных в рамках кластерного анализа [27, 28] с радиусом обрезки rcut = 1.5. Для найденных пространственно-разделенных кластеров были выполнены расчеты тензоров инерции и найдены их собственные значения. Из полученных собственных значений тензоров инерции для каждого отдельного агрегата был посчитан параметр асферичности A = ${{g}_{z}} - \frac{1}{2}\left( {{{g}_{x}} + {{g}_{y}}} \right)$ [39], где ${{g}_{x}} \leqslant {{g}_{y}} \leqslant {{g}_{z}}$ – собственные значения тензора инерции. Параметр A характеризует степень отклонения геометрии агрегата от сферически симметричной (A = 0 для идеальной сферы, сферического слоя или шара и тем выше, чем больше отклонение). Для данной модели условную границу между сферическим и вытянутым агрегатом можно установить при значении A ~ 4. Дополнительный анализ формы для уточнения геометрии некоторых систем был проведен с помощью параметров формы k1 = $\frac{{{{g}_{1}} + {{g}_{2}}}}{{{{g}_{2}} + {{g}_{3}}}}$, k2 = $\frac{{{{g}_{1}} + ~{{g}_{3}}}}{{{{g}_{2}} + ~{{g}_{3}}}}$ [40, 41]. Два этих параметра позволяют различить сферическую (k1 = 1, k2 = 1), цилиндрическую (k1 = 0, k2 = 1) и дискообразную геометрии (k1 = 0.5, k2 = 0.5). Также был выполнен анализ внутренней структуры некоторых агрегатов на основании расчетов приведенной радиальной плотности распределения p(r) = $\frac{{n\left( r \right)}}{{\rho {{V}_{{sl}}}\left( r \right)}}$ отдельных частиц A, B и S в объеме агрегата, где r – расстояние от центра масс кластера, n(r) – число частиц в сферическом слое на расстоянии r от центра масс кластера; Vsl(r) – объем сферического слоя толщиной 0.5${{r}_{c}}$, находящегося на расстоянии r от центра масс агрегата; $\rho $ – среднечисленная плотность частиц в системе. По определению, максимально возможное значение p(r) = 1, что соответствует ситуации, когда только данный тип частиц представлен в сферическом слое.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В данном разделе представлены результаты компьютерных экспериментов по самосборке амфифильных гомополимеров в разбавленном растворе в различных селективных растворителях в зависимости от степени смешиваемости сольвофобного остова и сольвофильных подвесок с растворителем. Особенности самосборки амфифильных гомополимеров подробно рассмотрены для трех различных случаев: 1) совместимость основной цепи с растворителем выше, чем совместимость двух составляющих звено частиц aAB > aAS; 2) отталкивание между частицами основной цепи и растворителем равно отталкиванию между частицами одного мономера aAB = aAS; 3) совместимость между частицами A и B выше, чем совместимость между основной цепью и растворителем aAB < aAS. Результаты представлены в виде морфологической диаграммы состояний раствора амфифильных гомополимеров в координатах aAS и aBS. Кроме того, они сопоставлены с результатами, полученными ранее для случая растворов гомополимера с сольвофильными остовом и сольвофобной подвеской.
На рис. 2 представлены результаты расчетов при различных aBS для случая aAB > aAS = 40, когда совместимость между растворителем и основной цепью выше, чем совместимость между частицами A и B (напомним, что во всех рассмотренных в данной работе случаях было выбрано значение aAB = 50). Показаны мгновенные снимки систем при некоторых значениях отталкивания между сольвофильными подвесками и растворителем aBS (рис. 2а), зависимость числа агрегатов в системе Magg от aBS (рис. 2б), а также распределения агрегационных чисел Nagg (рис. 2в) и параметров асферичности A (рис. 2г) для некоторых случаев, в которых в ячейке моделирования наблюдалось несколько полимерных агрегатов.
Рис. 2.
Мгновенные снимки систем (красный – частицы подвески, серый – частицы основной цепи) (а), число агрегатов в системе Magg в зависимости от aBS (б), а также распределения агрегационных чисел Nagg (в) и параметра асферичности A (г) агрегатов в системе при aBS = 10 (1), 15 (2), 20 (3), 25 (4) и 27 (5). aAS = 40.
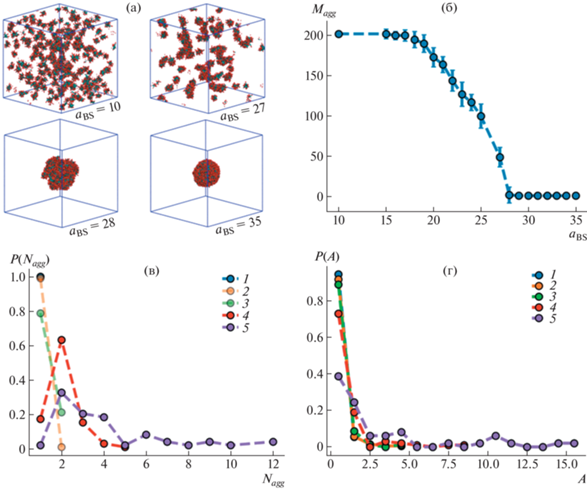
При aBS = 10 амфифильные гомополимеры в растворе самособираются в сферические агрегаты со структурой ядро–оболочка, в которых ядро состоит из сольвофобных частиц основной цепи, а оболочка – из сольвофильных подвесок. Число агрегатов в системе Magg (aBS = 10) = 202, каждый состоит из одной цепи, т.е. в данном случае в системе образуются структурированные глобулы (мономолекулярные мицеллы). Расчеты параметра асферичности A подтверждают визуально наблюдаемую сферичность агрегатов: 〈A〉 = 0.5 ± 0.3.
Число агрегатов, формирующихся в системе, не меняется до aBS = 15. При aBS = 15 наблюдается самосборка небольшого числа мицелл, состоящих из двух цепей. При этом среднее значение параметра асферичности всех мицелл в ячейке не меняется, но увеличивается ширина распределения (〈A〉 = 0.5 ± 0.5) – мицеллы, состоящие из двух цепей, оказываются менее сферичными. При уменьшении совместимости сольвофильных подвесок с растворителем вплоть до aBS = 27 наблюдается монотонное нелинейное уменьшение числа агрегатов в системе, увеличение среднего агрегационного числа и ширины распределения агрегационных чисел. Начиная с aBS = 25 максимум распределения агрегационных чисел приходится на мицеллы, состоящие из двух цепей. Увеличение агрегационных чисел происходит одновременно с постепенным уширением распределения параметра асферичности. Так, при aBS = 27 цепи полимера собираются не только в сферические, но и в цилиндрические мицеллы с такой же структурой ядро–оболочка. Максимум распределения Nagg приходится на значение 2, но самый большой наблюдаемый агрегат включает в себя 12 цепей. Сравнивая распределения агрегационных чисел и параметра асферичности, приходим к выводу, что большинство мицелл в системе имеют сферическую морфологию, хотя доля агрегатов с A > 2 значительна и составляет 37%.
Дальнейшее ухудшение качества растворителя (aBS = 28) для сольвофильной подвески приводит к объединению всех цепей в системе в единый рыхлый агрегат. Макромолекулы объединились таким образом, что частицы основной цепи сформировали единую компактную систему сильно разветвленных червеобразных нитей, стабилизированных частицами подвески (рис. 3а). Локальная структура таких червеобразных формирований такая же, как у сферических и цилиндрических мицелл. В объеме агрегата содержится большое число молекул растворителя, собранных в пространстве между разветвленными червеобразными нитями основной цепи. Данный агрегат по структуре сильно напоминает частицу микрогеля, если рассматривать червеобразные нити между отдельными точками ветвлений как “субцепи”, а сами точки ветвлений – как физические сшивки. Увеличение отталкивания между сольвофильными частицами и растворителем до aBS = 35 ведет к тому, что структура агрегата всех цепей амфифильного гомополимера меняется – кластер цепей приобретает более сферическую геометрию. Внутри агрегата частицы A и B собрались в чередующиеся слои, а ядро состоит из частиц A (рис. 3б). При этом число частиц растворителя в объеме данного слоистого агрегата мало.
Рис. 3.
Визуализация срезов агрегатов, самособравшихся в растворе амфифильных гомополимеров при aBS = 28 (а) и 35 (б). Цветовая схема соответствует таковой на рис. 1.
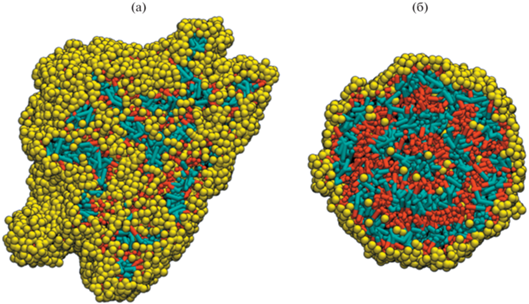
На рис. 4 представлены мгновенные снимки агрегатов, собирающихся в растворе амфифильных гомополимеров при aAS = 40 и aBS ≥ 28 вместе с приведенными радиальными плотностями распределения p(r) частиц полимера A и B и молекул растворителя S относительно центра масс агрегатов.
Рис. 4.
Мгновенные снимки гелеобразных агрегатов и приведенные радиальные плотности распределения p(r) от центра масс для частиц полимера А (1) и B (2) и растворителя (3) внутри агрегатов при aAS = 40. Серым цветом показана поверхность агрегата, сформированная основной цепью макромолекул (визуализирована с помощью Quicksurf VMD), красными полупрозрачными шариками – частицы подвески.
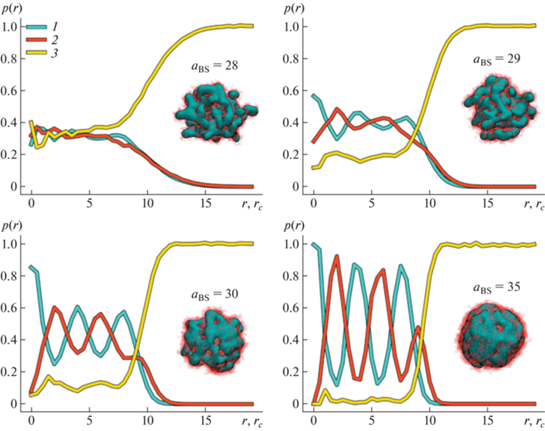
Из радиальных функций плотности p(r) для отдельных частиц A, B и S внутри гелеобразного агрегата, собравшегося при aBS = 28, видно, что в центре агрегата находятся в одинаковой доле как частицы полимера, так и молекулы растворителя. Затем, вплоть до r ~ 7${{r}_{c}}$, плотность всех частиц сохраняется примерно одинаковой. При дальнейшем удалении от центра агрегата мы наблюдаем постепенный рост радиальной плотности молекул растворителя и уменьшение локальной плотности макромолекул. Локальная плотность полимера падает до нуля при r ~ 15${{r}_{c}}$, что соответствует среднему размеру асферического агрегата. Заметим, что p(r) для A и для B на всем рассмотренном интервале расстояний от центра кластера одинаковы. Описанные радиальные плотности указывают на отсутствие выраженной внутренней структуры гелеобразной частицы при aBS = 28 и на наличие захваченных молекул растворителя в объеме агрегата.
Ситуация меняется при aBS = 29. Теперь в центре агрегата преобладают сольвофобные частицы основной цепи, а доля подвесок по сравнению с ними сильно падает. На ненулевом расстоянии от центра агрегата на распределениях p(r) частиц полимера появляются два слабо выраженных пика, причем локальные минимумы для частиц одного типа соответствуют локальным максимумам для другого типа. Доля растворителя в объеме агрегата становится существенно меньше доли частиц макромолекул, а локальный максимум p(r) частиц S отвечает первому локальному максимуму для p(r) сольвофильных частиц B.
Максимумы радиальных плотностей распределения частиц полимера внутри агрегата становятся более выраженными при aBS = 30, а сам агрегат теряет гелеобразную структуру – теперь его внешняя оболочка представляет собой перфорированный сферический слой. В центре агрегата плотность частиц основной цепи является высокой, с увеличением расстояния от центра она сначала уменьшается, а затем проходит через два последовательных максимума одинаковой амплитуды. На распределении p(r) сольвофильных частиц подвески присутствуют три последовательных максимума, каждый из которых ниже предыдущего вдоль оси r. Данная картина указывает на слоистую структуру агрегата, в котором последовательно расположены слои частиц A и B. При этом доля растворителя внутри частицы не нулевая, но она заметно меньше, чем при aBS = 29.
В случае сильного отталкивания между частицами подвески и растворителя (aBS = 35) агрегат становится более сферическим, и число дырок во внешнем слое сильно уменьшается. Слоистая структура проявляется более отчетливо, что подтверждается чередованием максимумов на зависимости p(r) для отдельных частиц полимера, а доля молекул растворителя в объёме агрегата становится почти нулевой.
Результаты компьютерных экспериментов при aAB = aAS = 50 представлены на рис. 5. Здесь показаны мгновенные снимки систем при различных aBS (рис. 5а); зависимости числа агрегатов в системе Magg и среднего радиуса инерции агрегатов Rg от aBS (рис. 5б); средние значения параметра асферичности A для различных aBS (рис. 5в); приведенные радиальные плотности распределения частиц в объёме агрегата p(r) и дополнительные мгновенные снимки агрегатов при aBS = 27 и 28 (рис. 5г).
Рис. 5.
Мгновенные снимки систем (красный – частицы подвески, серый – частицы основной цепи) (а), число агрегатов в системе Magg (1) и средний радиус инерции $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ агрегатов (2) в зависимости от aBS (б), средние значения параметра асферичности 〈A〉 при различных aBS (в) и приведенные радиальные плотности распределения p(r) частиц A (1), B (2) и S (3) внутри агрегатов и их мгновенные снимки при aBS = 27 и aBS = 28 (г). aAS = 50.
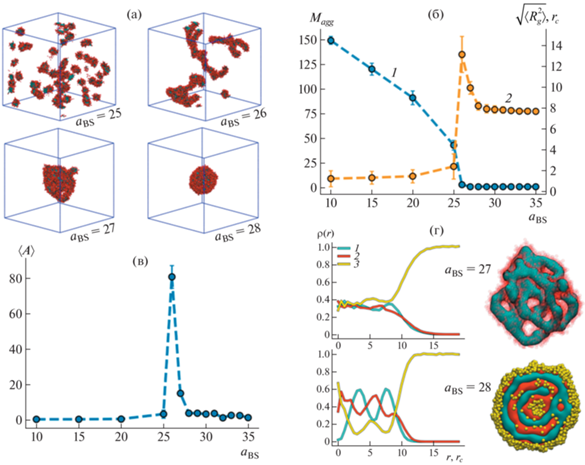
При наибольшей из рассмотренных степени смешиваемости между подвеской и растворителем aBS = 10 в системе самособрались 149 ± 4 сферических мицелл (〈A〉 = 0.4), состоящих из одной и двух макромолекул со средним радиусом инерции $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ = 1.20${{r}_{c}}$. Последовательное увеличение отталкивания между сольвофильными частицами подвески и растворителем приводит к монотонному уменьшению числа агрегатов в системе, увеличению их среднего размера и параметра асферичности. Так, при aBS = 25 в растворе 41% всех агрегатов составляют цилиндрические мицеллы, а средние размер и асферичность по всем мицеллам – $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ = 2.2${{r}_{c}}$ и 〈A〉 = 3.3 соответственно. При aBS = 26 в растворе гомополимер агрегирует в червеобразные разветвленные мицеллы, что отвечает максимумам зависимостей $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $(aBS) (рис. 5б) и 〈A〉(aBS) (рис. 5в). Червеобразные агрегаты обладают структурой ядро–оболочка, а точки ветвления соответствуют местам, в которых сходятся хотя бы три “червеобразные” мицеллы. Интересно, что в первом случае (при aAS < aAB) такие достаточно длинные структуры не наблюдались в системе, а небольшие цилиндрические агрегаты почти сразу коллапсировали в единую компактную структуру.
Все цепи объединились в один агрегат при aBS = 27. Данный агрегат представляет собой компактную гелеобразую частицу из разветвленных “червеобразных” нитей с радиусом инерции $\sqrt {\left\langle {R_{g}^{2}} \right\rangle ~} $ ~ 10${{r}_{c}}$. В нем отсутствует слоистая внутренняя структура, и он заполнен молекулами растворителя. При aBS = 28 частицы A и B в едином агрегате сегрегированы по сферическим чередующимся слоям. При этом растворитель внутри кластера строго занимает пространство в центре частицы и во втором от центра слое частиц B, который соответствует второму пику p(r) для подвески (рис. 5г). Данная структура имеет область, свободную от полимера и заполненную растворителем, в своем геометрическом центре и два бислоя. Таким образом, мы наблюдаем формирование в системе мультислойной везикулы. Дальнейшее ухудшение совместимости между растворителем и группами подвески приводит к постепенному понижению доли растворителя внутри агрегата, уменьшению радиуса инерции частицы и формированию мультиламелярной структуры с сольвофобным доменом в центре агрегата – это так называемая луковичная (onion) структура.
На рис. 6 представлены результаты для случая aAS = 100: зависимости числа агрегатов в системе Magg и среднего радиуса инерции агрегатов $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $от aBS (рис. 6а); средние значения параметра асферичности A для различных aBS (рис. 6б); мгновенные снимки отдельных везикул различных морфологий и соответствующие им параметры формы k1 и k2 (рис. 6в).
Рис. 6.
Число агрегатов в системе Magg (1) и средний радиус инерции $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ агрегатов (2) в зависимости от aBS (А), средние значения параметра асферичности 〈A〉 при различных aBS (Б) и мгновенные снимки везикул различной морфологии и соответствующие им параметры формы k1 и k2 (В). aAS = 100.
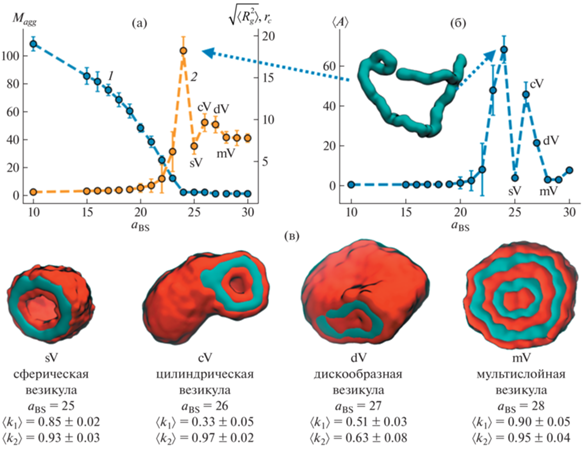
В данном случае при aBS = 10 в растворе собираются в среднем 108 сферических мицелл, причем доля мономолекулярных мицелл составляет ~30% от всех агрегатов в системе. Увеличение отталкивания растворителя от подвески полимера приводит, как и в рассмотренных ранее случаях, к монотонному уменьшению числа агрегатов в системе, повышению среднего радиуса инерции и росту асферичности. Первый и глобальный максимум обеих функций $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $(aBS) и 〈A〉(aBS) приходится на aBS = 24 – в этом случае все макромолекулы в ячейке объединены в червеобразный разветвленный агрегат. Дальнейшее увеличение отталкивания между A и S (aBS = 25) приводит к резкому спаду данных функций – в системе формируются сферические везикулы, которые представляют собой свернутую двойную мембрану BAAB, внутренняя часть которой состоит из частиц основной цепи, а два внешних слоя – из частиц подвески. Такая двойная мембрана называется бислоем. Сферический бислой окружает пространство, заполненное молекулами растворителя. Средний размер собравшихся в растворе сферических везикул $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ ~ 7${{r}_{c}}$. Обратимся к параметрам формы k1 и k2. На рис. 6в даны их средние значения для различных везикул. В случае визуально наблюдаемой сферической везикулы 〈k1〉 = 0.85 и 〈k2〉 = 0.97, что близко к значениям для идеальной сферы (k1 = 1 и k2 =1). Увеличение aBS до 26 приводит к росту асферичности и радиуса инерции, причем изменение асферичности намного значительнее, чем изменение радиуса инерции. В данном случае в системе формируется везикула с вытянутой геометрией. Ее средний размер $\sqrt {\left\langle {R_{g}^{2}} \right\rangle } $ ~ 9.6${{r}_{c}}$, а параметры формы 〈k1〉 = 0.33 и 〈k2〉 = 0.93 дают понять, что морфология агрегата близка к цилиндрической (k1 = 0 и k2 = 1). Таким образом, вторые максимумы на зависимости радиуса инерции и асферичности от aBS соответствуют везикуле цилиндрической геометрии. При aBS = 27 макромолекулы агрегируют в сплюснутую везикулу с параметрами формы 〈k1〉 = 0.51 и 〈k2〉 = 0.63, что ближе всего к геометрии диска (k1 = 0.5 и k2 = 0.5). Радиус инерции такой дискообразной везикулы слабо отличается от радиуса инерции наблюдаемой ранее цилиндрической везикулы, а асферичность у двух описанных агрегатов различается в два раза – дискообразная везикула менее асферична, чем цилиндрическая. Далее, при aBS = 28, везикула снова приобретает сферическую геометрию с параметрами формы 〈k1〉 = 0.90 и 〈k2〉 = 0.95, но теперь она имеет два бислоя в своей внутренней структуре. Последующее увеличение aBS приводит к уменьшению доли растворителя внутри агрегата и формированию плотной слоистой частицы при aBS > 30.
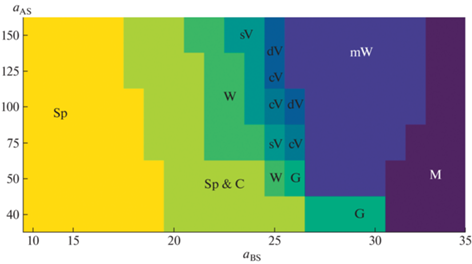
Морфологическая диаграмма состояний раствора амфифильного гомополимера в координатах параметров отталкивания между подвеской и растворителем aBS и между основной цепью и растворителем aAS представлена на рис. 7. На диаграмме области, отвечающие различным структурам, формирующимся в растворе, отмечены разными цветами и буквенными символами. Выделены следующие области – область сферических мицелл (Sp), область сосуществования сферических и цилиндрических мицелл (Sp & C), область червеобразных разветвленных агрегатов (W), компактной гелеобразной структуры (G), однослойных (состоящих из одного бислоя) сферической, цилиндрической и дискообразной везикул (sV, cV и dV соответственно), область существования сферической мультислойной везикулы (mV) и область плотной слоистой частицы (M). Видно, что сферические и цилиндрические мицеллы наблюдались при малых и средних значениях aBS на всем рассмотренном интервале aAS, как и плотная слоистая частица при высоких значениях aBS. Все три области Sp, Sp&C и M сужаются вдоль оси aBS при увеличении aAS. В нижней части диаграммы при сравнительно малых aBS переход от мицеллярного состояния раствора к плотному одиночному слоистому агрегату при повышении отталкивания между подвеской и растворителем происходит через промежуточную гелеобразую фазу, структура которой была описана выше. При увеличении несмешиваемости основной цепи и растворителя (aAS = 50) на диаграмме возникают два новых типа структур – червеобразные агрегаты и мультислойная везикула. Последующее увеличение aAS приводит к появлению областей стабильности сферической и цилиндрической везикул в промежутке между червеобразными агрегатами и мультислойной везикулой, а при aAS = 100 появляется область дискообразной везикулы. Таким образом, формирование везикул амфифильных гомополимеров с сольвофобным остовом и сольвофильной подвеской в разбавленных растворах происходит при сильном отталкивании между растворителем и основной цепью, в то время как при умеренном отталкивании между ними возможно образование гелеобразных структур.
Рис. 7.
Морфологическая диаграмма в координатах aAS – aBS параметров отталкивания между двумя различными частицами мономера и растворителем. Sp и C – сферические и цилиндрические мицеллы соответственно; W – червеобразные разветвленные агрегаты; G – гелеобразная частица; sV, сV, dV и mV – сферическая, цилиндрическая, дискообразная и мультислойная везикулы; M – плотная слоистая частица без растворителя внутри.
Сравнение со случаем одиночной цепи
Сравним текущие результаты моделирования раствора амфифильного гомополимера с сольвофобным остовом и сольвофильными подвесками со случаем моделирования одиночной цепи, для которой морфологии были посчитаны в рамках представления мономера-гантели методом молекулярной динамики в условиях неявного растворителя [27]. Как установлено ранее, одна цепь рассматриваемого гомополимера может собираться в сферические, цилиндрические и червеобразные мицеллы и сферическую везикулу с тонкой бислойной оболочкой. Данные структуры, как показано выше, могут наблюдаться и в растворах многих цепей. Кроме того, в зависимости от длины цепи для одной макромолекулы возможны конформации “ожерелья” и тора. Мы не наблюдали эти структуры в исследуемых нами растворах многих цепей. Аналогом “ожерелья” в нашем случае можно считать систему многих сферических мицелл, тогда как для тора, возможно, требуется меньшая по сравнению с выбранной нами объемная доля полимера.
Для случая одной цепи не были обнаружены такие структуры, как гелеобразные агрегаты, мультислойные везикулы, цилиндрические и дискообразные везикулы. В то время как формирования трех описанных типов везикул из одной цепи можно ожидать при увеличении длины цепи в модели с неявным растворителем [27], возможность образования гелеобразной частицы остается под вопросом.
Стоит заметить, что для случая одной цепи переходы от сферической мицеллы к цилиндрической и далее к везикуле наблюдались при повышении степени полимеризации макромолекулы, а аналогичные переходы в растворе происходили при увеличении отталкивания между частицами подвески и растворителем.
Сравнение со случаем сольвофильного остова и сольвофобной подвески
В предыдущей работе мы рассматривали разбавленный раствор амфифильного гомополимера в селективном растворителе при условии, что растворитель эффективно притягивается к основной цепи и эффективно отталкивается от подвески [28]. Сравнение двух диаграмм, построенных для пересекающихся интервалов параметров взаимодействия растворителя с полимером, показывает, что замена селективности растворителя по отношению к одной из двух различных групп полимера приводит к сильному изменению морфологического состояния раствора. Так, в рассмотренной в данной работе системе самое узкое распределение агрегационных чисел для сферических агрегатов имело место при относительно слабом отталкивании между сольвофобными группами основной цепи и растворителем, тогда как в случае, приведенном в работе [28], сферические агрегаты существовали при очень сильном отталкивании растворителя от сольвофобных подвесок. Для представленного в данной работе случая не наблюдался эффект перехода раствора из системы многих клубков сначала в мультидоменную структуру, а затем в систему сферических мицелл при ухудшении качества растворителя для сольвофобных групп (снизу вверх на диаграмме, рис. 7). Возможная природа этого различия лежит в эффективном притяжении, названном нами ориентационно-индуцированным, которое имеет энтропийную природу и возникает между сольвофобными доменами из подвесок вследствие их стремления увеличить число доступных ориентационных состояний. Такой механизм был описан нами в работе [23]. Указанное притяжение отсутствует для случая цепей с сольвофобным остовом и сольвофильной подвеской. Это объясняет, почему в данном случае в растворе наблюдалось образование длинных червеобразных разветвленных мицелл, в то время как такие структуры не были замечены в работе [28]. Более того, для амифильных гомополимеров с сольвофильным остовом при данной объемной доле отмечалось существование стабильных тороидальных структур, чего не было в настоящем случае.
Далее, везикулы, образованные макромолекулами с сольвофобным остовом, обладают большим агрегационным числом и большим размером ядра, заполненного растворителем по сравнению с везикулами из макромолекул с сольвофильным остовом. При прочих равных значениях параметров модели в этом случае мы наблюдали везикулы самой разной формы и, в частности, многослойные везикулы, что не было обнаружено в работе [28]. Важно отметить также, что в двух указанных случаях отличаются структура гелеобразных агрегатов и границы области их существования на диаграмме.
Диаграммы растворов двух типов амфифильных гомополимеров качественно схожи в следующем: тенденции морфологических переходов при ухудшении качества растворителя для сольвофильных частиц аналогичны тем, что имеют место при повышении концентрации низкомолекулярных поверхностно-активных веществ. Кроме того, стоит отметить, что везикулы в обоих случаях образуются только при высокой степени несмешиваемости между сольвофобными частицами и растворителем и сравнительно низкой смешиваемости между растворителем и сольвофильными группами полимера.
Сравнение с экспериментальными данными
С помощью численного моделирования мы исследовали общие закономерности самосборки в разбавленных растворах макромолекул с амфифильным повторяющимся звеном в условиях растворителя, селективного для групп звена. На данный момент экспериментально в таких системах были получены сферические и цилиндрические мицеллы, червеобразные агрегаты и везикулы [16–18].
Для поли(4-этинилбензоил-L-лейцин метилового эфира) был обнаружен переход от сферических частиц в метаноле к червеобразным агрегатам в тетрагидрофуране [42]. Замена метанола тетрагидрофураном соответствует небольшому увеличению отталкивания между подвеской и растворителем (параметра aBS) и уменьшению отталкивания между основной цепью и растворителем (параметра aAS), что согласуется с возможным, согласно полученной нами диаграмме, переходом от сферических мицелл к червеобразным агрегатам. Переходы от мономолекулярных сферических мицелл к сферическим агрегатам и далее к цилиндрическим мицеллам при направленном уменьшении гидрофильности подвески наблюдались, например, в работе [22], что соответствует описанным нами переходам при сравнительно малых aAS (например, aAS = 40) по мере увеличения aBS. В работе [43] поли-2-гидрокси-3-феноксипропилакрилат в смеси воды и ДМФА самособирался в рыхлые частицы со сложной внутренней структурой при pH 11.0 и в везикулы при pH 7.0. Предполагается, что уменьшение pH приводило к росту возможного числа внутри- и межмолекулярных водородных связей, что эффективно ухудшало качество растворителя. Аналогом такого перехода в данной работе является переход от гелеобразной частицы к везикуле при aAS = 50 при увеличении aBS. Как показано в работе [24], ПНИПА в комплексе с солью NaSCN проявляет свойства амфифильного гомополимера. С ростом температуры в такой системе возможна последовательность переходов сферические мицеллы–червеобразные агрегаты–везикула–плотная сферическая частица. Поскольку одной из причин агрегации ПНИПА при повышении температуры является увеличение внутримолекулярных водородных связей групп подвески, экспериментально наблюдаемые переходы качественно соотносятся с переходами в моделировании при aAS > 50 при увеличении aBS.
ЗАКЛЮЧЕНИЕ
В настоящей работе были исследованы особенности самосборки в разбавленных растворах амфифильных гомополимеров A–graft–B с сольвофобной основной цепью и сольвофильными подвесками в рамках модели мономера-“гантели” методом диссипативной динамики частиц с явным учетом селективного растворителя.
Найдены области стабильности таких самособирающихся в растворе агрегатов, как мицеллы и везикулы различной геометрии (сфера, цилиндр, диск), червеобразные разветвленные агрегаты и гелеобразные частицы, а также многослойные структуры. Все обнаруженные морфологические состояния растворов амфифильных гомополимеров суммированы в виде диаграммы в координатах параметров отталкивания между отдельными группами полимера и растворителем. Проведено сравнение морфологий растворов двух типов амфифильных гомополимеров – с сольвофобным остовом и сольвофильными подвесками и наоборот – и выявлены принципиальные различия их самосборки.
Работа выполнена при финансовой̆ поддержке Российского фонда фундаментальных исследований (код проекта 20-33-90320) и с использованием ресурсов суперкомпьютерного комплекса МГУ имени М.В. Ломоносова. Анализ данных выполнен на базе межлабораторного компьютерного центра ИНЭОС РАН при поддержке Министерства науки и высшего образования Российской Федерации.
Список литературы
Whitesides G.M., Grzybowski B. // Science. 2002. V. 295. № 5564. P. 2418.
Philp D., Stoddart J. F. // Angew. Chem. Int. Ed. Eng. 1996. V. 35. № 11. P. 1154.
Tanaka S., Kerfeld C.A., Sawaya M.R., Cai F., Heinhorst S., Cannon G.C., Yeates T.O. // Science. 2008. V. 319. № 5866. P. 1083.
Kulkarni C. V. // Nanoscale. 2012. V. 4. № 19. P. 5779.
Ariga K., Hill J.P., Lee M.V., Vinu A., Charver R., Acharya S. // Sci. Technol. Adv. Mater. 2008. V. 9. № 1 P. 014109.
Liu K., Sun Y., Cao M., Wang J., Lu J. R., Xu H. // Current Opinion Colloid Interface Sci. 2020. V. 45. P. 57.
Wang C., Wang Z., Zhang X. //Acc. Chem. Res. 2012. V. 45. № 4. P. 608.
Siddique B., Duhamel J. // Langmuir. 2011. V. 27. № 11. P. 6639.
Dreher M.R., Simnick A.J., Fischer K., Smith R.J., Patel A., Schmidt M., Chilkoti A. // J. Am. Chem. Soc. 2008. V. 130. № 2. P. 687.
Zhong T., Min L., Wang Z., Zhang F., Zuo B. // RSC Adv. 2018. V. 8. № 25. P. 13806.
Douglas S.M., Dietz H., Liedl T., Hogberg B., Graf F., Shih W.M. // Nature. 2009. V. 459. P. 414.
Hung A., Mager M., Hembury M., Stellacci F., Stevens M.M., Yarovsky I. // Chem. Sci. 2013. V. 4. № 3. P. 928.
Miller R.D., Riblet R. // Nucl. Acids Res. 1995. V. 23. № 12. P. 2339.
Mai Y., Eisenberg A. // Chem. Soc. Revs. 2012. V. 41. № 18. P. 5969.
Atanase L.I., Riess G. // Polymers. 2018. V. 10. № 1. P. 62.
Vasilevskaya V.V., Govorun E.N. // Polym. Rev. 2019. V. 59. № 4. P. 625.
Kale T.S., Klaikherd A., Popere B., Thayumanavan S. // Langmuir. 2009. V. 25. № 17. P. 9660.
Zhang J., Liu K., Mullen K., Yin M. // Chem. Commun. 2015. V. 51. № 58. P. 11541.
You J., Liu L., Huang W., Manners I., Dou H. // ACS Appl. Mater. Interfaces. 2021. V.13. № 11. P. 13648.
Guazzelli E., Masotti E., Calosi M., Kriechbaum M., Uhlig F., Galli G., Martinelli E. // Polymer. 2021. V. 231. P. 124107.
Swan S., Egermole F.O., Nguyen S.T., Kim J.-H. // Langmuir. 2020. V. 36. № 16. P. 4548.
Kimura Y., Terashima T. // Eur. Polym. J. 2020. V. 139. № 5. P. 110001.
Buglakov A.I., Larin D.E., Vasilevskaya V.V. // Polymer. 2021. V. 232. P. 124160.
Wang L.-H., Wu T., Zhang Z., You Y.-Z. // Macromolecules. 2016. V. 49. № 1. P. 362.
Baptista J.G.C., Rodrigues S.P.J., Matsushita A.F.Y., Vitorino C., Maria T.M.R., Burrows H.D., Pais A.A.C.C., Valente A.J.M. // J. Molec. Liq. 2016. V. 222 P. 287.
Vasilevskaya V.V., Khalatur P.G., Khokhlov A.R. // Macromolecules. 2003. V. 36. № 26. P. 10103.
Larin D.E., Glagoleva A.A., Govorun E.N., Vasilev-skaya V.V. // Polymer. 2018. V. 146. P. 230.
Buglakov A.I., Larin D.E., Vasilevskaya V.V. // Macromolecules. 2020. V. 53. № 12. P. 4783.
Lazutin A.A., Kosmachev A.N., Vasilevskaya V.V. // J. Chem. Phys. 2019. V. 151. № 15. P. 154903.
Glagoleva A.A., Vasilevskaya V.V. // J. Chem. Phys. 2017. V. 147. № 18. P. 184902.
Groot R.D., Warren P.B. // J. Chem Phys. 1997. V. 107. № 11. P. 4423.
Espanol P., Warren P.B. // J. Chem. Phys. 2017. V. 146. № 15. P. 150901.
Nam J., Kim Y.J., Kim J.G., Seo M. // Macromolecules. 2019. V. 52. № 24. P. 9484.
Rudyak V.Yu., Efimova E.A., Guseva D.V., Chertovich A.V. // Polymers. 2019. V. 11. № 11. P. 36.
Zhu Q., Scott T.R., Tree D.R. // Soft Matter. 2020. V. 17. № 1. P. 24.
Feng Y.H., Zhang X.P., Zhao Z.Q., Guo X.D. //Mol. Pharmaceut. 2020. V. 17. № 6. P. 1778.
Anderson R.L., Bray D.J., Ferrante S., Noro M.G., Stott I.P., Warren P.B. // J. Chem. Phys. 2017. V. 147. № 9. P. 094503.
Humphrey W., Dalke A., Schulten K. // J. Molec. Graphics. 1996. V. 14. № 1. P. 33.
Theodorou D.N., Suter U.W. // Macromolecules. 1985. V. 18. P. 1206.
Solc K., Stockmayer W.H. // J. Chem. Phys. 1971. V. 54. № 1. P. 2756.
Khalatur P.G., Khokhlov A.R., Mologin D.A., Zhelogovskaya E.A. // Macromol. Theory Simul. 1998. V. 7. № 3. P. 299.
Li B.S., Cheuk K.K.L., Yang D., Lam J.W.Y., Wan L.J., Bai C., Tang B.Z. // Macromolecules. 2003. V. 36. № 15. P. 5447.
Zhu Y., Liu L., Du J. // Macromolecules. 2013. V. 46. № 1. P. 194.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


