Высокомолекулярные соединения (серия А), 2022, T. 64, № 3, стр. 171-178
Влияние низкомолекулярных солей на набухание полиэлектролитных и амфифильных гидрогелей парных полимеров поли-N-винилпирролидона
В. Н. Кижняев a, *, Е. В. Акамова a, Ф. А. Покатилов a, О. А. Эдельштейн a
a Иркутский государственный университет
664003 Иркутск, ул. К. Маркса, 1, Россия
* E-mail: kizhnyaev@chem.isu.ru
Поступила в редакцию 11.01.2022
После доработки 07.02.2022
Принята к публикации 15.02.2022
- EDN: KPYLHU
- DOI: 10.31857/S2308112022200020
Аннотация
Продемонстрировано влияние низкомолекулярных солей (Na2SO4, KCl, NaF и NaSCN) на набухание в водных средах полиэлектролитных и амфифильных гидрогелей сетчатых парных полимеров поли-N-винилпирролидона с поли-5-винилтетразолом, полистиролом и полиметилметакрилатом. Показано, что амплитуда и характер коллапса гидрогелей определяется природой соли и составляющих парный полимер макромолекул.
Поли-N-винилпирролидон (ПВП) благодаря набору таких свойств, как водо- и биосовместимость, отсутствие токсичности, комплексообразующая способность по отношению к ионам металлов и различным органическим веществам, включая лекарственные субстанции [1], является одним из наиболее востребованных синтетических полимерных соединений медико-биологического назначения. Наиболее перспективные и универсальные материалы на основе ПВП для использования в медицинских целях – гидрогели, сочетающие наряду с перечисленными выше определенные механические и эластические свойства. Это обусловливает их использование в качестве носителей иммобилизованных лекарственных субстанций, среды для выращивания биологических тканей, и биоматериалов [2–10].
Особым направлением при разработке материалов биомедицинского применения является создание так называемых “умных” полимерных систем (включая гидрогелевые), способных направленно и обратимо изменять свои свойства под воздействием внешних факторов (состава, ионной силы, рН и температуры окружающей среды) [11–17]. Конкретный тип чувствительности задается структурой макромолекулярных цепей, формирующих пространственную сетку гидрогелевых систем. Например, введение ионогенных фрагментов обеспечивает проявление гидрогелями полиэлектролитных свойств, что выражается в существенной зависимости их степени набухания от рН и ионной силы водной среды. Подбором гидрофильно-гидрофобного баланса полимерной цепи посредством введения гидрофобных структурных фрагментов в макромолекулы водосовместимых полимеров получают термочувствительные гидрогелевые системы. В случае полимерных сеток на основе ПВП существуют различные варианты придания им полиэлектролитных или амфифильных свойств, например синтез блок-сополимерных сеток (“conetworks”), содержащих между узлами сшивки цепочечные фрагменты различных по сродству к воде макромолекул [18] или прививочная полимеризация N-винилпирролидона на готовый гомополимер [19]. Наиболее популярный подход к получению полиэлектролитных или амфифильных сеток – сшивание макромолекул ПВП с макромолекулами гомополимеров ионогенной или гидрофобной природы посредством инициаторов радикальных процессов [20], ультразвуковым воздействием [21], а также действием УФ- или радиационного облучения [22–29]. Частным случаем сшивания полимерных цепей двух различных линейных гомополимеров служат процессы реакционного смешения, приводящие к образованию так называемых парных полимеров [30]. Формирование пространственной сетки происходит в результате взаимодействия обладающих химическим сродством “якорных” функциональных групп, расположенных случайным образом в структуре разнородных макромолекул, что приводит к их ковалентному связыванию. Подобным образом на основе ПВП, модифицированного введением в структуру небольшого количества “якорных” оксирановых циклов, получены сетчатые парные полимеры с ионогенным поли-5-винилтетразолом (ПВТ), гидрофобными ПС и ПММА, макромолекулы которых содержат небольшое количество “якорных” N–H незамещенных тетразольных циклов [31]. В водной среде указанные парные полимеры ограниченно набухают с образованием полиэлектролитных и амфифильных гидрогелей, проявляющих рН- и термочувствительность. Можно ожидать, что на состояние подобного типа гидрогелевых систем существенное влияние будет оказывать и присутствие в водной среде низкомолекулярных солей. Тем более, водные системы линейных ПВТ и ПВП в присутствии солей претерпевают критические изменения. Так, водные растворы ПВП, существующие однофазными в диапазоне температур 0–100оС, при добавлении ряда низкомолекулярных солей приобретают критические температуры фазового разделения (НКТР) [32, 33], а не растворимый в воде ПВТ становится растворимым в водно-солевых средах [34].
В настоящей работе представлены результаты исследования влияния различных низкомолекулярных солей на поведение в водно-солевых средах гидрогелей сетчатых парных полимеров ПВП ионогенной и амфифильной природы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали гидрогели парных полимеров ПВП с ПВТ, ПС и ПММА, которые синтезировали в соответствии с методикой [31] реакционным смешением указанных полимеров, модифицированных посредством введения в их макромолекулы небольших количеств ”якорных” функциональных групп. В качестве полимерных реагентов для реакционного смешения были выбраны образцы ПВП, содержащего 0.09 мол. долей мономерных звеньев 2-(винилоксиэтокси)метилоксирана, ПВТ, представляющего собой сополимер 5-винилтетразола с акрилонитрилом эквимольного состава, ПС и ПММА, содержащие в своей структуре 0.06 и 0.05 мол. долей звеньев 5-винилтетразола соответственно:
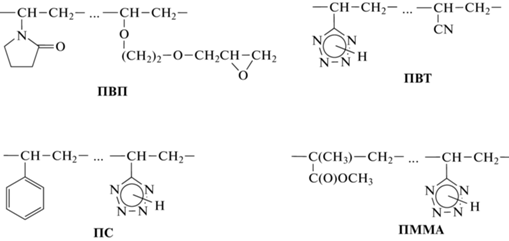
Ковалентное связывание разнородных макромолекул и формирование сетчатой структуры парных полимеров ПВП с ПВТ, ПС и ПММА является результатом реакции между “якорными” оксирановыми и тетразольными циклами. Синтез парных полимеров осуществляли ампульным методом в среде ДМФА при разном соотношении, но одинаковой суммарной концентрации полимерных реагентов 10 г/дл, при температуре 80°С. Реакция между полимерами сопровождалась гелеобразованием системы. Для завершения процесса формирования парного полимера реакционную массу после момента потери текучести системой выдерживали еще в течение недели при указанной температуре. Остаточное количество непрореагировавших исходных полимерных реагентов из полученных гелей удаляли вымыванием ДМФА. С целью получения гидрогелей парных полимеров набухшие в ДМФА гели выдерживали в течение трех недель под периодически заменяемой дистиллированной водой до равновесного набухания. В случае парного полимера ПВП с ПВТ подобным образом получали гидрогели, содержащие неионизованные тетразольные фрагменты. С целью перевода кислотных N–Н незамещенных тетразольных циклов в солевую форму образцы гидрогелей погружали в 0.1 М водный раствор NaOH до равновесного набухания, после чего ионизованный гидрогель выдерживали в течение недели под периодически заменяемой дистиллированной водой до нейтральной рН реакции промывных вод.
Низкомолекулярные соли Na2SO4, KCl, NaF, NaSCN квалификации х.ч. использовали без дополнительной очистки. Для изучения влияния низкомолекулярных солей на поведение гидрогелей парных полимеров в водно-солевых средах навеску набухшего в дистиллированной воде гидрогеля помещали в раствор соли известной концентрации и выдерживали при заданной температуре до равновесного набухания. Сорбционную способность полимерных образцов по отношению к водным средам характеризовали коэффициентом набухания Кнаб, который определяли гравиметрическим методом и вычисляли по формуле
где mг и mп – масса равновесно набухшего гидрогеля и сухого полимера соответственно. Гравиметрические измерения выполняли на весах “Ohaus Pioneer” (точность ±0.1 мг). Требуемую температуру при исследовании процессов набухания поддерживали воздушным термостатом (точность термостатирования ±0.5°С).РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Реакционным смешением неионогенного, водорастворимого ПВП с ионизующимся полимером ПВТ и гидрофобными полимерами ПС и ПММА были получены сетчатые парные полимеры, склонные к ограниченному набуханию в воде с образованием гидрогелей. Степень набухания подобных гидрогелей определяется как соотношением, так и природой второго компонента парного полимера. Сорбционная способность по отношению к воде парных полимеров ПВП с ПВТ в неионизованном и ионизованном состоянии снижается по мере увеличения в структуре доли неионогенных макромолекул ПВП (рис. 1, кривые 1, 2). Ионизация макромолекулярных цепей ПВТ посредством перевода тетразольных фрагментов в форму натриевой соли способствует двукратному возрастанию водопоглощения гидрогелями. В случае парных полимеров ПВП с гидрофобными ПС и ПММА, наоборот, повышение содержания макромолекул ПВПД сопровождается увеличением степеней набухания гидрогелей (рис. 1, кривые 3, 4). Полиэлектролитный характер гидрогелей парного полимера ПВП–ПВТ проявляется и в возрастании значений степеней набухания с повышением температуры (рис. 2, кривые 1, 2). При этом с увеличением доли макромолекул ионогенного компонента (ПВТ) в структуре парного полимера амплитуда изменения набухания с температурой более существенна. Амфифильная природа гидрогелей парных полимеров ПВП с ПС и ПММА обусловливает обратную температурную зависимость (рис. 2, кривые 3, 4). Водопоглощение гидрогелей с повышением температуры уменьшается вследствие усиления гидрофобных взаимодействий между структурными фрагментами полимерных цепей.
Рис. 1.
Степень набухания гидрогелей парных полимеров ПВП–ПВТ в неионизованной (1) и ионизованной форме (2), ПВП–ПС (3) и ПВП–ПММА (4) в воде при 25°С в зависимости от массовой доли ПВП в парном полимере.
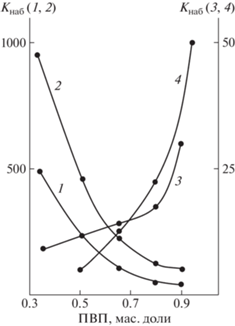
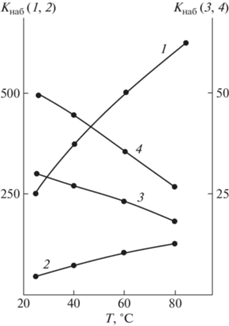
Рис. 2.
Степень набухания гидрогелей парных полимеров ПВП–ПВТ состава 1 : 1 (1) и 9 : 1 (2), ПВП–ПС (3) и ПВП–ПММА (4) состава 9 : 1 в воде в зависимости от температуры среды.
Отличия в природе компонентов полученных парных полимеров на основе ПВП сказываются и в реакции их гидрогелей на введение в водную среду различных низкомолекулярных солей. В случае полиэлектролитных гидрогелей парного полимера ПВП–ПВТ присутствие Na2SO4 в воде в уже незначительной концентрации (0.005 моль/л) вызывает резкий коллапс геля (рис. 3). Амплитуда изменения степени набухания в водно-солевом растворе возрастает с увеличением доли макромолекул ионогенного ПВТ в структуре парного полимера (кривые 1, 3), а также при ионизации макромолекул ПВТ (кривые 2, 4). В диапазоне концентраций водного раствора Na2SO4, равном 0.01–0.05 моль/л, водопоглощение практически не меняется. Подобная реакция на изменение концентрации низкомолекулярного электролита типична для полиэлектролитных гидрогелей [13]; низкое содержание соли обусловливает выраженный коллапс гелей, при достижении определенного содержания соли в водном растворе степень набухания достигает своего минимума и при дальнейшем увеличении концентрации соли практически не изменяется. Аналогичное поведение гидрогелей парного полимера ПВП–ПВТ наблюдается и в присутствии в водном растворе других солей – KCl, NaF и NaSCN; отличие только в интенсивности эффекта уменьшения степени набухания гелей. Так, наиболее резкий коллапс полиэлектролитных гидрогелей вызывает добавление Na2SO4, в меньшей степени KCl и наименьший NaF (рис. 4). Однако влияние всех указанных солей на набухание гидрогелей усиливается с увеличением доли макромолекул ионогенного ПВТ в структуре парного полимера. В этом плане несколько неожиданным представляется влияние NaSCN на количественные стороны набухания гидрогелей парного полимера ПВП–ПВТ. При преобладающем содержании в парном полимере макромолекулярных цепей ионогенного ПВТ эффект, создаваемый роданидом, соизмерим с действием на гидрогели добавок KCl (рис. 4). Влияние на набухание гидрогелей парного полимера с наибольшим содержанием в структуре макромолекул ПВП сопоставимо с действием NaF. Однако эффект коллапсирования гидрогелей в присутствии Na2SO4, KCl и NaF вполне предсказуем, поскольку указанные соли оказывают дестабилизирующее действие на водные растворы ПВП и полиэлектролитов, уменьшая термодинамическую совместимость между водой и растворенным полимером. В водных растворах ПВП добавление подобных солей приводит даже к появлению критической температуры фазового разделения (НКТР) [32, 33]. В случае водонаполненных сетчатых структур это проявляется в виде коллапса гидрогелей. Как для гидрогелевых систем, так и для полимерных растворов сильнее всего влияет Na2SO4, который среди изученных солей имеет наиболее выраженный высаливающий эффект по отношению к растворенному полимеру. Присутствие NaF, обладающего наименьшим дестабилизирующим действием на водно-полимерные системы, сопровождается менее существенными изменениями параметров системы. Роданид натрия (NaSCN) относится к другому типу солей, которые оказывают на водные растворы ПВП и ПВТ обратное действие улучшения совместимости растворителя и растворенного вещества (т.е. “всаливающий эффект”). Так, не растворимый в воде в неионизованном состоянии ПВТ растворим в водных растворах NaSCN [34]. В связи с этим от роданида можно было ожидать противоположного с Na2SO4, KCl и NaF действия на гидрогели парного полимера ПВП–ПВТ. Вероятно, при изученных (относительно невысоких) концентрациях вводимых солей в поведении гидрогелей превалирует их полиэлектролитная природа, обусловливающая коллапс гелей в присутствии низкомолекулярных электролитов [13]. Амфифильные гидрогели парных полимеров ПВП с ПС и ПММА с преобладанием в структуре макромолекулярных цепей ПВП также реагируют на присутствие низкомолекулярных электролитов, но при гораздо больших концентрациях солей и с меньшей амплитудой снижения степеней набухания, нежели полиэлектролитные гидрогели. И их поведение в водно-солевых средах в большей степени коррелирует с влиянием солей на водные растворы гомополимера ПВП [32]. Наиболее сильно коллапс гидрогелей проявляется в водных растворах Na2SO4, причем степень набухания монотонно понижается по мере увеличения концентрации соли (рис. 5, кривые 1, 4). В меньшей степени коллапс гидрогелей выражен в водных растворах KCl и, начиная с концентрации соли в водном растворе 0.25 моль/л перестает изменяться (рис. 5, кривые 2, 5). Зависимость степени набухания гидрогелей в водном растворе NaSCN в изученном диапазоне концентраций соли носит экстремальный вид с минимумом водопоглощения при 0.25 моль/л. При концентрации солевого раствора 1 моль/л значения степени набухания гидрогелей вновь достигают величин, соответствующих набуханию в бессолевой среде (рис. 5, кривые 3, 6). Таким образом, при определенной концентрации NaSCN, начинает проявляться “всаливающий эффект” низкомолекулярной соли по отношению к парным полимерам, что способствует возрастанию водопоглощения гидрогелями.
Рис. 3.
Степень набухания гидрогелей парных полимеров ПВП–ПВТ состава 1 : 1 (1, 2) и 9 : 1 (3, 4) при 25°С в водных растворах Na2SO4 в зависимости от концентрации соли в воде. Неионизованная (1, 3) и ионизованная (2, 4) форма парного полимера.
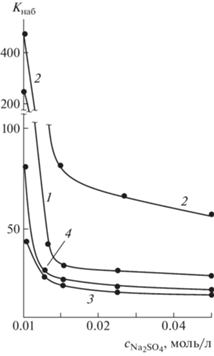
Рис. 4.
Отношение степеней набухания в водно-солевом растворе и чистой воде Кнаб (сол.)/Кнаб (вода) гидрогелей парных полимеров ПВП–ПВТ при 25°С в зависимости от массовой доли ПВП в парном полимере. Концентрация соли в водно-солевом растворе 0.01 моль/л. 1 – NaF, 2 – NaSCN, 3 – KCl, 4 – Na2SO4.
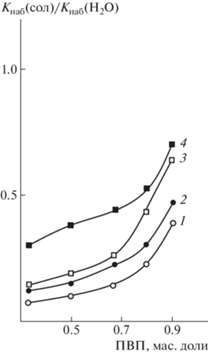
Рис. 5.
Степень набухания гидрогелей парных полимеров ПВП–ПС (1–3) и ПВП–ПММА состава 9 : 1 (4–6) при 25°С в водно-солевых растворах в зависимости от концентрации соли. 1, 4 – Na2SO4; 2, 5 – KCl; 3, 6 – NaSCN.
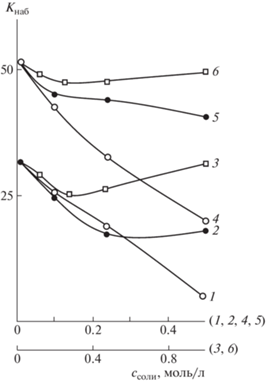
Отличия в природе полученных на основе ПВП парных полимеров и присутствующих в водной среде низкомолекулярных солей сказываются и на поведении гидрогелей в водно-солевых средах при варьировании температуры. Так, для полиэлектролитных гидрогелей парного полимера ПВП–ПВТ состава 1 : 1 в водных растворах Na2SO4, KCl и NaF, как и в отсутствие низкомолекулярной соли, характерно возрастание степени набухания с повышением температуры среды (рис. 6, кривые 1–3). Если в водном растворе присустствует NaSCN, то температура не влияет на водопоглощение указанного гидрогеля (рис. 6, кривая 4). В случае гидрогеля парного полимера ПВП–ПВТ с преобладанием в структуре макромолекулярных цепей неионогенного ПВП незначительная температурная зависимость водопоглощения наблюдается для всех изученных солей (рис. 6, кривые 5–8). Вероятно, в отличие от бессолевой среды в водно-солевых растворах для данного гидрогеля в большей степени проявляется влияние гидрофобных взаимодействий фрагментов полимерных цепей, усиливающихся с повышением температуры и препятствующих набуханию геля.
Рис. 6.
Степень набухания гидрогелей парных полимеров ПВП–ПВТ состава 1 : 1 (1–4) и 9 : 1 (5–8) в водно-солевых растворах в зависимости от температуры среды. Концентрация соли в водно-солевом растворе 0.01 моль/л. 1, 5 – Na2SO4; 2, 6 – KCl; 3, 7 – NaF; 4, 8 – NaSCN.
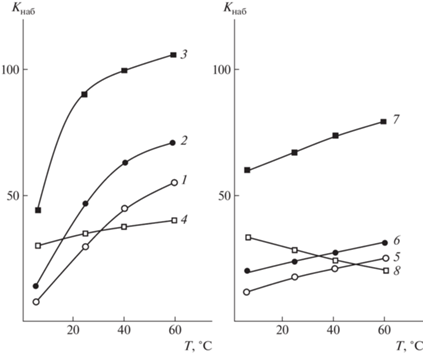
Температурная зависимость водопоглощения амфифильными гидрогелями парных полимеров ПВП с ПС и ПММА в водно-солевых средах, как и в бессолевых, характеризуется уменьшением значений степеней набухания с повышением температуры. Однако в водных растворах KCl и NaSCN амплитуда изменения водопоглощения меньше, чем в отсутствие соли (рис. 7, кривые 7–14).
Рис. 7.
Степень набухания гидрогелей парных полимеров ПВП–ММА (1–3, 11–14) и ПВП–ПС состава 9 : 1 (4–6, 7–10) в водно-солевых растворах в зависимости от температуры среды. Концентрация растворов солей 0.1 (1, 4, 7, 11), 0.25 (2, 5, 9, 13), 0.5 (3, 6, 8, 12) и 1.0 моль/л (10, 14). 1–6 – Na2SO4; 7, 8, 11, 12 – KCl; 9, 10, 13, 14 – NaSCN.
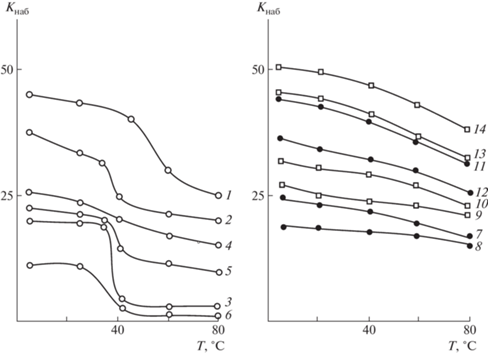
В водных растворах Na2SO4, начиная с концентрации соли 0.25 моль/л, для обоих типов гидрогелей проявляется скачкообразное уменьшение степеней набухания в диапазоне температур 35–40°С (рис. 7, кривые 1–6). С повышением концентрации соли резкий коллапс гидрогелей становится более выраженным, причем для парного полимера ПВП–ПММА в большей степени. В бессолевой среде подобного эффекта не наблюдали. Вероятно, присутствие в водном растворе сульфата натрия способствует не только усилению, но и проявлению кооперативности гидрофобных взаимодействий структурных фрагментов полимерной сетки при определенной температуре, что и приводит к резкому коллапсу гидрогеля.
Таким образом, в работе изучено влияние низкомолекулярных солей (Na2SO4, KCl, NaF и NaSCN) на количественные характеристики набухания гидрогелей парных полимеров ПВП полиэлектролитной и амфифильной природы. Продемонстрировано, что для обоих типов гидрогелей наиболее выраженный эффект коллапсирования вызывает присутствие в водной среде Na2SO4, что находится в согласии с результатами влияния указанных солей на водные растворы линейного ПВП [32]. Более того, в присутствии Na2SO4 для амфифильных гидрогелей парных полимеров ПВП с ПММА и ПС отмечен резкий коллапс в узком диапазоне температур. Подобный эффект резкого изменения характеристик полимера (в данном случае степени набухания) при незначительном изменении внешних условий является характерной чертой так называемых “умных” полимерных систем [11]. Несколько необычным представляется влияние NaSCN, вызывающее коллапс полиэлектролитных гидрогелей парного полимера ПВП–ПВТ, несмотря на то, что данная соль в водном растворе оказывает “всаливающее” действие на исходные гомополимеры (ПВП и ПВТ) и даже на полиакрилонитрил, мономерные звенья которого присутствуют в образце тетразолсодержащего полимера. Вероятно, это связано с особенностями диффузии ионов указанной соли в полимерную матрицу и различной концентрацией соли внутри и снаружи набухшего гидрогеля.
Работа выполнена в рамках базовой части государственного задания в сфере научной деятельности Министерства образования и науки Российской Федерации (соглашение № 075-03-2020-176/3; код проекта в Парусе 8: FZZE-2020-0022).
Список литературы
Kirsh Y.E. Water Soluble Poly-N-vinylamides. Weinheim: Wiley-VCH, 1998.
Risbud M., Hardikar A., Ramesh Bhonde R. // Cell Transplant. 2000. V. 9. P. 25.
Doria-Serrano M.C., Riva-Palacio G., Ruiz-Trevin F., Hernandez-Esparza A.M. // Ind. Eng. Chem. Res. 2002. V. 41. P. 3163.
Wei Q., Luo Y., Ga L., Wang Q., Wang D. // Polymer Science A. 2011. V. 53. № 8. P. 707.
Young-Chang Nho, Youn-Mook Lim, Hui-Jeong Gwon, Eun-Kyung Choi // Korean J. Chem. Eng. 2009. V. 26. № 6. P. 1675.
Offenbrite R.M., Park K., Okano T. Biomedical Applications of Hydrogels Handbook. New York: Springer, 2010.
Ozay H., Kubilay S., Aktas N., Sahiner N. // Int. J. Polym. Mater. Polym. Biomater. 2011. V. 60. № 2. P. 163.
Ahmad B., Abbas S., Iqbal Z., Bashir Sh., Ali J. // Middle-East J. Sci. Res. 2013. V. 14. № 2. P. 273.
Husain M.S.B., Gupta A., Alashwal B.Y., Sharma S. // Energ. Sources. A. 2018. V. 40. № 20. P. 2388.
Oliver-Urrutia C., Ibañez R.R., Flores-Merino M.V., Vojtova L., Salplachta J., Čelko L., Kaiser J., Montufar E.B. // Materials. 2021. V. 14. № 1. P. 227.
Philippova O.E. // Polymer Science C. 2000. V. 42. № 2. P. 208.
Aseyev V.O., Tenhu H., Winnik F. M. // Adv. Polym. Sci. 2006. V. 196. P. 1.
Kramarenko E.Yu., Philippova O.E., Khokhlov A.R. // Polymer Science C. 2006. V. 48. № 1. P. 1.
Chaterji S., Kwon I.K., Park K. // Prog. Polym. Sci. 2007. T. 32. C. 1083.
Galaev I., Mattiasson B. Smart Polymers: Applications in Biotechnology and Biomedicine. New York: CRC Press, 2007.
Starodubtsev S.G., Vasilevskaya V.V., Khokhlov A.R. // Smart Polymers: Applications in Biotechnology and Biomedicine, Second Edition / Ed. by I. Galaev, B.O. Mattiasson. London; New York: CPC Press, 2008. P. 81.
Philippova O.E., Khokhlov A.R. // Polymer Science: A Comprehensive Reference/ Ed. by K. Matyjaszewski, M. Möller. Amsterdam: Elsevier, 2012. V. 1. P. 339.
Erdodi G., Kennedy J.P. // Progr. Polym. Sci. 2006. V. 31. № 1. P. 1.
Skorokhoda M., Melnyk Yu., Semenyuk N., Ortynska N., Suberlyak O. // Chem. Chem. Technol. 2017. V. 11. № 2. P. 171.
Lakouraj M.M., Tajbakhsh M., Mokhtary M. // Iranian Polym. J. 2005. V. 14. № 12. P. 1022.
Bonelli N., Poggi G., Chelazzi D., Giorgi R., Baglioni P. // J. Coll. Int. Sci. 2019. V. 536. P. 339.
Lope’rgolo L.C., Luga A.B., Catalani L.H. // Polymer. 2003. V. 44. P. 6217.
Kadłubowski S., Henke A., Ulański P., Rosiak J.M., Bromberg L., Hatton T.A. // Polymer. 2007. V. 48. P. 4974.
Dergunov S.A., Mun G.A. // Radiat. Phys. Chem. 2009. V. 78. № 1. P. 65.
Abd El-Mohdy H.L., Ghanem S. // J. Polym. Res. 2009. V. 16. P. 1.
Kadłubowski S., Henke A., Ulański P., Rosiak J. M. // Radiat. Phys. Chem. 2010. V. 79. № 3. P. 261.
Hill D.J.T., Whittaker A.K., Zainuddin // Radiat. Phys. Chem. 2011. V. 80. № 2. P. 213.
Dafader N.C., Tahmina Akter, Haque M.E., Swapna S.P., Sadia Islam, Huq D. // African J. Biotechnol. 2012. V. 11. № 66. P. 13049.
Abd El-Wahab H., Ghobashy1 M.M., Nady N., Naser A.M., Abdelhai F., El-Damhougy B.Kh. // Azhar Bull. Sci. 2018. V. 29. № 2. P. 1.
Askadskii A.A. // Russ. Chem. Rev. 1999. V. 68. № 4. P. 317.
Kizhnyaev V.N., Pokatilov F.A., Akamova E.V. // Polymer Science B. 2020. V. 62. №. 5. P. 483.
Nakhmanovich B.I., Pakuro N.I., Akhmet’eva E.I., Litvinenko G.I., Arest-Yakubovich A.A. // Polymer Science B. 2007. V. 49. № 5–6. P. 136.
Pakuro N.I., Nakhmanovich B.I., Pergushov D.V., Chibirova F.Kh. // Polymer Science A. 2011. V. 53. № 1. P. 6.
Kizhnyaev V.N., Pokatilov F.A., Vereshchagin L.I. // Polymer Science C. 2008. V. 50. № 1. P. 1.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


