Высокомолекулярные соединения (серия А), 2022, T. 64, № 6, стр. 441-451
МОДЕЛЬ АТОМНО-МОЛЕКУЛЯРНОЙ СТРУКТУРЫ НИТРАТОВ ЦЕЛЛЮЛОЗЫ ИЗ MISCANTHUS SACCHARIFLONIS
А. И. Прусский a, *, Л. А. Алешина a, И. В. Люханова a, О. В. Сидорова a, В. В. Будаева b, Г. В. Сакович b
a Петрозаводский государственный университет
185910 Петрозаводск, пр. Ленина, 33, Россия
b Институт проблем химико-энергетических технологий Сибирского отделения Российской академии наук
659322 Бийск, ул. Социалистическая, 1, Россия
* E-mail: prusskiiandrey@gmail.com
Поступила в редакцию 07.07.2022
После доработки 13.10.2022
Принята к публикации 25.10.2022
- EDN: KTSXRF
- DOI: 10.31857/S2308112022700274
Аннотация
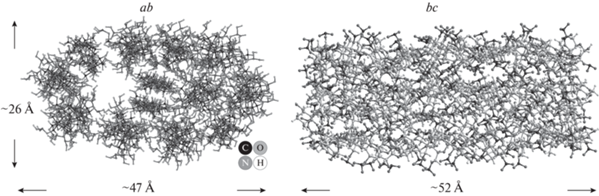
Опираясь на результаты рентгеновского дифракционного эксперимента, методом компьютерного моделирования с использованием программы HyperChem8 была построена атомно-молекулярная конфигурация в области ближнего упорядочения аморфной нитроцеллюлозы из мискантуса. Показано, что расположение атомов в области ближнего порядка в аморфной нитроцеллюлозе удовлетворительно описывается кластером, который содержит девять цепочек нитроцеллюлозы и две цепочки целлюлозы I, закрученных на угол 72°, и две незакрученные цепочки целлюлозы I. Каждая цепочка включает в себя десять глюкозных остатков. В итоговом кластере указанные выше цепочки образуют приблизительно гексагональный слой в проекции на плоскость ab с расстоянием между ними 12.2 Å. В проекции на плоскость bc конечный кластер имеет размеры 28 Å вдоль оси b и 54 Å вдоль оси c. Общее количество атомов 3300, степень полимеризации равна 130; формульная единица асимметричного фрагмента [C6H7.24O2(OH)0.92(ONO2)2.08]130. Достоверность результата доказана совпадением экспериментальной и рассчитанной для кластера кривых распределения интенсивности рентгеновского рассеяния I(s) с точностью до 7.5%.
ВВЕДЕНИЕ
Нитраты целлюлозы широко используются с одной стороны как компоненты твердого ракетного топлива и порохов, с другой – как составляющие лакокрасочных материалов, мембраны для иммобилизации белков [1–3]. В последнее десятилетие выполнено большое количество работ по исследованию нитратов, синтезированных из целлюлозы быстро воспроизводимого сырья: плодовых оболочек овса [4], мискантуса [5–7], целлюлозы травы альфа (эспарто, или ковыль) [8], бурых водорослей Posidonia oceanica [9] и хлопка [10]. Эти исследования показали, что физико-химические свойства нитратов зависят от качества и природы исходной целлюлозы и способа нитрования. Полная характеризация структуры альтернативных хлопковым нитратов целлюлозы является фундаментальной задачей и раскрывает сходство и различие этих эфиров, полученных из разных источников.
Одним из методов изучения структуры материалов – метод рентгеновской дифракции. Рентгеновские дифракционные картины нитратов целлюлозы, синтезированных разными способами и из различных видов целлюлозы, качественно однотипны и представляют собой диффузный максимум, на фоне которого наблюдается отражение от кристаллической фазы в области углов рассеяния 2θCu ~ 12°–13° [1–3, 8–19].
Изменения рентгенограмм, полученных фотографическим методом в процессе нитрации целлюлозы Рами, были исследованы в серии работ японских авторов в 1968–1973 гг. [20–24].
Аналогичные дифрактометрические исследования были выполнены в 2006 г. на образцах бактериальной целлюлозы [15], в 2016 г. – на промышленных целлюлозах различного происхождения, включая хлопковую [19], и в 2019 г. на хлопковой целлюлозе [2]. В результате было показано, что в начале процесса нитрации целлюлозы происходит ее аморфизация, о чем свидетельствует размытие и постепенное исчезновение отражений от кристаллической фазы целлюлозы на рентгенограммах и появление широкого диффузного максимума. Затем с увеличением времени нитрации появляется отражение от кристаллической компоненты, классифицированное авторами работ [15, 19, 22, 24] как линия (110) тринитрата целлюлозы.
Строение молекулярной цепочки тринитрата целлюлозы предсказали в работе [24], опираясь на анализ меридиональной рентгенограммы и данные поляризационной ИК-спектроскопии. Длина цепочки (период идентичности вдоль оси фибриллы) составляла 2.54 нм. Было установлено, что винтовая ось симметрии цепочки тринитрата − это ось 52, т.е. на 2 витка спирали приходится 5 элементарных звеньев (глюкозных остатков).
Позднее в работе [25] авторы сгенерировали асимметричную единицу цепочки в модели связанных атомов. При построении атомной модели использовали известные стереохимические параметры планарной группы ОNО2. В процессе релаксации модели подбирались углы связи O–NO2 (в пределах от 109.5° до 120°). Все остальные величины длины и углов связей были постоянны, в том числе и угол гликозидной связи, принятый равным 116.6°. Из асимметричных единиц с конформацией гош-транс были построены молекулы тринитрата целлюлозы с осью симметрии спирали 52. Длина молекулы соответствовала периоду идентичности, определенному в работе [24]. Упаковка молекул в элементарную ячейку выполнялась в работе [25] для двух ячеек, различающихся размерами периода b: a = 0.90 нм, b = 1.224 нм, с = 2.54 нм и a = 0.90 нм, b = 1.46 нм, с = 2.54 нм. Эти данные согласуются с результатами других авторов, приведенными в работе [26].
Значения межплоскостных расстояний и индексов отражений для модели кристаллического тринитрата целлюлозы сравнивали с экспериментальными данными, рассчитанными по рентгенограмме высокоориентированных фибрилл (СN = 13.9%). Рентгенограмма была получена фотометодом на медном излучении с никелевым фильтром. Анализируя возможность размещения молекул тринитрата в элементарной ячейке, авторы [25] установили, что, если разместить молекулы (конформация гош-транс) в углах и в центрах граней гранецентрированной ромбической элементарной ячейки с периодом b = 14.6 Å, то упаковка получается приблизительно гексагональная. При этом молекулы хаотически ориентированы (развернуты вокруг оси фибриллы) относительно друг друга. Как указывали авторы [25], модель кристаллического тринитрата целлюлозы нельзя было считать окончательной, так как наблюдались короткие расстояния между атомами соседних молекул.
Структура аморфной нитроцеллюлозы до сих пор не исследовалась. Ряд работ, выполненных в последние годы методом молекулярной динамики, имел своей целью изучение следующих процессов: диффузия пластификатора [27] в нитроцеллюлозе, перемешивание в смесях нитроцеллюлозы с жидкими этанолом или диэтиловым эфиром [28], проникновение салициловой кислоты через нитроцеллюлозную мембрану [29], влияние смешанных пластификаторов (нитроглицерина/триацетата глицерина) на пластифицирующую способность нитроцеллюлозы [30]; динамическая механическая релаксация нитроцеллюлозы, пластифицированной N-бутил-N-(2-нитроксиэтил)нитрамином (NC/Bu-NENA) [31].
В работах [27–29] на начальном этапе работы строились модели цепочек нитроцеллюлозы, в основе которых была предложенная авторами [25] асимметричная единица. Длина цепочек была различной в разных работах, цепочки оптимизировались геометрически, а затем транслировались в двух направлениях для построения таким образом, чтобы плотность кластера лежала в пределах от 1.49 [29] до 1.619 г/см3 [27].
В работе [30] молекулярные конфигурации как чистой нитроцеллюлозы, так и ее смеси со сложными пластификаторами были сконструированы как аморфные системы без конкретного анализа атомно-молекулярной конфигурации в области ближнего упорядочения.
В работе [31] построенные с помощью Material Studio (Accelrys) две молекулярные цепи нитроцеллюлозы со степенью замещения 11.6%, представляли собой крупные фрагменты гауссовых цепей, состоящие из 320 и 240 димерных единиц нитроцеллюлозы соответственно.
Основное внимание в работах [27–31] уделялось процессам проникновения реагентов внутрь матрицы нитроцеллюлозы, построенной тем или иным способом, при этом структура нитроцеллюлозы в исходном состоянии не анализировалась.
Цель настоящей работы – исследование расположения молекул в области ближнего упорядочения аморфной составляющей нитроцеллюлозы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Рентгенографический эксперимент и обработка данных
Исходное сырье (целлюлоза мискантуса) представляло собой целлюлозу Iβ. Значения периодов элементарной ячейки: а = 0.778(3) нм, b = = 0.812(2) нм, c = 1.054(1) нм, угол моноклинности γ = 96.3(2)° [32]. Синтезированная из нее нитроцеллюлоза по данным химического анализа имеет степень замещения 2.29 [7].
Дифрактограммы образцов нитроцеллюлозы регистрировались на дифрактометрах ДРОН-3 и ДРОН-6 на излучениях Cu и МоKα в геометриях на отражение и прохождение.
Из пересчитанных в электронные единицы данных эксперимента, выполненного на излучении МоKα, методом Финбака–Уоррена рассчитывались кривые распределения s-взвешенной интерференционной функции H(s) и затем парных функций D(r). Методика расчета представлена в работах [33, 34].
Рассчитанные методом Финбака кривые D(r) характеризуют распределение электронной плотности материала и позволяют найти координационные числа Nij (число атомов j, центры которых находятся на расстоянии rij ± σij от атома i, образуя сферу, которая называется координационной) методом наименьших квадратов, применяя СВД-разложение для повышения устойчивости решения [33, 34]. Радиусы rij (средние значения расстояний между атомом i и атомами j, находящимися от атома i на расстоянии rij) и размытия σij (дисперсия межатомных расстояний относительно среднего значения rij) координационных сфер устанавливаются методом последовательных приближений, используя в качестве исходных данных значения, полученные для полиморфных модификаций исследуемого соединения [7, 33]. Для нитроцеллюлозы стартовыми значениями радиусов и размытий координационных сфер служили соответствующие данные для предложенной в работах [24, 25] модели кристаллической фазы тринитрата целлюлозы.
Методика построения компьютерных моделей
На рентгенограммах исследуемых образцов нитроцеллюлозы наряду с размытым максимумом рассеяния аморфной компонентой наблюдается линия, классифицируемая в многочисленных исследованиях как отражение (110) от кристаллической фазы тринитрата целлюлозы. Выполненные нами расчеты показали, что количество ее в аморфной матрице исследуемой нитроцеллюлозы порядка 5%. Кроме того, линия тринитрата наблюдается в области начальных углов рассеяния и не оказывает влияния на ход кривых H(s) и D(r).
В связи с этим под аморфным объектом будем понимать такое структурное состояние, в котором аморфная составляющая заметно превалирует над кристаллической.
Используя теоретические представления о структуре нитроцеллюлозы (асимметрические структурные единицы нитроцеллюлозы, параметры элементарных ячеек для целлюлозы и тринитрата нитроцеллюлозы с различным содержанием нитрогрупп), которые описывают объект как кристаллическое вещество, мы создавали упорядоченные конфигурации, в которых затем можно было бы разрушить порядок в расположении атомов тем или иным способом.
Построение атомно-молекулярной конфигурации в области ближнего упорядочения нитроцеллюлозы выполнялось с помощью программного комплекса HyperChem8 с использованием силового поля Mm+.
С помощью данного комплекса геометрическая оптимизация полученных кластеров производилась методом Полака–Рибьера [33, 35].
Ранее в работах [7, 33] было успешно выполнено построение атомно-молекулярных моделей для аморфной регенерированной лиственной целлюлозы, этилцеллюлозы [34] и лиофильно-высушенных гидрогелей на основе лиственной целлюлозы [34]. Все указанные объекты характеризовались диффузными дифракционными картинами.
Построение атомно-молекулярной конфигурации в каждом случае начиналось с построения исходной модели на основе известных кристаллографических данных для кристаллических модификаций целлюлозы. В результате исходные модели представляли собой кристаллиты целлюлозы, размеры которых определялись числом трансляций элементарной ячейки по кристаллографическим осям.
Построение исходной модели нитроцеллюлозы – процесс гораздо более сложный. Авторами в работе [25] получены промежуточные значения кристаллографических параметров расположения молекул в кристалле тринитрата. Кроме того, в работе [25] приведены размеры элементарной ячейки (два варианта [25, 26]) и координаты повторяющихся асимметричных структурных единиц, представляющих собой глюкозный остаток с нитрогруппами в гош-гош, гош-транс и транс-гош конформациях [25] (рис. 1).
Рис. 1.
Модели асимметричных структурных единиц молекулы тринитрата целлюлозы в конформации нитрогрупп гош-гош (а), гош-транс (б) и транс-гош (в), с указанной нитрогруппой (г) [25].
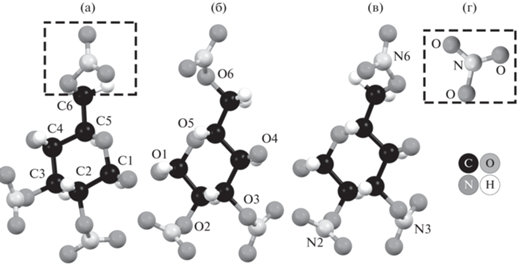
На начальном этапе была построена единичная цепочка целлюлозы длиной, равной длине пяти глюкозных остатков, в которой гидроксильные группы ОН углеродов С2, С3 и С6 (рис. 1а, 1б) были заменены на нитрогруппы (рис. 1г).
Как отмечает автор [26], в молекулах нитроцеллюлозы со степенью замещения меньше трех угол закручивания спирали может лежать в диапазоне от 180° для целлюлозы (винтовая ось второго порядка 21) до 144° для нитроцеллюлозы (винтовая ось пятого порядка 52). В последнем случае каждая асимметричная единица поворачивается на 72° относительно соседней (левый винт) [24].
При скручивании молекулы нитроцеллюлозы цепочка целлюлозы с нитрогруппами разбивалась на целое число фрагментов n, в состав которых входило целое число асимметричных единиц. Поворот каждого участка на угол α производился таким образом, чтобы первый и последний участок цепочки составляли заданный угол θ = nα, где n – целое число. Угол разворота θ можно было варьировать от 0° до 360° с шагом 1°.
При построении моделей из двух и более цепочек учитывалось также, что наилучший результат в работе [25] отвечал антипараллельному расположению соседних цепочек, а упаковка элементарных ячеек такова, что образуется приблизительно гексагональная конфигурация молекул. Размеры моделей изменялись путем трансляции вдоль осей x, y, z ромбической элементарной ячейки c периодами a = 0.90 нм, b = 1.39 нм, c = = 2.56 нм [25]. В данной работе число трансляций вдоль осей x и y варьировалось от 1 до 5, а вдоль оси z был взят фрагмент, длина которого составляла 10 глюкозных остатков соответственно.
Критерием приемлемости полученной модели служил фактор недостоверности Rpm:
(1)
${{R}_{{pm}}} = \frac{{\sum\limits_k {{{{\left| {{{I}_{{\exp }}}(s) - {{I}_{{\bmod }}}(s)} \right|}}_{k}}} }}{{\sum\limits_i {{{I}_{{\bmod k}}}(s)} }}*100\% ,$РЕЗУЛЬТАТЫ РЕНТГЕНОГРАФИЧЕСКОГО ЭКСПЕРИМЕНТА
На рис. 2 представлены типичные картины рассеяния целлюлозой мискантуса (рис. 2а) и синтезированной из нее нитроцеллюлозы (рис. 2б), зарегистрированные на излучении CuKα.
Рис. 2.
Нормированные кривые распределения интенсивности рассеяния образцом целлюлозы мискантуса и нитроцеллюлозы, полученной из данного сырья. Указаны индексы отражений целлюлозы (а) и НЦ (б).
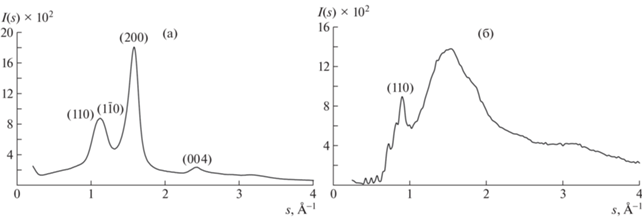
На рентгенограммах образцов синтезированной из данной целлюлозы нитроцеллюлозы наблюдается типичная для таких объектов (полученных разными способами и из различного сырья [1–3, 8–19]) диффузная интерференционная картина, на фоне которой присутствует отражение в области углов рассеяния 2θCu ~ 12°–13°, соответствующее, согласно литературным данным [20–25], линии (110) нитроцеллюлозы.
Результаты обработки рентгенограмм, полученных методом Финбака на излучении МоКα в геометрии на прохождение, представлены на рис. 3. Использование коротковолнового излучения позволило увеличить область обратного пространства, в которой регистрировалась дифракционная картина, т.е. уменьшить пики обрыва на кривой D(r).
Рис. 3.
Кривые распределения интенсивности I(s) (а), s-взвешенной интерференционной функции H(s) (б) и парных функций D(r) (в) исследованной нитроцеллюлозы.
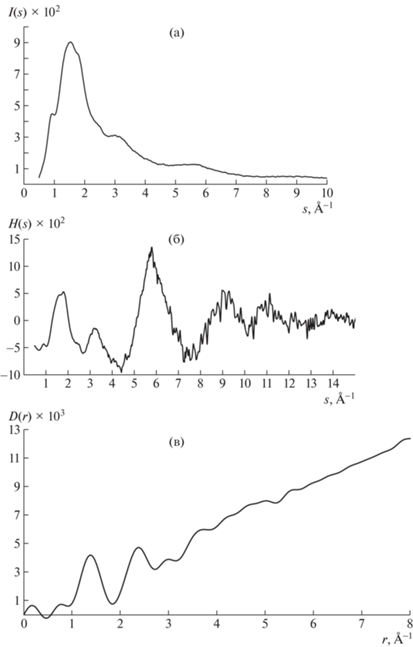
В табл. 1 приведены результаты расчета радиусов и размытий координационных сфер из кривой D(r) (рис. 3в) в сравнении с теоретическими расчетами, выполненными для асимметричной структурной единицы молекулы тринитрата.
Таблица 1.
Радиусы rij и размытия σij координационных сфер и координационные числа Nij
| Тип сферы (номер сферы) | rij, нм | Nij, ат | σij, нм | rij, нм | Nij, ат |
|---|---|---|---|---|---|
| нитроцеллюлоза из мискантуса (эксперимент) | теоретические значения для асимметричной структурной единицы гош-транс (рис. 1б) | ||||
| ON (1) | 0.130 | 0.7 | 0.018 | 0.130 | 0.8 |
| CO (1) | 0.136 | 0.8 | 0.010 | 0.142 | 1.4 |
| CC (1) | 0.160 | 3.5 | 0.015 | 0.152 | 1.7 |
| CO (2) | 0.230 | 2.9 | 0.020 | 0.240 | 2.7 |
| OO (2) | 0.252 | 4.5 | 0.040 | 0.256 | 4.6 |
Рассчитанные из данных рентгенографического эксперимента для нитроцеллюлозы значения радиусов координационных сфер хорошо согласуются с соответствующими теоретическими значениями для ассиметричной структурной единицы молекулы тринитрата целлюлозы (табл. 1). Расхождения в значениях координационных чисел обусловлены тем, что теоретические расчеты выполнялись для одной отдельно взятой асимметричной единицы. Характеристики ближнего порядка рассчитывались (табл. 1) до сферы OO (2) при rij ≈ 0.25 нм, так как мы наблюдаем хорошо различающиеся максимумы на кривой D(r) (рис. 3в) до 0.3 нм. В области от 0.3 до 0.5 нм максимумы плохо разрешаются. Следует отметить, что после 0.5 нм можно говорить о затухании корреляции в расположении атомов.
На рис. 4 экспериментальные кривые H(s) сравниваются с таковыми, полученными для исходной и спиральной с осью закручивания спирали 52 моделей молекул нитроцеллюлозы, состоящих из 10 глюкозных остатков. Длина молекул соответствовала удвоенному периоду ромбической элементарной ячейки, предложенной в работе [25] для тринитрата целлюлозы. В исходном варианте (рис. 4а) нитрогруппы находились в позициях C2, C3 и C6 (рис. 1), т.е. степень замещения равна трем. Фактор недостоверности составлял 49%.
Рис. 4.
Интерференционные функции H(s) (s – взвешенные): 1 – экспериментальные кривые, 2 – кривые, рассчитанные для представленных на данном рисунке исходной (а) и спиральной (б) молекул нитроцеллюлозы.
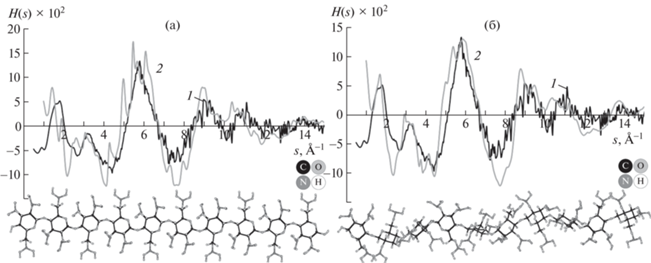
Наименьший фактор недостоверности для моделей спиральных цепочек (30%) был достигнут при значении угла закручивания спиральной цепочки на 72° и степени замещения 2.29.
Далее двойные цепочки упаковывались в элементарные ячейки двух размеров: согласно моделям, предложенным в работе [25]. Следуя такой модели, в плоскости ab было размещено семь оптимизированных одинарных закрученных цепочек. Вид модели кластера с расстоянием между центрами соседних цепочек 14.6 Å в проекции на плоскость ab представлен на рис. 5а. Далее для данной конфигурации была рассчитана теоретическая кривая H(s), приведенная на рис. 5б.
Рис. 5.
а – Модель кластера в проекции на плоскость ab; б – расстояние между центрами цепочек 14.6 Å; s – взвешенная интерференционная функция рассеяния H(s). 1 – эксперимент, 2 – модель, представленная на рисунке.
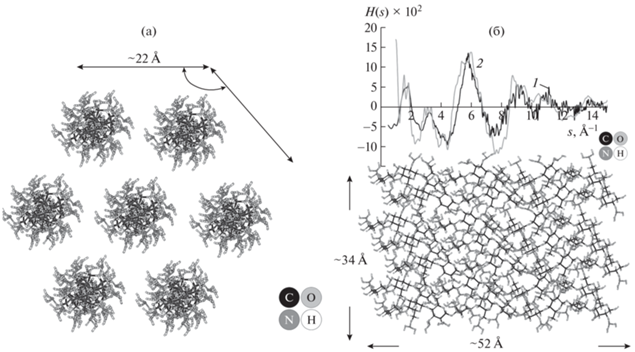
Фактор недостоверности для данных кривых (рис. 5б) составил 18%. На данном расстоянии (14.6 Å) при оптимизации кластера не возникало взаимодействия между соседними цепочками: цепочки релаксируют у своих центров тяжести, не влияя на релаксацию соседних. Методом последовательных итераций было установлено, что оптимальное значение, при котором начинает наблюдаться межцепочечное взаимодействие, составило 12.2 Å (рис. 6), что соответствовало данным работы [25] для второй модели. В связи с этим модель, представленная на рис. 5, была модернизирована путем уменьшения межцепочечного расстояния до 12.2 Å.
Рис. 6.
а – Модель кластера в проекции на плоскость ab; б – расстояние между центрами цепочек 12.2 Å; s – взвешенная интерференционная функция рассеяния H(s) (II). 1 – эксперимент, 2 – модель, представленная на рисунке.
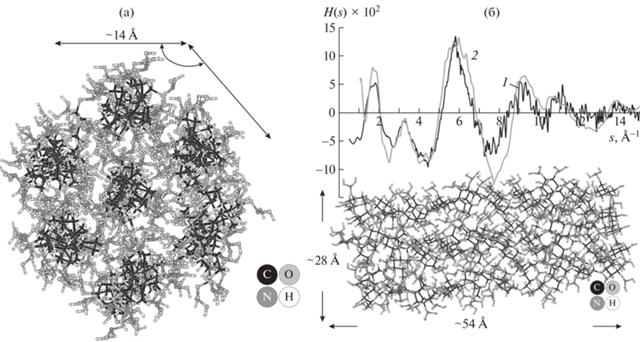
Для данной конфигурации с новым межцепочечным расстоянием 12.2 Å также была рассчитана теоретическая кривая и сопоставлена с экспериментальной кривой H(s) (рис. 6б). Процент несоответствия составил 14% для данных кривых.
Поскольку уменьшение расстояния (рис. 6) привело к взаимодействию целлюлозных цепочек, но не улучшило качественно корреляцию экспериментальных и теоретических кривых H(s), была сделана попытка установить влияние изменения фазового состава на межцепочечное взаимодействие. Было сделано предположение, что в процессе приготовления исследуемого образца нитроцеллюлозы не все цепочки целлюлозы были пронитрованы.
При трансляции кластера, представленного на рис. 6, получили в конечном итоге конфигурацию, показанную полужирным на рис. 7Б.
Рис. 7.
Схема выбора расположения цепочек в кластере в плоскости ab (А, Б), а также схемы расположения цепочек целлюлозы I и нитроцеллюлозы в проекции ab (В); a – одинарная закрученная цепочка целлюлозы I, b – одинарная закрученная цепочка нитроцеллюлозы, c – двойная цепочка нитроцеллюлозы, d – двойная цепочка целлюлозы I. Пояснения в тексте.
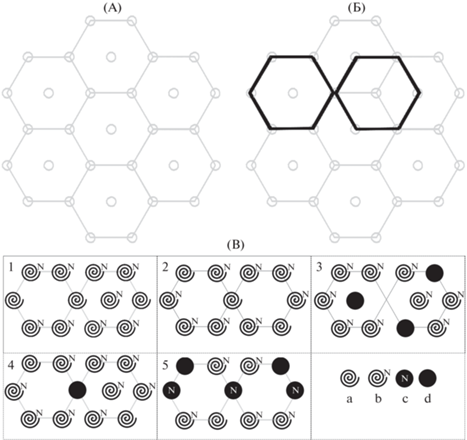
Были рассмотрены разные конфигурации расположения цепочек целлюлозы I и нитроцеллюлозы. В узлы, которые представлены на рисунке 7Б, были помещены (и в дальнейшем оптимизированы) различные цепочки целлюлозы I и нитроцеллюлозы (как продемонстрировано на рис. 7В). Методом подбора были предложены различные кластеры, в узлах которых помещались одинарные цепочки целлюлозы I (a), одинарные закрученные цепочки нитроцеллюлозы (b), две закрученные цепочки нитроцеллюлозы (c), две незакрученные цепочки целлюлозы I (d), или данная позиция оставалась пустой. Все цепочки имели длину, равную длине десяти глюкозных остатков (52 Å).
Для всех рассмотренных вариантов были построены кривые H(s) и рассчитаны коэффициенты Rp. Минимальный фактор недостоверности (7.5%), и лучшее совпадение экспериментальных и теоретических кривых H(s) (рис. 8) наблюдается для варианта 4 (рис. 7). Окончательный кластер представлен на рис. 9 в проекции ab и bc.
Рис. 8.
Кривые распределения I(s) (а), функций радиального распределения W(r) (б) и интерференционных функций H(s) (в). 1 – эксперимент, 2 – модель, представленная на рисунке.
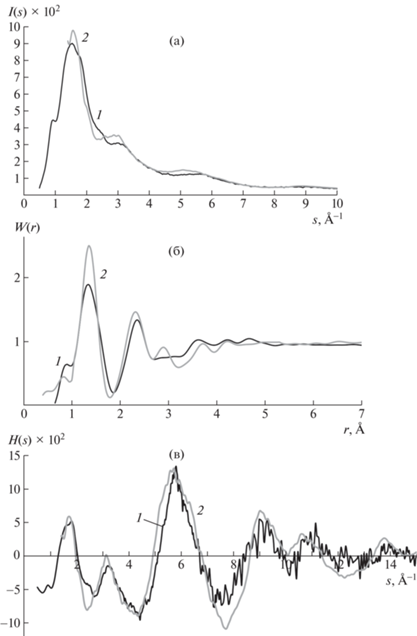
Итоговый кластер (рис. 9) состоит из 3300 атомов, степень полимеризации n = 130; формульная единица асимметричного фрагмента [C6H7.24O2(OH)0.92(ONO2)2.08]130. Таким образом, степень замещения получилась равной 2.08. Энергия данного кластера после геометрической оптимизации (рис. 9) равна 1456.26 ккал/моль. Процесс релаксации занял 993 итерации с шагом 0.1 ккал/моль.
Как показали соответствующие расчеты, средний угол между закрученными соседними глюкозными остатками итогового кластера (рис. 9) составляет ≈75°, что также коррелирует с данными работ [24, 25].
В табл. 2 усредненные значения межатомных расстояний в асимметричных единицах итогового кластера сравниваются с соответствующими данными, представленными в работе [28] и данными, рассчитанными по приведенным в работе [25] координатам атомов асимметричной единицы с гош-транс-конформацией нитрогрупп. Из табл. 2 следует, что межатомные расстояния в асимметричных единицах достаточно хорошо коррелируют между собой.
Таблица 2.
Значения межатомных расстояний и углов связей для асимметричной единицы
| Пара атомов | Межатомное расстояние, Å | Пара атомов | Угол связи, град | ||||
|---|---|---|---|---|---|---|---|
| [28] | [25] | настоящая работа | [28] | [25] | настоящая работа | ||
| O31–N3 | 1.232 | 1.22 | 1.368 | O31–N3–O32 | 131.29 | 124.03 | 108.30 |
| O32–N3 | 1.236 | 1.22 | 1.366 | O31–N3–O3 | 112.96 | 117.96 | 106.72 |
| N3–O3 | 1.485 | 1.37 | 1.367 | O32–N3–O3 | 115.74 | 118.01 | 105.86 |
| O3–C3 | 1.441 | 1.43 | 1.443 | N3–O3–C3 | 111.26 | 117.53 | 111.26 |
| C3–C4 | 1.520 | 1.52 | 1.553 | O3–C3–C4 | 109.97 | 109.71 | 112.75 |
| C4–O4 | 1.446 | 1.42 | 1.438 | C3–C4–O4 | 109.94 | 110.45 | 107.83 |
| C4–C5 | 1.540 | 1.52 | 1.558 | C3–C4–C5 | 106.85 | 110.2 | 108.74 |
| C5–C6 | 1.529 | 1.51 | 1.552 | C5–C6–O6 | 109.36 | 111.3 | 110.23 |
| C6–O6 | 1.447 | 1.44 | 1.442 | C5–O5–C1 | 116.58 | 112.28 | 112.70 |
| N6–O6 | – | 1.37 | 1.372 | O61–N6–O62 | – | 123.95 | 111.13 |
| O61–N6 | – | 1.22 | 1.367 | O61–N6–O6 | – | 118.04 | 110.80 |
| O62–N6 | – | 1.22 | 1.367 | O62–N6–O6 | – | 118.00 | 110.17 |
| C5–O5 | 1.444 | 1.44 | 1.445 | O5–C1–O1 | 110.13 | 107.31 | – |
| O5–C1 | 1.420 | 1.43 | 1.443 | O5–C1–C2 | 107.31 | 109.35 | 109.87 |
| C1–O1 | 1.431 | 1.39 | 1.440 | C1–C2–O2 | 111.73 | 108.35 | – |
| C1–C2 | 1.544 | 1.52 | 1.558 | C2–O2–N2 | 111.3 | 117.30 | 112.74 |
| C2–O2 | 1.444 | 1.43 | 1.443 | O2–N2–O22 | 111.71 | 117.87 | 106.96 |
| O2–N2 | 1.518 | 1.37 | 1.367 | O22–N2–O21 | 130.24 | 124.00 | 107.27 |
| N2–O22 | 1.226 | 1.22 | 1.368 | O21–N2–O2 | 118.05 | 118.03 | 105.45 |
| N2–O21 | 1.235 | 1.22 | 1.365 | C1–C2–C3 | 106.32 | 110.55 | 110.51 |
| C2–C3 | 1.559 | 1.52 | 1.556 | C2–C3–C4 | 109.19 | 110.35 | 112.74 |
ЗАКЛЮЧЕНИЕ
Таким образом, в работе получены данные об атомно-молекулярном строении аморфной компоненты нитроцеллюлозы из мискантуса. Установлено, что ближний порядок в расположении молекул в аморфной составляющей нитроцеллюлозы соответствует искаженной гексагональной упаковке из двух шестиугольников, ориентированных в проекции кластера на плоскость ab.
Наилучшее совпадение (фактор недостоверности Rpm = 7.5%) с результатами рентгенографического эксперимента было получено при замене части молекул нитроцеллюлозы на две закрученные и две незакрученные молекулы непронитрованной целлюлозы. Возможно, что добавление нитрогрупп в эти молекулы в количестве, соответствующем степени замещения, характерной для моно- и динитрата, приведет к дальнейшему уменьшению фактора недостоверности.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (код проекта 20-03-00699).
Список литературы
Mattar H., Baz Z., Saleh A., Shalaby A.S.A., Azzazy A.E., Salah H., Ismail I. // Wat. Ener. Food. Env. J. 2020. V. 1. № 3. P. 1.
Nikolsky S.N., Zlenko D.V., Melnikov V.P., Stovbun S.V. // Carbohydr. Polymers. 2019. V. 204. P. 232.
Trache D., Tarchoun A.F. // J. Chemometrics. 2019. V. 33. № 8. P. 3163.
Korchagina A.A., Gismatulina Yu.A., Budaeva V.V., Kukhlenko A.A., Vdovina N.P., Ivanov P.P. / Izv. Vyssh. Uchebn. Zaved. Khim. Khim. Tekhnol. 2020. V. 63. № 1. P. 92.
Gismatulina Yu.A., Budaeva V.V., Sakovich G.V. // Russ. Chem. Bull., Int. Ed. 2015. V. 64. № 12. P. 949.
Gismatulina Y.A., Budaeva V.V., Sakovich G.V. // Propellants Explos. Pyrotech. 2018. V. 43. P. 96.
Sakovich G.V., Mikhailov Yu.M., Budaeva V. V., Korchagina A.A., Gismatulina Yu.A., Kozyrev N.V. // Dokl. Chem. 2018. V. 483. P. 287.
Trache D., Khimeche K., Mezroua A., Benziane M. // J. Thermal Analysis Calorimetry. 2016. V. 124. P. 1485.
Tarchoun A.F., Trache D., Klapötke T.M., Chelouche S., Derradji M., Bessa W., Mezroua A.A. // Macromol. Chem. Phys. 2019. V. 220. P. 1900358.
Tarchoun A.F., Trache D., Klapötke T.M., Krumm B., Khimeche K., Mezroua A. // Carbohydr. Polymers. 2020. V. 249. P. 116820.
Chelouche S., Trache D., Tarchoun A.F., Khimeche A.A., Mezroua K.A. // Thermochim. Acta, 2019. V. 673. P. 78.
Trache D., Tarchoun A.F., Klapötke T.M., Krumm B., Kofen B. // Fuel. 2021. V. 292. P. 1.
Tarchoun A.F., Trache D., Klapötke T.M., Krumm B., Mezroua A., Derradji M., Bessa W. // Cellulose. 2021. V. 48. P. 6107.
Chelouche S., Trache D., Tarchoun A.F., Khimeche A.A., Mezroua K.A. // J. Thermal Analysis Calorimetry. 2019. P. 1.
Yamamoto H., Horii F., Hirai A. // Cellulose. 2006. V. 13. P. 327.
Yu J., Wu Y., Wang S., Ma X. // Carbohydr. Polymers. 2007. V. 70. P. 8.
Косточко А.В., Валишина З.Т., Лузянина М.В. // Вестн. Казанского технол. ун-та. 2012. № 9. P. 45.
Валишина З.Т., Клочков В.В., Галиуллина Г.Н., Лошиева К.А., Косточко А.В. // Вестн. технол. ун-та. 2015. Т. 18. № 18. P. 142.
Stovbuna S.V., Nikol’skii S.N., Mel’nikov V.P., Mikhaleva M.G., Litvin Ya.A., Shchegolikhin A.N., Zlenko D.V., Tverdislov V.A., Gerasimov D.S., Rogozin A.D. // Russ. J. Phys. Chem. B. 2016. V. 10. № 2. P. 245.
Watanabe S., Imai K., Hayashi J. // J. Chem. Soc. Jpn., Ind. Chem. Sec. 1971. V. 74. P. 1420.
Watanabe S., Imai K. Hayashi J. // J. Chem. Soc. Jpn., Ind. Chem. Sec. 1971. V. 74. P. 1427.
Hayashi J., Imai K., Hamazaki T., Watanabe S. // Jpn J. Chem. 1973. № 8. P. 1582.
Hayashi J., Imai K., Hamazaki T., Watanabe S. // Jpn J. Chem. 1973. № 8. P. 1587.
Watanabe S., Hayashi J., Imai K.A. // J. Polym. Sci. 1968. № 23. P. 809.
Meader D., Atkins E.D.T., Happey F. // Polimer. 1978. V. 19. P. 1371.
Kovalenko V.I. // Russ. Chem. Revs. 1995. V. 64. P. 753.
Richards L.A., Nash A., Phipps M.J.S., de Leeu N.H. // New J. Chem. 2018. V. 42. P. 17420.
Liu P., Sun R., Sui P., Gao S., Feng Zh, Zou G., Qi H. // Mater. Res. Express 7. 2020. P. 1.
Otto D.P., Combrinck J., Otto A., Tiedt L.R., de Villiers M.M. // Pharmaceuticals. 2018. V. 11. P. 134.
Yang L., Wu X., Li J., Chen T., Liu M., He Q. // Roy. Soc. Open Sci. 2021. V. 8. P. 211033.
Qi X., Li H., Zhao Yu, Liu P., Yan Q. // Cellulose. 2022. V. 29. P. 1307.
Алешина Л.А., Люханова И.В., Будаева В.В., Золотухин В.Н., Митрофанов Р.Ю., Сакович Г.В. // Уч. записки Петрозаводского гос. ун-та. Сер. Естественные и технические науки. 2011. № 8. С. 114.
Prusskii A.I., Aleshina L.A. // Polymer Science A. 2016. V. 58. № 3. P. 386.
Melekh N.V., Frolova S.V., Aleshina L.A. // Polymer Science A. 2014. V. 56. № 2. P. 129.
Tsai C.S. An Introduction to Computational Biochemistry. New York: Wiley-Liss, 2002.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)