Высокомолекулярные соединения (серия Б), 2020, T. 62, № 3, стр. 177-182
ВЛИЯНИЕ АЛКИЛИРОВАНИЯ ТЕТРАЗОЛЬНЫХ ЦИКЛОВ НА СВОЙСТВА КАРБО- И ГЕТЕРОЦЕПНЫХ ТЕТРАЗОЛСОДЕРЖАЩИХ ПОЛИМЕРОВ
Ф. А. Покатилов a, *, В. Н. Кижняев a, Е. В. Акамова a, О. А. Эдельштейн a
a Иркутский государственный университет
664003 Иркутск, ул. К. Маркса, 1, Россия
* E-mail: pfa72@rambler.ru
Поступила в редакцию 26.09.2019
После доработки 18.11.2019
Принята к публикации 03.12.2019
Аннотация
Изучены некоторые свойства продукта алкилирования тетразолилэтилового эфира целлюлозы. Проведен сравнительный анализ изменения свойств гетероцепного (тетразолированная целлюлоза) и карбоцепного (поли-5-винилтетразол) полимера при замене в их макромолекулярной структуре ионогенных N–H незамещенных тетразольных циклов на N-метилзамещенные. Продемонстрировано определяющее влияние на поведение полимеров строения бокового гетероциклического заместителя, а не природы основной цепи.
Продукты модификации природного полимера целлюлозы, благодаря многообразию ценных в практическом отношении свойств, нашли широкое применение в различных сферах жизнедеятельности человека [1], в том числе и в качестве полимерных связующих ингредиентов в рецептурах высокоэффективного твердого ракетного топлива, взрывчатых и газогенерирующих составов [2, 3]. В зависимости от строения производные целлюлозы подразделяются на “инертные” (например, бутират-ацетат целлюлоза) и “активные” связующие, содержащие эксплозофорные группы (тринитроцеллюлоза). Одним из структурных фрагментов, способных существенно повысить энергетические характеристики высокомолекулярных соединений, является тетразольный цикл [4–6].
Попытки введения в макромолекулярную структуру целлюлозы тетразольных фрагментов предпринимались неоднократно [7, 8], в частности для улучшения энергетических характеристик продуктов нитрования целлюлозы [9]. Кроме того, такие полимеры должны обладать хорошей совместимостью и химической инертностью по отношению к другим компонентам смесей. Так, исследования свойств карбоцепных тетразолсодержащих полимеров продемонстрировали наилучшую совместимость среди представителей различных классов соединений с поливинилтетразолами, содержащими 2,5-диалкилтетразольные структурные фрагменты [10]. Поэтому наиболее перспективным “активным” связующим компонентом твердотопливных систем считается не поли-5-винилтетразол, а продукт его метилирования – поли-N-метил-5-винилтетразол:

хотя и уступающий ПВТ по энергетическим характеристикам и плотности, но более совместимый с другими ингредиентами и обеспечивающий лучшие физико-механические свойства композиций [11–13].
Синтезированный посредством реакций цианоэтилирования целлюлозы акрилонитрилом с последующим азидированием нитрильных групп тетразолилэтиловый эфир целлюлозы (ТЭЦ) [8]:
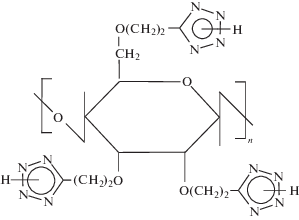
относится к энергонасыщенным высокомолекулярным соединениям, аналогам тринитроцеллюлозы. Однако ТЭЦ, как и все полимеры, имеющие в структуре N–Н незамещенные тетразольные циклы, характеризуется очень узким набором растворяющих его органических жидкостей (ДМФА, ДМСО). Можно ожидать, что по аналогии с карбоцепными поливинилтетразолами, алкилирование тетразольных циклов в структуре ТЭЦ будет способствовать существенному улучшению совместимости гетероцепного полимера с соединениями различной природы.
В настоящей работе представлен сравнительный анализ влияния модификации гетероцепного полимера ТЭЦ и карбоцепного ПВТ посредством метилирования тетразольных циклов в их структуре на изменение свойств тетразолсодержащих полимеров.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследовали образец тетразолилэтилового эфира целлюлозы – (степень замещения гидроксильных групп 2.85), синтезированный согласно методике [8]. Для сравнительного анализа свойств тетразолсодержащих полимеров различной природы использовали результаты, полученные для коммерческих образцов ПВТ и МПВТ (Открытое акционерное общество “Сибреактив”, Россия), синтезированных модификационным способом – азидированием полиакрилонитрила с последующим метилированием получаемого ПВТ [11, 13]. Алкилирование тетразолированной целлюлозы осуществляли следующим образом. К предварительно приготовленному раствору ТЭЦ в ДМФА последовательно добавляли тонко измельченный K2CO3 и воду. Далее в полученный раствор калиевой соли ТЭЦ с использованием капельной воронки в течение 30 мин вводили алкилирующий реагент – диметилсульфат (эквимольное количество по отношению к тетразольным циклам). Смесь выдерживали при комнатной температуре и постоянном перемешивании 2 ч, после чего образовавшийся полимерный продукт высаживали в воду. Выпавший в осадок полимер промывали дистиллированной водой до нейтральной реакции промывных вод, затем сушили под вакуумом до постоянной массы.
Строение продукта метилирования ТЭЦ устанавливали по данным ИК-спектроскопии, ЯМР 13С и ЯМР 1Н, элементного анализа и потенциометрического титрования. Элементный анализ осуществляли на CHN-анализаторе “FLASHBA 1112 Series”. ИК-спектры образцов полимеров в виде пленок снимали на ИК-фурье-спектрометре “Инфралюм ФТ-801”. Спектры ЯМР 13С и ЯМР 1Н регистрировали на спектрометре “VarianVXR-500” в растворах дейтерированного ДМСО. Термический анализ полимеров проводили на термогравиметрическом анализаторе “NETZSCHSTA 449 F3 Jupiter” в динамическом режиме; скорость нагревания на воздухе составляла 5 град/мин. Потенциометрические измерения для установления остаточного содержания N–H незамещенных тетразольных фрагментов выполняли на иономере ЭВ-74. Фазовые диаграммы систем тетразолсодержащий полимер–вода получали методом равновесного набухания образца полимера в парах воды при заданной температуре. Плотность определяли пикнометрическим способом, вискозиметрические измерения растворов полимеров осуществляли с использованием вискозиметра Уббелоде при 20°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В результате реакции алкилирования ТЭЦ диметилсульфатом в щелочной среде был получен (N-метилтетразолил)этиловый эфир целлюлозы (МТЭЦ):
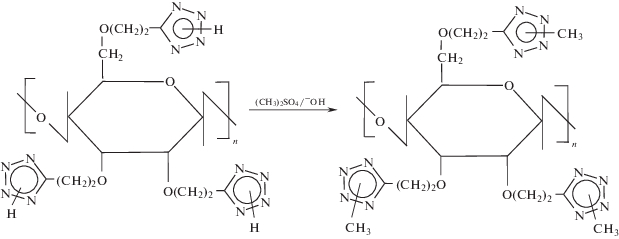 ,
,
который, по данным элементного анализа (найдено – 32.9% N, вычислено – 33.2%) и потенциометрии, практически не содержит N–H незамещенных тетразольных фрагментов. Данный факт подтверждается и результатами спектральных исследований. В ИК-спектрах исходного ТЭЦ и продукта его метилирования присутствуют полосы поглощения, характерные для тетразольного цикла, при 1060–1063, 1097, 1397, 1464 и 1496 см–1. Однако в спектре МТЭЦ отсутствует ряд полос, соответствующих различным типам колебаний связи N–H в незамещенном тетразольном цикле, в областях 1250, 1550–1560 и 2200–3700 см–1 [14]. Алкилирование тетразольного цикла в присутствии основания всегда влечет формирование двух изомерных форм с расположением метильных групп при первом (N1-изомер) и втором (N2-изомер) атомах азота гетероцикла. Как следствие, в ЯМР 13С-спектрах МТЭЦ исчезает сигнал атома углерода N–H незамещенного тетразольного цикла при 156.4 м.д., а появляются два сигнала, относящиеся к атомам углерода двух изомерных форм N-метильных производных тетразола, при 154.2 м.д. (N1-изомер) и 164.1 м.д. (N2-изомер). Как и для ТЭЦ, в спектре МТЭЦ присутствуют сигналы метиленовых групп боковых заместителей при 23.9 и 63.0–63.8 м.д., а также уширенные сигналы 18–22, 57–62 и 68–71 м.д., соответствующие атомам углерода основной цепи макромолекулы целлюлозы. Сигнал метильного заместителя N1 изомерной формы гетероцикла проявляется при 33.9 м.д., сигнал же метильной группы N2 изомерной формы в области 38–39 м.д. перекрывается интенсивным сигналом растворителя ДМСО. В спектрах ЯМР 1Н сигналы протонов метильных заместителей, находящихся у разных атомов азота тетразольного цикла, четко проявляются при 4.01 м.д. (для N1-изомера) и при 4.26 м.д. (для N2-изомера). Согласно спектрам, соотношение изомеров N1 : N2 = 1 : 2.
Замена кислотного протона в тетразольном цикле на метильную группу сказывается на некоторых физико-химических свойствах полимера, например, может приводить к незначительному увеличению плотности полимерного продукта: 1.33–1.37 г/см3 для образцов МТЭЦ против 1.30–1.32 г/см3 у ТЭЦ. Вместе с тем, для пары карбоцепных поливинилтетразолов прослеживается совершенно иная тенденция: 1.4–1.45 г/см3 у ПВТ и 1.25–1.33 г/см3 для образцов метилзамещенного полимера МПВТ. Вероятно, причина различного влияния алкилирования бокового тетразолильного заместителя на плотность полимеров заключается в природе модифицируемых макромолекул полимеров. В случае гибкоцепного полимера метилирование гетероцикла приводит к разрыхлению полимерной упаковки вследствие исчезновения двутяжных участков полимерных цепей ПВТ [10], стабилизированных водородными связями и диполь-дипольными взаимодействиями, способствующих компактизации макромолекул и их более плотной упаковке. Для пары жесткоцепных полимеров ТЭЦ–МТЭЦ, вероятно, проявляется обратный эффект; исчезновение сильных внутри- и межмолекулярных взаимодействий, вследствие замены кислотного протона на метильную группу, сопровождается возрастанием гибкости макромолекул, что благоприятствует их более плотной упаковке, способствующей повышению плотности метилированных образцов полимеров.
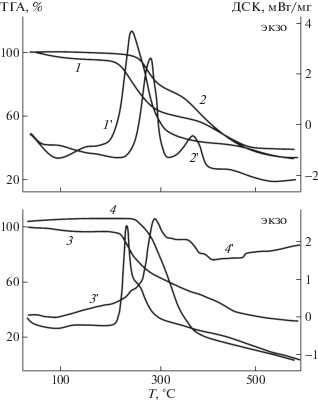
Поведение тетразолсодержащих полимеров при температурном воздействии определяется термической стабильностью тетразольного фрагмента, которая в некоторой степени варьируется в зависимости от природы заместителей в гетероцикле. Так, алкилирование тетразольного фрагмента в структуре ПВТ и ТЭЦ обусловливает повышение температуры начала разложения для модифицированных полимерных продуктов на 20–40°С (рис. 1, кривые термогравиметрического анализа 1–4); с 200–220°С у ТЭЦ до 240–260°С для МТЭЦ и с 230 до 250°С для пары поливинилтетразолов ПВТ и МПВТ. Процесс термического разложения тетразольных циклов сопровождается высоким экзотермическим эффектом (рис. 1, кривые ДСК 1'–4').
Рис. 1.
Кривые динамического ТГА (1–4) и ДСК (1'–4') для ПВТ (1, 1'), МПВТ (2, 2'), ТЭЦ (3, 3') и МТЭЦ (4, 4').
Растворимость выступает как одно из важнейших свойств у полимеров, поскольку определяет совместимость их с различными классами соединений, а также возможные варианты переработки и практического применения. В этой связи представляло интерес провести сравнительный анализ влияния модификации посредством метилирования тетразольных циклов в макромолекулах отличных по природе тетразолсодержащих полимеров на их совместимость с различными жидкими системами. Присутствие в структуре ТЭЦ и ПВТ незамещенных тетразольных циклов N–H, склонных к донорно-акцепторным и диполь-дипольным взаимодействиям, обусловливает способность указанных полимеров растворяться только в полярных сильно донорных органических жидкостях ДМФА и ДМСО (табл. 1). Существенное ослабление внутри- и межмолекулярных взаимодействий при алкилировании тетразольных циклов в карбоцепном полимере помогает существенному расширению арсенала органических жидкостей, являющихся растворителями для МПВТ. Гораздо менее критические изменения отмечены при модификации жесткоцепного тетразолсодержащего полимера; к числу органических растворителей для МТЭЦ также можно отнести нитрометан. Еще в ряде жидкостей, растворяющих МПВТ, полимер на основе целлюлозы лишь ограниченно набухает. Возможно, причиной этому послужило присутствие в структуре производного целлюлозы остаточных гидроксильных групп, способствующих проявлению более сильных, чем в случае МПВТ, полимер-полимерных взаимодействий и препятствующих растворимости МТЭЦ.
Таблица 1.
Растворимость тетразолсодержащих полимеров
| Растворитель | Растворимость тетразолсодержащих полимеров | |||
|---|---|---|---|---|
| ПВТ [10] | МПВТ [10] | ТЭЦ [8] | МТЭЦ | |
| ДМСО | р | р | р | р |
| ДМФА | р | р | р | p |
| Ацетон, ацетонитрил, дихлорэтан, этилацетат | н | р | н | Набухает |
| Нитрометан | н | р | н | р |
| Вода | н | н | н | н |
| Водный раствор NaOH | р | н | р | н |
| Водный раствор Н2SO4 | 36% | 20% | 50% | 28% |
| Водный раствор муравьиной кислоты | н | 24% | 48% | 44% |
| Водный раствор NH4CNS | 2.0 моль/л | 0.8 моль/л | 5.0 моль/л | 1.0 моль/л |
| Водный раствор LiClO4* | 2.1 моль/л | 0.9 моль/л | 2.5 моль/л | 2.2 моль/л |
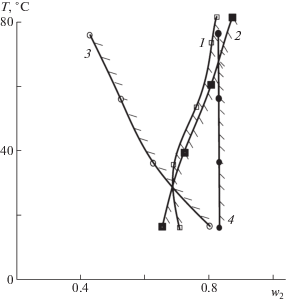
Вода не служит растворителем ни для одного из рассматриваемых полимеров, даже по отношению к ТЭЦ и ПВТ, в структуре которых присутствуют кислотные N–H незамещенные тетразольные циклы, так как имеет место сильное внутри- и межмолекулярное водородное связывание с участием боковых гетероциклических фрагментов. Однако определенное сродство у всех четырех тетразолсодержащих полимеров к воде проявляется в виде способности к ограниченному набуханию (рис. 2).
Рис. 2.
Фазовая диаграмма полимер–вода: 1 – ПВТ, 2 – МПВТ, 3 – ТЭЦ и 4 – МТЭЦ. Заштрихованная область отвечает гомогенному состоянию системы; w2 – массовая доля полимера.
Нарушение системы водородных связей в макромолекулах ПВТ и ТЭЦ посредством добавления к воде некоторых органических жидкостей (этанол, ацетон, ацетонитрил), даже не принадлежащих к растворителям по отношению к указанным полимерам, способствует растворимости последних в водно-органических смесях [8, 10]. Аналогичная особенность сохраняется и у соответствующих алкилированных производных – МПВТ и МТЭЦ, вероятно, вследствие присутствия в структуре незначительного количества N–H незамещенных тетразольных циклов. Однако диапазон соотношений вода : органический растворитель, проявляющих растворяющую способность, заметно сужается и сдвигается в область бóльшего содержания органической компоненты смешанного растворителя (рис. 3). Повышение температуры мало сказывается на растворяющей способности смешанного растворителя.
Рис. 3.
Фазовые диаграммы систем полимер–вода–ацетонитрил: 1 – ПВТ, 2 – МПВТ, 3 – ТЭЦ и 4 – МТЭЦ. Заштрихованная область отвечает однофазному состоянию системы; ws – объемная доля ацетонитрила в смеси с водой.

Зависимость вязкости растворов всех изученных полимеров от соотношения компонентов водно-органической смеси носит экстремальный характер с максимумом при соотношении жидкостей, отвечающему наилучшему термодинамическому качеству растворителя (рис. 4). Так, для системы вода–ацетонитрил наилучшей растворяющей способностью по отношению к ПВТ, ТЭЦ, МТЭЦ и МПВТ обладают смеси с содержанием ацетонитрила 0.25, 0.6, 0.7 и 0.9 массовых долей соответственно.
Рис. 4.
Зависимость приведенной вязкости систем полимер–вода–ацетонитрил от объемной доли ws ацетонитрила в смеси с водой: 1 – ПВТ, 2 – МПВТ, 3 – ТЭЦ и 4 – МТЭЦ.
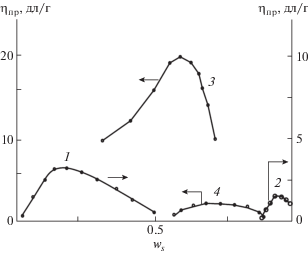
Можно отметить еще одно отличие в поведении незамещенных и метилзамещенных тетразолсодержащих полимеров в смешанных растворителях. Изменение значений вязкостных характеристик растворов, а следовательно, и конформационного состояния макромолекулярных клубков при варьировании состава смешанного растворителя в случае неионогенных полимеров МТЭЦ и МПВТ существенно менее критично, чем для ионогенных растворов, содержащих в структуре N–H незамещенные тетразольные циклы, ПВТ и ТЭЦ.
Ионизация тетразольных циклов влечет неограниченную совместимость с водой образцов ТЭЦ и ПВТ в солевой форме. Модификация же ТЭЦ и ПВТ посредством алкилирования тетразольных циклов приводит к утрате кислотных свойств и, как следствие, потери способности МТЭЦ и МПВТ растворяться в водных растворах щелочей. Между тем, наличие слабых основных свойств у тетразольного цикла способствует растворимости изучаемых тетразолсодержащих полимеров в некоторых минеральных кислотах (кроме ПВТ) и даже в муравьиной кислоте (таблица). Повышение основных свойств тетразольного фрагмента при замене протона на метильную группу приводит к снижению минимальной растворяющей концентрации водных растворов кислот, как в случае гибкоцепных (ПВТ и МПВТ), так и жесткоцепных тетразолсодержащих полимеров (ТЭЦ и МТЭЦ).
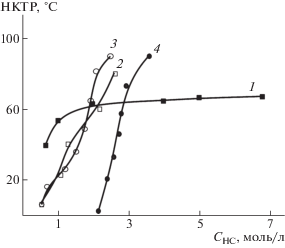
Еще одним типом растворителей для тетразолсодержащих полимеров служат водные растворы некоторых солей, в частности роданида аммония и перхлората лития [10]. Сравнивая поведение ПВТ, ТЭЦ и их метильных производных в растворах указанных солей, можно выделить две тенденции. Во-первых, для растворения жесткоцепных полимеров на основе целлюлозы требуется более концентрированный водный раствор соли по сравнению с соответствующим гибкоцепным поливинилтетразолом (табл. 1). Во-вторых, метилзамещенные производные МПВТ и МТЭЦ растворяются при меньших значениях концентрации низкомолекулярных солей в воде, чем их незамещенные предшественники ПВТ и ТЭЦ. Причиной этого является ослабление тенденции к ассоциативным процессам у полимеров при замене кислотного протона на метильную группу в тетразольных циклах. В свою очередь, гидрофобизация макромолекул, обусловленная введением метильного радикала в тетразольный цикл, приводит к тому, что для водно-солевых растворов МПВТ и МТЭЦ характерно наличие нижней критической температуры растворения. Для обоих полимеров температура фазового разделения возрастает с увеличением концентрации низкомолекулярной соли в растворе (рис. 5).
Рис. 5.
Зависимость НКТР водно-солевых растворов ПВТ (1), МПВТ (2), ТЭЦ (3) и МТЭЦ (4) от концентрации роданида аммония (1, 3) и перхлората лития (2, 4).
Еще одна общая закономерность отмечена при модификации как гибкоцепных, так и жесткоцепных тетразолсодержащих полимеров. Полимеры, содержащие в структуре метилзамещенные тетразольные циклы (МПВТ и МТЭЦ) обладают пленкообразующими свойствами, в то время как ПВТ и ТЭЦ, содержащие N–H незамещенные тетразольные циклы, лишены этого свойства. Этот факт предполагает, что МТЭЦ, как и МПВТ, может являться эффективным связующим для конденсированных многокомпонентных энергетических систем, обеспечивающим требуемые физико-механические характеристики композиций.
Таким образом, замена N–H незамещенных тетразольных циклов на N-метилзамещенные тетразольные фрагменты в структуре карбо- и гетероцепных полимеров обусловливает ожидаемо схожие изменения в физико-химических свойствах модифицированных полимеров, а потеря полиэлектролитных и усиление органофильных свойств – появление способности к пленкообразованию. Однако, несмотря на определяющее влияние на поведение полимеров природы бокового гетероциклического заместителя, в случае гетероцепных полимеров ТЭЦ и МТЭЦ амплитуда изменения свойств выражена в меньшей степени, нежели для пары ПВТ и МПВТ.
Работа выполнена при финансовой поддержке Министерства образования и науки (Госзадание № 4.5183.2017/БЧ).
Список литературы
Tkacheva N.I., Morozov S.V., Grigor’ev I.A., Mognonov D.M., Kolchanov N.A. // Polymer Science B. 2013. V. 55. № 7–8. P. 409.
Volk F., Bathelt H. // Propellants, Explosives, Pyrotechnics. 1997. V. 22. № 3. P. 120.
Agrawal J.P., Field J.E. // Prog. Energy Combust. Sci. 1998. V. 24. № 1. P. 1.
Ha H.X., Cao Y.L., Sun Z.X. // Chin. J. Energetic Mater. 2007. V. 15. № 5. P. 492.
Гапоник П.Н., Ивашкевич О.А. // Вестн. Белорусского гос. ун-та. Сер. 2. 2013. № 1. С. 3.
Ostrovskii V.A., Popova E.A., Trifonov R.E. // Adv. Heterocycl. Chem. 2017. V. 123. P. 1.
Dietrich M., Delaittre G., Blinco J.P., Inglis A.J., Bruns M., Barner-Kowollik Ch. // Adv. Funct. Mater. 2012. V. 22. № 2. P. 304.
Pokatilov F.A., Kizhnyaev V.N. // Polymer Science A. 2012.V. 54. № 11. P. 894.
Betzler F.M., Klapotke Th.M., Sproll S. // Centr. Eur. J. Energetic Mater. 2011. V. 8. № 3. P. 157.
Kizhnyaev V.N., Pokatilov F.A., Vereshchagin L.I. // Polymer Science C. 2008. V. 50. № 1. P. 1.
Gaponik P.N., Ivashkevich O.A., Chernavina N.I., Lesnikovich A.I., Sukhanov G.T., Gareev G.A. // Angew. Makromol. Chem. 1994. V. 219. № 1. P. 89.
Belousov A.M., Orlova N.A., Paznikov E.A. // Int. Sci. J. Alternative Energy Ecology. 2005. V. 26. № 6. P. 44.
Reddy T.S., Satpute R.S., Nair J.K. // J. Polym. Mater. 2008. V. 25. № 4. P. 557.
Kizhnyaev V.N., Vereshchagin L.I. // Russ. Chem. Rev. 2003. V. 72. № 2. P. 143.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)


