Высокомолекулярные соединения (серия С), 2020, T. 62, № 2, стр. 237-244
ВЛИЯНИЕ ТЕМПЕРАТУРЫ СТАБИЛИЗАЦИИ И КАРБОНИЗАЦИИ НА СВОЙСТВА МИКРОПОРИСТЫХ УГЛЕРОДНЫХ НАНОВОЛОКОННЫХ КАТОДОВ ДЛЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ НА ПОЛИБЕНЗИМИДАЗОЛЬНОЙ МЕМБРАНЕ
К. М. Скупов 1, *, И. И. Пономарев 1, Ю. М. Вольфкович 2, А. Д. Модестов 2, Ив. И. Пономарев 1, Ю. А. Волкова 1, Д. Ю. Разоренов 1, В. Е. Сосенкин 2
1 Институт элементоорганических соединений им. А.Н. Несмеянова Российской академии наук
119991 Москва, ул. Вавилова, 28, Россия
2 Институт физической химии и электрохимии им. А.Н. Фрумкина Российской академии наук
119071 Москва, Ленинский пр., 31, корп. 4, Россия
* E-mail: kskupov@ineos.ac.ru
Поступила в редакцию 24.01.2020
После доработки 28.04.2020
Принята к публикации 12.05.2020
Аннотация
Композитные материалы, содержащие Ni и Zr, на основе пиролизованных нановолокон полиакрилонитрила, полученных методом электроспиннинга, исследованы методом эталонной контактной порометрии. Установлено, что повышение температуры окисления с 330 до 350°С и пиролиза с 900 до 1000°С приводит к уменьшению удельной площади поверхности пор и доли удельной площади поверхности микропор. Для платинированных образцов получены удовлетворительные величины электрохимически активной площади поверхности платины 12–35 м2 г$_{{{\text{Pt}}}}^{{ - 1}}$. Эти образцы испытаны в качестве катода для высокотемпературных топливных элементов на полибензимидазольной мембране. Зафиксировано увеличение показателей мощности и вольтамперной характеристики при уменьшении доли удельной площади поверхности микропор электрода.
ВВЕДЕНИЕ
Развитие водородной энергетики, в частности области топливных элементов на полимерных мембранах, требует устойчивой и стабильной работы мембранно-электродного блока [1–11]. Однако высокотемпературные (по более общей классификации среднетемпературные) топливные элементы на полимерной протон-проводящей мембране (ВТ-ПОМТЭ), несмотря на многочисленные преимущества, нуждаются в дальнейшем усовершенствовании. Поиск стабильных материалов мембранно-электродного блока в условиях эксплуатации ВТ-ПОМТЭ (фосфорнокислотная среда, 150–200°С) можно назвать необходимым условием развития данной области [6, 9]. Так, в наиболее часто используемых электродах ВТ-ПОМТЭ на основе платинированной сажи, углеродный материал подвергается усиленной деградации в процессе работы мембранно-электродного блока. Как следствие, платиновый электрокатализатор перестает быть связанным с углеродным носителем, что влечет потерю производительности топливных элементов. Наноструктурированные углеродные материалы (нанотрубки, нановолокна и т.д.) являются более устойчивыми и способны заменять сажу в ряде случаев [12–15]. Карбонизованные углеродные нановолокна могут быть получены методом электроспиннинга из полимерного раствора с последующим пиролизом [16–21]. В предыдущих работах [22–29] показано, что данные углеродные нановолокона на основе как полиакрилонитрила, так и других полимеров, например полибензимидазола (ПБИ) или PIM-1 (один из полимеров с внутренней микропористостью; аббр. от англ. “Polymer of Intrinsic Microporosity” − авт.) [30, 31], могут выступать носителями электрокатализатора для ВТ-ПОМТЭ для мембраны ПБИ–OPht, [28]. Тем не менее поиск новых устойчивых наноструктурированных углеродных материалов по-прежнему остается важной задачей.
В настоящей работе исследованы микропористые катоды, полученные методом электроспиннинга из раствора ПАН с добавлением поливинилпирролидона, сажи “Vulcan®XC-72” и солей Zr и Ni, с последующими стабилизацией и карбонизацией для применения в качестве катодов ВТ-ПОМТЭ. Проведены тесты топливных элементов, подтверждающие возможность их использования, а также выполнено моделирование влияния суммарного содержания электролита на его распределение между электродом и мембраной, что позволило осуществить оптимизацию пористой структуры мембранно-электродного блока.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Электроспиннинг из полимерного раствора осуществляли на установке “Elmarco NanospiderTM NS Lab” (Чехия) с получением нановолоконного мата. Исходный раствор состоял из 3.25 г полиакрилонитрила с Mw = 150 × 103, 0.3 г поливинилпирролидона (ПВП) с Mw = 58 × 103 и 0.25 г сажи “Vulcan® XC-72” с добавками 0.37 г Ni(OAc)2⋅4H2O и 0.03 г ZrCl4 в 50 мл ДМФА. Раствор диспергировали в течение 3 ч на ультразвуковой бане. Электроспиннинг проводили при относительной влажности 18% и температуре 28°С. Расстояние между электродами составляло 190 мм при напряжении 69 кВ. ПВП удаляли из полученного нановолоконного мата экстракцией этанолом в аппарате Сокслета в течение 6 ч до полного исчезновения ИК-полосы поглощения группы СО поливинилпирролидона при 1660 см–1.
Образцы нановолоконного карбонизованного материала получали путем термической обработки электроспиннингового мата при 330 или 350°С в течение 2 ч на воздухе с последующим пиролизом в вакууме в течение 2 ч при 900 или 1000°С.
Элементный состав устанавливали с помощью C,H,N-анализатора с термодесорбционной колонкой “VarioMicroCube” (“Elementar”, Германия). Zr и Ni определяли методом рентгено-флуоресцентного анализа с помощью рентгенофлуоресцентного спектрометра “VRA-30” (“CarlZeiss”, Германия). Температура отжига, электропроводности и элементный состав для каждого образца указаны в табл. 1. Измерения продольной электрической проводимости пиролизованных нановолоконных матов выполняли с помощью четырехконтактного цифрового измерителя “RLC E7-8” (Россия), для чего образец шириной 1 см закрепляли между электродами с расстоянием между ними 1.2 см. Толщину образца устанавливали с помощью толщиномера “eXacto ElektroPhysik” (Германия).
Таблица 1.
Температура стабилизации (окисления) и карбонизации (пиролиза), электрическая проводимость и элементный состав образцов
| Образец, № | Температура, °С | S, См см–1 | Элементный состав, % | |||||
|---|---|---|---|---|---|---|---|---|
| окисления | пиролиза | С | N | H | Ni | Zr | ||
| 1 | 350 | 1000 | 20.8 | 86.63 | 2.33 | 0.63 | 1.98 | 0.72 |
| 2 | 330 | 1000 | 33.9 | 87.32 | 2.26 | 0.53 | 1.83 | 0.67 |
| 3 | 350 | 900 | 8.3 | 76.19 | 7.75 | 0.83 | 1.87 | 0.71 |
| 4 | 330 | 900 | 10.4 | 75.66 | 8.09 | 0.91 | 1.88 | 0.63 |
Представление порограмм, а также определение пористости и удельной поверхности образцов осуществляли с помощью метода эталонной контактной порометрии (МЭКП) [32–34]. Данный метод дает возможность получать кривые распределения объема и поверхности пор по радиусу в максимальном диапазоне от ∼1 до 105 нм и, в отличие от других методов, исследовать гидрофильно-гидрофобные свойства материалов. Далее образцы и эталоны (диски из кермета диаметром 20 мм и толщиной 1.4 мм) выдерживали в вакууме при температуре 170°С и таким образом из их пор удаляли все содержавшиеся в них вещества, включая сконденсированную воду. После чего образцы и эталоны взвешивали и выполняли измерения согласно работам [32, 33]. Полученные результаты для каждой точки порометрической кривой выдерживали до достижения равновесия.
Нанесение платины на углеродный карбонизованный нановолоконный мат площадью 6.76 см2 проводили в 10 мл смеси изопропанол:вода в соотношении 1 : 2 по объему, содержащей 0.5 г HCOOH и рассчитанное количество добавленного H2[PtCl6] ⋅ 6H2O, с целью получения материала с содержанием платины 1.0–1.2 мг см–2.
Электрохимически активную поверхность платины в синтезированных катализаторах измеряли в трехэлектродной ячейке с разделением пространства электродов в 0.5 моль/л H2SO4. В качестве электрода сравнения применяли Ag/AgCl–KClнас. Также использовали противоэлектрод из платиновой проволоки. Значения потенциала на кривых приводили относительно стандартного водородного электрода сравнения (СВЭ). Растворенный в электролите кислород удаляли с помощью барботажа азота. В качестве рабочего электрода использовали полированный диск из пиролитического графита диаметром 1.6 см с нанесенным тонким слоем исследуемого катализатора. Боковые поверхности диска изолировали фторопластом. К навеске катализатора 2–3 мг добавляли 1 мл смеси вода : изопропанол (1 : 1) и 5 мкл 5%-ного раствора иономера “Nafion”. После обработки в ультразвуковой ванне в течение 30 мин имели суспензию, 100 мкл которой с промежуточным просушиванием равномерно наносили на торцевую поверхность диска. Циклические вольтамперограммы адсорбции/десорбции водорода получали на платине при скорости развертки потенциала 50 мВ с–1 в интервале значений потенциала 0–1.3 В стандартного водородного электрода сравнения. Обычно для стабилизации вольтамперограмм достаточно тридцати циклов. Электрохимически активную площадь поверхности Pt (ЭАПП) определяли интегрированием области электрохимической десорбции водорода с поправкой на значения тока заряжения двойного слоя, принимая величину удельного заряда 0.21 мКл см–2 [35].
Испытания катодов топливных элементов осуществляли в стандартных ячейках “Arbin Instruments” при температуре 180°С. Стандартные коммерческие образцы анодов “Celtec®-P Series 1000 MEA”, содержащие платину, нанесенную на сажу “Vulcan® XC-72” с общей загрузкой Pt 1 мг см–2 [36, 37], и мембрану ПБИ-OPht, разработанную в нашей группе ранее [28], сшитую с помощью Zr(acac)2 и допированную o-фосфорной кислотой (350–400%, до 25 молекул H3PO4 на полимерное звено), применяли для сборки топливных элементов. Сборку мембранно-электродного блока проводили из анода, мембраны и катода, используемого в виде целостного пиролизованного мата. Мембранно-электродный блок зажимали между двумя графитовыми биполярными пластинами. Площадь рабочей поверхности составляла 5 см2. На анод подавали водород, полученный с помощью генератора ГВЧ-6 (“Химэлектроника”, Россия), методом электролиза, на катод – атмосферный воздух. Все газы находились при атмосферном давлении без дополнительного увлажнения.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для получения нановолоконных матов осуществлен электроспиннинг из раствора полиакрилонитрила в ДМФА. При добавлении ПВП к раствору ПАН наблюдалась полная совместимость компонентов при выбранной концентрации, что в дальнейшем приводило к равномерному распределению ПВП в нановолокне. Впоследствии экстракционного удаления ПВП этанолом и разложения его остатков при температуре >220°C ожидалось, что произойдет образование микропористости после стабилизации (330–350°С) и пиролиза (900–1000°С). Также для получения формовочного раствора в него были введены соли циркония и никеля. По нашим представлениям никель способен увеличивать степень графитизации материала при пиролизе [38], и еще, благодаря восстановлению никеля при пиролизе, играть роль центров, на которых предпочтительно происходит количественное осаждение платины из водного раствора H2[PtCl6]. После пиролиза цирконий существует в виде ZrOx [27] и, предположительно, в условиях работы мембранно-электродного блока образует кислые фосфаты циркония, которые могли бы способствовать увеличению протонной проводимости.
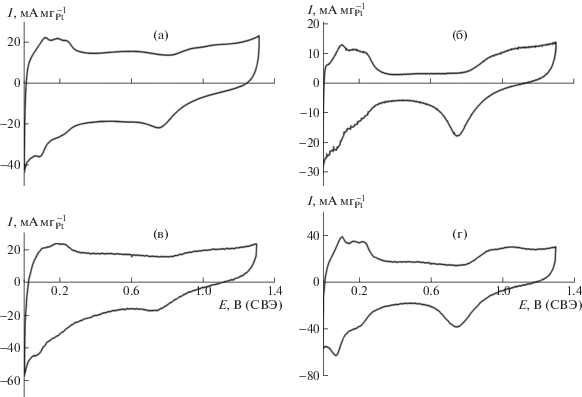
Данные циклической вольтамперометрии приведены на рис. 1 и в табл. 2. Видно, что показатели ЭАПП Pt оказались удовлетворительными для возможной работы электрокатализаторов в качестве электродов для топливных элементов. Несколько завышенное значение ЭАПП Pt 35.4 м2г–1 для платинированного образца 4, вероятно, объясняется большей площадью поверхности микропор по сравнению с другими образцами. Тем не менее точно предсказать характеристики ВТ-ПОМТЭ на основании данных ЭАПП Pt по циклическим вольтамперограммам нельзя, в том числе из-за работы электрокатализатора в ВТ-ПОМТЭ при повышенной температуре в фосфорнокислотной среде.
Таблица 2.
Данные по электрохимически активной поверхности для образцов с нанесенной платиной, а также по общей пористости и общей удельной поверхности для неплатинированных образцов, доля удельной площади поверхности микропор χ
| Образец, № | ЭАПП Pt, м2 г$_{{{\text{Pt}}}}^{{ - 1}}$ | V, см3 см–3 | Sуд, м2 г–1 | χ, % | ||
|---|---|---|---|---|---|---|
| макро- и мезопор | микропор | общая | ||||
| 1 | 12.4 | 0.819 | 54 | 38 | 92 | 41 |
| 2 | 19.0 | 0.876 | 53 | 40 | 93 | 43 |
| 3 | 13.4 | 0.882 | 42 | 66 | 108 | 61 |
| 4 | 35.4 | 0.875 | 27 | 84 | 111 | 76 |
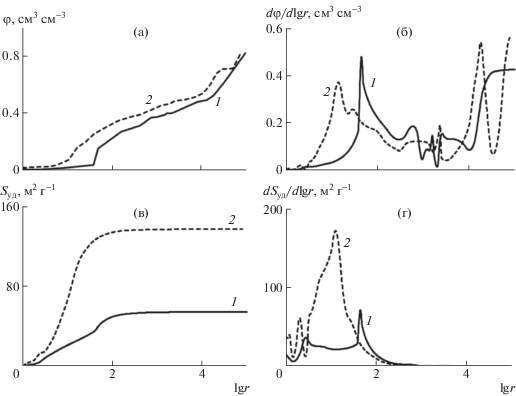
Рис. 2.
Интегральное (а, в) и дифференциальное (б, г) распределение объема (а, б) и поверхности (в, г) пор по логарифму радиуса пор (r/нм), измеренное с помощью МЭКП по октану (1) и воде (2) для образца 1.
Исследования пористой структуры образцов были проведены методом эталонной контактной порометрии по октану (табл. 2; рис. 3). В целом, после пиролиза при 900°С общая удельная площадь поверхности оказалась немного выше (108 и 111 м2 г–1) по сравнению с материалом после пиролиза при 1000°С (92 и 93 м2 г–1). Вместе с тем доля удельной площади поверхности микропор уменьшалась, а доля удельной площади поверхности мезо- и макропор повышалась. Увеличение температуры предварительного окисления с 330 до 350°С также повышает долю площади поверхности мезо- и макропор и уменьшает общую удельную площадь поверхности и долю площади поверхности микропор. Такие эффекты, возможно, связаны с частичным “схлопыванием” микропор после пиролиза при более высокой температуре. Результаты детального исследования пористой структуры представлены на рис. 3, где показаны интегральные и дифференциальные кривые распределения объема и поверхности пор по радиусам. Значения радиусов приведены в логарифмической шкале вследствие их очень широкого диапазона в пять порядков.
Рис. 3.
Интегральное (а, в) и дифференциальное (б, г) распределение объема (а, б) и поверхности (в, г) пор по логарифму радиуса пор (r/нм), измеренное с помощью МЭКП по октану для образцов 1 (1), 2 (2), 3 (3) и 4 (4).
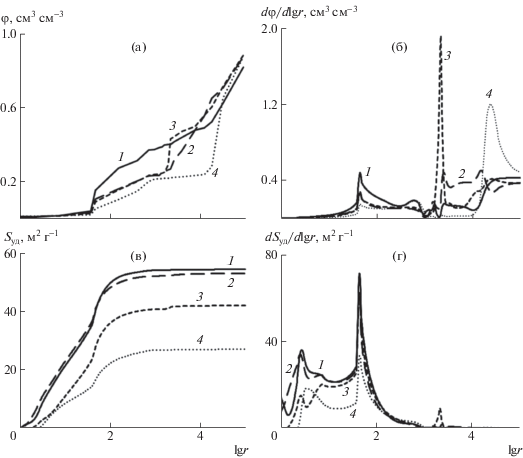
Гидрофильно-гидрофобные свойства материалов можно оценить при получении порограмм по октану и воде (рис. 3). Так, интегральные значения пористости и удельной площади поверхности при измерении по воде превышают аналогичные интегральные значения в случае измерения по октану (рис. 3а, 3в). Для образца 1 дифференциальные величины пористости и удельной площади поверхности в случае измерений по воде существенно превышают аналогичные значения при измерении по октану в диапазоне радиусов пор ∼3–30 нм (рис 3б, 3г). Это свидетельствует о “супергидрофильных” свойствах мезопор, тогда как более крупные поры (макропоры) смачиваются хуже.
Результаты испытаний платинированных образцов в качестве катодов для ВТ-ПОМТЭ представлены в табл. 3. Из таблицы видно, что величины напряжения при заданных значениях плотности тока не слишком высоки. Широко используемый для многочисленных применений метод спектроскопии электрохимического импеданса (СЭИ) позволяет установить величину сопротивления мембраны топливного элемента [39–42]. Так, в процессе работы топливного элемента величина сопротивления мембраны увеличивается для образца 1 с 70 до 90 мОм см2, для образца 2 c 60 до 70 мОм см2 и для образца 3 с 85 до 95 мОм см2. Для более детального анализа данного эффекта был проведен анализ порометрических кривых для мембранно-электродного блока с использованием двух электродов (образец 1) и мембраны ПБИ-OPht (рис. 4).
Таблица 3.
Мощность и вольтамперная характеристика для мембранно-электродного блока ВТ-ПОМТЭ с платинированными образцами в качестве катодов при 180°С
| Образец, № | U, В | W, Вт см–2 | |||
|---|---|---|---|---|---|
| напряжение разомкнутой цепи | 0.2 А cм–2 | 0.4 А cм–2 | 0.2 А cм–2 | 0.4 А cм–2 | |
| 1 | 0.903 | 0.601 | 0.500 | 0.120 | 0.200 |
| 2 | 0.890 | 0.599 | 0.481 | 0.120 | 0.192 |
| 3 | 0.850 | 0.507 | 0.406 | 0.101 | 0.162 |
Рис. 4.
а – Зависимость объема пор V(r) от логарифма радиуса пор (r/нм) для мембраны ПБИ-OPht (1) и электродов (2) для образца 1; б – зависимость объема пор V(r) мембраны ПБИ-OPht (1) и удвоенного объема пор (2) для образца 1 от суммарного объема пор мембранно-электродного блока ΣV(r).
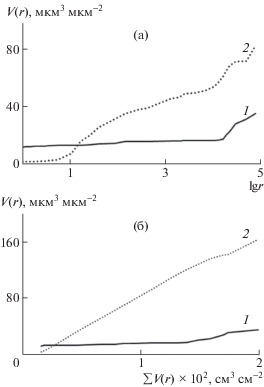
На рис. 4а для сравнения показана зависимость объема пор для мембраны ПБИ‑OPht (кривая 1) и для электродов (образец 1) по воде от логарифма радиуса пор. Толщина мембраны и каждого электрода L принималась равной 100 мкм. Также допускалось, что пористость платинированного электрода почти не отличается от пористости неплатинированного образца, как это было представлено в предыдущей работе [24].
График на рис. 4б был построен следующим образом. Каждому значению объема пор V(r) на кривых 1 и 2 (рис. 4а) ставится в соответствие ΣV(r), полученная суммированием значений на этих двух кривых при одном и том же значении r. Далее величина ΣV(r) откладывается по оси абсцисс, а соответствующие ей значения V(r) располагаются на оси ординат (рис. 4б). Данные графика демонстрируют, что (в предположении близких смачивающих свойств фосфорной кислоты и воды [43]) при уменьшении влагосодержания в мембранно-электродном блоке, очевидно, в первую очередь будет происходить относительно существенный отток влаги из крупных пор электрода и мембраны. Для газодиффузионного электрода это не так важно, потому что в электроде должна реализовываться диффузия газов, но это имеет критическое значение для мембраны, так как отток кислоты из нее способен приводить к увеличению ее сопротивления и ухудшению основных показателей работы блока. Можно предположить, что фосфорная кислота перемещается в микропоры электрода. Из-за размерного эффекта (молекулы фосфорной кислоты крупнее молекул воды) попадание кислоты в микропоры замедляется (по сравнению с водой), и начинает происходить только при работе мембранно-электродного блока. Таким образом, рис. 4 моделирует влияние изменений суммарного содержания электролита на его распределение между электродом и мембраной.
ЗАКЛЮЧЕНИЕ
Показана возможность изменения доли удельной площади поверхности микропор в зависимости от температуры окисления и пиролиза полиакрилонитрильных материалов на основе композиционных углеродных пиролизованных электроспиннинговых нановолоконных матов, содержащих никель и цирконий. Доля удельной площади поверхности микропор в образце влияет на основные характеристики работы мембранно-электродного блока и должна быть оптимизирована для работы топливных элементов. Полученные вольтамперные характеристики топливных элементов и значения электрохимически активной поверхности платины подтверждают возможность использования данных материалов в мембранно-электродном блоке ВТ-ПОМТЭ.
Исследование выполнено за счет гранта Российского научного фонда (проект № 18-13-00421). Элементный анализ проведен при поддержке Министерства науки и высшего образования Российской Федерации с использованием научного оборудования Центра исследования строения молекул ИНЭОС РАН.
Список литературы
Zhang J. PEM Fuel Cell Electrocatalyst and Catalyst Layers. London: Springer, 2008.
Li Q., Aili D., Hjuler H.A., Jensen J.O. High Temperature Polymer Electrolyte Membrane Fuel Cells, Approaches, Status and Perspectives.Cham; Heidelberg; New York; Dordrecht; London: Springer, 2016.
Wang Y., Chen K.S., Mishler J., Cho S.C., Adroher X.C. // Appl. Energy. 2011. V. 88. P. 981.
Borup R., Meyers J., Pivovar B., Kim Y.S., Mukundan R., Garland N., Myers D., Wilson M., Garzon F., Wood D., Zelenay P., More K., Stroh K., Zawodzinski T., Boncella J., McGrath J.E., Inaba M., Miyatake K., Hori M., Ota K., Ogumi Z., Miyata S., Nishukata A., Siroma Z., Uchimoto Y., Yasuda K., Kimijima K., Iwashita N. // Chem. Rev. 2007. V. 107. P. 3904.
Myles T., Bonville L., Maric R. // Catalysts. 2017. V. 7. P. 16.
Araya S.S., Zhou F., Liso V., Sahlin S.L., Vang J.R., Thomas S., Gao X., Jeppesen C., Kaer S.K. // Int. J. Hydrogen Energy. 2016. V. 41. P. 21310.
Debe M.K. // Nature. 2012. V. 486. P. 43.
Chandan A., Hattenberger M., El-kharouf A., Du S., Dhir A., Self V., Pollet B.G., Ingram A., Bujalski W. // J. Power Sources. 2013. V. 231. P. 264.
Zeis R. // Beilstein J. Nanotechnol. 2015. V. 6. P. 68.
Steele B.C., Heinzel A. // Nature. 2001. V. 414. P. 345.
Arsalis A. // Renew. Sust. Energ. Rev. 2019. V. 105. P. 391.
Zamora H., Plaza J., Canizares P., Lobato J., Rodrigo M.A. // Chem. Sus. Chem. 2016. V. 9. P. 1187.
Wang X.X., Tan Z.H., Zeng M., Wang J.N. // Sci. Rep. 2014. V. 4. P. 4437.
Jeon Y., Park J.-I., Ok J., Dorjgotov A., Kim H.-J., Kim H., Lee C., Park S., Shul Y.-G. // Int. J. Hydrogen Energy. 2016. V. 41. P. 6864.
Chan S., Jankovic J., Susac D., Saha M.S., Tam M., Yang H., Ko F. // J. Mater. Sci. 2018. V. 53. P. 11633.
Inagaki M., Yang Y., Kang F. // Adv. Mater. 2012. V. 24. P. 2547.
Tenchurin T.Kh., Krasheninnikov S.N., Orekhov A.S., Chvalun S.N., Shepelev A.D., Belousov S.I., Gulyaev A.I. // Fibre Chem. 2014. V. 46. P. 151.
Kopec M., Lamson M., Yuan R., Tang C., Kruk M., Zhong M., Matyjaszewski K., Kowalewski T. // Prog. Polym. Sci. 2019. V. 92. P. 89.
Dong Z., Kennedy S.J., Wu Y. // J. Power Sources. 2011. V. 196. P. 4886.
Yusof N., Ismail A.F. // J. Anal. Appl. Pyrol. 2012. V. 93. P. 1.
Zhang B., Kang F., Tarascon J.-M., Kim J.-K. // Prog. Mater. Sci. 2016. V. 76. P. 319.
Ponomarev I.I., Skupov K.M., Razorenov D.Yu., Zhigalina V.G., Zhigalina O.M., Ponomarev Iv.I., Volkova Yu.A., Kondratenko M.S., Bukalov S.S., Davydova E.S. // Russ. J. Electrochem. 2016. V. 52. P. 735.
Zhigalina V.G., Zhigalina O.M., Ponomarev I.I., Skupov K.M., Razorenov D.Y., Ponomarev I.I., Kiselev N.A., Leitinger G. // Cryst. Eng. Comm. 2017. V. 19. P. 3792.
Skupov K.M., Ponomarev I.I., Razorenov D.Yu., Zhigalina V.G., Zhigalina O.M., Ponomarev Iv.I., Volkova Yu.A., Volfkovich Yu.M., Sosenkin V.E. // Russ. J. Electrochem. 2017. V. 53. P. 728.
Skupov K.M., Ponomarev I.I., Razorenov D.Y., Zhigalina V.G., Zhigalina O.M., Ponomarev I.I., Volkova Y.A., Volfkovich Y.M., Sosenkin V.E. // Macromol. Symp. 2017. V. 375. P. 1600188.
Ponomarev I.I., Skupov K.M., Ponomarev Iv.I., Razorenov D.Yu., Volkova Yu.A., Basu V.G., Zhigalina O.M., Bukalov S.S., Volfkovich Yu.M., Sosenkin V.E. // Russ. J. Electrochem. 2019. V. 55. P. 552.
Ponomarev I.I., Skupov K.M., Naumkin A.V., Basu V.G., Zhigalina O.M., Razorenov D.Y., Ponomarev Iv.I., Volkova Yu.A. // RSC Adv. 2019. V. 9. P. 257.
Kondratenko M.S., Ponomarev I.I., Gallyamov M.O., Razorenov D.Y., Volkova Y.A., Kharitonova E.P., Khokhlov A.R. // Beilstein J. Nanotechnol. 2013. V. 4. P. 481.
Vol’fkovich Y.M., Ponomarev Iv.I., Sosenkin V.E., Ponomarev I.I., Skupov K.M., Razorenov D.Y. // Prot. Met. Phys. Chem. Surf. 2019. V. 55. P. 195.
Low Z.-X., Budd P.M., McKeown N.B., Patterson D.A. // Chem. Rev. 2018. V. 118. P. 5871.
McKeown N.B. // Sci. China Chem. 2017. V. 60. P. 1023.
Volfkovich Yu.M., Sakars A.V., Volinsky A.A. // Int. J. Nanotechnol. 2005. V. 2. P. 292.
Volfkovich Yu.M., Filippov A.N., Bagotsky V.S. Structural Properties of Porous Materials and Powders Used in Different Fields of Science and Technology. London: Springer, 2014.
Rouquerol J., Baron G., Denoyel R., Giesche H., Groen J., Klobes P., Levitz P., Neimark A.V., Rigby S., Skudas R., Sing K., Thommes M., Unger K. // Pure Appl. Chem. 2011. V. 84. P. 107.
Conway B.E., Angerstein-Kozlowska H. // Acc. Chem. Res. 1981. V. 14. P. 49.
Schmidt T.J., Baurmeister J. // J. Power Sources. 2008. V. 176. P. 428.
Vielstich W., Gasteiger H.A., Yokokawa H. // Handbook of Fuel Cells, Fundamentals, Technology and Applications. Chichester: Wiley, 2009. V. 5.
Shiota I., Watanabe O. // J. Mater. Sci. 1979. V. 14. P. 1121.
Lasia A. Electrochemical Impedance Spectroscopy and Its Applications, in Modern Aspects of Electrochemistry / Ed. by B.E. Conway, J. Bockris, R.E. White. New York: Kluwer Academic/Plenum Publ., 1999.
Pajkossy T., Jurczakowski R. // Curr. Opin. Electrochem. 2017. V. 1. P. 53.
Skupov K.M., Hobbs J., Claverie J.P. // Prog. Org. Coat. 2009. V. 65. P. 314.
Niya S.M.R., Hoorfar M. // J. Power Sources. 2013. V. 240. P. 281.
Halter J., Gloor T., Amoroso B., Schmidt T.J., Buchi F.N. // Phys. Chem. Chem. Phys. 2019. V. 21. P. 13126.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия С)