Химия высоких энергий, 2020, T. 54, № 3, стр. 186-191
Исследование фотопроцессов 3,3'-диэтил-5,5'-дихлортиакарбоцианина в воде и метаноле
Т. В. Федотова a, b, Г. В. Захарова a, *, В. Н. Гутров a, В. П. Маркелов a, Т. А. Святославская a, Н. Л. Святославский a, А. К. Чибисов a, b, **, С. К. Сазонов a, С. П. Громов a
a Центр фотохимии РАН, Федеральное государственное учреждение “Федеральный научно-исследовательский центр “Кристаллография и фотоника” Российской академии наук”
119421 Москва, ул. Новаторов, 7а, кор. 1, Россия
b Московский физико-технический институт (государственный университет)
141701 Московская обл., Долгопрудный, Институтский пер., Россия
* E-mail: gvzakharova@gmail.com
** E-mail: alexander.chibisov@gmail.com
Поступила в редакцию 08.10.2019
После доработки 04.12.2019
Принята к публикации 04.12.2019
Аннотация
Исследованы фотопроцессы 3,3'-диэтил-5,5'-дихлортиакарбоцианина при прямом и сенсибилизированном фотовозбуждении в метаноле и в воде в отсутствие и в присутствии кукурбит[7]урила. При импульсном лазерном возбуждении имеет место преимущественно процесс транс-цис изомеризации красителя, протекающий через синглетно-возбужденное S*-состояние красителя. Населенность молекул красителя на триплетном Т-уровне возрастает при сенсибилизированном возбуждении в результате триплет-триплетного переноса энергии от донора триплетной энергии (антрацен и антраценкарбоновая кислота) на краситель (акцептор). Одними из путей дезактивации молекул в Т-состоянии являются перенос электрона и обратный интеркомбинационный Т→S* переход. Составляющими компонентами процесса дезактивации S*-состояния, образующегося при Т→S* переходе, являются как быстрая, так и замедленная флуоресценции. Присутствие кукурбит[7]урила в водном растворе красителя не оказывает заметного влияния на механизм фотопроцессов красителя, однако, способствует димеризации и увеличению выхода в Т-состояние, главным образом, димеров, а также времени жизни цис-изомеров красителя.
Известно, что молекулы полиметиновых красителей проявляют способность к транс-цис фотоизомеризации в растворах [1–12]. Ранее нами было показано, что реакция транс-цис фотоизомеризации 3,3'-диэтилтиакарбоцианина протекает через синглетно-возбужденное состояние [1–3]. Основанием для сделанного вывода были впервые полученные спектры поглощения 3,3'-диэтилтиакарбоцианина при прямом и сенсибилизированном импульсном фотовозбуждении красителя в растворе. Существенное различие в спектрах поглощения свидетельствовало о том, что при сенсибилизированном возбуждении красителя имело место заселение триплетного уровня красителя. При прямом возбуждении наблюдаемые спектральные изменения обусловлены переходом исходной транс-формы красителя в цис-форму. Подобные результаты были получены для многих полиметиновых красителей [6, 7, 9, 10]. Особенностью молекул полиметиновых красителей является их способность к агрегации и, в частности, к димеризации в водных растворах [13]. Образование димеров проявляется в возникновении двух полос поглощения, смещенных в коротковолновую и длинноволновую области спектра, что является следствием расщепления синглетно-возбужденного уровня на два с более высоко и более низко расположенными уровнями по отношению к уровню свободного мономера (Давыдовское расщепление) [14]. Другой особенностью полиметиновых красителей является их склонность к образованию с молекулами кукурбит[7,8]урилов комплексов состава 1 : 1, 2 : 1 и 2 : 2 [15]. Было показано, что, образование комплексов оказывает влияние на протекание фотопроцессов в водных растворах. Стерические препятствия вращению концевых бензтиазольных групп способствуют усилению флуоресценции и интеркомбинационной конверсии в триплетное состояние красителя.
В настоящей работе приведены результаты ис-следования фотоники 3,3'-диэтил-5,5'-дихлортиакарбоцианина в метаноле и воде, полученные как при прямом импульсном лазерном возбуждении, так и при сенсибилизированном возбуждении путем триплет-триплетного переноса энергии, а также данные по влиянию кукурбит[7]урила на фотопроцессы красителя.
МЕТОДИКА ЭКСПЕРИМЕНТА
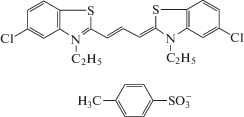
В качестве объекта исследования использовали катионный краситель 3,3'-диэтил-5,5'-дихлортиакарбоцианин (Кр+), имеющий в качестве противоиона п-толуолсульфонат, синтезированный в ЦФ РАН ФНИЦ “Кристаллография и фотоника” РАН по методике аналогично [16] и кукурбит[7]урил (КБ7) фирмы Aldrich. В качестве фотосенсибилизаторов применяли антрацен и 9-антраценкарбоновую кислоту (для водных растворов), Aldrich.
Измерение разностных спектров триплет-триплетного (Т-Т) поглощения и поглощения фотоизомера красителя, а также кинетики дезактивации триплетного состояния и перехода цис-изомера красителя в транс-изомер проводили на установке импульсного лазерного фотолиза [17]. Растворы красителя облучали импульсами лазера на иттрий-алюминий гранате (Nd : YAG, “Solar”, λ = 532 нм) с длительностью импульса 10 нс и энергией до 150 мДж. Облучение сенсибилизатора проводили лазерными импульсами при λ = 355 нм (энергия до 70 мДж). Измерение спектра замедленной флуоресценции проводили при отключенном зондирующем источнике света. Удаление кислорода воздуха достигали путем продувки раствора газообразным аргоном. Спектры основного поглощения регистрировали на спектрофотометре Agilent 8453, спектры флуоресценции – на спектрофлуориметре Varian Cary Eclipse. В качестве растворителя использовали метанол (Aldrich) и воду, очищенную с помощью системы Direct–Q3 Millipore. Концентрации реагентов: [Кр+] = (0.2–3) × × 10–5 моль/л; [КБ7] = (0.4–5) × 10–4 моль/л.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Поглощение и флуоресценция
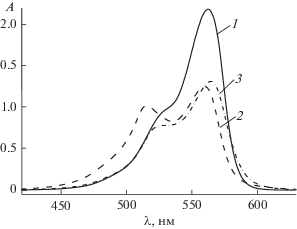
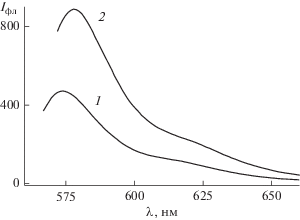
Известно, что тиакарбоцианиновые красители, не имеющие заместителя в полиметиновой цепи, находятся в растворе в виде транс-изомеров [4–6, 11, 12]. На рис. 1 приведены спектры поглощения Кр+ в метаноле и в воде (спектры 1, 2). Спектр Кр+ в метаноле с максимумом при 563 нм отвечает поглощению мономеров красителя. Спектр Кр+ в воде характеризуется двумя максимумами при 560 и 516 нм, относящимися к поглощению мономеров и димеров красителя, соответственно. Добавление КБ7 к раствору Кр+ в воде приводит к спектральным изменениям, проявляющимся, во-первых, в уменьшении поглощения димеров и росте поглощения мономеров и, во-вторых, в батохромном сдвиге максимумов поглощения на 10 и 5 нм соответственно (рис. 1, спектр 3). Наблюдаемые изменения в спектре поглощения указывают на образование комплексов между Кр+ и КБ7, как это было показано для 3,3'-диэтил-5,5'-дихлор-9-этилтиакарбоцианина [18, 19]. Образование комплекса подтверждается люминесцентными измерениями. На рис. 2 приведены спектры флуоресценции водного раствора Кр+, измеренные в отсутствие и в присутствии КБ7, из которых следует батохромный сдвиг максимума флуоресценции на 4 нм и увеличение интенсивности флуоресценции в 1.9 раза в присутствии КБ7 для мономеров красителя.
Импульсное фотовозбуждение
При импульсном лазерном облучении обескислороженных растворов Кр+ в метаноле и воде наблюдали кратковременные обратимые изменения в спектре поглощения красителя. На рис. 3 приведены разностные спектры поглощения растворов Кр+, измеренные к различным моментам времени после лазерного облучения.
Рис. 3.
Разностные спектры поглощения Кр+ (1.8 × 10–5 моль/л) в обескислороженных метаноле (а) и воде в отсутствие (б) и в присутствии (в) КБ7 при прямом (в) и сенсибилизированном (г) возбуждении, измеренные через различные промежутки времени после лазерного импульса. Вставка – кинетические кривые образования и гибели триплетного состояния и катион-радикала красителя в комплексе с КБ7 (4 × 10−4 моль/л) при сенсибилизированном возбуждении.
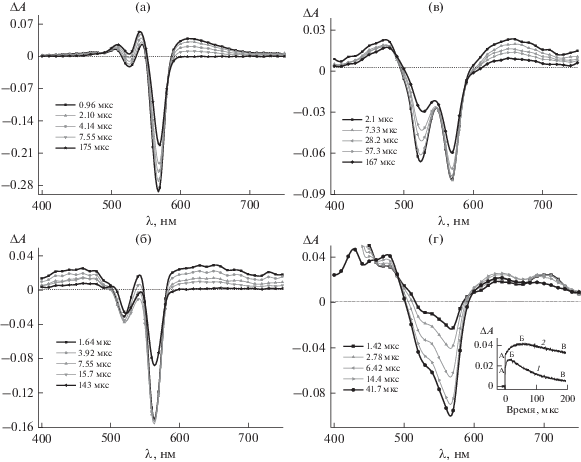
Разностные спектры поглощения характеризуются положительными и отрицательными максимумами. Положительные максимумы (рис. 3а) при 50–510 и 540–545 нм относятся к поглощению цис-изомера, образующегося из исходной транс-формы красителя. Вывод об образовании цис-изомера следует из сходства приведенных результатов с ранее полученными данными для ти-акарбоцианинов [2, 6, 8, 9]. Положительные максимумы при 600–620 нм в метаноле относятся к Т-Т поглощению мономеров Кр+. Широкая бесструктурная длинноволновая полоса (λ > 590 нм) в водном растворе (рис. 3б) обусловлена суммарным Т-Т поглощением димеров и мономеров Кр+, находящихся в равновесии. Бесструктурную длинноволновую полосу ранее наблюдали для димеров сульфопроизводных тиакарбоцианинов в воде при лазерном возбуждении [13]. Т-Т поглощение исчезает при впуске воздуха в обескислороженный раствор в результате тушения Т-состояния красителя кислородом. Отрицательные максимумы при 520 и 570 нм в метаноле (рис. 3а) являются характерными для спектров выцветания Кр+ и обусловлены различием в коэффициентах экстинкции транс- и цис-изомеров, а также молекул Кр+ в Т-состоянии, тогда как в водном растворе (рис. 3б) отрицательный максимум при 520 обусловлен обеднением основного уровня димеров Кр+. При лазерном возбуждении было обнаружено поглощение в области 420–480 нм. Полосу при 470 нм можно отнести к суммарному поглощению цис-изомера и полуокисленной формы красителя (дикатион-радикал, Кр2+•). Образование Кр2+• подтверждается сокращением времени жизни в присутствии донора электрона – аскорбиновой кислоты, восстанавливающей Кр2+• до исходного красителя Кр+. Наряду с Кр2+• можно было ожидать образование полувосстановленной формы (нейтральный радикал, Кр•). Радикалы Кр2+• и Кр• могут образоваться в результате переноса электрона между двумя триплетными молекулами красителя, а также при взаимодействии триплетной молекулы Кр+ с невозбужденным красителем.
Лазерное возбуждение обескислороженного водного раствора Кр+ в присутствии КБ7 сопровождается изменениями в разностном спектре поглощения (рис. 3в), проявляющимися в увеличении отрицательного поглощения при 520 нм и появлении положительных максимумов при 650 и 470 нм. Максимумы обусловлены Т-Т поглощением и поглощением Кр2+• в комплексе Кр+ с КБ7. Максимум при 650 нм отвечает в основном Т-Т поглощению димеров Кр+ в комплексе с КБ7. Возникновение широкой длинноволновой полосы Т-Т с максимумом при 650 нм было зарегистрировано в [15] для димеров 3,3'-диэтилтиакарбоцианина в комплексе с кукурбит[8]урилом. Увеличение выцветания при 520 нм в разностном спектре Кр+ в присутствии КБ7 по сравнению с выцветанием свободного красителя (рис. 3б) указывает на более эффективно протекающую интеркомбинационную конверсию в Т-состояние димеров Кр+ в комплексе с КБ7 по сравнению со свободным красителем. Поглощение цис-изомера маскируется выцветанием димера красителя. Кинетические измерения показали увеличение времен жизни Т-состояния димеров, мономеров и катион-радикалов красителя в комплексе.
В работе были также выполнены спектрально-кинетические измерения при сенсибилизированном лазерном возбуждении Кр+ в воде в присутствии КБ7, используя в качестве сенсибилизатора 9-антраценкарбоновую кислоту. Необходимо отметить, что Кр+ образует комплекс с антраценкарбоновой кислотой, для которого характерна низкая фотоустойчивость. Добавление кукурбит[7]урила в раствор приводит к образованию фотоустойчивого комплекса Кр+ с КБ7, что препятствует взаимодействию Кр+ с антраценкарбоновой кислотой. Лазерное возбуждение антраценкарбоновой кислоты в присутствии Кр+ и КБ7 приводит к заселению триплетного уровня сенсибилизатора с последующим переносом энергии на молекулу Кр+. Положение триплетного уровня сенсибилизатора EТ = 14706 см–1 [20], положение триплетного уровня красителя ${\text{E}}_{{\text{T}}}^{{{\text{Кр}}}}$ = 13514 см–1 определили из спектра фосфоресценции Кр+ в ацетонитриле при 77 К. Следствием Т-Т переноса энергии явилось образование триплетных молекул и катион-радикала красителя (рис. 3г), поглощающих при 640 и 480 нм соответственно. Поглощение при λ > 680 нм и λ < 460 нм обусловлено поглощением продуктов фотовозбуждения антраценкарбоновой кислоты [21]. На вставке рис. 3г приведены кинетические кривые образования и гибели Т-состояния и катион-радикала Кр+ в комплексе с КБ7. Участок АБ (кривая 1) – заселение Т-уровня Кр+ в комплексе с КБ7 при Т-Т переносе энергии, участок БВ – дезактивация триплетного состояния Кр+. Участок АБ (кривая 2) – образование Кр2+•, участок БВ – кинетика исчезновения Кр2+•. Из вставки рис. 3г следует, что время достижения максимальной концентрации катион-радикала (60 мкс) превышает время достижения максимальной концентрации Кр+ в триплетном состоянии (15 мкс). Наблюдаемый временной сдвиг (18 мкс) обусловлен меньшей скоростью гибели катион-радикала по сравнению со скоростью дезактивации Т-состояния Кр+.
Результатом Т-Т переноса явилось также обнаружение замедленной флуоресценции мономеров и димеров Кр+ в комплексе с КБ7, как следствие заселения возбужденного уровня красителя при обратном интеркомбинационном переходе Т→${\text{S}}_{1}^{*}.$ На рис. 4 приведен спектр замедленной флуоресценции, характеризующийся двумя максимумами, расположенными при 590 и 630 нм и соответствующими мономерам и димерам Кр+ в комплексах с КБ7.
Рис. 4.
Спектр замедленной флуоресценции Кр+ в комплексах с КБ7 в обескислороженном водном растворе, измеренный при сенсибилизированном возбуждении красителя через 10 мкс после лазерного импульса.
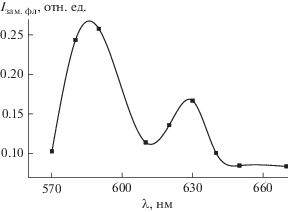
Отнесение максимума в спектре замедленной флуоресценции при 630 нм к димерам Кр+ в комплексе следует из спектров обычной (быстрой) флуоресценции и возбуждения флуоресценции в обескислороженных растворах (рис. 5). Из рис. 5а следует, что при возбуждении флуоресценции в полосе поглощения димеров Кр+ в комплексе с КБ7 (525 нм) в спектре обычной флуоресценции происходит увеличение интенсивности в области > 600 нм по сравнению со спектром флуоресценции, полученным при возбуждении в полосе поглощения мономеров Кр+ (560 нм). Кроме того, при измерении спектров возбуждения флуоресценции и регистрации флуоресценции при 630 нм наблюдали увеличение интенсивности флуоресценции при 530 нм, соответствует поглощению димеров Кр+ в комплексе с КБ7 (рис. 1). Время жизни замедленной флуоресценции составляет 15 и 18 мкс для димеров и мономеров красителя в комплексе с КБ7.
Рис. 5.
Нормированные спектры флуоресценции (а) и возбуждения флуоресценции (б) обескислороженного раствора Кр+ (2.2 × 10–6 моль/л) в присутствии КБ7 (4 × × 10–5 моль/л). (а) λex = 560 нм (1) и λex = 525 нм (2); (б) λem = 580 нм (1) и λem = 630 нм (2).
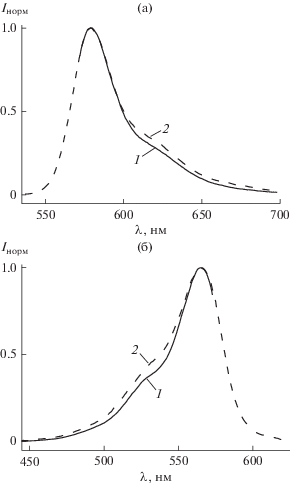
Таким образом, на основании полученных результатов можно сделать следующие выводы:
1. Краситель 3,3'-диэтил-5,5'-дихлортиакарбоцианин (Кр+) проявляет способность к транс-цис изомеризации и интеркомбинационной конверсии в триплетное состояние в метаноле и воде.
2. Кр+ в воде обнаруживает склонность к димеризации, при этом димеры Кр+ способны к переходу в триплетное состояние.
3. Димеры красителя в комплексе с КБ7 характеризуются увеличением эффективности интеркомбинационной конверсии в триплетное состояние.
4. Мономеры и димеры красителя в комплексах с КБ7 проявляют способность к замедленной флуоресценции при сенсибилизированном заселении триплетного уровня красителя.
5. Наличие замедленной флуоресценции указывает на возможность процесса обратной (Т→S*) интеркомбинационной конверсии.
6. При сенсибилизированном возбуждении триплетное состояние может выступать в качестве промежуточного продукта на пути транс-цис фотоизомеризации.
Список литературы
Чибисов А.К. // Журн. эксперим. и теорет. химии. 1966. Т. 2. № 6. С. 825.
Лифанов Ю.И., Кузьмин В.А., Карякин А.В., Чибисов А.К., Левкоев И.И. // Изв. АН СССР. Cер. хим. 1973. № 4. С. 1933.
Лифанов Ю.И., Кузьмин В.А., Чибисов А.К., Левкоев И.И., Карякин А.В. // Журн. прикл. спектроскопии. 1974. Т. 20. № 2. С. 221.
Колесников А.М., Михайленко Ф.А. // Успехи химии. 1987. Т. 56. Вып. 3. С. 466.
Ponterini G., Momicchioli F. // Chem. Phys. 1991. V. 151. № 1. P. 111.
Tyutyulkov N., Fabian J., Mehlhorn A., Dietz F., Tadjer A. Polymethine Dyes, Sofia: St. Kliment Ohridski Univ. Press, 1991.
Чибисов А.К., Захарова Г.В. // Журн. науч. и прикл. фотографии. 1995. Т. 40. № 6. С. 1.
Khimenko V.N., Chibisov A.K., Görner H. // J. Phys. Chem., A. 1997. V. 101. № 39. P. 7304.
Шведов С.В., Чибисов А.К. // Журн. науч. и прикл. фотографии. 2000. Т. 45. № 6. С. 35.
Chibisov A.K., Shvedov S.V., Görner H. // J. Photochem. Photobiol. A: Chemistry. 2001. V. 141. № 1. P. 39.
Görner H., Chibisov A.K. // CRC Handbook Organic Photochemistry & Photobiology, 2nd Edition. 2004. P. 36-1.
Pronkin P., Tatikolov A. // Sci – Open Access Journal. 2019. V. 1. № 1. P. 19. https://doi.org/10.3390/sci1010019
Чибисов А.К. // Химия высоких энергий. 2007. Т. 41. № 3. С. 451.
Давыдов А.С. Теория твердого тела. М.: Наука, 1978.
Чибисов А.К., Алфимов М.В., Захарова Г.В., Атабекян Л.С., Авакян В.Г., Плотников В.Г. // Химия высоких энергий. 2017. Т. 51. № 6. С. 480.
Лазукина Л.А., Мушкало И.Л., Неплюев В.М., Кухар В.П. // Журн. орг. хим. 1983. Т. 19. № 11. С. 2417.
Захарова Г.В., Авакян В.Г., Маркелов В.П. и др. // Химия высоких энергий. 2015. Т. 49. № 6. С. 451.
Захарова Г.В., Жижимов Д.А., Авакян В.Г., Сазонов С.К., Громов С.П., Чибисов А.К. // Химия высоких энергий. 2014. Т. 48. № 2. С. 104.
Zakharova G.V., Zhizhimov D.A., Sazonov S.K., Avakyan V.G., Gromov S.P., Görner H., Chibisov A.K. // J. Photochem. Photobiol. A: Chemistry. 2015. V. 302. P. 69.
Rao M., Kanagaraj K., Fan C., Ji J., Xiao C., Wei X., Wu W., Yang C. // Org. Lett. 2018. V. 20. № 6. P. 1680.
Williams S.L., Kirkpatrick I., Worrall D.R. // Photochem. Photobiol. Sci. 2010. V. 9. № 7. P. 937.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий