Химия высоких энергий, 2020, T. 54, № 3, стр. 235-244
Моделирование СВЧ разряда в жидком н-гептане в присутствии аргона в области разряда
Ю. А. Лебедев a, *, А. В. Татаринов a, И. Л. Эпштейн a
a ФГБУН Институт нефтехимического синтеза им. А.В. Топчиева РАН
119991 Москва, Ленинский пр., д. 29, Россия
* E-mail: lebedev@ips.ac.ru
Поступила в редакцию 19.11.2019
После доработки 19.11.2019
Принята к публикации 27.12.2019
Аннотация
Представлена нульмерная модель для СВЧ разряда в жидком н-гептане при атмосферном давлении при непрерывном вводе аргона в область плазмы. Модель включает в себя уравнения, описывающие образование твердой фазы из продуктов разложения н-гептана. Наряду с подробной кинетикой термического пиролиза н-гептана включены процессы, происходящие с участием атомов аргона и процессы с участием электронов, ионов и возбужденных частиц. Для определения функции распределения электронов по энергии используется уравнение Больцмана. Для сравнения со спектральными характеристиками разряда в кинетическую схему включены процессы возбуждения излучающих состояний атома водорода и молекулы С2. Проведенные расчеты позволили объяснить появление линий Hα при достаточно больших концентрациях вводимого аргона.
ВВЕДЕНИЕ
В последнее время интенсивно исследуются разряды в жидкостях [1–5] и, в частности, СВЧ разряды [6–8]. СВЧ разряды могут быть использованы для получения водорода, покрытий, наночастиц и нанотрубок, очистки воды и др. Для создания плазмы используются СВЧ разряды, возникающие в газовых пузырях у поверхности СВЧ антенн разных типов. Образование газовых пузырей происходит за счет разогрева антенны и интенсивного испарения окружающей жидкости, либо с помощью принудительного ввода газа (например, аргона), через канал в антенне. Опубликовано несколько работ по моделированию таких разрядов [9–18].
Ранее при экспериментальном исследовании было показано, что при непрерывном вводе аргона через торец антенны (начиная с некоторой величины вводимого потока) в спектре СВЧ разряда в жидком н-гептане обнаружены линии излучения Hα и Hβ, не наблюдаемые в экспериментах без подвода аргона [19]. В [13–16] представлены модели СВЧ разряда в жидком н-гептане без газовых добавок с учетом образования твердой фазы. Настоящая работа продолжает цикл работ по моделированию СВЧ разряда в жидком н-гептане и посвящена моделированию кинетических процессов в газовой смеси продуктов разложения н-гептана и аргона с учетом образующейся твердой фазы и процессов под действием электронного удара.
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ
Сначала опишем экспериментальные условия, которые моделируются в настоящей работе. В работах [20, 21] подробно описана использованная нами экспериментальная установка. Рабочая камера представляла собой кварцевую кювету в защитном металлическом экране. СВЧ энергия (2.45 ГГц, 500 Вт) вводилась в камеру через дно с помощью коаксиальной линии, центральный проводник которой был длиннее наружного и служил СВЧ антенной. Центральный проводник имел канал, по которому могли подаваться дополнительные газы (в частности, аргон). Жидкий н-гептан заливался в реактор (объем порядка 40 мл) и полностью закрывал антенну. Давление над поверхностью жидкости равнялось атмосферному давлению. При включении установки на конце антенны образовывался газовый пузырь и инициировался СВЧ разряд. Исследовался состав газовых продуктов и спектры излучения разряда. Полученная на основе обработки спектров излучения полос Свана молекулы С2 вращательная (газовая) температура была порядка 2000 K [22].
Представленная ниже нестационарная нульмерная модель описывает процессы в СВЧ плазме в газовом пузыре в жидком н-гептане в смеси паров н-гептана с аргоном. Модель содержит балансные уравнения для нейтральных газовых компонент плазмы, электронно-возбужденных состояний молекулы С2, атомов водорода и аргона, балансные уравнения для заряженных компонент плазмы, уравнения роста частиц твердой фазы, уравнение для среднего СВЧ поля. Включение в модель уравнений для возбужденных состояний С2 и атома Н необходимо для сопоставления результатов расчетов с результатами экспериментов. Эмиссионная спектроскопия является основным методом изучения разрядов в жидкостях. Температура газа считалась равной 2000 К и не зависела от состава плазмы. Это соответствует экспериментальным результатам [19].
Балансные уравнения для нейтральных газовых компонент плазмы
В модели предполагается, что все процессы происходят внутри однородного по пространству сферического пузыря при постоянном объеме и давлении, который рассматривается как реактор идеального смешения непрерывного действия (РИС-Н). Диаметр газового пузыря считался равным 3.0 мм, что соответствует размеру, определенному из экспериментов. Через внешние стенки реактора задается поток паров н-гептана, а также вводится газ аргон. Поток вводимого пара соответствует испарению кипящего вне реактора жидкого н-гептана внутрь пузыря. Содержимое РИС-Н регулируется входящими и выходящими из реактора потоками частиц [23]. Концентрации компонент в выходящем потоке совпадают с концентрациями в объеме реактора. Баланс массы газовых нейтральных и заряженных компонент в этом случае задается как в [23]
(1)
$\begin{gathered} {{V}_{r}}\frac{{d{{n}_{i}}}}{{dt}} = {{{v}}_{f}}\left( {{{n}_{h}} + {{n}_{{Ar}}}} \right) - \left( {{{{v}}_{f}} + {{{v}}_{p}}} \right){{n}_{i}} + \\ + \,\,{{V}_{r}}{{R}_{i}} - {{V}_{r}}\left( {{{6{{D}_{i}}} \mathord{\left/ {\vphantom {{6{{D}_{i}}} {r_{{bl}}^{2}}}} \right. \kern-0em} {r_{{bl}}^{2}}}} \right){{n}_{i}}. \\ \end{gathered} $Коэффициенты диффузии для нейтральных газовых компонент рассчитываются с помощью данных для вириальных коэффициентов потенциала Леннарда–Джонса [24].
Для всех ионов рассчитывался коэффициент амбиполярной диффузии ${\text{D}}_{{{\text{am}}}}^{{\text{i}}}$ в аргоне: ${\text{D}}_{{{\text{am}}}}^{{\text{i}}}$ ≈ ${{{\mu }}_{i}}{{{\varepsilon }}_{x}},$ где µi – подвижность i-го иона, εx – характеристическая энергия электронов.
Диффузионная убыль электронов принималось равной суммарной убыли всех ионов:
Отметим, что такой учет амбиполярной диффузии является достаточно грубым приближением, однако дает правильный порядок потерь. Предварительные расчеты показали, что основным каналом потерь заряженных частиц является объемная рекомбинация, поэтому неточность в описании амбиполярной диффузии в данной постановке задачи не влияет на результаты расчетов.
Механизм разложения н-гептана опубликован ранее в [25]. Основные классы элементарных реакций, рассмотренных в настоящем механизме, следующие: мономолекулярные реакции разложения; отрыв атомов водорода от н-гептана; разложение алкильных радикалов; изомеризация алкильных радикалов; отрыв Н и СН3 от олефинов; присоединение радикалов к олефинам; алкенил-радикальное разложение; разложение олефинов. Для описания пиролиза ацетилена, мы использовали механизм, опубликованный Вангом и Френклахом в [26]. Полная схема включает детальный пиролиз как н-гептана, так и ацетилена состоит из 584 элементарных реакций для 112 компонент и не представлена здесь из-за его большого объема.
Процессы с участием электронов, ионов, возбужденных молекул и C2, и атомов H, и Ar в разряде n-гептана с аргоном
Учитывались следующие процессы: ионизация, диссоциация и возбуждение прямым электронным ударом, электрон-ионная рекомбинация, реакции тушения, ионного обмена, излучения и реакции между нейтральными частицами, приводящие к образованию C2(d) (табл. 1). В модель было включено только одно эффективное состояние возбужденного аргона Ar*, представляющее из себя сумму нижних метастабильных и резонансных состояний с энергией 11.55 eV (1s5, 1s4, 1s3, 1s2). Такое упрощение не сильно повлияло на результаты, так как в наших условиях, как показали расчеты, вклад Ar* в процессы диссоциации не существенен. Радиационный распад резонансных состояний Ar(1s2) и Ar(1s4) учитывался в приближении эффективного времени жизни [47].
Таблица 1.
Процессы с электронами, ионами, возбужденными молекулами C2 и атомами H и Ar в разряде н-гептана с аргоном
| № | Реакции | Константы скоростей реакций м6 моль–2сек–1; м3 моль–1сек–1; 1/сек |
Литература |
|---|---|---|---|
| Диссоциация электронным ударом | |||
| 1. | nC7H16 + ne → C7H15 + H + ne | k(E/N) | [27] |
| 2. | CH4 + ne → CH3 + H + ne | k(E/N) | [28] |
| 3. | C2H4 + ne → C2H3 + H + ne | k(E/N) | [29] |
| 4. | C2H2 + ne → C2H + H + ne | k(E/N) | [29], [30] |
| C2H2 + ne → C2 + H2 + ne | k(E/N) | [29], [30] | |
| C2H2 + ne → C2(d) + H2 + ne | k(E/N) | [31] | |
| 5. | H2 + ne → H + H + ne | k(E/N) | [32] |
| Возбуждение электронным ударом | |||
| 6. | Ar + ne → Ar* + ne | k(E/N) | [29] |
| 7. | H + ne → H(3s3p3d) + ne | k(E/N) | [33] |
| 8. | H2 + ne → H(3s3p3d) + H + ne | k(E/N) | [34] |
| 9. | C2 + ne → C2(d) + ne | k(E/N) | [35] |
| 10. | C2(a) + ne → C2(d) + ne | k(E/N) | [35] |
| Ионизация прямым электронным ударом | |||
| 11. | nC7H16 + ne → ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{16}}}}^{ + }$ + ne + ne | k(E/N) | [36] |
| 12. | Ar + ne → Ar+ + ne + ne | k(E/N) | [29] |
| 13. | CH4 + ne → ${\text{CH}}_{{\text{4}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| 14. | H2 + ne → ${\text{H}}_{{\text{2}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| 15. | CH3 + ne → ${\text{CH}}_{{\text{3}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| 16. | C2H4 + ne → ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{4}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| 17. | C2H2 + ne → ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| 18. | C3H6 + ne → ${{{\text{C}}}_{{\text{3}}}}{\text{H}}_{{\text{6}}}^{ + }$ + ne + ne | k(E/N) | [29] |
| Ступенчатая ионизация | |||
| 19. | Ar* + ne → Ar+ + ne + ne | k(E/N) | [37] |
| Хемоионизация | |||
| 20. | Ar* + Ar* → Ar+ + ne+Ar | 7.2 × 108 | [38] |
| Тушение Ar* и С2(a) | |||
| 21. | Ar* + nC7H16 → Ar + C7H14-1 + H2 | 6 × 108 | [39] |
| 22. | Ar* + CH4 → Ar + CH2 + H + H | 2 × 108 | [39] |
| 23. | Ar* + CH4 → Ar + CH2 + H2 | 3.5 × 108 | [39] |
| 24. | Ar* + C2H6 → Ar + C2H4 + H + H | 4.2 × 108 | [39] |
| 25. | Ar* + C2H4 → Ar + C2H2 + H + H | 4.2 × 108 | [39] |
| 26. | Ar* + C3H8 → Ar + C3H6 + H + H | 4.8 × 108 | [39] |
| 27. | Ar* + C2H2 → Ar + C2H + H | 2.1 × 108 | [40] |
| 28. | С2(a) + H2 → C2H + H | 9.6 × 106exp(–25 000/RgT) | [41] |
| 29. | С2(a) + CH4 → C2 + CH4 | 2.1 × 105exp(–23 281.5/RgT) | [41] |
| 30. | С2(a) + C2H2 → C2 + C2H2 | 5.78 × 107 | [41] |
| 31. | С2(a) + C2H4 → C2 + C2H4 | 5.78 × 107 | [41] |
| Ион-молекулярные реакции | |||
| 32. | Ar+ + nC7H16 → Ar + ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{15}}}}^{ + }$ + H | 6 × 108 | [39] |
| 33. | Ar+ + C2H6 → Ar + ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{4}}}^{ + }$ + H2 | 6.6 × 108 | [39] |
| 34. | Ar+ + C2H4 → Ar + ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + }$ + H2 | 2.4 × 108 | [42] |
| 35. | Ar+ + C2H2 → Ar + ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + }$ | 2.4 × 108 | [42] |
| 36. | Ar+ + C3H8 → Ar + ${{{\text{C}}}_{{\text{3}}}}{\text{H}}_{{\text{6}}}^{ + }$ + H2 | 6.6 × 108 | [39] |
| 37. | Ar+ + CH4 → Ar + ${\text{CH}}_{{\text{2}}}^{ + }$ + H2 | 6.6 × 108 | [39] |
| 38. | Ar+ + Ar + Ar → ${\text{Ar}}_{{\text{2}}}^{ + }$ + Ar | 8.3 × 104 | [43] |
| 39. | Ar+ + H2 → ArH+ + H | 4.5 × 106 | [44] |
| 40. | Ar + ${\text{H}}_{{\text{2}}}^{ + }$ → ArH+ + H | 1.4 × 106 | [44] |
| 41. | Ar + ${\text{H}}_{{\text{3}}}^{ + }$ → ArH+ + H2 | 6.0 × 103 | [44] |
| 42. | ArH+ + H2 → Ar + H3+ | 9.1 × 105 | [44] |
| 43. | ${\text{H}}_{{\text{2}}}^{ + }$ + H2 → ${\text{H}}_{{\text{3}}}^{ + }$ + H | 1.2 × 109 | [44] |
| Электрон-ионная рекомбинация | |||
| 44. | ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{15}}}}^{ + }$ + ne → C7H13 + H2 | 7.4 × 109/$T_{e}^{{0.5}}$ | [39] |
| 45. | ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{16}}}}^{ + }$ + ne → C7H14 + H2 | 7.4 × 109/$T_{e}^{{0.5}}$ | [39] |
| 46. | ${\text{Ar}}_{{\text{2}}}^{ + }$ + ne → Ar + Ar | 6.0 × 1010/$T_{e}^{{0.5}}$ | [42] |
| 47. | ${\text{CH}}_{{\text{4}}}^{ + }$ + ne → CH3 + H | 3.3 × 1010/$T_{e}^{{0.5}}$ | [39] |
| 48. | ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{4}}}^{ + }$+ ne → C2H2 + H2 | 7.2 × 1010/$T_{e}^{{0.5}}$ | [39] |
| 49. | ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + }$ + ne → C2H + H → C2+H + H → C2(d) + H2 | 2.9 × 1010/$T_{e}^{{0.5}}$ × 0.7 | [45], [30] |
| 2.9 × 1010/$T_{e}^{{0.5}}$ × 0.28 | [45], [30] | ||
| 2.9 × 1010/$T_{e}^{{0.5}}$ × 0.02 | [45], [30] | ||
| 50. | ${\text{H}}_{{\text{2}}}^{ + }$ + ne → H + H | 1.25 × 109/$T_{e}^{{0.43}}$ | [45] |
| 51. | ${\text{CH}}_{{\text{3}}}^{ + }$ + ne → CH2 + H → C + H2 + H | 3.4 × 1010/$T_{e}^{{0.5}}$ × 0.57 3.4 × 1010/$T_{e}^{{0.5}}$ × 0.43 |
[45], [30] [45], [30] |
| 52. | ${{{\text{C}}}_{{\text{3}}}}{\text{H}}_{{\text{6}}}^{ + }$ + ne → C3H5 + H | 7.2 × 1010/$T_{e}^{{0.5}}$ | [39] |
| 53. | ${\text{H}}_{{\text{3}}}^{ + }$ + ne → H + H + H | 1.53 × 109/$T_{e}^{{0.52}}$ | [45] |
| Излучение | |||
| 54. | H(3s3p3d) → H(2s2p) + hν | 4.4 × 107 | [46] |
| 55. | С2(d) → С2(a) + hν | 9.3 × 107 | [41] |
| 56. | Ar* → Ar + hν | 6.3 × 104 | [47] |
| Образование С2(d) в реакциях с нейтралами | |||
| 57. | H + CH → C + H2 | 7.89 × 107exp(–670/RgT) | [48] |
| 58. | C + H2 → H + CH | 3.98 × 108exp(–97300/RgT) | [49] |
| 59. | С2H + H → H2 + С2(d) | 3.6 × 10 exp(–118 000/RgT) | [48] |
| 60. | С2H + C2H → C2H2 + С2(d) | 1.86 × 106 | [50] |
| 61. | С2 + H2 → C2H + H | 6.62 × 107exp(–33300/RgT) | [51] |
| 62. | CH + CH → C2(d) + H2 | 1.56 × 107 | [52] |
| 63. | C + CH2 → C2(d) + H2 | 2.4 × 106 | [52] |
| 64. | С + CH2 → C2H + H | 5.0 × 107 | [53] |
| 65. | С + CH3 → C2H2 + H | 5.0 × 107 | [53] |
| 66. | С + CH → C2(d) + H | 5.0 × 107 | [54] |
| 67. | C2H + M → C2(d) + H + M | 1.74 × 1023T –5.16exp(–477 000/RgT) | [55] |
| 68. | C + C + M → C2(d) + M | 50exp(–4174.9/RgT) | [54] |
Предварительные расчеты показали, что термическое разложение н-гептана при температуре 2000 К преобладает над процессами разложения за счет прямого электронного удара и тушения аргона (рис. 1). Полное разложение н-гептана заканчивается на временах порядка 10–7 сек. К этому времени в составе полностью отсутствуют тяжелые углеводороды CiHk с i > 3. Поэтому в табл. 1 включены все перечисленные процессы только для легких углеводородов и для самого н-гептана.
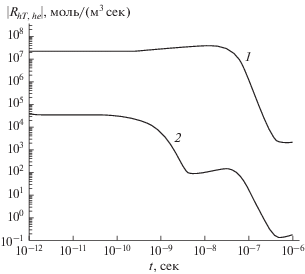
Рис. 1.
Суммарная скорость разложения н-гептана за счет термопроцессов (кривая 1) и суммарная скорость процессов разложения н-гептана под электронным ударом и при столкновениях с возбужденным аргоном (кривая 2) в зависимости от времени. Доля аргона составляла 50%, вложенная в разряд мощность – 50 Вт.
Для оценки излучения молекул C2 [С2(d) → → С2(a)] был включен механизм образования, возбуждения и излучения данной молекулы. В модель также включены упрощенные механизмы для возбуждения и излучения атомов водорода.
В модели проводится расчет баланса для электронов и следующих ионов: ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{16}}}}^{ + },$ ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{15}}}}^{ + },$ ${\text{CH}}_{{\text{4}}}^{ + },$ ${\text{CH}}_{{\text{3}}}^{ + },$ ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{4}}}^{ + },$ ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + },$ ${{{\text{C}}}_{{\text{3}}}}{\text{H}}_{{\text{6}}}^{ + },$ ${\text{H}}_{{\text{2}}}^{ + },$ ${\text{H}}_{{\text{3}}}^{ + },$ Ar+, ${\text{Ar}}_{{\text{2}}}^{ + },$ ArH+. Для определения коэффициентов скоростей реакций под электронным ударом и значения температуры электронов Te для каждого шага по времени должна быть рассчитана ФРЭЭ с учетом состава основных газовых компонент смеси. Использовалось уравнение Больцмана для стационарной, изотропной части ФРЭЭ, записанное в двухчленном приближении разложения распределения по сферическим гармоникам. Предварительные расчеты показали, что основными газовыми компонентами в разряде являются водород, ацетилен, этилен, метан и аргон. Остальные компоненты составляют в сумме доли процента, поэтому состав газовых компонент плазмы определялся на каждом шагу по пяти перечисленным компонентам. Поскольку самосогласованный набор сечений для гептана не известен, как и ранее в [14], в начальный момент времени, использовался набор сечений для пропана.
Сечения диссоциации под электронным ударом для большинства углеводородов не известны. В [30] были аналитически оценены величины сечений для многих углеводородов, в том числе и для этилена и ацетилена. Однако эти данные справедливы только для больших энергий (>20 eV). Считается, что диссоциация углеводородов под электронным ударом осуществляется через возбуждение электронных состояний. Поэтому для этилена, ацетилена и гептана (табл. 1, реакции 1, 3, 4) для расчета констант диссоциации под электронным ударом использовались сечения возбуждения электронных состояний. Для анализа каналов диссоциации использовались данные [30].
Частицы твердой фазы
Для описания формирования частиц сажи был разработан механизм генерации твердых частиц [15]. Согласно [15], плоской модели роста полиароматического углеводорода (ПАУ), механизм роста зародыша состоит из повторяющейся последовательности присоединения к нему новых ароматических колец в реакциях с ацетиленом. Рост частиц сажи включает три физико-химических механизма: нуклеация, поверхностный рост и коагуляция. Подробности механизма формирования и роста твердых частиц можно найти в работах [15, 16].
По аналогии с работой [15] твердые частицы разделяются на 17 групп в зависимости от их размера. Концентрация каждой группы обозначается через Fi, i = 4, …, 20 и вычисляется с помощью уравнения (1). Индекс i характеризует твердую частицу, содержащую 2i колец ПАУ.
Уравнение для среднего СВЧ поля в разряде
Поскольку определить вложенную в разряд мощность в экспериментах не представляется возможным, то эта величина рассматривается в задаче как параметр. Величина среднего значения СВЧ поля связана с удельной вложенной в разряд мощностью ${{P}_{{abs}}}$ (Вт/м3) как
здесь ${\sigma } = {{{\varepsilon }}_{0}}{{{\nu }}_{{\text{с}}}}\left[ {\frac{{{{n}_{{\text{e}}}}}}{{{{n}_{{{\text{norm}}}}}}}} \right];$ ${{{\varepsilon }}_{0}},$ Ф/м – диэлектрическая проницаемость вакуума; ${{{\nu }}_{{\text{с}}}}$ – частота столкновений электронов с нейтралами, 1/с; ${{n}_{{\text{e}}}}$ – концентрация электронов, м–3; ${{n}_{{{\text{norm}}}}} = {{m\left( {{{{\omega }}^{2}} + {\nu }_{{\text{с}}}^{2}} \right)} \mathord{\left/ {\vphantom {{m\left( {{{{\omega }}^{2}} + {\nu }_{{\text{с}}}^{2}} \right)} {4{\pi }{{{\text{e}}}^{2}}}}} \right. \kern-0em} {4{\pi }{{{\text{e}}}^{2}}}}$ – константа нормировки для концентрации электронов, м–3; ${\omega }$ – круговая частота задающего СВЧ генератора, 1/с; e и m – заряд и масса электрона. Для расчета с заданным значением параметра ${{P}_{{abs}}}$ на каждом шаге по времени вычисляется значение электронной концентрации и затем из (2) определяется среднее значение СВЧ поля E. По значению E/N определяются константы скорости процессов под электронным ударом.Начальные условия и задаваемые параметры расчета
В начальный момент времени задавалось начальное значение концентрации электронов, которое составляло 1013 см–3. Начальные значения концентраций ионов ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{16}}}}^{ + }$ и Ar+ в сумме брались равными заданной концентрации электронов. В этом случае условие квазинейтральности плазмы выполняется в течение всего расчета. Значение начальной концентрации электронов не влияло на стационарные распределения всех компонент, установившиеся при временах больше 10–3–10–2 с. Стационарное решение также не зависело от выбора ионов с ненулевой начальной концентрацией. Необходимо лишь, чтобы в начальный момент выполнялось условие квазинейтральности.
Объемная доля вводимого в пузырь аргона${\text{\;}}$ по отношению к объемной доле н-гептана была изменяемым параметром. Доля аргона ${\theta }$ составляла в различных расчетах соответственно 0, 25, 50, 70 и 90%. Она регулировалась при помощи заданных соответствующим образом значений вводимых концентраций гептана ${{n}_{h}}$ и аргона ${{n}_{{{\text{Ar}}}}}.$ В начальный момент концентрации всех газовых и твердых компонент кроме гептана и аргона полагались равными нулю. Сумма начальных концентраций н-гептана и аргона равнялась 6 моль/м3.
Значение вложенной в разряд мощности $P = {{P}_{{abs}}}{{V}_{r}}$ также варьировалось. Расчеты проводились для фиксированного набора значений ${\text{P}}$: 10, 30, 50, 75 и 100 Вт. Газовая температура внутри пузыря задавалась равной 2000 К. Моделирование проводилось при помощи программы COM-SOL Multiphysics – Reaction Engineering Laboratory [23].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Расчеты показали, что состав и величина газовых компонент очень слабо зависят от уровня подводимой мощности. Ввод аргона прежде всего приводит к обогащению ФРЭЭ быстрыми электронами. При постоянном значении E/N константа ионизации бы возросла и, соответственно, возросла бы концентрация электронов. Однако, поскольку суммарная концентрация газовых частиц N = 3.6 × 1018 см–3 не изменяется (расчет производится при постоянном давлении и температуре), то в соответствии с формулой (2) при фиксированном значении вложенной мощности значения E/N уменьшаются при повышении доли аргона θ (рис. 2). Несмотря на небольшое падение E/N, количество электронов с энергией порядка 10 эВ выше при больших θ (рис. 3). Поэтому при повышении доли вводимого в разряд аргона ≥50% наблюдается заметный рост концентрации электронов (рис. 4).
Рис. 2.
Зависимости стационарных значений E/N от объемной доли аргона, вводимого в разряд. Значения мощности, вложенной в разряд, соответствуют: ◼ – 10, ⚫ – 30, ▲ – 50, ▼ – 75 и ◆ – 100 Вт.
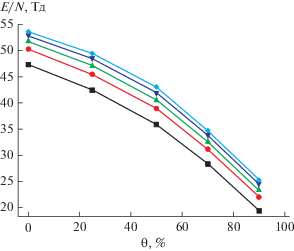
Рис. 3.
ФРЭЭ, рассчитанные при отсутствии аргона для E/N = 49 Тд (кривая 1) и при вводе аргона при θ = 70%, E/N = 33 Тд (кривая 2) при 50 Вт вложенной в разряд мощности.
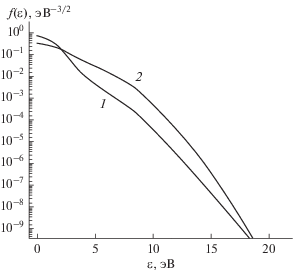
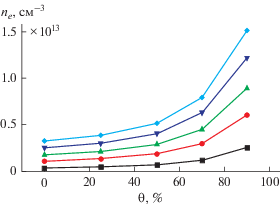
Рис. 4.
Зависимости стационарной электронной концентрации от объемной доли аргона, вводимого в разряд. Значения мощности, вложенной в разряд, соответствуют: ◼ – 10, ⚫ – 30, ▲ – 50, ▼ – 75 и ◆ – 100 Вт.
В установившемся режиме горения СВЧ разряда основными газовыми компонентами в разряде являются водород, ацетилен, диацетилен, метан, этилен и аргон. Основным плазмообразующим ионом является ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + }$ (рис. 5). Ионы ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{4}}}^{ + }$ и ${\text{CH}}_{{\text{3}}}^{ + }$ в сумме составляют 3–5%, а остальные используемые в модели ионы – доли процента.
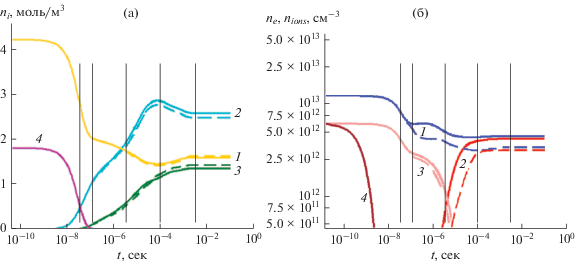
Рис. 5.
(a) – эволюция основных продуктов газовой фазы в разряде смеси н-гептана с аргоном. 1 – аргон; 2 – водород; 3 – ацетилен; 4 – н-гептан. (б) – эволюция заряженных частиц в разряде смеси н-гептана с аргоном. 1 – электроны; 2 – ${{{\text{C}}}_{{\text{2}}}}{\text{H}}_{{\text{2}}}^{ + };$ 3 – Ar+; 4 – ${{{\text{C}}}_{{\text{7}}}}{\text{H}}_{{{\text{16}}}}^{ + }.$ Доля аргона, вводимого в разряд, 70%. Мощность, вложенная в разряд, 50 Вт. Пунктирные линии соответствуют решениям с изменяемой ФРЭЭ. Вертикальными линиями обозначены моменты времени τi, когда ФРЭЭ пересчитывалась в соответствии с составом газовой фазы. Слева направо τ1 – τ5: 3 × 10–8; 10–7; 3 × 10–6; 10–4; 3 × 10–3 с.
Исследовалось влияние изменения состава продуктов газовой смеси на ФРЭЭ и, как следствие, на возможное изменение решений в стационарном состоянии. Поскольку пакет Comsol3.5а не позволяет пересчитывать функцию распределения на каждом шаге по времени, расчет был разбит на отдельные интервалы, на каждом из которых состав газовой смеси изменялся не очень сильно. В конце каждого временного интервала определялся состав газовой фазы и пересчитывалась ФРЭЭ из уравнения Больцмана. На следующем интервале расчет продолжался с учетом коэффициентов для электронных процессов, вычисленных по новой функции распределения.
На рис. 5a, 5б такие решения приведены для случая θ = 70%, P = 50 Вт. Они представлены пунктирными линиями для всех приводимых компонент. Очевидно, что учет влияния состава газовой фазы на ФРЭЭ не приводит к заметному изменению решений для газофазных продуктов разложения н-гептана. Стационарное распределение заряженных частиц чувствительнее к изменению ФРЭЭ, и дает для концентраций электронов и основного иона значения в 1.5 раза меньшие. Однако, поскольку учет влияния состава на ФРЭЭ не вносит качественных изменений в стационарные решения, то все приведенные в статье результаты расчетов выполнены для конечного состава продуктов, взятого из предварительного расчета.
Исследование излучения разряда [19] показало, что в СВЧ разряде в жидком н-гептане не наблюдается линия излучения Hα. Однако, при введении аргона внутрь разрядной области излучение Hα становится заметным и его интенсивность сравнима с интенсивностью полос Свана молекулы С2. Для исследования этого вопроса в кинетическую схему были включены процессы возбуждения атома водорода и молекулы С2.
Атом H(3s3p3d) образуется как за счет прямого электронного удара, так и за счет диссоциативного возбуждения (табл. 1, реакции 7, 8). Расчеты показали, что основным каналом наработки атома H(3s3p3d) является реакция 7. Скорость этого процесса растет с увеличением доли вводимого в разряд аргона. Это связано с обогащением ФРЭЭ быстрыми электронами (порядка 12.1 эВ), несмотря на небольшое падение E/N (рис. 2 и 3). Отметим, что этот рост не является монотонным. В диапазоне примеси аргона от 25% до 50% и соответственных этим случаям рассчитанным нами значениям E/N ФРЭЭ практически не меняется, следовательно, концентрация H(3s3p3d) тоже остается практически неизменной. При дальнейшем увеличении доли аргона ФРЭЭ сильно обогащается быстрыми электронами, что приводит к увеличению концентрации H(3s3p3d).
Наряду с процессами возбуждения прямым электронным ударом существенную роль в формировании возбужденной молекулы C2(d) играют процессы:
(3)
${{{\text{C}}}_{2}}{\text{H}} + {\text{H}} \Rightarrow ~{{{\text{C}}}_{2}}\left( d \right) + ~{{{\text{H}}}_{2}},$(4)
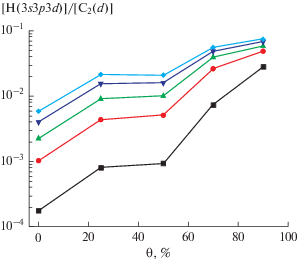
${{{\text{C}}}_{2}}{\text{H}} + {{{\text{C}}}_{2}}{\text{H}} \Rightarrow {{{\text{C}}}_{2}}\left( d \right) + ~{{{\text{C}}}_{2}}{{{\text{H}}}_{2}}.$Заметим, что в процессе (3) в принципе молекула C2 может образовываться как в основном состоянии [55], так и в возбужденном состоянии. Но энергетика этой реакции, как и реакции (4) позволяет получить состояние C2(d). Мы считали, что в реакциях (3) и (4) образуется молекула C2(d). Скорость этих реакций практически не зависит от величины θ. Скорость процесса возбуждения молекулы С2 прямым электронным ударом (табл. 1, реакция 9) вплоть до доли аргона в смеси равной 70% на несколько порядков меньше. В дальнейшем вклад электронного удара в процесс образования C2(d) становится существенным, а при θ равном 90% – сравнимым с вкладом реакций (3) и (4). Приведенные нами соображения позволяют объяснить зависимость величины отношения [H(3s3p3d)]/[C2(d)] от величины θ (рис. 6). Отметим, что при ${\theta } = 90{\text{\% }}$ и при вложенных мощностях 75 и 100 Вт небольшое замедление роста этого отношения объясняется влиянием электронного удара на образование C2(d). Таким образом нам удалось объяснить наличие линий Hα в экспериментальных спектрах при достаточно больших концентрациях вводимого аргона, которых нет в экспериментах без подвода аргона.
Рис. 6.
Зависимости отношения стационарных концентраций H(3s3p3d) и C2(d) в СВЧ разряде в жидком н-гептане от объемной доли аргона, вводимого в разряд. Значения мощности, вложенной в разряд, соответствуют: ◼ – 10, ⚫ – 30, ▲ – 50, ▼ – 75 и ◆ – 100 Вт.
При обсуждении результатов, касающихся выхода твердых частиц сажи следует отметить, что эффект отрицательного заряжения частиц не учитывался. Заряд частиц приведет к уменьшению коагуляции за счет взаимного отталкивания. Это является предметом дальнейшего исследования.
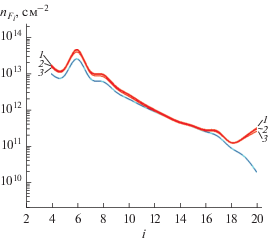
Ввод аргона в область разряда приводит к незначительному увеличению количества легких твердых частиц Fi (i < 10) при всех рассчитываемых значениях вкладываемой мощности, и существенному росту числа тяжелых частиц (для i ~ ~ 19–20 для θ = 70%) (рис. 7). Обобщая полученные данные можно сделать вывод, что общее количество твердых частиц вырастает на 10–20% при добавлении аргона. При этом относительная доля тяжелых частиц возрастает.
Рис. 7.
Концентрации твердых частиц Fi в зависимости от их размера. Индекс i характеризует твердую частицу, содержащую 2i колец ПАУ. Стационарные распределения относятся к двум случаям: нижняя линия соответствуeт 10, 50, 100 Вт вложенной в разряд мощности при отсутствии аргона; сплошные линии 1, 2, 3 соответствуют 10, 50, 100 Вт вложенной в разряд мощности при доле аргона 70%.
Из расчетов следует, что суммарная скорость поверхностного роста и коагуляции тяжелых твердых частиц (i > 10) растет с добавлением аргона. Это объясняет наблюдаемый рост хвоста функции распределения тяжелых частиц.
ЗАКЛЮЧЕНИЕ
Представлены первые результаты нульмерного моделирования СВЧ разряда в жидком н-гептане с вводом аргона в область разряда. Модель включает в себя балансные уравнения для нейтральных газовых компонент плазмы, балансные уравнения для заряженных компонент плазмы, уравнения роста частиц твердой фазы, уравнение для среднего СВЧ поля. Кроме этого, модель содержит кинетическую схему образования излучающего состояния молекулы С2 и линий излучения атомарного водорода.
Ввод аргона в разряд приводит к изменению ФРЭЭ и, как следствие, к изменению плотности электронов и приведенного поля, а концентрация H(3s3p3d) становится сравнимой с концентрацией возбужденных молекул С2(d).
Показано, что ввод аргона в разряд не приводит к заметному изменению количества частиц твердой фазы. Относительная доля тяжелых частиц возрастает за счет увеличения скорости процессов поверхностного роста и коагуляции. Таким образом, с помощью добавления аргона можно управлять количеством образующихся твердых частиц большого размера.
Список литературы
Bruggeman P., Leys C. // J. Phys. D. Appl. Phys. 2009. V. 42. P. 053001.
Samukawa S., Hori M., Rauf S. et al. // J. Phys. D. Appl. Phys. 2012. V. 45. P. 253001.
Bruggeman P. J., Kushner M. J., Locke B. R. et al. // Plasma Sources Sci. and Technol. 2016. V. 25. P. 053002.
Foster J. // Phys. Plasmas. 2017. V. 24. P. 055501.
Vanraes P., Bogaerts A. // Appl. Phys. Rev. 2018. V. 5. P. 031103.
Лебедев Ю.А. // Физика плазмы. 2017. Т. 43. P. 577.
Horikoshi S., Serpone N. // RSC Adv. 2017. V. 7. P. 47196.
Lebedev Yu. A. // High Temperature. 2018. V. 56. P. 811.
Hattori Y., Mukasa S., Nomura S., Toyota H. // J. Appl. Phys. 2010. V. 107. P. 063305.
Hattori Y., Mukasa S., Toyota H., Yamashita H., Nomura S. // Surf. Coat. Technol. 2012. V. 206. P. 2140.
Mukasa S., Nomura S., Toyota H. // Jap. J. Appl. Phys. 2007. V. 46. P. 6015.
Gidalevich E., Boxman R.L. // J. Phys. D Appl. Phys. 2012. V. 45. P. 245204.
Tatarinov A.V., Lebedev Yu.A., Epstein I.L. // High Energy Chem. 2016. V. 50. P. 144.
Lebedev Yu.A., Tatarinov A.V., Epstein I.L., Averin K.A. // Plasma Chemistry and Plasma Processing. 2016. V. 36. P. 535.
Lebedev Yu.A., Tatarinov A.V., Epstein I.L., Bilera I.V. // J. Phys. D: Appl. Phys. 2018. V. 51. P. 214007.
Lebedev Yu.A., Tatarinov A.V., Epstein I.L. // Plasma Chemistry and Plasma Processing. 2019. V. 39. P. 787.
Levko D., Sharma A., Raja L.L. // J. Phys. D Appl. Phys. 2016. V. 49. P. 285205.
Levko D., Sharma A., Raja L.L. // J. Phys. D Appl. Phys. 2016. V. 49. P. 22LT01.
Averin K.A., Bilera I.V., Lebedev Yu.A., Shakhatov V.A., Epstein I.L. // Plasma Process Polym. 2019. V. 16. P. e1800198.
Averin K.A., Lebedev Yu.A., Shchegolikhin A.N., Yablokov M.Yu. // Plasma Process Polym. 2017. V. 14. Iss. 9. P. e201600227.
Averin K.A., Lebedev Yu. A., Shakhatov V.A. // Plasma Phys. Reports. 2018. V. 44. P. 110.
Lebedev Yu.A., Shakhatov V.A. // Eur. Phys. J. D. 2019. V. 73. P. 167.
COMSOL Multiphysics. https://comsol.com/chemical-reactionengineering
Westbrook C.K., Pitz W.J., Curran H.J., Mehl M. // Lawrence Livermore National Laboratory. May 19, 2004.
Wang H., Frenklach M. // Combust. Flame. 1994. V. 96. P. 163.
Mehl M., Pitz W.J., Westbrook C.K., Curran H.J. // Proc. Combust. Inst. 2011. V. 33. P. 193.
Словецкий Д.И. // Химия плазмы / Под ред. Смирнова Б.М. М.: Энергиздат. 1981. С. 189.
Winters H. // J. Chem. Phys. 1975. V. 63. P. 3462.
Morgan Database (2014). www.lxcat.net. Retrieved 29 Aug. 2014.
Janev R., Reiter D. // Phys. Plasmas. 2004. V. 11. P. 780.
Országh J., Danko M., Čechvala P., Štefan Matejčík S. // The Astrophysical J. 2017. V. 841. P. 17.
Cacciatore M., Capitelli M., Dilonardo M. // Chem. Phys. 1978. V. 34. P. 19.
Mahan A.H., Gallaher A., Smith S. // Phys. Rev. A. 1976. V. 13. P. 156.
Tawara H., Itikawa Y., Nishimura H., Yoshono M. // J. Phys. Chem. Ref. Data. 1990. V. 19. P. 617.
Halmova G., Gorfinkiel J., Tennyson J. // J. Phys. B: At. Mol. Opt. Phys. 2006. V. 39. P. 2849.
Vacher J.R., Jorand F., Blin-Simiand N., Pasquiers S. // International J. Mass Spectrometry. 2010. V. 295. P. 78.
Hyman H. // Phys. Rev. A. 1979. V. 20. P. 855.
Karoulina E., Lebedev Yu. // J. Phys. D. 1992. V. 125. P. 401.
Starikovsky A., Aleksandrov N. // Progress in Energy and Combustion Science. 2013. V. 39. P. 61.
Denysenko I., Wahl E. et al. // Plasma Phys. Control. Fusion. 2019. V. 61. P. 014014.
Лосев С., Ярыгина В. // Физико-химическая кинетика в газовой динамике. 2012. Т. 13. Вып. 2
Gordillo-Vzques F., Albella J. // Plasma Sources Sci. Technol. 2004. V. 13. P. 50.
Epstein I., Gavrilovic M. et al. // Eur Phys. J. D. 2014. V. 68. P. 334.
Lebedev Yu., Tatarinov A. et al. // J. Phys. D. Appl. Phys. 2014. V. 47. P. 335203.
JQC http://massey.dur.ac.uk/drf/protostellar/species_chemistry
Wiese W., Smith M., Glennon B. // Atomic Transition Probabilities. N.Y.: Iov. Print. Opt., 1966.
Walsh P. // Phys. Rev. 1959. V. 116. P. 511.
Merlo-Sosa L., Soucy G. // International J. Chemical Reactor Engineering. 2005. V. 3. Article A4.
Dean A., Davidson D., Hanson R. // J. Phys. Chem. 1991. V. 95. P. 183.
TsangW., Hampson R. // J. Phys. Chem. Ref. Data. 1986. V. 15 P. 1087.
Kruse T., Roth, P. // J. Phys. Chem. A. 1997. V. 101. P. 2138.
Smith G., Park C., Schneiderman J., Luque J. // Combustion and Flame. 2005. V. 141. P. 66.
Zhang Y, Dunn-Rankin D., Taborek P. // J. Appl. Phys. 1993. V. 74. P. 6941.
Tsyganov D., Bundaleska N. et al. // Plasma Sources Sci. Technol. 2016. V. 25. P. 015013.
Mankelevich Y. et al. // Diamond and Related Materials. 2003. V. 12. P. 383.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий


