Химия высоких энергий, 2021, T. 55, № 1, стр. 76-80
Синтез и свойства катализатора СО на основе плазмохимического карбонитрида титана, диоксида титана и палладия
Н. Н. Вершинин a, *, И. Л. Балихин a, В. И. Берестенко a, О. Н. Ефимов a, Е. Н. Кабачков a, Е. Н. Куркин a
a Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. Академика Семенова, 1, Россия
* E-mail: vernik@icp.ac.ru
Поступила в редакцию 26.07.2020
После доработки 19.08.2020
Принята к публикации 02.09.2020
Аннотация
Синтезирован катализатор СО на основе плазмохимического карбонитрида титана TiC0.2N0.8 и ТiO2 с содержанием палладия 10 мас. %. Исследована зависимость скорости реакции окисления СО при комнатной температуре и малых концентрациях СО (менее 100 мг/м3) от содержания TiC0.2N0.8. Найдено, что при содержании TiC0.2N0.8от 8 до 10 мас. % катализатор обладает максимальной скоростью реакции окисления СО, превышающей в 2.5 раза скорость реакции на катализаторе на основе чистого ТiO2, включающего кластеры палладия. Катализаторы перспективны для применения в каталитических и фотокаталитических системах очистки воздуха.
В фотокаталитических очистителях воздуха от токсичных газов, вирусов и бактерий в качестве активного материала используют диоксид титана [1–3]. Так как фотокаталитический метод очистки воздуха от угарного газа (СО) в непрерывном режиме на чистом диоксиде титана малоэффективен, поэтому необходимо создание комбинированных катализаторов для фотокаталитических устройств с эффективной очисткой воздуха, как от органических примесей, так и СО. При исследовании катализаторов СО на основе наноматериалов нами найдено, что можно сформировать нанокластеры каталитического металла (Pd,Pt) на поверхности наноалмаза (ND) [4, 5], β–SiC [6] и TiN [7], обладающих структурным подобием к палладию и платине. При этом толщина кластера близка к нескольким параметрам решетки каталитического металла, что обеспечивает высокую скорость реакции окисления СО при комнатной температуре при малых концентрациях СО. Задачей данной работы является синтез и исследование свойств катализатора в реакции окисления СО на основе TiO2 с добавками наночастиц плазмохимического TiC0.2N0.8, включающего кластеры Pd, с целью оценки перспективности его применения в фотокаталитических системах очистки воздуха.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Методика синтеза карбонитрида титана
Используемый в работе порошок TiC0.2N0.8 был получен водородным восстановлением тетрахлорида титана в потоке микроволновой плазмы азота при атмосферном давлении. Смесь паров тетрахлорида титана с водородом и октаном в необходимом соотношении вводилась в плазменный поток азота со среднемассовой температурой около 3000 К, полученный в плазмотроне с помощью микроволнового генератора с частотой 2450 МГц и максимальной полезной мощностью 5 кВт. Объемный расход азота составлял 2.5 м3/ч. Расход TiCl4 составлял 3 г/мин, расход водорода 0.4 м3/ч. Химическое взаимодействие реагентов и конденсация наночастиц TiC0.2N0.8 происходило в трубчатом реакторе диаметром 50 мм и длиной 250 мм, внутренние стенки которого были футерованы кварцем. Образовавшиеся в реакторе частицы после охлаждения потока отделялись от газовой фазы фильтрацией на рукавном фильтре.
Методика синтеза катализаторов
В качестве носителя для палладия использовали TiO2 марки HombiсаtUV-100 (SachtlebenChemieGmbH, Germany) и TiC0.2N0.8, полученный нами плазмохимическим методом. Средний размер частиц TiC0.2N0.8 близок 32 ± 4 нм, а удельная поверхность TiO2 близка к 380 ± 15 м2/г со средним размером кристаллитов 5–8 нм. Для получения катализаторов был использован метод формирования кластеров палладия на поверхности частиц носителя в водном растворе, содержащем хлорид палладия и восстановитель – формиат лития LiCOOH, аналогичный методу, впервые описанному нами в патенте [8]. Катализатор получали следующим образом: при 20°С водный раствор PdCI2 (10–3–10–2 моль/л) смешивали с водным раствором формиата лития (0.02–0.2 моль/л). Затем, в нагретую до 45–50°С водную суспензию TiC0.2N0.8 и диоксида титана с концентрацией твердых частиц 2 г/л, вводили необходимое количество водного раствора PdCI2 и формиата лития. После периода индукции (5–10 мин) кластеры палладия осаждаются на поверхности частиц TiC0.2N0.8 и диоксида титана. Затем раствор охлаждали до комнатной температуры в течение 6 ч и проводили промывку дистиллированной водой (5–6 раз) катализатора от продуктов реакции и сушили при 80°С в течение 24 ч. Для приготовления водной суспензии TiO2 и TiC0.2N0.8 использовали ультразвуковой (УЗ) гомогенизатор марки HD 3200. После приготовления катализатора вновь получали водную суспензию катализатора, которую наносили на пористую пластину (40 × 40 × 6 мм), спеченную из стеклянных шариков диаметром 1 мм, а затем сушили при 80°С в течение 24 ч.
Приборы для исследования физико-химических свойств катализатора
Изотермы адсорбции/десорбции азота и измерение удельной поверхности образцов нитрида титана методом БЭТ получали при температуре жидкого азота (77 K) c помощью анализатора QuantachromeQuadrasorb SI. Образцы TiC0.2N0.8 были кондиционированы при 573 K в среде гелия на станции дегазации FloVacDegasser в течение 3 ч непосредственно перед измерениями. Спектры рентгеновской дифракции регистрировались с помощью дифрактометра DRON ADP-2-02, применяя Cu Kα-излучение (λ = 0.154056 нм). Для исследования структуры и состава поверхности катализатора c кластерами Pd, использовали электронный просвечивающий микроскоп марки JEOL JEM 2100 и электронный спектрометр для химического анализа SPECS PHOIBOS 150 MCD-9 с рентгеновским источником с магниевым анодом (MgKα-излучение 1253.6 эВ). Для взвешивания реактивов и образцов использовали электронные весы Асculab марки ALC-80d4.
Методика исследования каталитических свойств
Исследование кинетики окисления СО в воздухе на катализаторе проводили по методике, описанной нами ранее [6]. Исследование каталитических свойств проводили следующим образом: испытательную камеру в течение 600 с продували газовой смесью оксида углерода с воздухом с концентрацией СО 150 мг/м3 со скоростью 50 см3/с. Затем закрывали входной и выходной вентили испытательной камеры и включали побудитель расхода, находящийся в испытательной камере, обеспечивая циркуляцию газовой смеси через образец с катализатором со скоростью 30 см3/с. После снижения концентрации СО за счет каталитической реакции до уровня 100 мг/м3 включали цифровой секундомер и регистрировали показания сенсоров. Испытательная камера объемом 0.3 ± 0.003 дм3 снабжена сенсорами СО, СО2, влажности и температуры (RH/Т). Для обработки сигналов сенсоров использовали микропроцессорный преобразователь. В качестве сенсоров использовали: сенсор СО марки NAP-505 (Nemoto), оптический сенсор СО2 марки MSH – P/CO2/NC/ 5/V/Р (Dynament), сенсор влажности и температуры марки SHT75 (Sensirion).
Результаты исследования физико-химических свойств катализатора
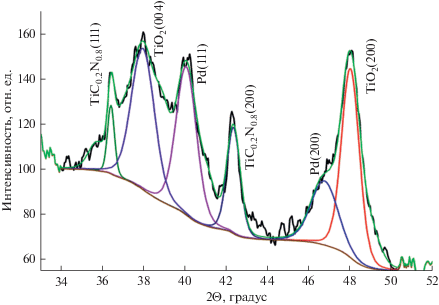
На рис. 1 приведены результаты рентгеновских исследований катализатора следующего состава: 81 мас. % TiO2 + 9 мас. % TiC0.2N0.8 + 10 мас. % Pd. Из рентгеновских данных было получено, что область когеретного рассеяния кластеров (ОКР) Pd близка к 6 нм. Ранее в статье [6] было найдено, что ОКР кластеров Pd близка к 3.5 нм для катализатора на основе чистого TiO2, содержащего 10 мас. % Pd.
На рис. 2 приведены результаты исследований катализатора (81 мас. % TiO2 + 9 мас. % TiC0.2N0.8 + + 10 мас. % Pd) методом РФЭС с примером разложения на индивидуальные компоненты фотоэлектронных спектров уровня Pd3d.
Рис. 2.
РФЭ-спектры области Pd3d поверхности кластера Pd для катализатора состава 81 мас. % TiO2 + 9 мас. % TiC0.2N0.8 + 10 мас. % Pd.
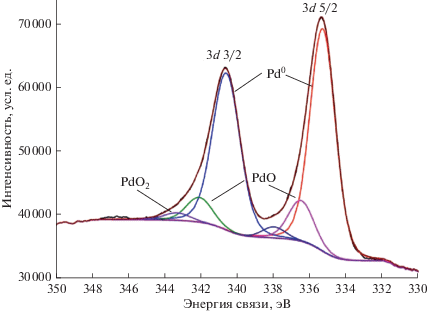
В спектрах уровня Pd3d возможно выделить три основных пика со значениями энергий связи Pd3d5/2, равными 335.4, 336.5, 337.8 эВ. Сигналы в спектрах хорошо согласуются с литературными данными и характеризуют палладий в металлическом состоянии с энергией связи Pd0 = 335.4 эВ (Pd3d5/2). Спин-орбитальное расщепление между подуровнями Pd3d5/2 и Pd3d3/2 составляет 5.26 эВ. Пик палладия с энергией связи ~336.5 эВ, наблюдаемый в спектрах образца катализатора с карбонитридом титана, может быть отнесен к оксиду палладия(II), который, вероятно, образовался в процессе хранения образцов на воздухе. Пик с энергией связи 337.8 эВ относится к состоянию Pd4+, например, в составе PdO2 или к кластерам, локализованным на дефектах поверхности носителя [9, 10].
Результаты исследования каталитических свойств катализатора
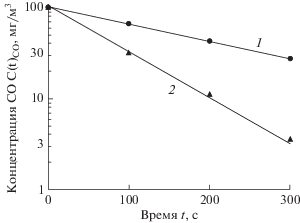
На рис. 3 представлены результаты исследования каталитических свойств катализаторов следующего состава: катализатор 1–90 мас. % TiO2 + + 10 мас. % Pd и катализатор 2–81мас. % TiO2 + + 9 мас. % TiC0.2N0.8 + 10 мас. % Pd. При снижении концентрации СО в испытательной камере одновременно происходит возрастание концентрации СО2 за счет необратимой реакции окисления СО кислородом воздуха (СО + 1/2 О2 = СО2) на поверхности катализатора.
Как видно из рис. 3 зависимость концентрации СО от времени в испытательной камере с катализатором описывается уравнением (1):
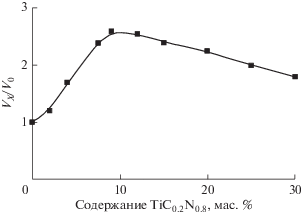
где ССО(t) – измеренное значение концентрации СО в испытательной камере, CCO(0) – значение концентрации СО в начальный (нулевой) момент времени, k – константа скорости реакции, t – время.Для исследования влияния состава катализатора на каталитические свойства были синтезированы и испытаны десять образцов катализатора на основе карбонитрида титана и диоксида титана с массовым содержанием палладия 10%, а содержание карбонитрида титана варьировали от 0 до 30 мас. %. Масса Pd в каждом исследованном образце близка к 1.5 мг. Скорости реакции окисления СО для каждого образца определяли после обработки экспериментальных данных на основании уравнения (1). Затем определяли отношение скоростей реакции Vx/V0, где V0 – скорость окисления СО при концентрации 100 мг/м3 для состава, содержащего 0 мас. % TiC0.2N0.8, а Vx – скорость окисления СО при концентрации 100 мг/м3 для катализатора содержащего x мас. % TiC0.2N0.8. На рис. 4 приведены результаты экспериментальных исследований.
Для определения адсорбционных свойств палладия в катализаторе 1 и катализаторе 2 проводили измерение поглощения СО катализатором из газовой фазы. Для этого образец с катализатором помещали в испытательную камеру объемом 50 см3 из нержавеющей стали, снабженную входным и выходным вентилем для подачи газовой смеси. Испытательную камеру продували сухим азотом со скоростью 50 см3/с в течение 100 с, а затем продували смесью СО и N2 в течение 5 с со скоростью 50 см3/с. Затем закрывали входной и выходной вентили и через 10 мин анализировали содержание объемной доли СО. Экспериментально установили, что в течение 10 мин устанавливается близкое к равновесному значению объемной доли СО в испытательной камере. Для анализа СО через 10 мин отбирали 3 см3 пробы из испытательной камеры, а затем впрыскивали пробу в измерительную камеру объемом 300 см3, заполненную воздухом. Объемную долю СО в измерительной камере анализировали сенсором СО марки NAP-505 (Nemoto). Количество адсорбированных поверхностью Pd молекул СО в расчете на единицу массы Pd в катализаторе можно вычислить по следующей формуле (2):
где Cic – начальная объемная доля СО в %, Cfc – конечная объемная доля СО в %, Vo – объем испытательной камеры в дм3, NA – число Авогадро, mPd – масса палладия в катализаторе в г, VM – молярный объем газа в дм3. Массу катализатора подбирали так, чтобы обеспечить значение конечной концентрации в пределах от 0.45 до 0.55 от начальной объемной доли СО равной 1%. После обработки экспериментальных результатов было найдено, что отношение NСО (Pd в катализаторе 1)/NСО(Pd в катализаторе 2) близко к 1.0 ± 0.15. Измерения проведены при температуре 295 К и давлении газовой смеси в испытательной камере 101 кПа.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Из экспериментальных результатов было найдено, что по адсорбционным свойствам палладия катализаторы близки. А из данных по кинетике окисления СО, представленных на рис. 3 и рис. 4 (в расчете на единицу массы Pd) найдено, что максимальная скорость окисления СО на палладии, нанесенном на диоксид титана с добавками карбонитрида титана, выше в 2.5 раза скорости реакции окисления СО на палладии, нанесенном на чистый диоксид титана. При этом увеличение скорости реакции окисления СО может быть связано со снижением энергии активации скорости реакции. Из уравнения Аррениуса следует, что при увеличении скорости реакции в 2.5 раза снижение энергии активации составит 2.2 ± 0.3 кДж/моль. Близкие результаты получены в статье [6] при исследовании добавок карбида кремния. При оптимальном содержании карбонитрида титана (8–10 мас. %) TiC0.2N0.8 выступает в качестве центра формирования кластеров палладия с низкой энергией активации в реакции окисления СО, а значит, максимальной скоростью реакции окисления. Предварительные испытания катализатора при фотокаталитическом окислении этилового спирта показали, что катализатор также эффективно окисляет этиловый спирт, поэтому катализатор перспективен также и для применения в каталитических и фотокататалитических системах очистки воздуха бытового применения.
ВЫВОДЫ
На основе плазмохимического TiC0.2N0.8 и ТiO2 синтезирован катализатор СО. В результате исследования скорости реакции окисления СО от содержанияTiC0.2N0.8 при комнатной температуре найдено, что при содержании карбонитрида титана от 8 до 10 мас. % катализатор обладает максимальной скоростью реакции окисления СО. При малых концентрациях СО (менее 100 мг/м3) скорость реакции окисления СО на разработанном катализаторе превышает в 2.5 раза скорость реакции на катализаторе на основе чистого ТiO2, включающего кластеры палладия. Катализаторы перспективны для применения в каталитических и фотокаталитических системах очистки воздуха.
Список литературы
Mo J. et al. // Atmospheric environment. 2009. V. 43. № 14. C. 2229.
Paz Y. // Appl. Catalysis B: Environmental. 2010. V. 99. № 3–4. C. 448.
Kolarik B. et al. // Building and Environment. 2010. V. 45. № 6. C. 1434.
Vershinin N.N., Efimov O.N., Bakaev V.A., Aleksenskii A.E., Baidakova M.V., Sitnikova A.A., Vul’ A.Ya. // Fullerenes, Nanotubes and Carbon Nanostructures. 2011. V. 19. P. 63.
Вершинин Н.Н., Балихин И.Л., Бакаев В.А., Берестенко В.И., Ефимов О.Н., Куркин Е.Н., Кабачков Е.Н. // Известия Академии наук. Серия химическая. 2017. Т. 66. № 4. С. 648.
Вершинин Н.Н., Бакаев В.А., Берестенко В.И., Ефимов О.Н., Куркин Е.Н., Кабачков Е.Н. // Химия высоких энергий. 2018. Т. 52. С. 78.
Вершинин Н.Н., Берестенко В.И., Ефимов О.Н., Куркин Е.Н., Кабачков Е.Н. // Химия высоких энергий. 2019. Т. 53. С. 400.
Вершинин Н.Н., Ефимов О.Н. // Патент РФ на изобретение № 2348090 от 27.02.2009. Катализатор и способ его получения.
Bukhtiyarov A.V., Prosvirin I.P., Bukhtiyarov V.I. // Applied Surface Science. 2016. T. 367. C. 214.
Yang F., Zhang B., Dong S., Wang C., Feng A., Fan, X., Li Y. // J. Energy Chemistry. 2019. T. 29. C. 72.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий