Химия высоких энергий, 2021, T. 55, № 5, стр. 388-392
Радиационно-химический синтез перфторированных теломеров тетрафторэтилена
Г. А. Кичигина a, *, П. П. Кущ a, Д. П. Кирюхин a, Ю. М. Шульга a, **
a ФГБУН Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. Академика Семенова, 1, Россия
* E-mail: kga@icp.ac.ru
** E-mail: yshulga@gmail.com
Поступила в редакцию 18.03.2021
После доработки 30.04.2021
Принята к публикации 11.05.2021
Аннотация
Исследована кинетика радиационной-инициированной теломеризации тетрафторэтилена в карбогале и хладоне 350, получены новые перфрорированные теломеры тетрафторэтилена. Подробное изучение ИК-спектров поглощения полученных теломеров подтверждает факт вхождения фрагментов молекул растворителей в состав полученных перфторированных теломеров, отсутствие в них двойных С=С связей и их более аморфную структуру. Анализ отличий ИК-спектров теломеров и политетрафторэтилена позволил также предположить, что полученные теломеры могут быть использованы для создания супергидрофобных покрытий.
Теломеризация тетрафторэтилена (ТФЭ) в ряде растворителей, инициированная различными способами [1], в том числе, и под действием γ-излучения при комнатной температуре, подробно исследована в ряде работ. В результате процесса радиационно-инициированной теломеризации получены теломеры с общей формулой R1(CF2CF2)nR2, где состав концевых групп R1 и R2 зависит от растворителя, в котором проводился синтез. Ранее были получены теломеры в ацетоне, этилацетате, хлорсодержащих растворителях, фторированных спиртах и бензоле, фреонах и хлорсиланах с различными концевыми группами [2–5]. Изучена кинетика процесса, ряд свойств, полученных теломеров (термостабильность, растворимость, молекулярное и морфологическое строение и др.), предложен механизм реакции. Эффективность процесса радиационной теломеризации определяется концентрацией мономера, дозой облучения и весьма существенно зависит от химической природы растворителя. Ряд теломеров успешно применен для создания гидрофобных покрытий различных материалов (ткань, стеклоткань, высокопористые керамические материалы и др.), получены образцы гидрофобных материалов, имеющих краевые углы смачивания 130°–140° [6–8]. Особый интерес вызывает радиационный синтез в перфторированных растворителях, поскольку позволяет получить перфторированные теломеры, которые по своим свойствам будут наиболее близки к высокомолекулярному политетрафторэтилену (ПТФЭ), обладающему уникальными свойствами, в том числе, высокой гидрофобностью. Важно отметить, что все синтезированные теломеры представляют собой коллоидные растворы, что значительно облегчает их использование, по сравнению с ПТФЭ, при создании покрытий и композиционных материалов.
В данной работе в качестве растворителей для синтеза перфторированных теломеров использованы карбогал и хладон 350. Основной целью работы на этом этапе был радиационно-химический синтез, изучение кинетики процесса и молекулярного строения полученных теломеров ТФЭ, а также проведение сравнительного анализа спектральных характеристик исследуемых теломеров и ПТФЭ.
МЕТОДИКА ЭКСПЕРИМЕНТА
Для радиационного синтеза теломеров тетрафторэтилена были использованы тетрафторэтилен (С2F4, ТФЭ), карбогал (перфтор-1,3-диметилциклогексан, C8F16) и хладон 350 (перфторметилциклогексан, C7F14) производства ООО “Завод полимеров Кирово-Чепецкого химического комбината”. Газообразный ТФЭ, содержащий 0.02% примесей, и растворители специальной очистке не подвергались. Радиационная теломеризация проводилась в запаянных стеклянных ампулах. Образцы готовились по стандартной методике: в стеклянную ампулу (объем ~5 мл) помещали определенное количество растворителя, освобождали от растворенного воздуха и при 77К намораживали необходимое количество ТФЭ, ампулу запаивали. Реакционную смесь перемешивали при комнатной температуре и подвергали облучению γ-лучами 60Со на УНУ “Гамматок-100”, мощность дозы облучения 3.2 Гр/c. Исходная концентрация ТФЭ в растворах телогенов составляла ~0.4–1.0 ± ± 0.02 моль/л. Концентрацию полученных растворов теломеров определяли гравиметрически после удаления растворителя из реакционной смеси. Ошибка измерений не превышала ± 0.5%.
ИК спектры нарушенного полного внутреннего отражения (ИК НПВО) образцов сухих теломеров регистрировали при комнатной температуре в диапазоне 400–4000 см–1 на ИК−Фурье-спектрометре “Perkin Elmer Spectrum Two” с приставкой НПВО.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В качестве растворителей для синтеза теломеров ТФЭ, как отмечено во введении, использовали карбогал и хладон 350. На рис. 1а приведены зависимости выхода теломера в карбогале от дозы облучения при двух концентрациях ТФЭ. Процесс протекает очень эффективно, для полной конверсии мономера при концетрации ТФЭ в растворе 0.83 моль/л требуется доза облучения всего 2 кГр. Была также изучена зависимость выхода теломера от концентрации мономера при фиксированной дозе облучения. При дозе облучения 0.9 кГр и изменении концентрации ТФЭ от 0.4 до 1.03 моль/л выход теломера меняется незначительно в интервале 71–79%.
Рис. 1.
Зависимость выхода теломера ТФЭ в карбогале при концентрации ТФЭ 0.83 (1) и 0.72 (2) моль/л (а) и хладоне 350 при концентрации ТФЭ 0.85 (1) и 0.75 (2) моль/л (б).
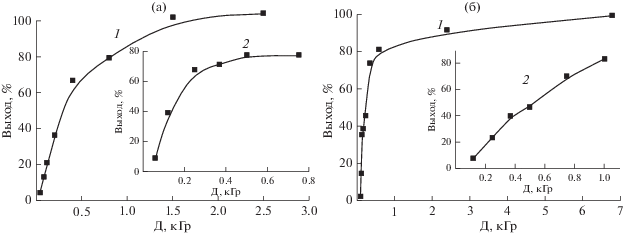
Аналогичные исследования были проведены для реакционной смеси ТФЭ + хладон 350 (рис. 1б). В хладоне скорости реакции ниже, но различие в скоростях незначительно. Выход теломера в карбогале при дозе 2.5 кГр составляет 100%, а в хладоне 350 – 90%. Отметим, что так эффективно процесс теломеризации протекает только во фторсодержащих растворителях, в частности, во фреоне-114В2 и фреоне-113 (рис. 2), где скорость процесса еще выше. При проведении процесса в ацетоне, хлорсодержащих растворителях требуемая доза облучения выше на порядок. Как отмечалось ранее [5], одной из возможных причин более эффективного протекания процесса теломеризации ТФЭ во фторированных растворителях является более высокая растворимость мономера в телогене. Молярная растворимость ТФЭ в ацетоне составляет 0.35%, в четыреххлористом углероде – 1.26%, а во фреоне-114В2 – 2.7%.
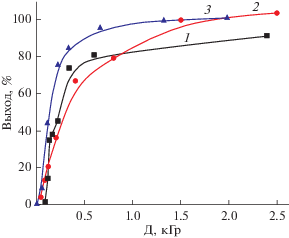
Рис. 2.
Зависимость выхода теломера от дозы облучения в хладоне 350 (1), карбогале (2) и фреоне- 114В2 (3) при концентрации ТФЭ ~ 0.8 моль/л.
Полученные теломеры представляют собой коллоидные растворы, которые разбавляются растворителем до необходимой концентрации, что важно при их практическом применении. Вязкость растворов и длина цепи теломеров определяются исходной концентрацией ТФЭ. Удаление растворителя из раствора приводит к получению белого порошка, который и был использован для регистрации ИК-спектров поглощения.
Для изучения молекулярной структуры теломеров были подробно изучены ИК-спектры поглощения и проведен их сравнительный анализ со спектрами ПТФЭ. В низкочастотной области спектра, где располагаются полосы поглощения деформационных веерных и маятниковых колебаний CF2-групп, никаких различий в положении пиков теломеров и ПТФЭ, не наблюдается (рис. 3а). Однако в случае дублета 638–626 см–1 наблюдается перераспределение интенсивностей. Ранее было замечено [9], что интенсивности пиков в этом дублете в спектре ПТФЭ меняются в соответствии с кристаллическими переходами от 19 к 30°С [10], а именно интенсивность компоненты при 638 см–1 уменьшается, а интенсивность компоненты при 626 см–1 увеличивается с ростом температуры. На основании этих наблюдений пики при 638 и 626 см–1 связывают со спиралями 136 и 157 соответственно [11]. Следовательно, соотношение концентраций (С) спиралей С(136)/С(157) при комнатной температуре в теломерах ниже, чем в ПТФЭ.
Рис. 3.
ИК-спектры ПТФЭ (1), теломера ТФЭ в хладоне 350 (2) и карбогале (3) в области 450–700 (а) и 1000–1400 (б) см–1.
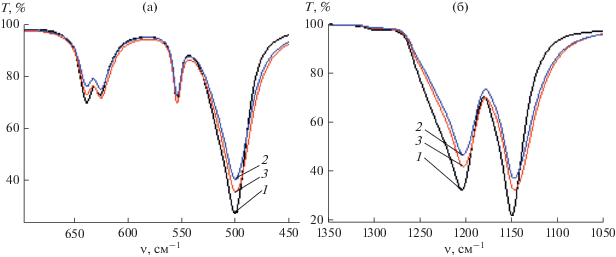
Полосы поглощения валентных колебаний связей С–F в теломерах расположены при 1146.6 и 1202.4 см–1 (рис. 3б), тогда как в ПТФЭ эти полосы находятся при 1149.4 и 1204.1 см–1. Следовательно, силовая постоянная связи С–F фрагмента СF2 в теломере слабее, чем в полимере.
В спектральном диапазоне 600–1000 см–1 (рис. 4), прежде всего, отметим пик при 936 см–1, который присутствует в спектрах всех трех образцов с примерно равной интенсивностью. В случае теломеров (кривые 2 и 3) резко возрастают интенсивности пиков при 720.6, 744.4 и 775.3 см–1. Известно, что многие авторы связывают интенсивность пика при 778 см–1 в спектре ПТФЭ с присутствием в образце аморфной фазы [9, 11]. В нашем случае можно предполагать, что широкий пик с максимумом при 775.3 см–1 также обусловлен аморфной фазой, что свидетельствует о более аморфной структуре теломеров по сравнению с ПТФЭ. Аналогичные выводы были сделаны при изучении молекулярной структуры теломеров ТФЭ во фреоне 114В2 методами ИК-спектроскопии и электронной силовой микроскопии [5].
Рис. 4.
(а) ИК-спектры ПТФЭ (1), теломера ТФЭ в хладоне 350 (2) и карбогале (3); (б) ИК спектры хладона 350 (1) и карбогала (2).
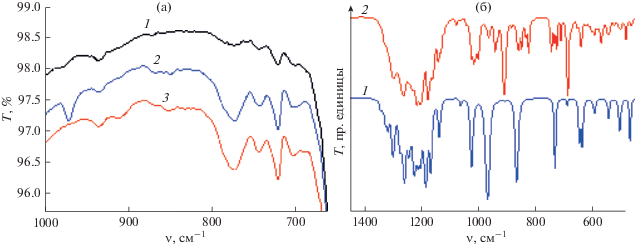
В спектрах теломеров появляется ряд дополнительных полос, которых нет в спектре ПТФЭ. Для их отнесения было проведено сравнение со спектрами растворителей, в которых проводился синтез (рис. 4б). В спектре образца теломера ТФЭ в хладоне 350 (рис. 4а, кривая 2) присутствуют полосы при 973 и 865 см–1, которых нет в спектрах образцов ПТФЭ и теломера ТФЭ в карбогале. В ИК-спектре хладона 350 наиболее интенсивные полосы расположены при 969 и 862 см–1. Исходя из этого можно полагать, что полосы 973 и 865 см–1 в спектре теломера относятся к колебаниям концевых групп теломера, они незначительно смещены по частоте на 2–4 см–1, по сравнению с хладоном, что свидетельствует о вхождении фрагментов его молекулы в состав теломера. Интенсивность полос, относящихся к концевым группам, мала, что свидетельствует об их малом количестве и, соответственно, достаточно большой длине цепи теломера. Аналогичная картина наблюдается для теломера ТФЭ в карбогале (рис. 4а, кривая 3). В спектре этого образца регистрируются дополнительные полосы при 912 и 687 см–1, которые отсутствуют в спектрах других образцов, они соответствуют полосам 909 и 686 см–1 в спектре карбогала. Как и в случае теломера в хладоне 350 наблюдается их небольшое смещение по частоте. Относительная интенсивность полос концевых групп зависит от длины цепи теломера, которая определяется, главным образом, концентрацией ТФЭ. С уменьшением концентрации мономера уменьшается длина цепи и растет интенсивность ИК-полос концевых групп. Сравнение спектров теломеров в карбогале при концентрациях ТФЭ 0.46 и 0.14 моль/л показывает, что с уменьшением концентрации мономера возрастает интенсивность полос 912 и 687 см–1. Это является дополнительным свидетельством того, что они связаны с наличием фрагментов молекулы карбогала в составе теломера. Таким образом, анализ ИК-спектров подтверждает факт вхождения фрагментов молекул растворителей в состав полученных перфторированных теломеров.
В теломерах (кривые 2 и 3, рис. 5а) отсутствуют двойные связи С=С, которые в исследуемом ПТФЭ проявляются в виде пиков при 1650, 1712 и 1741 см–1 (кривая 1).
Рис. 5.
ИК-спектры ПТФЭ (1), теломера ТФЭ в хладоне 350 (2) и карбогале (3) в области 1400–1800 (а) и 2800–3600 (б) см–1.
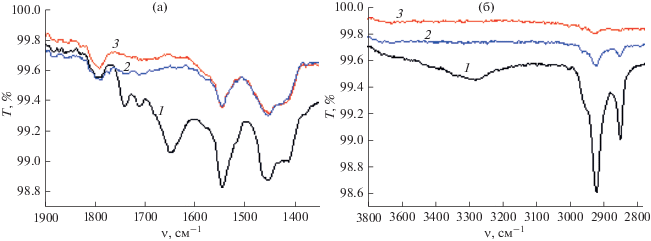
Интересный результат наблюдается также при анализе высокочастотной области спектра, где располагаются валентные колебания связей С–Н (2924 и 2854 см–1) и О–Н (3283 см–1). Мы видим, что количество углеводородов в порошках полученных теломеров (рис. 5б, кривые 2 и 3) существенно меньше таковых в ПТФЭ (кривая 1). В качестве образца сравнения (ПТФЭ) мы использовали PTFE (HMH, Германия), возможно, используемая лента была специально замаслена. Однако отсутствие пика в области колебаний связей О–Н в обоих теломерах позволяет предположить, что исследуемые перфторированные теломеры будут более эффективными гидрофобизаторами и позволят получить супергидрофобное покрытие. В подтверждение этого заключения можно привести такие наблюдения. Теломеры с концевыми ацетоновыми, гидроксильными и аминогруппами, использованные ранее для гидрофобизации ряда материалов, по данным ИК-спектров в большей или меньшей степени содержали ОН-группы. Их максимальное количество регистрировалось в теломерах, полученных во фреоне 113 с добавлением этанола, где были получены теломеры с концевыми ОН-группами [3]. При этом минимальные краевые углы смачивания (110°–115°) при получении гидрофобных покрытий стеклоткани [6] и пористых керамических материалов [8] были получены при использовании именно этих теломеров. Для тех же материалов краевые углы смачивания при применении теломеров с NH2 и ацетоновыми концевыми группами достигали 140°. Исследования свойств новых перфторированных теломеров другими методами и перспективы их дальнейшего использования для гидрофобизации различных материалов будут продолжены.
Анализ результатов, полученных на данном этапе исследований, позволяет сделать заключение, что с использованием в качестве растворителей карбогала и хладона 350, в процессе радиационно-инициированной теломеризации были получены растворы новых перфторированных теломеров ТФЭ. Спектральные характеристики синтезированных теломеров позволяют надеяться, что их использование в качестве гидрофобизаторов позволит получить покрытие, обладающее высокой гидрофобностью.
Список литературы
Ameduri B., Boutevin B. // Well_Architectured Fluoropolymers: Synthesis, Properties and Applications. Am-ster-dam–Boston–Heidelberg–London–New York: Elsevier, 2004.
Кирюхин Д.П., Кичигина Г.А., Кущ П.П., Бузник В.М. // Низкомолекулярные фторполимерные материалы. Монография “Фторполимерные материалы” (гл. 4). Томск: Изд-во НТЛ, 2017. 600 с.
Кущ П.П., Кичигина Г.А., Кирюхин Д.П., Баринов Д.Я. // Химия высоких энергий. 2018. Т. 52. № 1. С. 38.
Кичигина Г.А., Кущ ПП., Кирюхин Д.П. // Химия высоких энергий. 2017. Т. 51. № 2. С. 103.
Кирюхин Д.П., Кичигина Г.А., Кущ П.П., Курявый В.Г., Бузник В.М. // Известия АН, серия химическая. 2013. № 7. С. 1659.
Кичигина Г.А., Кущ П.П., Кирюхин Д.П., Дорохов В.Г., Барелко В.В. // Химия высоких энергий. 2020. Т. 54. № 5. С. 387.
Prorokova N.P., Kumeeva T.Yu., Kiryukhin D.P., Kichigina G.A., Kushch P.P. // Progress in Organic Coatings. 2020. V. 139. P. 105485.
Кичигина Г.А., Кущ П.П., Кирюхин Д.П. // Журн. прикладной химии. 2020. Т. 93. № 2. С. 214.
Moynihan R.E. // J. Am. Chem. Soc. 1959. V. 81. P.1045.
Василец В.Н., Шульга Ю.М., Иржак А.В., Мележик А.В., Ткачев А.Г. // Химия высоких энергий. 2019. Т. 53. № 4. С. 274.
Quarti C., Milani A., Castiglioni C. // J. Phys. Chem. B 2013. V. 117. P. 706.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий


