Химия высоких энергий, 2021, T. 55, № 6, стр. 499-501
Влияние внешнего тяжелого атома на выходы продуктов фотоиндуцированной гетероциклизации 2-азидобензойной кислоты
А. В. Будруев a, *, М. А. Гиричева a, Д. А. Давыдов a, А. В. Покровская a, А. Л. Пронина a
a Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр. Гагарина, 23/5, Россия
* E-mail: budruev@gmail.com
Поступила в редакцию 26.05.2021
После доработки 01.07.2021
Принята к публикации 06.07.2021
В органическом синтезе ароматические азиды используются в качестве генераторов высокоактивных короткоживущих интермедиатов [1–4]. Первая стадия реакции включает образование арилнитренов, мультиплетность которых определяет направление последующих стадий реакции.
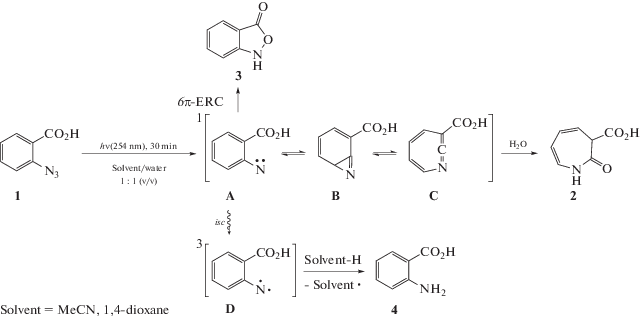
Образование при фотолизе 2-азидобензойной кислоты 1 3H-азепин-2(1Н)-он-3-карбоновой кислоты 2, 2,1-бензизоксазол-3(1H)-она 3 и 2-аминобензойной кислоты 4 иллюстрирует сложность фотохимических реакций ароматических азидов [5].
Азепин 2 образуется при нуклеофильном присоединении воды к 1,2-дидегидроазепину С – продукту электроциклической перегруппировки синглетного нитрена А, в то время как 2-аминобензойная кислота 4 является продуктом реакций триплетного нитрена D. Внутримолекулярная 6π‑электроциклизация (6π-ERC) синглетного нитрена ведет к образованию 2,1-бензизоксазол-3(1H)-она 3 (Схема 1 ).
Введение в реакционную смесь соединений, облегчающих интеркомбинационную конверсию синглетного нитрена А в триплетное состояние D (isc), например, соединений, содержащих атомы тяжелых элементов (HA), может привести к изменению направления реакции [6, 7]. Цель работы состояла в проверке возможности изменения выходов продуктов реакции при добавке соединений, содержащих атомы тяжелых элементов, не образующие устойчивых комплексов с интермедиатами фотолиза азида.
Схема 1 . Фотолиз 2-азидобензойной кислоты в органо-водных смесях.
Азид и продукты реакции синтезировали, выделяли по методикам работы [5] и охарактеризовали спектральными методами.
Растворы азида 1 (6 ммоль/л) в смеси ацетонитрила (MeCN) или 1,4-диоксана с водой облучали при 25°С в кварцевом реакторе 30 мин спаренной ртутно-кварцевой лампой низкого давления БУФ‑15 (2 × 15 Вт) (LP) или ртутно-кварцевой лампой сверхвысокого давления ДРК-120 (120 Вт) со светофильтром СЗС-24/BGG24 (длина волны обрезания УФ-излучения 310 нм) (HP). Выходы гетероциклов 2 и 3 определяли с использованием внешнего стандарта на приборе Shimadzu LC-20AD с детектором SPD-M20A, петлей 20 мкл (колонка Discovery C-18, 5 мкм, 3 мм, l 25 см и градиентным элюированием – этанол 65.5%: фосфорная кислота (0.01%) с линейным уменьшением до 0% к 20 мин и продолжением элюирования этанолом до 45 мин. Скорость потока 0.15 мл/мин).
Для изучения влияния триплетного состояния нитрена на фотохимическую гетероциклизацию азида 1 исследовали зависимости выходов гетероциклов 2 и 3 от мольного избытка введенных в реакционную смесь: бромида калия, бромэтана, 1‑бромбутана и хлорида бария, взятых в мольном соотношении азид 1/добавка: 1 : 1, 1 : 3, 1 : 5 и 1 : 10.
В отсутствие соединений, содержащих тяжелые атомы, выходы 3H-азепин-2(1Н)-она 2 и 2,1-бензизоксазол-3(1H)-она 3 составили 42 и 11% соответственно. Добавка бромида калия приводила к уменьшению выходов 3Н-азепинона 2 до 35% при этом выходы 2,1-бензизоксазол-3(1H)-она 3 не изменялись (табл. 1, № 2). Замена бромида калия на бромэтан и 1-бромбутан приводила только к незначительному уменьшению гетероциклов 2 и 3 (табл. 1).
Таблица 1.
Влияние содержащих тяжелые атомы добавок на выходы продуктов фотолиза азида 1
| № | Добавка HA | Органический растворитель (вода об. %) | Выходы продуктов, % | Степень конверсии азида 1, % | |
|---|---|---|---|---|---|
| 2 | 3 | ||||
| 1 | Нет | 1,4-диоксан (50) | 42 | 11 | 67 |
| 2 | KBr | 1,4-диоксан (50) | 35 | 11 | 65 |
| 3 | KBr | MeCN (50) | 30 | 9 | 64 |
| 4 | EtBr | MeCN (50) | 30 | 9 | 62 |
| 5 | 1-BuBr | MeCN (50) | 34 | 6 | 60 |
| 6 | 1-BuBr | 1,4-диоксан (20) | 27 | 10 | 80 |
| 7 | 1-BuBr | MeCN (20) | 33 | 12 | 92 |
| 8 | 1-BuBr | MeCN (50) | 40 | 10 | 67 |
| 9 | BaCl2 | 1,4-диоксан (33) | 39 | 11 | 74 |
При уменьшении содержания воды в реакционной смеси с 50 до 20 об. %, замене источника излучения с LP на HP (табл. 1, № 7) и органического растворителя в реакционной смеси с 1,4-диоксана на ацетонитрил, а также фотолизе азида 1 в присутствии 30-кратного мольного избытка 1‑бромбутана (табл. 1, № 6) приводила лишь к уменьшению выходов как 3Н-азепинона 2, так и 2,1-бензизоксазол-3(1H)-она 3 не более чем на 25%. Замена бромида калия на хлорид бария не изменяла выходов гетероциклов.
Таким образом, уменьшение выходов продуктов гетероциклизации подтверждает предположение о синглетном пути образования обоих продуктов реакции. Отсутствие значительных изменений выходов продуктов гетероциклизации при добавлении HA указывает на низкую вероятность образования диффузионно-столкновительного комплекса добавки с интермедиатами фотолиза азида, что, вероятно, связано с их малым временем жизни.
Список литературы
Bräse S., Gil C., Knepper K. и дp. // Angew. Chem. Int. Ed. 2005. V. 44. № 33. P. 5188.
Hoffmann N. // Chem. Rev. 2008. V. 108. № 3. P. 1052.
Gritsan N., Platz M. Photochemistry of azides: the azide/nitrene interface Wiley Online Library, 2010. C. 311–372.
Azides and nitrenes: reactivity and utility. / Scriven E.: Elsevier, 2012.
Dzhons D.Y., Budruev A.V. // Beilstein J. Org. Chem. 2016. V. 12. № 1. P. 874.
Soto J., Otero J.C., Avila F.J. Peláezb D. // Phys. Chem. Chem. Phys. 2019. V. 21. № 5. P. 2389.
Koziar J.C., Cowan D.O. // Acc. Chem. Res. 1978. V. 11. № 9. P. 334.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий