Химия высоких энергий, 2022, T. 56, № 5, стр. 334-339
Фотовосстановление и фотоинициирующая способность 1-гексадецильных производных изатина, содержащих в положении 5 заместители различной природы
Н. А. Леньшина a, *, М. В. Арсеньев a, А. А. Фагин a, А. В. Богданов b, С. А. Чесноков a
a Федеральное государственнoe бюджетное учреждение науки Институт металлоорганической химии
им. Г.А. Разуваева Российской Академии наук
603950 Нижний Новгород, ул. Тропинина 49, Россия
b Институт органической и физической химии им. А.Е. Арбузова – обособленное структурное подразделение Федерального государственного бюджетного учреждения науки “Федеральный исследовательский центр
“Казанский научный центр” Российской Академии наук
420111 Казань, ул. Лобачевского 2/31, Россия
* E-mail: lennin@iomc.ras.ru
Поступила в редакцию 25.04.2022
После доработки 16.05.2022
Принята к публикации 19.05.2022
- EDN: WSIMLT
- DOI: 10.31857/S0023119322050096
Аннотация
Синтезированы и охарактеризованы новые 1-гексадецильные производные изатина, содержащие в положении 5 заместители различной природы. Исследована кинетика их фотовосстановления под действием видимого излучения в присутствии 4-метил-N,N-диметиланилина и триэтиламина. Установлено, что константа скорости фотовосстановления увеличивается в ряду замещенных изатинов CH3 < H < Cl < Br. Показано, что система “изатин–амин” инициирует фотополимеризацию видимым излучением олигокарбонатдиметакрилата ОКМ-2. Эффективность фотоинициирования коррелирует с активностью изатинов в реакции фотовосстановления.
ВВЕДЕНИЕ
Большая часть фотоиницииирующих систем, чувствительных к УФ и видимому излучению, основана на реакции фотовосстановления карбонилсодержащего соединения, в ходе которой происходит генерация иницирующих фотополимеризацию радикалов [1–6]. Изатин – хорошо известное природное карбонилсодержащее соединений, поглощающее излучение в видимом диапазоне. Ввиду наличия у него, а также у гетероциклических соединений, включающих изатиновый фрагмент, разнонаправленной биологической активности, изатин и его производные обычно используется в качестве прекурсоров для синтеза широкого спектра биологически активных соединений [7–10]. В полимерной химии изатины служат структурными блоками для получения полимеров [11–13], в то время как использованию изатинов в системах фотоинициирующих радикальную полимеризацию посвящены лишь единичные исследования. Так, авторами [14] показано, что изатин может быть использован в качестве фотосенсибилизатора для фотополимеризации метилметакрилата под действием видимого излучения при 40°С в атмосфере азота. Известно, что изатин и N-метилизатин способны к фотовосстановлению с образованием радикалов при облучении видимым светом в присутствии доноров водорода, таких как третичные амины, фенолы и ароматические соединения [15, 16]. Это позволяет говорить о потенциальной способности систем “изатин–донор водорода” инициировать радикальную полимеризацию (мет)акриловых мономеров.
1-Гексадецильные производные изатина поглощают излучение в диапазоне 400–500 нм и, в сравнении с изатином, лучше растворяются в органических растворителях и мономерах. Это делает 1-гексадецильные производные изатина более подходящими, чем изатин компонентами фотоинициирующих систем для свободнорадикальной полимеризации под действием видимого излучения.
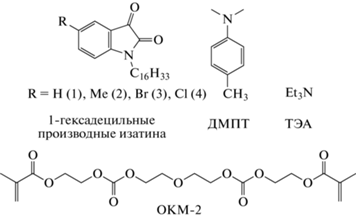
Данная статья посвящена синтезу новых 1‑гексадецильных производных изатина с различными заместителями в 5-положении, изучению реакция их фотовосстановления в присутствии доноров водорода 4-метил-N,N-диметиланилина (N,N-диметил-пара-толуидин, ДМПТ) и триэтиламина (ТЭА) (схема 1), а также исследованию возможности использования системы “изатин–амин” для фотоинициирования радикальной полимеризации на примере олигокарбонатдиметакрилата ОКМ-2. Структурные формулы объектов исследования приведены на схеме 1.
Схема 1. Объекты исследования.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты
1-гексадецилизатин 1 синтезировали по ранее описанной методике [17]. Триэтиламин (“Aldrich”) очищали перегонкой. 4-Метил-N,N-диметиланилин (“Aldrich”) очищали перегонкой при пониженном давлении. Бензол (“ХимРеактив”) и α,ω-бис-(метакрилоилоксиэтиленоксикарбонилокси) этиленоксиэтилена (ОКМ-2, “Репер-НН”) очищали по известным методикам [18, 19]. Перхлорат тетрабутиламмония Bu4NClO4 (99%, “Aldrich”) дважды перекристаллизовывали из водного этилового спирта и сушили в вакууме при 50°C.
Оборудование
Спектры ЯМР 1Н регистрировали на приборах Bruker Avance-400 в CDCl3, ДМСО-d 6 или смеси CDCl3/ДМСО-d 6. Масс-спектры MALDI регистрировали на масс-спектрометре UltraFlex III TOF/TOF. ИК спектры изатинов получены на приборе “Bruker Vector-22”. Элементный анализ выполнен на анализаторе EuroVector 2000 CHNS-O. Электронные спектры поглощения регистрировали на спектрофотометре СФ-56. Цикловольтамперометрические эксперименты проводили с помощью потенциостата “Elins P-45X”. ИК спектры для исследования кинетики фотополимеризации регистрировали на Фурье-спектрометре ФТ-801 с универсальной приставкой НПВО-А (Симэкс, Россия).
Синтез 1-гексадецильных производных изатина, содержащих в положении 5 заместители различной природы
Общая методика синтеза производных изатина (2–4). К раствору производного изатина (10 ммоль) в 20 мл ДМФА при перемешивании на магнитной мешалке при 5°С медленно присыпали 0.42 г (10 ммоль, 60% суспензия в минеральном масле) гидрида натрия. Через 30 мин в реакционную массу при 20°С добавляли по каплям 0.95 ммоль 1-бромгексадекана. Полученный раствор перемешивали при 60°С в течение 6 ч, выливали в смесь 100 г льда с 50 мл воды. После самопроизвольного нагревания раствора до 20°С выпавший осадок отфильтровывали, промывали несколько раз водой (5 × 20 мл) и сушили при пониженном давлении.
1-Гексадецил-5-метилизатин (2). Красный порошок, выход 89%, т. пл. 63–64°С. ИК спектр, ν, см–1: 2962, 2927, 1733, 1696, 1608, 1507, 1460, 1332, 1275, 1164, 1095, 1022. Спектр ЯМР 1Н (ДМСО-d6, δ м.д., J Гц): 0.83 т (3Н, 3JНССН 7.0, CH3), 1.20–1.28 м (26Н, 13CH2), 1.58–1.61 м (2Н, CH2), 2.18 с (3Н, CH3), 3.61 т (2Н, 3JНССН 7.2, NCH2), 6.96 д (1Н, 3JНССН 8.6), 7.07 д (1Н, 4JНССН 2.6), 7.16 д. д (1Н, 3JНССН 8.6, 4JНСССН 2.6). Масс-спектр, m/z: 386 [M + H]+. Найдено, %: C, 77.69; H, 10.00; N, 3.55. C25H39NO2. Вычислено, %: C, 77.87; H, 10.19; N, 3.63.
1-Гексадецил-5-бромизатин (3). Оранжевый порошок, выход 95%, т. пл. 123–125°С. ИК спектр, ν, см–1: 2962, 2927, 1733, 1696, 1608, 1507, 1460, 1332, 1275, 1164, 1095, 1022. Спектр ЯМР 1Н (CDCl3, δ м.д., J Гц): 0.87 т (3Н, 3JНССН 7.0, CH3), 1.24–1.33 м (26Н, 13CH2), 1.63-1.71 м (2Н, CH2), 3.69 т (2Н, 3JНССН 7.4, NCH2), 6.80 д (1Н, 3JНССН 9.0), 7.67–7.69 м (2Н). Масс-спектр, m/z: 450 [M + H]+. Найдено, %: C, 63.85; H, 7.90; Br, 17.67; N, 3.01. C24H36BrNO2. Вычислено, %: C, 63.99; H, 8.06; Br, 17.74; N, 3.11.
1-Гексадецил-5-хлоризатин (4). Оранжевый порошок, выход 92%, т. пл. 115–116°С. ИК спектр, ν, см–1: 2962, 2927, 1733, 1696, 1608, 1507, 1460, 1332, 1275, 1164, 1095, 1022. Спектр ЯМР 1Н (CDCl3/ДМСО-d6, δ м.д., J Гц): 0.79 т (3Н, 3JНССН 7.0, CH3), 1.17–1.26 м (26Н, 13CH2), 1.56–1.63 м (2Н, CH2), 3.62 т (2Н, 3JНССН 7.2, NCH2), 6.91 д (1Н, 3JНССН 8.4), 7.44 д (1Н, 4JНССН 2.0), 7.51 д. д (1Н, 3JНССН 8.4, 4JНСССН 2.0). Масс-спектр, m/z: 406 [M + H]+. Найдено, %: C, 70.87; H, 8.80; Cl, 8.60; N, 3.29. C24H36ClNO2. Вычислено, %: C, 71.00; H, 8.94; Cl, 8.73; N, 3.45.
Описание цикловольтамперометрического эксперимента
Потенциалы окисления измеряли методом циклической вольтамперометрии (ЦВА) в трехэлектродной ячейке в среде аргона. В качестве рабочего электрода использовали стеклоуглеродный электрод (d = 2 мм), в качестве вспомогательного электрода – платиновую проволоку. В качестве электрода сравнения использовали электрод Ag/AgCl/KCl (нас.) с водонепроницаемой диафрагмой. Скорость развертки потенциала составляла 0.1 В с–1. В качестве фонового электролита использовали 0.1 М Bu4NClO4. Концентрация изатинов составляла 2 ммоль л–1 для соединений 1 и 2, и 1 ммоль л–1 для соединений 3 и 4.
Кинетика фотовосстановления
Кинетику фотореакций 1-гексадецильных производных изатина в бензоле исследовали спектрофотометрически по убыли полосы поглощения (λ = 438 нм) в соответствии с законом Бугера–Ламберта–Бера. Бензольные растворы изатинов с концентрацией 1.1 ммоль/л в присутствии 50-тикратного избытка аминов дегазировали вакуумированием, насыщали аргоном, затем помещали в атмосфере аргона в спектрофотометрическую кювету l = 1.0 см и экспонировали на расстоянии 12 см от фокусирующего устройства. В качестве источника излучения использовали проектор BenQ MP622c. Эффективную константу скорости фотореакций изатинов (kH) определяли по тангенсу угла наклона прямолинейного участка зависимости ln([D0]/[Dt]) – τ, где τ – время облучения раствора.
Кинетика фотополимеризации
Фотополимеризующиеся композиции готовили растворением изатина (концентрация 2.2 ммоль/л) и амина в ОКМ-2. Кинетику фотополимеризации ОКМ-2 исследовали методом RT-FTIR-спектроскопии [20]. Регистрировали изменение интенсивности полосы двойной связи C=C метакрилата в ближней инфракрасной области в интервале от 1630 до 1640 см–1. В качестве источника излучения использовался белый LED (Cree Xlamp XP-E2, диапазон излучения 400–740 нм, λмакс = 445, 540 нм).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
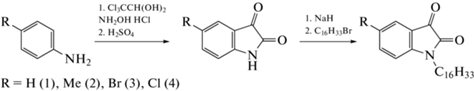
Производные изатина были получены в два этапа: на первом этапе по реакции Зандмайера [21] из соответствующих анилинов были получены 5-замещенные изатины (хлор-, бром-, метил-), которые на втором были введены в реакцию алкилирования с 1- бромгексадеканом (схема 2).
Схема 2. Синтез 1-гексадецильных производных изатина, содержащих в положении 5 заместители различной природы.
В электронных спектрах поглощения бензольных растворов полученных изатинов длинноволновая полоса поглощения наблюдается в области 350–550 нм. Положение максимумов поглощения полосы для различных изатинов приведены в табл. 1. Облучение видимым светом бензольных растворов 1-гексадецильных производных изатина в присутствии третичных аминов приводит к обесцвечиванию растворов. В качестве типичного примера на рис. 1 приведены изменения спектральных характеристик бензольного раствора 3 в присутствии триэтиламина при облучении раствора в течение одинаковых промежутков времени (15 с).
Таблица 1.
Электрохимические характеристики реагентов и величины констант скорости фотовосстановления изатинов в присутствии третичных аминов (kH)
| Изатин (R) | λмакс, нм (ε, л моль–1 см–1) | E1/2(A–/A), В | kH × 10–3, с–1 (ТЭА) |
kH × 10–3, с–1 (ДМПТ) |
|---|---|---|---|---|
| 1 (Н) | 430 (721) | –0.96 | 0.74 | 0.8 |
| 2 (Me) | 438 (625) | –0.96 | 0.24 | 0.3 |
| 3 (Br) | 438 (834) | –0.78 | 3 | 3.2 |
| 4 (Cl) | 439 (712) | –0.76 | 1.4 | 1.3 |
Рис. 1.
Спектральные изменения, наблюдаемые при облучении бензольного раствора 3 в присутствии триэтиламина (концентрация изатина 1.1 ммоль, мольное соотношение 1/50, вакуум, общее время облучения 150 с, интервал между спектрами 15 с).
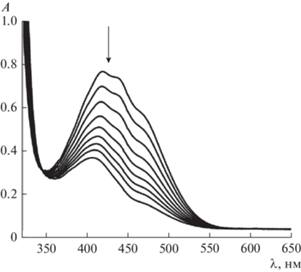
Определение величины эффективной константы фотовосстановления проводили по изменению интенсивности полосы поглощения изатинов при λ = 438 нм. Полученные значения приведены в табл. 1. Видно, что и для пар “изатин-триэтиламин”, и для пар “изатин–ДМПТ” наблюдается тенденция к росту константы скорости фотовосстановления изатина (kH) с увеличением электроноакцепторности изатина. Наибольшая величина kH наблюдается для пар ТЭА и ДМПТ с изатином 3.
Облучение растворов изатина и N-метилизатина в присутствии различных доноров водорода, в том числе аминов, приводит к образованию продуктов восстановления изатинов–изатидов [15]. Исследование методом флеш-фотолиза (λвозб = 355 нм) [16] показало, что процесс протекает через образование триплетного возбужденного состояния изатинов, энергия которого для незамещенного изатина находится в интервале от 49.3 до 54.3 ккал/моль, а для N-метилизатина не превышает 49.3 ккал/моль. Наличие в молекуле изатина тяжелого атома должно приводить к увеличению вероятности перехода из возбужденного синглетного в триплетное состояние. Последнее является активным в реакции отрыва атома водорода от молекулы амина и восстановлении изатина. Можно полагать, что значительное увеличение kH при переходе от изатинов 1 и 2 к хлор- и особенно бромсодержащему изатинам 4 и 3, соответственно, связано не только с усилением электроноакцепторности изатинов, но и с “эффектом тяжелого атома”.
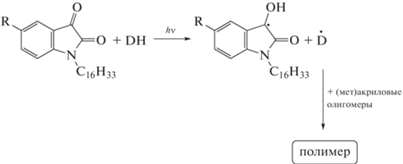
Фотовзаимодействие изатина с донором водорода (DH)приводит к образованию радикальныхпродуктов (схема 3). При использовании в качестведонора водорода аминов образующийсяаминильный радикал способен инициироватьполимеризацию мономеров (мет)акрилового ряда.
Схема 3. Фотоинициирование радикальной полимеризации системой “изатин–амин”.
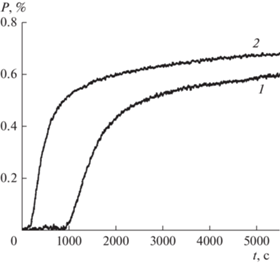
На рис. 2 приведены кинетические кривые фотополимеризации ОКМ-2 в присутствии инициирующих систем из комбинаций изатинов 2 и 3 с ТЭА. Видно, что в условиях эксперимента эффективность фотоинициирующей системы на основе изатина 3 существенно выше, чем на основе изатина 2: период индукции – 170 против 900 с; максимальная скорость полимеризации – 2 против 1 ммоль л–1 с–1, конверсия мономера через 1 ч экспонирования – 65 против 54%. Полученные различия в фотоинициирующей способности изатинов 2 и 3 коррелируют с различием реакционной способности данных изатинов в реакции фотовосстановления (табл. 1).
ЗАКЛЮЧЕНИЕ
Получены новые 1-гексадецильные производные изатина, содержащие в положении 5 заместители различной природы. Все синтезированные изатины способны к фотовосстановлению в присутствии третичных аминов при облучении видимым светом, при этом наличие атомов хлора и брома в 5 положении увеличивает скорость реакции. Показано, что система “изатин–амин” способна инициировать фотополимеризацию ОКМ-2 под действием видимого излучения.
Список литературы
Garra P., Fuassier J.P., Lakhdar S., Yagci Y., Lalevée J. // Prog. Polym. Sci. 2020. V. 107. P. 101277.
Pigot C., Noirbent G., Brunel D., Dumur F. // Eur. Polym. J. 2020. V. 133. P. 109797.
Леньшина Н.А., Шурыгина М.П., Чесноков С.А. // Высокомолекулярные соединения. Серия Б. 2021. Т. 63. № 6. С. 383.
Чесноков С.А., Шурыгина М.П., Абакумов Г.А. // Химия высоких энергий. 2011. Т. 45. №. 4. С. 319.
Zhiganshina E.R., Arsenyev M.V., Chubich D.A., Kolymagin D.A., Pisarenko A.V., Burkatovsky D.S., Baranov E.V., Vitukhnovsky A.G., Lobanov A.N., Matital R.P., Aleynik D.Ya., Chesnokov S.A. // European Polymer Journal. 2022. V. 162. P. 110917.
Жиганшина Э.Р., Лысенков В.С., Лопатина Т.И., Арсеньев М.В., Чесноков С.А. // Химия высоких энергий. 2022. Т 56. № 3. С. 1.
Pandeya S.N., Smitha S., Jyoti M., Sridhar S.K. // Acta Pharm. 2005 V. 55. № 1. P. 27.
Pakravan P., Kashanian S., Khodaei M.M., Harding F.J. // Pharmacological Reports. 2013. V. 65. № 2. P. 313.
Kakkar R. // MedChemComm. 2019. V. 10. № 3. P. 351.
Nath R., Pathania S., Grover G., Akhtar M.J. // Journal of Molecular Structure. 2020. V. 1222. P. 128900.
Yang W., Sun M., Wang Y., Yan H., Zhang G., Zhang Q. // Polymer Chemistry. 2021. V. 12. № 15. P. 2317.
Kasi B., Kaliaperumal N., Murugesan V. // Journal of Molecular Structure. 2021. V. 1242. P. 130714.
Zhang S., Zhu X., Jin C. // Journal of Materials Chemistry A. 2019. V. 7. № 12. P. 6883.
Som P.K., Banerjee A.N. // European polymer journal. 1993. V. 29. № 6. P. 889.
Haucke G., Seidel B., Graness A. // Journal of photochemistry. 1987. V. 37. № 1. P. 139.
Silva M.T., Netto-Ferreira J.C. // Journal of Photochemistry and Photobiology A: Chemistry. 2004. V. 162. № 2–3. P. 225.
Bogdanov A.V., Pashirova T.N., Musin L.I., Krivolapov D.B., Zakharova L.Y., Mironov V.F., Konovalov A.I. // Chem. Phys. Lett. 2014. V. 594. P. 69.
Гордон А., Форд Р. Спутник химика. Физико-химические свойства, методики, библиография. М.: Мир, 1976. 541 с.
Берлин А.А., Кефели Т.Я., Королев Г.В. Полиэфиракрилаты. М.: Наука, 1967. 372 с.
Boddapati A., Rahane S.B., Slopek R.P., Breedveld V., Henderson C.L., Grover M.A. // Polymer. 2011. V. 52. № 3. P. 866.
Sandmeyer T. // Helv. Chim. Acta. 1919. V. 2. P. 234.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий