Неорганические материалы, 2019, T. 55, № 1, стр. 67-79
Влияние условий синтеза на люминесценцию европийсодержащих композиций на основе оксида и оксифторидов иттрияВ. П. Смагин, А. П. Худяков
В. П. Смагин 1, *, А. П. Худяков 1
1 Алтайский государственный университет
656049 Барнаул, пр. Ленина, 61, Россия
* E-mail: smaginV@yandex.ru
Поступила в редакцию 17.04.2018
Аннотация
Исследована люминесценция композиций на основе оксида и оксифторидов иттрия, активированных ионами европия(III). Композиции синтезированы термическим разложением тиоацетамидных фторсодержащих комплексов иттрия и европия(III) при температурах 400, 600 и 800°С в течение 2–6 ч. В составе композиций зарегистрированы фазы (EuхY1 – х)F3, (EuхY1 – х)5O4F7, (EuхY1 – х)OF и (EuхY1 – х)2O3. Приведена схема, отражающая последовательность образования основных компонентов композиции в указанном температурном интервале. Узкополосная люминесценция композиций возникает вследствие электронных переходов 5D0 → 7Fj ионов Eu3+. Широкая полоса люминесценции с максимумом в области 490–500 нм связана с дефектностью структуры поверхности, размером и дисперсностью частиц. Показаны зависимости спектра люминесценции от состава реагентов, условий синтеза, состава матрицы, длины волны возбуждающего излучения. Выявлены особенности в спектрах люминесценции, которые вызваны влиянием ионов S2– в составе европийсодержащих активаторных центров.
ВВЕДЕНИЕ
Керамические композиции представляют большой интерес в качестве активных лазерных сред, визуализирующих покрытий, основы люминофоров и других применений [1, 2]. Основными стадиями их синтеза являются: получение неагломерированных порошков заданных состава и размера частиц, приготовление из них образцов высокой плотности и последующее их спекание до состояния керамики [3, 4]. Процесс изготовления керамики экономически выгоднее, чем выращивание монокристаллов и “варка” стекол. Он происходит при значительно более низкой температуре и менее требователен к соблюдению условий синтеза.
Среди керамических материалов выделим композиции на основе оксида иттрия [5–11]. Керамика на основе оксида иттрия прозрачна в видимой и инфракрасной областях спектра. Технология ее получения достаточно хорошо изучена. Y2O3 является одной из наиболее перспективных матриц для ионов лантаноидов. После легирования ионами лантаноидов свойства керамики приближаются к свойствам монокристаллов и стекол [1, 2]. При введении в состав керамики атомов фтора и при сочетании их в различных пропорциях с атомами кислорода изменяются характер химической связи, структурный тип матрицы, симметрия окружения ионов активатора и сила действующих на них полей [12–15]. Эти изменения оказывают влияние на электрические, оптические и магнитные свойства керамики. Увеличивается эффективность преобразования поглощенной энергии при уменьшении энергии фононов во фторидных и оксифторидных матрицах по сравнению с оксидами [15]. Данный эффект связан с уменьшением безызлучательных потерь энергии возбуждения, которые происходят при тепловых колебаниях атомов кристаллической решетки матрицы. Также возрастает эффективность обмена энергией между частицами активаторов при реализации каскадных и сенсибилизационных схем передачи энергии возбуждения [15].
В последнее десятилетие актуальной остается проблема, связанная с синтезом предшественников керамики. Для ее решения применяется метод осаждения прекурсоров из водных растворов солей металлов [7, 16–18]. После термической обработки они образуют порошки активированных оксидов. Получение слабо агломерированных порошков этим способом является сложной задачей. Кроме того, присутствие воды в реакционной смеси и гидроксильных производных в продуктах синтеза отрицательно влияет на люминесценцию керамики, легированной ионами лантаноидов. Применяются и другие методы синтеза композиций [19–28]. Высокотемпературные, лазерные, гидротермальные методы синтеза оксидов требуют значительных затрат энергии, а последний – специальных мер для предотвращения гидролиза. Положительный оптический эффект многие авторы связывают с наноразмерным состоянием порошков [11, 16, 20, 21, 29–32].
На первой стадии синтеза широко применяется золь–гель-технология [5, 6, 24, 26, 28]. Интересным решением является коллоидный синтез из неводных сред [33–36]. Применение малополярных органических растворителей на первой стадии синтеза композиций исключает воду из процесса синтеза. Замена воды на органическую реакционную среду позволяет удалить О–Н-группы из состава предшественников и продуктов синтеза, минимизировав этим тушение люминесценции активаторов в составе керамики. Также это способствует равномерному распределению активаторов в матрице и уменьшает температуру второй стадии – термолиза продуктов и гомогенизации композиций в процессе отжига. Как следствие, можно ожидать положительных изменений люминесцентных характеристик.
Цель данной работы состояла в разработке синтеза люминесцирующих композиций на основе легированных оксида и оксифторидов иттрия с применением малополярных органических сред и установление зависимостей спектрально-люминесцентных свойств от состава реагентов, условий синтеза и возбуждения люминесценции.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Композиции YF3–Y2O3, легированные ионами Eu3+, синтезированы в две стадии. На первой, низкотемпературной, стадии синтеза навески трифторацетатов иттрия и европия, полученных взаимодействием оксидов металлов с трифторуксусной кислотой (“х. ч.”) [37], растворяли в этилацетате (ЭА) (“х. ч.”). Количество трифторацетата европия рассчитывали исходя из его содержания в конечном продукте, равного 1.0 или 10 ат. % от содержания атомов иттрия. Для ряда образцов одновременно с трифторацетатами металлов в раствор вводили тиоацетамид (ТАА) в мольном соотношении с трифторацетатом иттрия, равном 1 : 1. При комнатной температуре испаряли растворитель до образования вязкой гелеобразной массы. Хорошая растворимость трифторацетатов металлов в ЭА и их склонность к образованию координационных полимерных структур в растворах, особенно при увеличении концентрации и комплексообразовании, способствовали равномерному распределению ионов активатора в матрице и их закреплению в определенных структурных позициях [37].
На второй стадии синтеза образовавшуюся массу помещали в муфельную печь и нагревали при температурах 400, 600 и 800°С. Время нагревания составляло от 2 до 6 ч. В результате получены порошки веществ. Окраска порошков зависела от температуры и времени синтеза, которые влияли на полноту “выгорания” органических компонентов композиций. Композиции идентифицированы методами РФА и ИК-спектроскопии. Исследована их люминесценция.
ИК-спектры веществ зарегистрированы на ИК-Фурье-спектрометре InfralumFT 801 в диапазоне 4000–500 см–1 (KBr). Рентгенофазовый анализ выполнен на рентгеновском дифрактометре XRD-6000 (CuKα-излучение) с использованием баз данных PCPDFWIN и программы полнопрофильного анализа POWDER CELL 2.4. Спектры возбуждения люминесценции и люминесценции зарегистрированы на спектрофлуориметре СМ 2203 (Республика Беларусь). Для исследования образец помещали между стеклянными пластинами. Возбуждающий свет ксеноновой дуговой лампы высокого давления ДКсШ 150–1М падал на образец перпендикулярно его поверхности. Люминесценцию регистрировали в идентичных условиях под углом 45°.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Спектры люминесценции композиций, синтезированных при температуре 600°С в течение 2, 4 и 6 ч из исходных смесей состава Y(CF3COO)3–Eu(CF3COO)3, содержащих 1.0 ат. % Eu3+, приведены на рис. 1. В спектрах наблюдаются полосы люминесценции, соответствующие 5D0 → 7F0,1,2,3,4-переходам 4f-электронов ионов Eu3+. Полосы в различной степени структурированы. Они неоднородно уширены, особенно у основания. Наиболее интенсивной является “красная” полоса сверхчувствительного электродипольного 5D0 → 7F2-перехода. В спектре она представлена в виде дублета. После двухчасового нагревания величина его расщепления составляла 9 нм. Положение максимумов в дублете соответствовало 618 и 627 нм. После нагревания в течение 4 и 6 ч (600°С) спектры композиций изменились. Между собой они практически не отличаются (рис. 1, спектры 2 и 3). Величина расщепления компонент 5D0 → 7F2 дублета в них составляла 18 нм. Максимумы соответствовали длинам волн 615 и 633 нм. Расщепление данной полосы авторами [13] объясняется изменением симметрии окружения ионов Eu3+ при переходе матрицы из ромбической фазы Y6O5F8 в ромбоэдрическую YOF, происходящем при увеличении концентрации ионов Eu3+. Как показывает РФА (табл. 1), состав композиций при указанных условиях синтеза более сложный. Особенно это проявилось для композиций, полученных при температуре 800°С с увеличением времени нагревания. Это является дополнительным доказательством неоднородности композиций и понижения симметрии активаторных центров. Более детальное обсуждение результатов РФА приведено в работе [36].
Рис. 1.
Спектры люминесценции (λв = 394 нм) продуктов прокаливания смеси Y(CF3COO)3 + Eu(CF3COO)3 при 600°С в течение 2 (1), 4 (2) и 6 ч (3); СEu = 1.0 ат. % от содержания атомов иттрия.

Таблица 1.
Результаты рентгенофазового анализа
| Исходная система (условия синтеза композиции) | Фаза, содержание, % | Параметры элементарной ячейки | Объем, V, Å3 |
Пр. гр. | Источник | Номер карты | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| а, Å | b, Å | c, Å | α, град | β, град | γ, град | ||||||
| Y(CF3COO)3–10 ат. % Eu(CF3COO)3–ЭА (5 ч, 600°С) |
YOF ((Y1 – xEux)OF), 85.4 (11) |
3.803 | 3.803 | 18.91 | 90 | 90 | 120 | 236.9 | 166 : R$\bar {3}$m, hex. |
ICDD (PDF-2/Release 2012 RDB) | 01-071-2100 |
| Y2O3 ((Y1 – xEux)2O3), 14.6 (4) |
10.63 | 10.63 | 10.63 | 90 | 90 | 90 | 1199.(8) | 206 : Ia$\bar {3}$, cub. | ICDD (PDF-2/Release 2012 RDB) | 01-089-5592 | |
| Y(CF3COO)3–1.0 ат. % Eu(CF3COO)3–ЭА (5 ч, 600°С) |
YOF ((Y1 – xEux)OF), 93 (9) |
3.793 | 3.793 | 18.85 | 90 | 90 | 120 | 234.9 | 166 : R$\bar {3}$m, hex. |
ICDD (PDF-2/Release 2012) | 01-071-2100 |
| Y2O3 ((Y1 – xEux)2O3), 7.1 (6) |
10.60 | 10.60 | 10.60 | 90 | 90 | 90 | 1191.(2) | 206 : Ia$\bar {3}$, cub. | ICDD (PDF-2/Release 2012 RDB) | 01-089-5592 | |
| Y(CF3COO)3–10 ат. % Eu(CF3COO)3–ЭА (3 ч, 800°С) |
Y5O4F7 (Y1 – xEux)5O4F7) |
5.407 | 27.55 | 5.520 | 90 | 90 | 90 | 822.2 | 39 : Abm2, romb. | ICDD (PDF-2/Release 2012 RDB) | 01-080-1124 |
| Y(CF3COO)3–10 ат. % Eu(CF3COO)3–ТАА–ЭА (6 ч, 800°С) |
Eu2O3 | 11.03 | 11.03 | 11.03 | 90 | 90 | 90 | 1342 | 206 : Ia$\bar {3}$, cub. | ICDD (PDF-2/Release 2012 RDB) | 00-034-0392 |
| EuOF | 3.869 | 3.869 | 19.21 | 90 | 90 | 120 | 248.9 | 166 : R$\bar {3}$m, hex. | ICDD (PDF-2/Release 2012 RDB) | 00-026-0636 | |
| YOF | 3.816 | 3.816 | 19.06 | 90 | 90 | 120 | 240.4 | 166 : R$\bar {3}$m, hex. | ICDD (PDF-2/Release 2012 RDB) | 01-071-2100 | |
| Y2O3 | 10.51 | 10.51 | 10.51 | 90 | 90 | 90 | 1161 | 206 : Ia$\bar {3}$, cub. | ICDD (PDF-2/Release 2012 RDB) | 01-089-5592 | |
| Eu(OH)3 | 6.359 | 6.359 | 3.574 | 90 | 90 | 120 | 125.1 | 176 : P63/m | ICDD (PDF-2/Release 2012 RDB) | 00-018-0504 | |
Магнитно-дипольный 5D0 → 7F1-электронный переход в спектрах образцов, полученных при двухчасовом нагревании, представлен в виде триплета (рис. 1, спектр 1). Его структура более выражена, чем в спектрах образцов, синтезированных в течение 4 и 6 ч (рис. 1, спектры 1 и 2, 3). В первую очередь это касается двух интенсивных компонент полосы. Они проявились двумя близкими по интенсивности максимумами. Положение максимумов соответствует длинам волн 592 и 598 нм. Как отмечается в работе [38], их соответствие данным значениям длин волн означает наличие C2-симметрии окружения ионов Eu3+. Признаком присутствия второго типа активаторных центров с С3i-симметрией окружения ионов Eu3+ является наличие в спектре полосы этого же перехода с максимумом в области 582 нм [38]. Ее связывают с асимметрией в расположении иона активатора в матрице [39]. Интенсивность полосы 5D0 → 7F1-электронного перехода практически не зависит от симметрии окружения ионов Eu3+. Поэтому ее часто используют в качестве стандарта для характеристики изменения интенсивностей других спектральных полос [12, 38]. Отношение интенсивностей в максимумах полос 5D0 → 7F2 и 5D0 → 7F1 в спектре композиции (2 ч, 600°С) I618/I598 ~ 2. В спектрах 2 и 3 (4 и 6 ч, 600°С) I615/I598 ~ ~ 4 (рис. 1). Эти отличия связаны с различной симметрией окружения ионов Eu3+ в продуктах, состав которых изменяется при увеличении времени синтеза: образуются оксифториды и оксид иттрия. Отмечается [12], что относительная интенсивность полосы 5D0 → 7F2-перехода уменьшается (уменьшается соотношение интенсивностей I615/I598) в случае, когда ионы Eu3+ находятся в локальном окружении более высокой симметрии. Исходя из температуры и времени нагревания (2 ч, 600°С) это может быть фаза фторидов. Подтверждением этому предположению служит полоса в спектрах возбуждения люминесценции с максимумом 537 нм. Ее появление в спектре связывают с фазой активированных фторидов [12]. Наличие в спектрах люминесценции композиций третьей компоненты полосы (582 нм, рис. 1) указывает на сложность их состава, связанную с начавшимся процессом перехода фторидов в оксифториды и далее в оксид. Еще одним важным фактором, который оказывает влияние на спектр люминесценции, является распределение ионов активатора на поверхности и в объеме частиц легированной фазы, отличающихся симметрией локального окружения [18, 39]. По данным [18], при увеличении времени нагревания возрастает доля ионов Eu3+ на поверхности частиц относительно их содержания в объеме кристаллов. Поверхность кристаллов характеризуется значительными нарушениями кристаллической структуры, особенно при уменьшении размера частиц, и, как следствие, искаженной локальной симметрией окружения ионов активатора. Это является одним из проявлений присутствия активаторов в локальном окружении с симметрией С3i [39] и увеличения интенсивности полосы 5D0 → 7F2-перехода. В исследованных композициях неравномерность распределения ионов Eu3+ может быть связана с “выгоранием” органики, которое сопровождается диспергированием и уменьшением размера частиц.
Кроме того, в спектрах композиций, полученных нагреванием в течение 2 ч, с большей интенсивностью проявляются полосы в коротковолновой части спектра с максимумами 516, 542 и 559 нм. Они могут быть связаны с 5D0 → 7F0-электронным переходом, а также с переходами электронов с высоколежащих 5Dj-электронных уровней иона Eu3+. Полоса 5D0 → 7F0-электронного перехода является синглетной. Она наблюдается при низкой симметрии локального окружения активатора. Наличие нескольких полос данного перехода связывают со сложностью состава композиции [12, 38].
Также отметим изменения относительной интенсивности, положения и структуры полосы в области 680–720 нм, соответствующей 5D0 → 7F4- электронному переходу.
В спектрах композиций, синтезированных при температуре 400°С (4 и 6 ч), пиковая интенсивность полосы люминесценции 5D0 → 7F2-электронного перехода (615 нм) примерно в 3 раза превосходит интенсивность полосы этого перехода в спектрах образцов, синтезированных в течение 2 ч. Она больше пиковой интенсивности соответствующей полосы в спектрах всех образцов, синтезированных при 600°С. Для этих полос различия в интенсивности в зависимости от времени синтеза (4, 6 или 2 ч, 600°С) не столь велики. Интенсивности полос 5D0 → 7F2- и 5D0 → 7F1-электронных переходов в спектре композиции, полученной в условиях 2 ч, 400°С, сопоставимы. Это можно связать с преимущественным образованием при более мягких условиях синтеза (2 ч, 400°С) продукта, кристаллическая структура которого обеспечивает относительно высокую локальную симметрию окружения ионов Eu3+. Таким продуктом может быть фторид иттрия. При дальнейшем нагревании он переходит в совокупность нестихиометрических оксифторидов общей формулы ${{\left( {{\text{E}}{{{\text{u}}}_{x}}{{{\text{Y}}}_{{1 - x}}}} \right)}_{{n \pm i}}}{{{\text{O}}}_{{(n \pm my) - 1}}}{{{\text{F}}}_{{(n \pm ky) + 2}}},$ где i – доля нестeхиометричности состава, $ \pm i = \pm (my + ky).$ Это приводит к существенному увеличению относительной интенсивности полосы 5D0 → 7F2-электронного перехода.
Спектры образцов композиций, синтезированных при 800°С (3 ч), отличаются от спектров, синтезированных при 400 и 600°С (2 ч), более выраженной структурой полос и меньшим уширением у их основания. Это объясняется улучшением однородности состава и структуры продуктов под влиянием температуры синтеза.
Полученные результаты можно объяснить следующими преобразованиями веществ, происходящими при нагревании композиций. При температуре 200°С начинается процесс разложения трифторацетатов лантаноидов. В основном он завершается к 400°С преимущественным образованием фторидов [37]. В продуктах синтеза (400°С) сохраняются не разрушившиеся фрагменты исходных веществ [36]. В ИК-спектрах обнаруживаются соответствующие им полосы в области поглощения карбонильной группы 1600–1500 см–1 и связей С–F при 1200–1100 см–1 (рис. 2а). Поглощение в области >3000 см–1 связано с валентными колебаниями гидроксильных групп. Их присутствие объясняется использованием при проведении синтеза кристаллогидратов солей. Полученные результаты соответствуют данным [15]. В спектре люминесценции (400°С, 2 ч) наблюдается бóльшая относительная интенсивность полосы 5D0 → 7F1-перехода. Полоса данного перехода сопоставима по интенсивности с полосой 5D0 → 7F2-электронного перехода. Относительно интенсивны полосы 5Dj → 7F0-электронных переходов, включая полосу 5D0 → 7F0-электронного перехода, в силу сложности состава продуктов, в том числе под влиянием неразложившихся органических структур.
Рис. 2.
ИК-спектры продуктов, полученных прокаливанием смеси Y(CF3COO)3 + Eu(CF3COO)3 при температуре 400°С в течение 2 ч (а) и 800°С в течение 3 ч (б); СEu = 1.0 ат. % относительно содержания атомов иттрия.

Далее, при увеличении температуры и времени синтеза, вероятно, образуется смесь нестехиометрических оксифторидов. Их структуры ведут свое происхождение от структур LnF3 и LnOF. Они могут рассматриваться в качестве их дефектных производных [12]. Происходящие процессы приводят к уменьшению локальной симметрии окружения люминесцирующих ионов. Увеличивается относительная интенсивность полосы 5D0 → 7F2-электронного перехода (400°С, 4 и 6 ч). Для полосы, соответствующей 5D0 → 7F1-электронному переходу, очевидно увеличение неоднородного уширения, особенно у основания. В продуктах еще сохраняются остатки “невыгоревшей” органики, которые исчезают при дальнейшем увеличении времени и температуры синтеза. Весьма важно то, что исчезает полоса поглощения в области >3000 см–1 (рис. 2б), так как соответствующие ей обертоны эффективно тушат люминесценцию лантаноидов.
При дальнейшем нагревании структура продуктов становится более однородной. Это может быть связано с образованием оксифторидов гомологического ряда LnnOn – 1Fn + 2 стехиометрического состава. Например, Y5O4F7 [36] и Y6O5F8 [12, 13]. Это подтверждено данными РФА [36]. Наряду с ними образуются оксифториды YOF и (EuxY1 – x)OY, что также подтверждено данными РФА [36]. Образование стехиометрических продуктов сопровождается увеличением однородности структур, повышением локальной симметрии окружения ионов Eu3+ и, соответственно, относительным уменьшением интенсивности полосы 5D0 → 7F2-перехода (600°С, 4 и 6 ч).
Увеличение температуры синтеза до 800°С (3 ч) приводит к образованию смеси, состоящей преимущественно из оксифторида YOF и оксида Y2O3, что подтверждается РФА (табл. 1), а также соответствует данным [36]. Соотношение фаз, по данным РФА, 83 мас. % YOF и 17 мас. % Y2O3. Внедрение ионов Eu3+происходит в первую очередь в кристаллическую структуру оксида иттрия [36]. Он занимает позиции с симметриями С2 и С3i. Теоретически их соотношение равно 3 : 1 [18]. Экспериментально его определяют по соотношению интенсивностей полос люминесценции 5D0 → 7F2 и 5D0 → 7F1 электронных переходов [40–42]. Для композиций с концентрацией ионов Eu3+ 10 ат. % оно примерно равно 5.7. В работах [18, 43] показано, что для образцов с размером частиц 10 нм это отношение практически не изменяется. Оно равно 4.7, 4.3, 5.2 при концентрации ионов Eu3+, 3.0, 5.0, 10 ат. % соответственно. Увеличение этого соотношения может быть связано со многими причинами, среди них – усложнение состава композиций, перераспределение ионов активатора между объемом кристаллов и их поверхностью, дисперсность частиц. В соответствии с приведенными рассуждениями, данными РФА и ИК-спектроскопии, а также литературными данными [12, 13, 15, 18, 36, 37] схема преобразований при нагревании исходных смесей в наиболее общем виде, т.е. с учетом только основного продукта каждой стадии, может быть следующей:
Завершение процесса образованием оксидов лантаноидов соответствует термодинамическим характеристикам соединений. Данный переход заканчивается при t > 1000°С.
Введение в исходные реакционные смеси ТАА приводит к появлению ряда особенностей в спектрах композиций (рис. 3). Во-первых, уменьшается время, в течение которого образуются продукты, локальная симметрия окружения ионов Eu3+ в которых создает энергетические поля, расщепляющие дублет 5D0 → 7F2 до 18 нм. Это видно при сопоставлении спектров 1 и 3 на рис. 3. Этими продуктами могут быть смесь оксифторидов гомологического ряда общей формулы (EuxY1 – x)nOn – 1Fn + 2 и оксифторида состава (EuxY1 – x)OF. Предпосылки этого возникают на первой, низкотемпературной, стадии синтеза. В реакционной смеси ТАА образует комплексные соединения с солями лантаноидов [44–46]. В подвергаемых термолизу образцах он связан с ионами лантаноидов через атомы серы. Термическое разложение тиоацетамидных комплексов приводит к изменению состава промежуточных продуктов и величине энергетических эффектов, соответствующих разрушению и окислению. В результате соответствующие европийсодержащие фазы могут образоваться при более низкой внешней температуре. Во-вторых, в спектрах композиций наблюдается широкая полоса с максимумом в области 480–500 нм и λ1/2 ~ 80 нм (рис. 3–5). Увеличение времени и температуры синтеза приводит к уменьшению относительной интенсивности или полному исчезновению данной полосы. Например, в спектрах продуктов, синтезированных при температуре 400°С, на фоне широкой полосы еще сохраняются полосы 5Dj → 7F0-электронных переходов (рис. 3, спектр 2). Увеличение температуры синтеза до 600°C нивелирует их (рис. 3, спектр 3). Относительная интенсивность полосы 5D0 → 7F4-электронного перехода уменьшается. Полоса занимает положение, аналогичное тому, которое приведено на рис. 1 (спектры 2 и 3).
Рис. 3.
Спектры люминесценции (λв = 394 нм) композиций, синтезированных из исходных смесей Y(CF3COO)3 + + Eu(CF3COO)3, 2 ч, 600°С (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 2 ч, 400°С (2), Y(CF3COO)3 + Eu(CF3COO)3 + + ТАА, 2 ч, 600°С (3); СEu = 1.0 ат. % относительно содержания атомов иттрия.

Рис. 4.
Спектры люминесценции (λв = 394 нм) композиций, синтезированных из исходных смесей состава Y(CF3COO)3 + Eu(CF3COO)3, 4 ч, 600°С (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 4 ч, 400°С (2), Y(CF3COO)3 + + Eu(CF3COO)3 + ТАА, 4 ч, 600°С (3); СEu = 1.0 ат. % относительно содержания атомов иттрия.

Рис. 5.
Спектры люминесценции (λв = 394 нм) композиций, синтезированных из исходных смесей Y(CF3COO)3 + + Eu(CF3COO)3, 6 ч, 600°С (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 6 ч, 400°С (2), Y(CF3COO)3 + Eu(CF3COO)3 + + ТАА, 6 ч, 600°С (3); СEu = 1.0 ат. % относительно содержания атомов иттрия.

При проведении синтеза в течение 4 ч во всех композициях сформировались фазы, обеспечивающие симметрию окружения ионов Eu3+, энергетические поля которой приводят к расщеплению дублета 5D0 → 7F2-электронного перехода, равному 18 нм (рис. 4). Широкая полоса поглощения в спектральной области <580 нм наиболее интенсивна. Она дает существенный фон в длинноволновой части спектра и влияет на относительные интенсивности полос люминесценции ионов Eu3+. Увеличение температуры синтеза до 600°С приводит к уменьшению относительной интенсивности этой полосы (рис. 4, спектр 3). Уменьшение интенсивности связано с формированием оксифторидов и оксида иттрия-европия, образующихся при “выгорании” органических продуктов с увеличением температуры. При увеличении времени синтеза до 6 ч интенсивность полосы уменьшается. Интенсивность полос дублета 5D0 → 7F2-электронного перехода при одинаковой концентрации ионов Eu3+, с учетом отличающегося фона, практически выравнивается (рис. 5, спектры 2 и 3). Это подтверждается равенством интенсивностей полос с максимумом 712 нм. Можно предположить, что появление широкой полосы люминесценции связано с дефектностью структуры поверхности частиц, образующихся из реакционных смесей, содержащих ТАА. Наиболее вероятной причиной возникновения дополнительных поверхностных дефектов являются ионы серы, посредством которых ТАА химически связан с лантаноидами в тиоацетамидных комплексах. Подобные эффекты отмечаются авторами [47]. При термолизе комплексов можно предположить образование европийсодержащих центров свечения, в которых ионы Eu3+ находятся в окружении не только ионов O2–, но и S2–. Такое предположение допускает вероятность участия в энергетических процессах межзонных переходов, возникающих в результате образования оксисульфидных структур. Данные переходы могут быть связаны с энергетическими потоками, проходящими с участием уровней энергии ионов Eu3+. Это приводит к изменению относительных интенсивностей полос люминесценции ионов Eu3+. Также это подтверждается исчезновением широкой полосы при нагревании композиций до t > 800°С, приводящем к “выгоранию” серосодержащих дефектов и замене ионов S2– ионами O2–.
В спектрах возбуждения люминесценции композиций, синтезированных без ТАА, в области >300 нм наблюдаются полосы, соответствующие собственному поглощению ионов Eu3+. Они соответствуют электронным переходам 7F0 → 5L8 (322 нм), 7F0 → 5D4 (363 нм), 7F0 → 5L7 (384 нм), 7F0 → 5L6 (394 нм), 7F0 → 5D3 (418 нм), 7F0 → 5D2 (466 нм) и 7F0 → 5D1 (537 нм) [38]. Полосы неоднородно уширены. Наиболее интенсивной, как правило, является полоса 7F0 → 5L6-перехода ионов Eu3+с максимумом 394 нм. В спектрах композиций, синтезированных при t < 400°С, разрешение полос значительно хуже. В интервале длин волн 300–450 нм они перекрываются и наблюдается широкая полоса. на ее фоне видны отдельные составляющие. С увеличением температуры синтеза разрешение улучшается. При увеличении времени синтеза композиций в их спектрах наблюдается перераспределение интенсивностей полос. Для композиций, синтезированных в течение 6 ч, наиболее интенсивной оказывается спектральная полоса с максимумом 466 нм (7F0 → 5D2). В спектрах композиций при увеличении концентрации ионов Eu3+ в интервале длин волн 230–280 нм проявляется широкая неинтенсивная полоса с максимумом в области 245 нм (рис. 6). Данную полосу связывают с сенсибилизационными схемами получения ионами Eu3+ дополнительной энергии неорганической матрицы [12, 13, 47, 48]. Механизм данного процесса объясняют [13, 48] переносом заряда с иона кислорода (О2–) через основное состояние иона Eu2+ посредством быстрого межсистемного перехода на возбужденные уровни иона Eu3+. Малая интенсивность данной полосы может быть обусловлена большим влиянием фторид-ионов в составе активаторных центров. Подтверждение этому – достаточно большая интенсивность полосы с максимумом 537 нм (7F0 → 5D1), которую относят к фазе (EuxY1 –x)F3 [12].
Рис. 6.
Спектр возбуждения люминесценции (λл = 615 нм) композиции, синтезированной из реакционной смеси Y(CF3COO)3 + Eu(CF3COO)3 при t = 600°C в течение 6 ч, СEu = 10 ат. % относительно содержания атомов иттрия.

В спектрах возбуждения люминесценции композиций, синтезированных с добавлением в реакционные смеси ТАА, наблюдается ряд изменений, которые мы связываем с его влиянием. В спектральном диапазоне 300 – 450 нм зарегистрирована широкая полоса с максимумом в области 390 нм (рис. 7, спектры 2 и 3). На ее фоне проявляются полосы собственного поглощения ионов Eu3+. В спектрах образцов, синтезированных при более высокой температуре, полуширина полосы уменьшается, относительная интенсивность в максимуме увеличивается, полосы собственного поглощения ионов европия становятся менее выраженными.
Рис. 7.
Спектры возбуждения люминесценции (λл = 618 нм) композиций, синтезированных из исходных смесей Y(CF3COO)3 + Eu(CF3COO)3, 2 ч, 600°С (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 2 ч, 400°С (2), Y(CF3COO)3 + + Eu(CF3COO)3 + ТАА, 2 ч, 600°С (3); СEu = 1.0 ат. % относительно содержания атомов иттрия.

Появление широкой полосы в спектрах возбуждения люминесценции (300–450 нм) у образцов, синтезированных без ТАА при температуре 400°С (2 ч) и при его введении в реакционную смесь при 400 и 600°С, объясняется существенной неоднородностью поглощающих центров. Она может быть связана со значительной дефектностью поверхности и дисперсностью частиц. Совпадение общей спектральной картины образцов, синтезированных без ТАА и в его присутствии, позволяет говорить о единой природе дефектов, а изменение интенсивности полос при разных температурах синтеза – о влиянии ионов S2–.
Кроме того, существенно увеличивается интенсивность (I240/I394) полосы в спектральной области <300 нм, связанной с передачей энергии возбуждения от матрицы ионам Eu3+ (рис. 7, спектры 2 и 3 и рис. 8). С увеличением температуры синтеза ниспадающая ветвь полосы претерпевает гипсохромный сдвиг (рис. 7, спектры 2 и 3). Это может происходить в результате уменьшения полуширины полосы при увеличении однородности композиции.
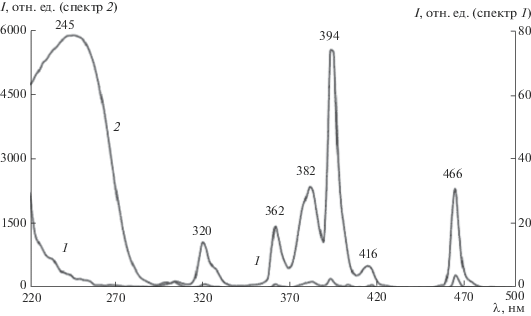
Рис. 8.
Спектры возбуждения люминесценции композиций, синтезированных из исходных смесей Y(CF3COO)3 + + Eu(CF3COO)3, 3 ч, 800°С, λл = 618 нм (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 6 ч, 800°С, λл = 615 нм (2); СEu = = 10 ат. % относительно содержания атомов иттрия.
На рис. 9 приведены спектры люминесценции композиций, синтезированных из исходных смесей Y(CF3COO)3 + Eu(CF3COO)3 и Y(CF3COO)3 + + Eu(CF3COO)3 + ТАА, содержащих по 10 ат. % ионов Eu3+, при 800°С в течение времени 3 и 6 ч. Их анализ показывает существенную зависимость интенсивности люминесценции от длины волны возбуждающего излучения (λв = 240 нм, спектр 3 и λв = 394 нм, спектры 1 и 2). Также подтверждается зависимость спектра люминесценции композиций от времени нагревания. Увеличение времени до 6 ч приводит к увеличению энергии расщепления дублета 5D0 → 7F2-электронного перехода до 18 нм. Наблюдаются ранее отмеченные изменения в областях 5D0 → 7F0,1,4-электронных переходов.
Рис. 9.
Спектры люминесценции композиций, синтезированных из исходных смесей Y(CF3COO)3 + Eu(CF3COO)3, 3 ч, 800°С (1), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 3 ч, 800°С (2), Y(CF3COO)3 + Eu(CF3COO)3 + ТАА, 6 ч, 800°С (3); 1 и 2 – λв = 394 нм, 3 – λв = 240 нм; СEu = 10 ат. % относительно содержания атомов иттрия.

Спектры возбуждения люминесценции данных образцов, зарегистрированные в максимумах полосы 5D0 → 7F2-электронного перехода для каждого состава 618 и 615 нм, приведены на рис. 8. Батохромное смещение полосы возбуждения люминесценции в области <300 нм является дополнительным подтверждением возможного участия ионов S2– в формировании поглощающих европийсодержащих центров. Гипсохромное смещение полосы возбуждения люминесценции (рис. 8 и рис. 7, спектр 2) можно объяснить совместным влиянием температуры и времени нагревания. Увеличение этих параметров направлено на “выгорание” серосодержащих центров свечения. По данным РФА, формируются фазы (EuxY1 –x)OF и (EuxY1 – x)2O3. Исходя из относительных интенсивностей полос спектральная картина стремится к виду, полученному для композиций, в синтезе которых ТАА не применялся.
ЗАКЛЮЧЕНИЕ
Термическим разложением трифторацетатов иттрия и европия, а также их тиоацетамидных комплексов при температурах 400, 600 и 800°С в течение времени от 2 до 6 ч синтезированы композиции на основе окифторидов и оксида иттрия, активированные ионами Eu3+. Предложена схема, отражающая состав основных продуктов, образующихся при увеличении температуры и времени синтеза. Выявлены зависимости спектров люминесценции и возбуждения люминесценции от состава реагентов, условий синтеза и других факторов.
Высказано предположение, что введение тиоацетамида в реакционные смеси приводит к формированию активаторных центров, содержащих ионы S2–. Дефектность, которую они создают на поверхности частиц, проявляется широкой полосой в спектре люминесценции с максимумом в интервале длин волн 480–500 нм. При увеличении температуры и времени синтеза данные дефекты “выгорают”, ионы S2– замещаются ионами O2–. Это приводит к уменьшению относительной интенсивности полосы и ее исчезновению в случае проведения синтеза при 800°С.
В спектрах возбуждения люминесценции увеличивается относительная интенсивность полос, связанных с сенсибилизационными процессами передачи энергии матрицы ионам Eu3+. Образование сульфоксидных активаторных центров проявляется в смещении полосы возбуждения в области <300 нм.
Список литературы
Ikesue A., Kinoshita T., Kamata K., Yoshida K. Fabrication and Optical Properties of High-Performance Polycrystalline Nd:YAG Ceramics for Solid-State Lasers // J. Am. Ceram. Soc. 1995. V. 78. № 4. P. 1033–1040.
Ikcsuc A., Aung Y.L., Taira T., Kamimura T., Yoshida K., Messing G.L. Progress in Ceramic Lasers // Ann. Rev. Mater. Res. 2006. V. 36. P. 397–429.
Сигловая Н.В. Исследование люминесцентных свойств и разработка технологии производства катодолюминофоров красного цвета свечения на основе Y2O3 для дисплейных и проекционных ЭЛТ: Дис … канд. хим. наук. Ставрополь, 2003. 143 с.
Михайлов М.Д., Семенча А.В. Колесников И.Е., Маньшина А.А. Синтез и исследование структуры наночастиц оксидов Y2O3:Eu // Современные проблемы науки и образования. 2012. № 2. С. 10–18.
Chong M.K., Pita K., Kam C.H. Photoluminescence of Y2O3:Eu3+ Thin Film Phosphors by Sol-Gel Deposition and Rapid Thermal Annealing // J. Phys. Chem. Solids. 2005. V. 66. № 1. P. 213–217.
Cho J.Y., Ko K.Y., Do Y.R. Optical Properties of Sol-Gel Derived Y2O3:Eu3+ Thin-Film Phosphors for Display // Thin Solid Films. 2007. V. 515. № 7–8. P. 3373–3379.
Anh T.K., Benalloul P., Barthou C. et al. Luminescence, Energy Transfer, and Upconversion Mechanisms of Y2O3 Nanomaterials Doped with Eu3+, Tb3+, Tm3+, Er3+, and Yb3+ Ions // J. Nanomater. 2007. V. 2007. Article ID 48247. P. 1–10.
Carrillo Romo F., García Murillo A., García Hernández M. et al. Structural and Luminescence Characterization of Silica Coated Y2O3:Eu3+ Nanopowders // Opt. Mater. 2010. V. 32. № 11. P. 1471–1479.
Gowd G.S., Patra M.K., Songara S. et al. Effect of Doping Concentration and Annealing Temperature on Luminescence Properties of Y2O3:Eu3+ Nanophosphor Prepared by Colloidal Precipitation Method // J. Luminescence. 2012. V. 132. № 8. P. 2023–2029.
Ray S., Manjón F.J., Mollar M.A. et al. Broadband, Site Selective and Time Resolved Photoluminescence Spectroscopic Studies of Finely Size-Modulated Y2O3:Eu3+ Phosphors Synthesized by a Complex Based Precursor Solution Method // Curr. Appl. Phys. 2014. V. 14. № 1. P. 72–81.
Грузинцев А.Н. Антистоксовая люминесценция Y2O3:Er // Неорган. материалы. 2014. Т. 50. № 1. С. 64–69.
Уклеина И.Ю. Оксифториды иттрия и РЗЭ: синтез, люминесценция и оптика. Дис. … канд. хим. наук. Ставрополь. СтГУ. 2005. 158 с.
Rakov N., Guimaraes R.B., Lozano W.B., Maciel G.S. Structural and Spectroscopic Analyses of Europium Doped Yttrium Oxyfluoride Powders Prepared by Combustion Synthesis // J. Appl. Phys. 2013. V. 114. № 4. P. 043517(1–7).
Wen T., Luo W., Wang Y. et al. Multicolour and Upconversion Fluorescence of Lanthanide Doped Vernier Phase Yttrium Oxyfluoride Nanocrystals // J. Mater. Chem. C. 2013. № 1. P. 1995–2001.
Rakov N., Maciel G.S. Comparative Study of Er3+ and Tm3+ Co-Doped YOF and Y2O3 Powders as Red Spectrally Pure Upconverters // Opt. Mater. 2013. № 35. P. 2372–2375.
Edelstein A.S., Cammarata R.C., Eds. Nanomaterials: Synthesis, Properties and Applications. London: Taylor & Francis, 1998. 687 p.
Nalwa H.S. Nanostructed Materials and Nanotechnology. San Diego: Academic Press., 2009. 609 p.
Помелова Т.А., Баковец В.В., Корольков И.В. и др. Об аномальной эффективности люминесценции субмикронного фосфора Y2O3:Eu3+ // Физика твердого тела. 2014. Т. 56. № 12. С. 2410–2419.
Kottaisamy M., Jeyakumar D., Jagannathan R., Rao M.M. Yttrium Oxide: Eu3+ Red Phosphor by Self-Propagating High Temperature Synthesis // Mater. Res. Bull.1996. V. 31. № 8. P. 1013–1020.
Konrad A., Fries T., Gahn A. et al. Chemical Vapor Synthesis and Luminescence Properties of Nanocrystalline Cubic Y2O3:Eu // J. Appl. Phys. 1999. V. 86. № 6. P. 3129–3133.
Capobianco J.A., Vetron F., D’Alesio T. et al. Optical Spectroscopy of Nanocrystalline Cubic Y2O3:Er3+ Obtained via Combustion Synthesis // Phys. Chem. Chem. Phys. 2000. V. 2. P. 3203–3207.
Lu J., Song J., Prabhu M. et al. High-Power Nd:Y3Al5O12 Ceramic Laser // Jpn. J. Appl. Phys. 2000. V. 39. № 10B. P. 1048–1050.
Hong G.Y., Jeon B.S., Yoo Y.K., Yoo J.S. Photoluminescence Characteristics of Spherical Y2O3:Eu Phosphors by Aerosol Pyrolysis // J. Electrochem. Soc. 2001. V. 148. № 11. P. H161–H166.
Zhang J., Zhang Z., Tang Z. et al. Luminescent properties of Y2O3:Eu Synthesized by Sol-Gel Processing // J. Mater. Proc. Technol. 2002. V. 121. № 2–3. P. 265–268.
Chavan S.V. Combustion Synthesis of Nanocrystalline Yttria: Tailoring of Powder Properties // Mater. Sci. Eng. B. 2006. V. 132. P. 266–271.
Jun Yeol Cho, Ki-Young Ko, Young Rag Do. Optical Properties of Sol-Gel Derived Y2O3:Eu3+ Thin-Film Phosphors for Display // Thin Solid Films. 2007. V. 515. № 7–8. P. 3373–3379.
Mangalaraja R.V. Combustion Synthesis of Y2O3 and Yb–Y2O3: Part I. Nanopowders and Their Characterization // J. Mater. Proc. Technol. 2008. V. 208. P. 415–422.
Garskaite E., Lindgren M., Einarsrud M.-A., Grande T. Luminescent Properties of Rare Earth (Er, Yb) Doped Yttrium Aluminium Garnet Thin Films and Bulk Samples Synthesised by an Aqueous Sol–Gel Technique // J. Eur. Ceram. Soc. 2010. T. 30. № 7. P. 1707–1715.
Belyakov A.V., Lemeshev D.O., Lukin E.S. et al. Optically Transparent Ceramics Based on Yttrium Oxide Using Carbonate and Alkoxy Precursore // Glass Ceramics. 2006. V. 63. № 7–8. P. 262–264.
Грузинцев А.Н., Ермолаева Ю.В., Матвеевская Н.А. и др. Зависимость люминесценции сферических наночастиц Y2O3:Er от их размера // Неорган. материалы. 2014. Т. 50. № 11. С. 1189–1194.
Иванов М.Г., Копылов Ю.Л., Кравченко В.Б. и др. Лазерная керамика ИАГ и Y2O3 из неагломерированных наноразмерных порошков // Неорган. материалы. 2014. Т. 50. № 9. С.1028–1036.
Багаев С.Н., Осипов В.В., Иванов М.Г. и др. Лазерная керамика из оксида иттрия, активированного неодимом // Квантовая электроника. 2008. Т. 38. № 9.С. 840–844.
Xu Y.-N., Ching W.Y., Gu Z.-Q. Electronic, Structural and Optical Properties of Crystalline Yttria // Phys. Rev. B. 1997. V. 56. № 23. P. 14993–15000.
Готовцева Е.Ю., Бирюков А.А., Светличный В.А. Стабильность и спектрально-люминесцентные свойства дисперсий наночастиц CdS и ZnS, синтезированных в различных растворителях // Изв. вузов. Физика. 2013. Т. 56. № 3. С. 32–37.
Смагин В.П., Давыдов Д.А., Унжакова Н.М., Бирюков А.А. Синтез и спектральные свойства коллоидных растворов сульфидов металлов // Журн. неорган. химии. 2015. Т. 60. № 12. С.1734–1740.
Смагин В.П., Еремина Н.С., Мичуева З.В. Синтез и спектрально-люминесцентные свойства композиций (Y2O3–YOF):Ln(III) // Неорган. материалы. 2017. Т. 53. № 8. С. 851–860.
Смагин В.П., Мокроусов Г.М. Физико-химические аспекты формирования и свойства оптически прозрачных металлсодержащих полимерных материалов. Барнаул: Изд-во Алт. ун-та, 2014. (http://elibrary.asu.ru/xmlui/bitstream/handle/asu/ 840/read.7book?sequence=1).
Колесников И.Е. Исследование люминесцентных свойств оксидных нанокристаллических порошков, легированных ионами европия. Дис. … канд. физ.-мат. наук. С-Петербург: СПбГУ, 2015. 134 с.
Спирина А.В. Люминесценция иттрий – алюминиевого граната и оксида иттрия, допированных неодимом: Автореф. дис. … канд. физ.-мат. наук. Екатеринбург: Институт электрофизики УрО РАН, 2011. 24 с.
Krsmanović R.M., Antić Z., Nikolić M.G. et al. Preparation of Y2O3:Eu3+ Nanopowders via Polymer Complex Solution Method and Luminescence Properties of the Sintered Ceramics // Ceram. Int. 2011. V. 37. № 2. P. 525–531.
Wang W.-N., Widiyastuti W., Ogi T. et al. Correlations between Crystallite/Particle Size and Photoluminescence Properties of Submicrometer Phosphors // Chem. Mater. 2007. V. 19. № 7. P. 1723–1730.
Srinivasan R., Yogamalar N.R., Elanchezhiyan J. et al. Structural and Optical Properties of Europium Doped Yttrium Oxide Nanoparticles for Phosphor Applications // J. Alloys. Compd. 2010. V. 496. № 1–2. P. 472–477.
Antic B., Rogan J., Kremenovic A. et al. Optimization of Photoluminescence of Y2O3:Eu and Gd2O3:Eu Phosphors Synthesized by Thermolysis of 2,4-Pentanedione Complexes // Nanotechnology. 2010. V. 21. № 24. P. 245702.
Физер Л., Физер М. Реагенты для органического синтеза. Т. 7. М.: Мир, 1978. 498 с.
Алексеева Л.В. Фотохимическое получение и свойства коллоидов на основе комплексов переходных металлов: Автореф. дис. … канд. хим. наук. С-Петербург: РГПУ им. А.И. Герцена, 1994. 18 с.
Туленин С.С. Гидрохимическое осаждение пленок In2S3, In2Se3 и халькопиритных структур на их основе: Дис. … канд. хим. наук. Екатеринбург: ФГАОУ ВПО “Уральский федеральный университет им. первого Президента России Б.Н. Ельцина”, 2015. 197 с.
Белобелецкая М.В., Стеблевская Н.И., Медков М.А. Люминофоры красного и зеленого свечения на основе оксидов, оксисульфидов и фосфатов РЗЭ // Вестн. ДВО РАН. 2013. № 5(171). С. 33–38.
Dorenbos P. Systematic Behaviour in Trivalent Lanthanide Charge Transfer Energies // J. Phys.: Condens. Matter. 2003. V. 15. № 49. P. 8417–8434.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


